1. 领域背景与文献
文献英文标题:Genetic suppressor of autophagy defects in huntingtin null cells identified using a mutagenesis screen in Dictyostelium discoideum;发表期刊:BMC Molecular and Cell Biology;影响因子:未公开;研究领域:神经退行性疾病(亨廷顿病)的自噬调控机制与治疗靶点筛选。
领域共识:亨廷顿病是一种常染色体显性遗传的神经退行性疾病,人群发病率约为1/10000,通常在30-50岁发病,发病后15-20年因肺部感染、运动功能衰竭等并发症死亡,目前尚无任何可延缓疾病进展的治疗手段,已获批的症状控制药物存在严重的精神类副作用。亨廷顿病的核心致病机制为亨廷顿蛋白(HTT)基因1号外显子中CAG三核苷酸重复序列异常扩增(>35次),导致突变亨廷顿蛋白错误折叠、形成聚集物无法被细胞清除,同时野生型亨廷顿蛋白的功能缺失也会加剧病理进程。现有研究已证实野生型亨廷顿蛋白在自噬的后期阶段发挥关键作用,参与自噬底物识别、自噬体沿细胞骨架运输、自噬体与溶酶体融合等过程,亨廷顿病中的自噬缺陷并非源于自噬起始异常,而是自噬底物运输和融合效率降低。
当前领域存在三大未解决核心问题:一是哺乳动物中亨廷顿蛋白全敲除会导致胚胎致死,无法单独研究野生型亨廷顿蛋白功能缺失导致的自噬缺陷机制;二是现有自噬干预策略多靶向自噬上游通路,无法有效解决亨廷顿蛋白缺失导致的自噬后期运输障碍;三是缺乏在无野生型亨廷顿蛋白背景下可稳定挽救自噬功能的遗传靶点。本研究针对上述空白,采用单倍体模式生物盘基网柄菌的亨廷顿蛋白缺失模型,通过化学诱变筛选可挽救自噬缺陷的二次突变株,为亨廷顿病的治疗提供潜在的新靶点,具有重要的基础研究价值。
2. 文献综述解析
本研究的文献综述部分按“疾病病理机制→自噬干预策略→模式生物应用”三个维度梳理现有研究,核心评述逻辑围绕“亨廷顿蛋白功能缺失导致自噬缺陷的研究空白”展开,为后续的诱变筛选实验提供理论依据。
现有研究中,疾病病理机制类研究的核心支持观点为亨廷顿蛋白的功能缺失是亨廷顿病病理的重要组成部分,而非仅由突变蛋白的毒性获得功能主导,这类研究的优势是明确了自噬缺陷是亨廷顿病的核心病理特征,局限性是多基于二倍体哺乳动物模型,无法排除野生型等位基因的干扰,对亨廷顿蛋白完全缺失下的细胞功能变化研究较少。自噬干预策略类研究的核心支持观点为增强自噬可促进突变亨廷顿蛋白的清除、缓解神经毒性,现有技术方法包括小分子自噬诱导剂、关键自噬基因过表达等,已在果蝇、细胞模型中实现部分表型挽救,这类研究的优势是验证了自噬干预的可行性,局限性是现有干预靶点多针对自噬上游的起始阶段,无法解决亨廷顿蛋白缺失导致的自噬后期自噬底物运输和融合障碍,且未在完全无野生型亨廷顿蛋白的背景下验证疗效。模式生物应用类研究的核心支持观点为盘基网柄菌作为单倍体模式生物,自噬通路与哺乳动物高度保守,亨廷顿蛋白敲除后细胞可存活,且存在单细胞到多细胞的发育阶段,适合进行大规模遗传筛选,这类研究的优势是可排除等位基因干扰,实现高效的正向遗传筛选,局限性是目前利用该模型筛选亨廷顿病自噬调控靶点的研究尚未见报道。
本研究的创新价值体现在三个方面:一是首次在盘基网柄菌亨廷顿蛋白缺失模型中开展全基因组化学诱变筛选,获得了可部分挽救自噬缺陷的突变株;二是联合全基因组测序和转录组测序,定位了4个候选突变基因和5个下游自噬相关差异表达基因;三是证实了囊泡运输、脂质代谢等通路的二次突变可补偿亨廷顿蛋白缺失的功能,填补了亨廷顿蛋白功能缺失背景下自噬挽救靶点的研究空白。
3. 研究思路总结与详细解析
本研究整体围绕“筛选可挽救亨廷顿蛋白缺失细胞自噬缺陷的遗传抑制子”的核心目标展开,核心科学问题为“二次突变通过哪些分子通路补偿亨廷顿蛋白缺失导致的自噬后期功能障碍”,技术路线遵循“化学诱变→表型初筛→多维度表型验证→多组学联合分析→候选靶点功能注释”的闭环逻辑,所有表型实验均设置3次生物学重复,测序分析采用严格的统计学过滤标准,结果可靠性较高。
3.1 诱变筛选与抑制子突变株获得
该环节的核心实验目的是筛选获得可在氯化铵(自噬溶酶体功能抑制剂)胁迫下存活的亨廷顿蛋白缺失突变株。方法细节:采用1-甲基-3-硝基-1-亚硝基胍(NTG)对亨廷顿蛋白缺失细胞进行化学诱变处理10分钟,将诱变后的细胞稀释后接种于含30mM氯化铵的SM培养基平板上,同时设置野生型盘基网柄菌AX3、未诱变的亨廷顿蛋白缺失细胞为对照,21℃培养14天,筛选可发育形成子实体的存活突变株,命名为亨廷顿蛋白缺失抑制子株(htt⁻;supX)。结果解读:在300块筛选平板中仅获得1株可在氯化铵胁迫下完成发育的突变株,表型验证显示该菌株可在30mM氯化铵条件下形成子实体,而未诱变的亨廷顿蛋白缺失细胞无法在该条件下存活(对应结果图1,
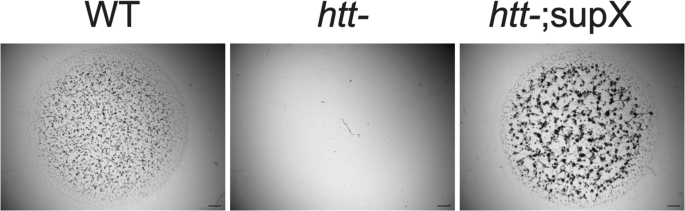
)。产品关联:文献未提及具体实验产品,领域常规使用化学诱变剂NTG、盘基网柄菌基础SM培养基进行诱变筛选实验。
3.2 多细胞发育表型验证
该环节的核心实验目的是验证亨廷顿蛋白缺失抑制子株的多细胞发育表型是否得到挽救。方法细节:将野生型、亨廷顿蛋白缺失株、亨廷顿蛋白缺失抑制子株分别接种于SM培养基平板,置于21℃湿度可控的黑暗培养箱中培养28小时,每小时采用体式显微镜拍照记录发育进程,在发育12小时的时间点统计细胞团(mound)的数量,实验设置3次生物学重复。结果解读:发育12小时时,野生型的细胞团数量为274±17.35个(n=3),亨廷顿蛋白缺失株为191±11.79个(n=3,与野生型相比t检验P=0.004,Bonferroni校正P=0.011),亨廷顿蛋白缺失抑制子株为234±13.20个(n=3,与亨廷顿蛋白缺失株相比t检验P=0.014,Bonferroni校正P=0.043);但亨廷顿蛋白缺失抑制子株的非细胞团结构数量与亨廷顿蛋白缺失株无统计学差异(P=0.23),而野生型无松散的非细胞团结构,说明该突变株的发育数量表型得到部分挽救,但细胞发育的同步性未恢复(对应结果图2,

)。产品关联:文献未提及具体实验产品,领域常规使用体式显微镜进行盘基网柄菌的发育表型观察。
3.3 自噬通量检测(自噬底物降解实验)
该环节的核心实验目的是验证亨廷顿蛋白缺失抑制子株的自噬底物降解能力是否恢复。方法细节:将融合表达磷酸甘油酸激酶与绿色荧光蛋白的PGK-GFP质粒通过电穿孔法导入三种细胞,通过无营养的KK2缓冲液处理诱导自噬,同时施加0、100、200mM氯化铵抑制溶酶体降解功能,培养4小时后收集细胞裂解液,采用蛋白免疫印迹(WB)检测游离绿色荧光蛋白的含量,以β-肌动蛋白为内参进行灰度定量,实验设置3次生物学重复。结果解读:100mM氯化铵处理条件下,野生型的游离绿色荧光蛋白相对灰度值为1.30±0.11AU(n=3),亨廷顿蛋白缺失株为0.58±0.15AU(n=3,与野生型相比P=0.006),亨廷顿蛋白缺失抑制子株为0.98±0.23AU(n=3,与野生型相比P=0.148,与亨廷顿蛋白缺失株相比P=0.055),说明该突变株的自噬底物降解能力得到部分恢复,自噬通量显著提升(对应结果图3,
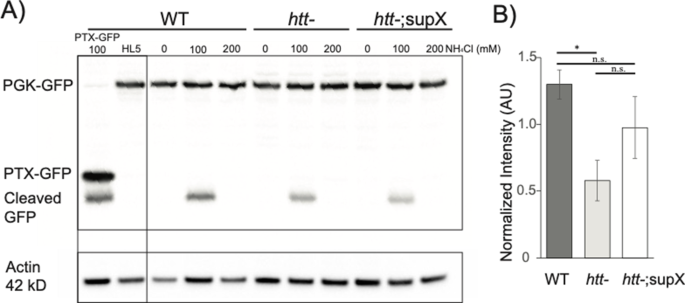
)。产品关联:实验所用关键产品:Abcam的抗绿色荧光蛋白兔多克隆抗体(货号ab290)、Abcam的抗β-肌动蛋白鼠单克隆抗体(货号ab8224)、Invitrogen的4-12% Bis-Tris蛋白凝胶(货号NP0322BOX)。
3.4 全基因组测序与突变位点鉴定
该环节的核心实验目的是定位亨廷顿蛋白缺失抑制子株中携带的二次突变位点。方法细节:分别提取亨廷顿蛋白缺失株和亨廷顿蛋白缺失抑制子株的基因组DNA,采用Illumina NextSeq500测序平台进行全基因组测序,测序深度大于50X,将reads比对到盘基网柄菌参考基因组后,采用FreeBayes进行变异检测,过滤条件为等位基因频率≥95%、测序深度≥20,筛选仅在亨廷顿蛋白缺失抑制子株中存在的突变位点。结果解读:共鉴定到4个可靠的差异突变位点,分别为:1)3号染色体DDB_G0280471基因启动子区的腺嘌呤插入突变,该基因预测参与金属离子结合,其拟南芥同源物参与囊泡分选和自噬调控;2)4号染色体DDB_G0281643基因编码区的2个氨基酸(甘氨酸、丝氨酸)缺失突变,该基因预测参与信号转导和跨膜运输;3)4号染色体DDB_G0283243基因编码区的天冬氨酸→酪氨酸错义突变,该基因含MRH结构域,预测具有Rab GTP酶激活活性、参与囊泡融合调控;4)6号染色体eloA基因编码区的半胱氨酸→酪氨酸错义突变,该基因编码长链脂肪酸延长酶,参与脂质代谢调控。产品关联:文献未提及具体实验产品,领域常规使用基因组提取试剂盒、Illumina测序建库试剂盒进行全基因组测序实验。
3.5 转录组测序与差异表达分析
该环节的核心实验目的是分析亨廷顿蛋白缺失抑制子株的基因表达变化,筛选下游参与自噬调控的差异表达基因。方法细节:将三种细胞分别置于营养充足的HL5培养基、缺乏精氨酸和赖氨酸的FM培养基(氨基酸剥夺诱导自噬)中培养1小时,提取总RNA进行3"mRNA测序,每个样本平均测序量为1420万reads,采用STAR比对参考基因组、featureCounts定量基因表达量、DESeq2进行差异表达分析,筛选标准为错误发现率(FDR)校正P值<0.05,同时采用加权基因共表达网络分析(WGCNA)构建基因共表达模块。结果解读:氨基酸剥夺条件下,亨廷顿蛋白缺失抑制子株与亨廷顿蛋白缺失株相比共存在208个差异表达基因,其中64个基因上调、144个基因下调;26个基因的表达水平恢复至野生型水平,包括5个已知的自噬相关基因:osbF(氧固醇结合蛋白,参与膜脂质运输)、DDB_G0280565(Rab GTP酶效应因子同源物,调控自噬通量)、DDB_G0276445(热休克蛋白HSPA8同源物,参与分子伴侣介导的自噬)、syn16a(突触融合蛋白16,SNARE家族蛋白,参与自噬溶酶体形成)、vacA(囊泡相关蛋白)(对应结果图4、图5,
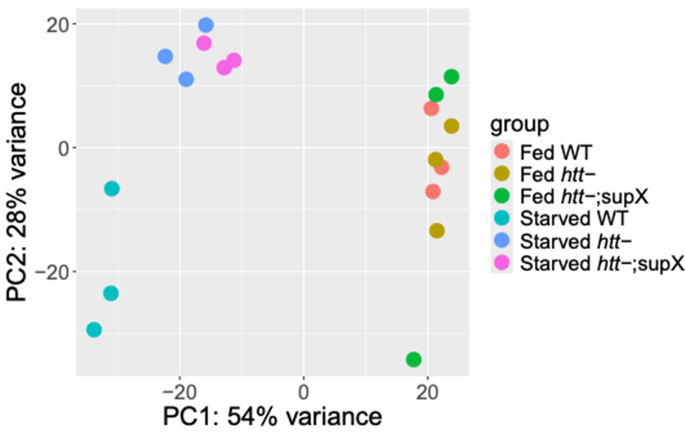
、
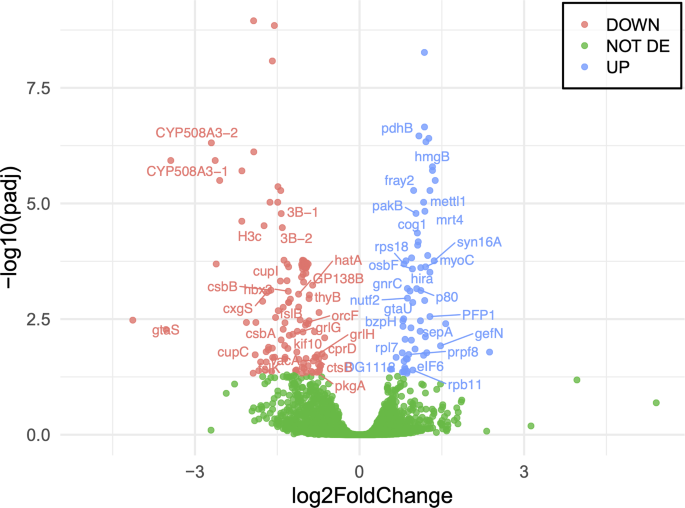
)。共表达网络分析显示,osbF、DDB_G0280565、DDB_G0276445三个自噬相关基因与含MRH结构域的突变基因位于同一共表达模块,该模块富集信号转导、蛋白磷酸化、环腺苷酸趋化等功能。产品关联:文献未提及具体实验产品,领域常规使用RNA提取试剂盒、3"mRNA测序建库试剂盒进行转录组测序实验。
4. Biomarker研究及发现成果
本研究未开发临床应用级Biomarker,而是鉴定得到9个可指示亨廷顿蛋白缺失背景下自噬功能挽救的候选分子Biomarker,包括4个基因组突变位点和5个转录水平差异表达的自噬相关基因,所有候选分子均经过多组学测序验证与功能注释,具有潜在的基础研究和转化应用价值。
本研究的候选Biomarker筛选逻辑为“化学诱变构建突变文库→氯化铵胁迫筛选存活株→全基因组测序定位特异突变位点→转录组测序验证基因表达变化→功能注释筛选自噬相关靶点”,逻辑链条完整。候选Biomarker的来源为盘基网柄菌亨廷顿蛋白缺失抑制子株的基因组和转录组样本,验证方法包括全基因组测序突变定位、转录组差异表达分析、共表达网络分析、同源基因功能注释;特异性方面,4个突变位点为亨廷顿蛋白缺失抑制子株特有,5个自噬相关基因的表达水平在亨廷顿蛋白缺失株中异常,在抑制子株中恢复至野生型水平,特异性良好;敏感性和诊断效能数据未在原文中提供。
核心成果提炼如下:一是4个突变基因可作为亨廷顿蛋白缺失背景下自噬缺陷挽救的候选功能Biomarker,其中含MRH结构域的DDB_G0283243基因与Rab GTP酶调控、囊泡融合相关,与下游3个自噬相关基因存在共表达关联,是核心候选靶点,所有突变位点的测序深度均≥20,等位基因频率≥95%,可靠性高;二是5个自噬相关基因可作为自噬功能恢复的表达Biomarker,其中syn16a在亨廷顿蛋白缺失抑制子株中显著过表达(FDR<0.05),其人类同源物参与自噬溶酶体形成,可作为亨廷顿病自噬干预的潜在靶点,所有差异表达基因的FDR校正P值均<0.05,样本量为生物学重复n=3;三是上述候选基因均参与囊泡运输、脂质代谢、分子伴侣调控等自噬后期通路,证实了这些通路在补偿亨廷顿蛋白功能缺失中的核心作用。推测:上述候选基因的人类同源物可能通过调控自噬体-溶酶体融合、自噬底物识别等通路挽救亨廷顿病模型中的自噬缺陷,需在哺乳动物细胞和动物模型中进一步验证功能。