1. 领域背景与文献引入
文献英文标题:Evaluation of the outgrowth technique for the isolation of epithelial cells from nasal polyps;发表期刊:BMC Ear, Nose and Throat Disorders;影响因子:未公开;研究领域:慢性鼻-鼻窦炎伴鼻息肉(CRSwNP)的上皮细胞生物学与实验模型构建。
慢性鼻-鼻窦炎伴鼻息肉是一类以2型炎症为核心特征的上呼吸道慢性炎症性疾病,临床证据显示嗜酸性粒细胞浸润、白细胞介素-4(IL-4)/白细胞介素-5(IL-5)/免疫球蛋白E(IgE)通路激活是其关键发病机制,现有靶向2型细胞因子的生物制剂如dupilumab等已显示出良好疗效,但上皮细胞在CRSwNP病理重塑(如基底细胞增生、纤毛功能障碍)中的具体调控机制尚未完全阐明,成为领域内未解决的核心问题。领域共识:上皮细胞作为CRSwNP病理过程中的重要效应细胞,可通过分泌白细胞介素-33(IL-33)等促炎介质激活2型免疫反应,推动疾病进展,因此建立稳定、可靠的鼻息肉上皮细胞体外培养模型是开展机制研究与药物筛选的关键前提。目前领域内常用的鼻上皮细胞分离方法存在局限性,如刷取法成功率有限、酶解离法易损伤细胞生理活性,因此亟需开发一种高效、低损伤的细胞分离技术,本研究正是针对这一需求,评估了生长法(outgrowth technique)用于鼻息肉上皮细胞分离的可行性,为后续研究提供实验基础。
2. 文献综述解析
本文献综述部分通过对比领域内现有鼻上皮细胞分离技术的优缺点,明确了本研究采用的生长法的创新价值与应用优势。
现有研究中,鼻上皮细胞分离主要采用刷取法或酶解离法,部分研究将两种方法结合。刷取法操作简便,可用于非手术志愿者的样本采集,但细胞分离成功率仅为63%-90%,难以保证稳定的细胞来源;酶解离法依赖手术获取的鼻组织,但由于鼻黏膜难以像皮肤组织那样实现完全去上皮化,酶处理会同时作用于黏膜下层组织,导致分离细胞的纯度降低,此外蛋白酶处理还可能改变细胞的DNA甲基化等生理状态,影响后续实验结果的可靠性,且所需的蛋白酶试剂成本较高。本研究首次将常用于成纤维细胞分离的生长法应用于鼻息肉上皮细胞分离,通过与现有方法对比,凸显了该技术的核心优势:一是细胞分离成功率达100%,所有纳入的3例鼻息肉样本均成功分离出上皮细胞;二是分离得到的细胞纯度高、增殖能力强,且保留了原有的2型炎症相关功能,同时该技术操作简便、成本较低,为CRSwNP上皮细胞研究提供了新的技术范式。
3. 研究思路总结与详细解析
本研究的核心目标是评估生长法分离鼻息肉上皮细胞的可行性,围绕“细胞分离效率-细胞生物学特性-细胞功能完整性”的逻辑链条开展实验,依次验证了生长法的分离成功率、细胞增殖能力、细胞纯度与分化状态,以及细胞的2型炎症相关功能,形成了完整的技术评估体系。
3.1 鼻息肉上皮细胞的生长法分离与增殖能力评估
实验目的:验证生长法能否从鼻息肉组织中成功分离上皮细胞,并评估分离细胞的体外增殖能力。
方法细节:选取3例CRSwNP患者的手术切除鼻息肉组织,将组织剪切成1-1.5mm的小块,每孔2块放置于12孔板中,干燥5-10min使组织块贴壁后,加入350μl支气管上皮细胞生长培养基(BEGM),每2天更换培养基,培养8天后收集细胞;将细胞以每孔5000个的密度接种于6孔板,每6天计数一次细胞总数,连续观察至第3代。
结果解读:培养8天内,3例样本的组织块上皮细胞生长成功率分别为79.2%(19/24)、100%(24/24)、100%(24/24),所有样本均成功分离出上皮细胞(n=3);第3代细胞的增殖倍数达7-23倍,显示出良好的体外增殖活性。
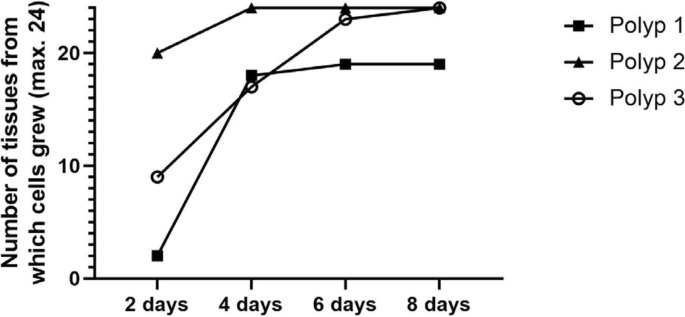
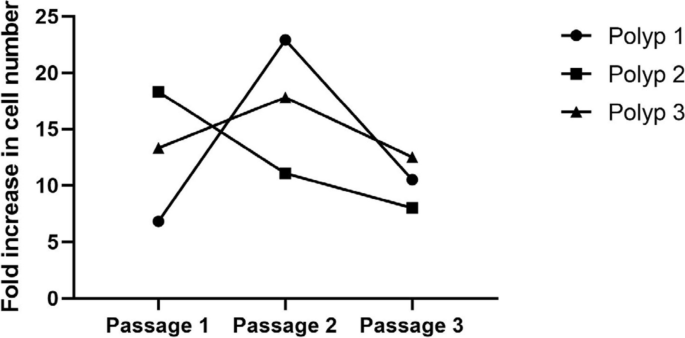
实验所用关键产品:Gibco的Dulbecco改良伊格尔培养基(货号1437676)、Lonza的支气管上皮细胞生长培养基(BEGM,货号CC-3170)、Bio&SELL的胎牛血清(货号FBS.S 0615 HI)与青霉素/链霉素(货号BS.A 2213)等。
3.2 流式细胞术鉴定细胞特性
实验目的:鉴定分离细胞的上皮细胞属性、分化状态与增殖活性。
方法细节:取第2或第3代细胞,经固定、通透处理后,依次用抗p63一抗、AlexaFluor633标记的二抗孵育,再用PE标记的抗细胞角蛋白抗体、FITC标记的抗Ki-67抗体孵育,通过流式细胞术检测细胞标志物的表达水平。
结果解读:流式细胞术结果显示,97.02%±0.2194%的细胞同时表达细胞角蛋白与p63(n=3),表明分离得到的细胞为未分化的上皮细胞;86.45%±2.532%的细胞表达Ki-67(n=3),进一步验证了细胞的高增殖活性,与前期细胞计数结果一致。
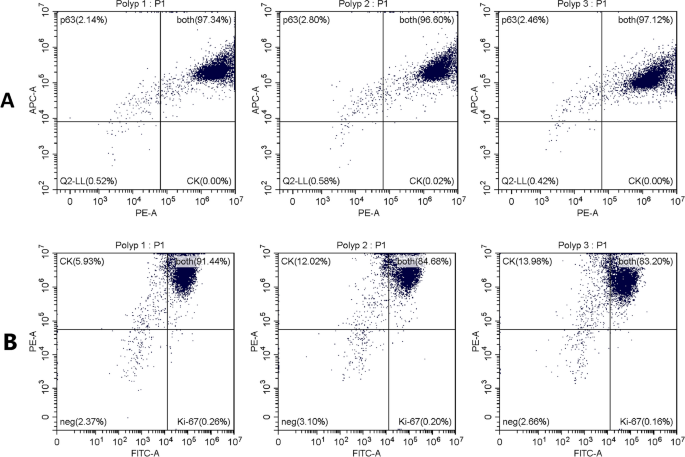
实验所用关键产品:Miltenyi Biotec的抗细胞角蛋白-PE抗体(克隆号REA831)、抗Ki-67-FITC抗体(克隆号REA183)、Ventana Medical的抗p63抗体(克隆号4A4)、Molecular Probes的AlexaFluor633标记的抗小鼠二抗(货号A-21052)等。
3.3 ELISA验证细胞功能
实验目的:验证分离得到的上皮细胞是否保留了CRSwNP病理状态下的2型炎症相关功能。
方法细节:选取另外3例CRSwNP患者的鼻息肉组织,采用生长法分离上皮细胞,将细胞接种于24孔板,待细胞汇合度达70%-80%后,分别收集培养24h、48h、72h的上清液,通过酶联免疫吸附试验(ELISA)检测上清液中IL-33与骨膜蛋白(periostin)的浓度。
结果解读:ELISA结果显示,分离的上皮细胞可稳定分泌IL-33与periostin:IL-33的浓度在24h、48h、72h分别为21.39±0.7679pg/ml、20.18±1.044pg/ml、21.18±1.491pg/ml(n=3);periostin的浓度在24h、48h、72h分别为147.5±15.92pg/ml、186.5±41.11pg/ml、250.3±18.60pg/ml(n=3),表明细胞保留了病理状态下的促炎功能,可用于后续2型炎症相关机制研究。
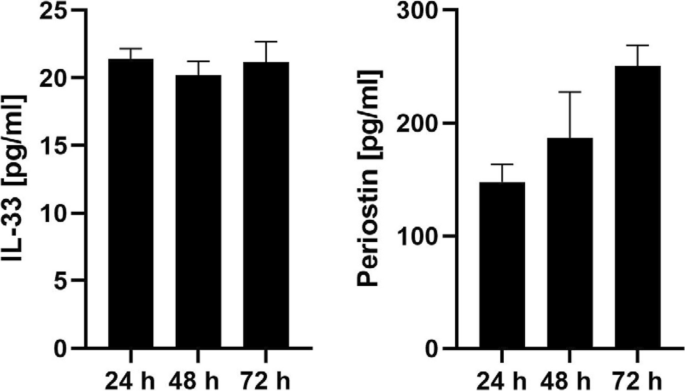
实验所用关键产品:Invitrogen的IL-33 ELISA试剂盒(货号BMS2048TEN)、R&D Systems的periostin ELISA试剂盒(货号DY3548B)等。
4. Biomarker研究及发现成果
本研究涉及两类生物标志物,一类用于鉴定上皮细胞的特性(细胞角蛋白、p63、Ki-67),另一类用于验证细胞的病理功能(IL-33、periostin),通过流式细胞术与ELISA技术,明确了生长法分离细胞的生物学特性与功能完整性。
Biomarker定位:细胞角蛋白与p63作为未分化上皮细胞的特异性标志物,Ki-67作为细胞增殖活性标志物,IL-33与periostin作为CRSwNP 2型炎症的关键效应标志物;筛选与验证逻辑为:先通过流式细胞术鉴定分离细胞的上皮细胞属性与增殖状态,再通过ELISA验证细胞是否保留分泌2型炎症相关介质的功能。研究过程详述:细胞标志物检测采用流式细胞术,样本为3例分离的第2或第3代上皮细胞,结果显示97.02%±0.2194%的细胞呈细胞角蛋白与p63双阳性(n=3),86.45%±2.532%的细胞呈Ki-67阳性(n=3);功能标志物检测采用ELISA,样本为另外3例细胞培养的上清液,IL-33在24h、48h、72h的分泌水平稳定,periostin分泌水平随培养时间延长呈上升趋势(n=3)。核心成果提炼:本研究首次证实生长法分离的鼻息肉上皮细胞可高表达未分化上皮细胞标志物,且具有强增殖活性,同时保留了分泌IL-33、periostin等2型炎症介质的功能,这些Biomarker的表达特征表明该细胞模型可真实反映CRSwNP病理状态下的上皮细胞特性,为后续研究上皮细胞在疾病重塑中的机制提供了可靠的实验工具;其中IL-33作为连接上皮细胞与2型免疫反应的关键介质,其稳定分泌特性为进一步探索上皮细胞与免疫细胞的相互作用机制奠定了基础,相关数据均以均值±标准误呈现,样本量n=3,结果具有统计学可靠性。