1. 领域背景与文献
文献英文标题:Establishment of an androgen-independent Lncap cell line and analysis of its biological characteristics;发表期刊:未明确提供;影响因子:未明确提供;研究领域:去势抵抗性前列腺癌(CRPC)细胞模型与生物学特性研究
领域共识:前列腺癌是全球男性十大恶性肿瘤之一,早期可通过磁共振成像及前列腺特异性抗原(PSA)筛查诊断,采用手术、放疗可获得良好预后;雄激素剥夺治疗(ADT)对早期前列腺癌疗效显著,但6-18个月后多数患者进展为去势抵抗性前列腺癌(CRPC),此类患者预后差且缺乏有效治疗手段。当前CRPC研究热点集中在其发生机制、新型治疗靶点及理想细胞模型构建,核心未解决问题包括:缺乏能模拟从雄激素依赖到非依赖转化过程的细胞模型,现有PC3、DU145等雄激素非依赖性细胞系不表达雄激素受体(AR),无法还原临床中ADT诱导的转化过程;同时,细胞黏附在肿瘤转移中的作用已被证实,但CRPC中细胞黏附与增殖、迁移等生物学行为的关联机制尚未明确。本研究针对上述空白,旨在通过优化培养方法构建稳定的雄激素非依赖性Lncap(Lncap-AI)细胞系,并系统解析其生物学特性,为CRPC的机制研究及药物研发提供理想模型。
2. 文献综述解析
作者从前列腺癌细胞模型分类、CRPC发生机制及细胞黏附研究现状三个维度对领域内现有研究进行评述,明确了当前研究的优势与局限性,进而提出本研究的创新方向。
现有研究中,针对前列腺癌细胞模型的研究显示,Lncap是唯一保留雄激素依赖特性并分泌PSA的人源前列腺癌细胞系,是构建CRPC转化模型的理想基础,但传统仅采用雄激素剥夺培养的方法构建Lncap-AI细胞系周期长、效率低;PC3、DU145等天然雄激素非依赖性细胞系虽可用于CRPC研究,但因不表达AR,无法模拟ADT诱导的转化过程。在CRPC发生机制研究中,AR通路重构被认为是核心机制之一,但不同模型中AR的表达模式存在差异,缺乏统一的验证体系;细胞黏附在肿瘤转移中起关键作用,已有研究证实部分黏附分子与前列腺癌转移相关,但CRPC中细胞黏附与增殖、迁移的关联及具体调控基因尚未系统解析。本研究的创新点在于,首次采用逐步增加氟他胺浓度结合雄激素剥夺的培养方法,高效构建了稳定的Lncap-AI细胞系,同时系统解析了该细胞系的增殖、迁移、黏附特性及相关基因表达,填补了CRPC转化模型及细胞黏附机制研究的空白。
3. 研究思路总结与详细解析
本研究以构建稳定的雄激素非依赖性Lncap细胞系并解析其生物学特性为目标,围绕“细胞转化-分子鉴定-功能解析-机制初探”的逻辑链条开展实验,通过多维度实验验证了Lncap-AI细胞系的特性及潜在调控机制。
3.1 雄激素非依赖性Lncap-AI细胞系构建
该环节核心目标是通过优化培养条件,诱导雄激素依赖性Lncap(Lncap-AD)细胞转化为雄激素非依赖性Lncap-AI细胞。实验采用5代Lncap细胞,使用含活性炭处理胎牛血清的RPMI 1640培养基进行雄激素剥夺培养,同时逐步增加氟他胺浓度:0-20代使用0.1μM氟他胺,21-40代使用0.5μM氟他胺,41-60代使用2.5μM氟他胺,持续培养16个月传代60次。通过光学显微镜观察细胞形态,结果显示Lncap-AD细胞呈球形、聚簇生长,而Lncap-AI细胞形态变为细长,细胞间间隙增大,苏木精-伊红(HE)染色显示其形态与PC3细胞相似,提示细胞已成功转化为雄激素非依赖性表型。实验所用关键产品:Solarbio的0.25%含EDTA胰酶(货号T1350)、Gibco的RPMI Medium 1640培养基(货号11835-030)、Biological Industries的活性炭处理胎牛血清(货号04-201-1 A)、Yuanye的氟他胺(货号H20A9Z68074)。
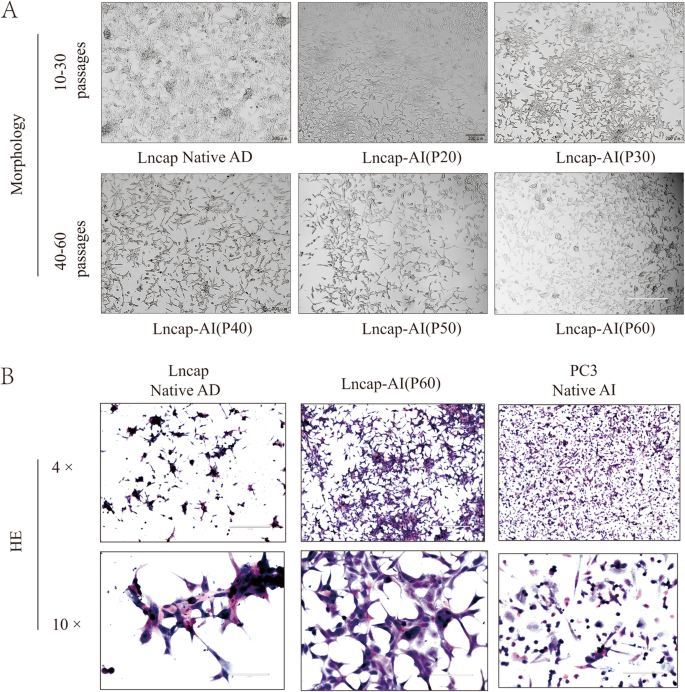
3.2 Lncap-AI细胞系分子鉴定
该环节核心目标是从分子水平验证Lncap-AI细胞系的雄激素非依赖性及AR通路变化。实验采用实时荧光定量PCR(qRT-PCR)检测AR及相关基因FKBP5、STEAP1的mRNA表达,蛋白质免疫印迹(Western Blot)检测AR、PSA、HK2的蛋白表达,并使用AR抑制剂恩杂鲁胺处理细胞,检测AR通路敏感性。结果显示,Lncap-AI细胞中AR、FKBP5、STEAP1的mRNA表达显著高于Lncap-AD细胞(文献未明确提供具体数值及P值);蛋白质免疫印迹结果显示Lncap-AI细胞中AR蛋白表达低于Lncap-AD细胞,PSA蛋白表达高于Lncap-AD细胞;恩杂鲁胺处理后,Lncap-AD细胞中AR、HK2蛋白表达下调,而Lncap-AI细胞中无明显变化,提示Lncap-AI细胞对AR抑制剂不敏感,已具备雄激素非依赖性特征。实验所用关键产品:Invitrogen的TRIzol试剂、TaKaRa的PrimeScript RT试剂 Kit(含gDNA Eraser)、Abcam的PSA抗体(货号ab53774)、Cell Signaling Technology的AR、HK2、β-肌动蛋白抗体、APExBIO的恩杂鲁胺(货号A3003)。
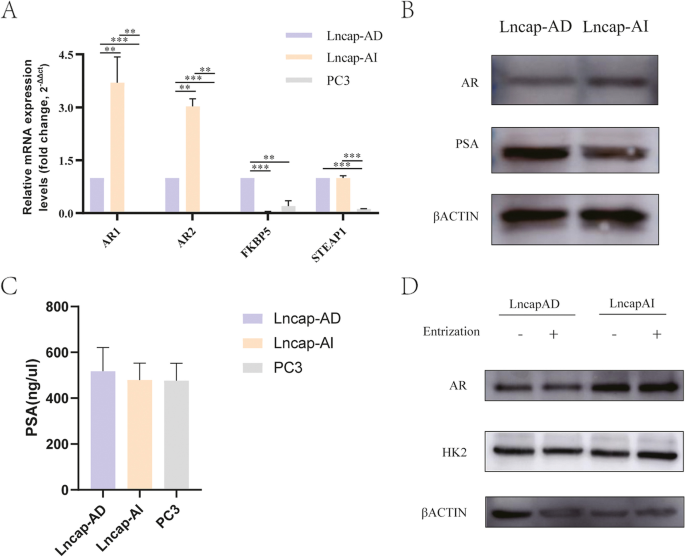
3.3 Lncap-AI细胞生物学功能解析
该环节核心目标是解析Lncap-AI细胞的增殖、迁移、黏附能力变化及相关基因调控机制。实验采用5-乙炔基-2"-脱氧尿苷(EdU)实验检测细胞增殖能力,细胞计数试剂盒-8(CCK-8)实验检测细胞活力,划痕实验检测迁移能力,细胞黏附实验检测黏附能力,并通过实时荧光定量PCR检测细胞黏附相关基因的表达。结果显示,EdU实验中Lncap-AI细胞的增殖标记阳性率高于Lncap-AD细胞(文献未明确提供具体数值及P值);CCK-8实验显示培养5天时,Lncap-AI细胞活力显著高于Lncap-AD细胞(文献未明确提供具体数值及P值);划痕实验显示48小时内Lncap-AI细胞的迁移距离显著大于Lncap-AD细胞(文献未明确提供具体数值及P值);细胞黏附实验显示Lncap-AI细胞的黏附能力显著高于Lncap-AD细胞(文献未明确提供具体数值及P值);实时荧光定量PCR结果显示,Lncap-AI细胞中MCAM、ICAM1、L1CAM、ALCAM的mRNA表达显著高于Lncap-AD细胞,其中MCAM(P<0.001)、ICAM1(P<0.001)的差异具有统计学意义,提示这些基因可能参与调控Lncap-AI细胞的黏附及迁移能力。实验所用关键产品:RIBBIO的Cell-Light Apollo 567 EdU试剂盒(货号C10371-1)、NCM的CCK-8试剂盒(货号C6005)、Solarbio的纤连蛋白、I型胶原。
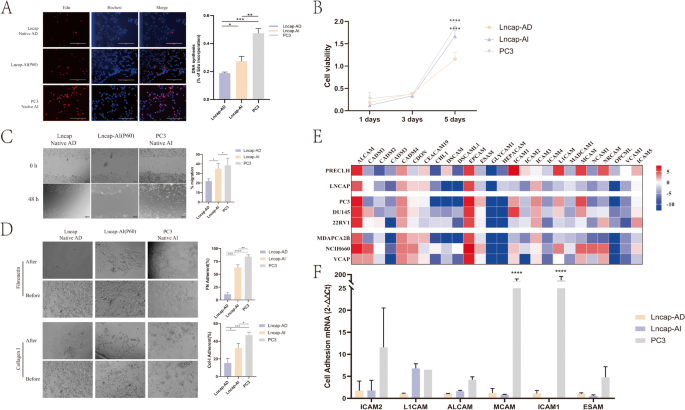
3.4 Lncap-AI细胞微观结构观察
该环节核心目标是从微观结构层面解析Lncap-AI细胞生物学特性变化的形态学基础。实验采用扫描电子显微镜(SEM)观察细胞膜表面形态,透射电子显微镜(TEM)观察细胞超微结构。结果显示,SEM下Lncap-AI细胞的细胞膜表面较Lncap-AD细胞粗糙,与PC3细胞相似;TEM下Lncap-AI细胞的伪足数量显著多于Lncap-AD细胞,接近PC3细胞的伪足数量,提示伪足数量增加可能是Lncap-AI细胞黏附、迁移能力增强的形态学基础。文献未提及具体实验产品,领域常规使用扫描电子显微镜、透射电子显微镜及配套的固定、脱水、包埋试剂。
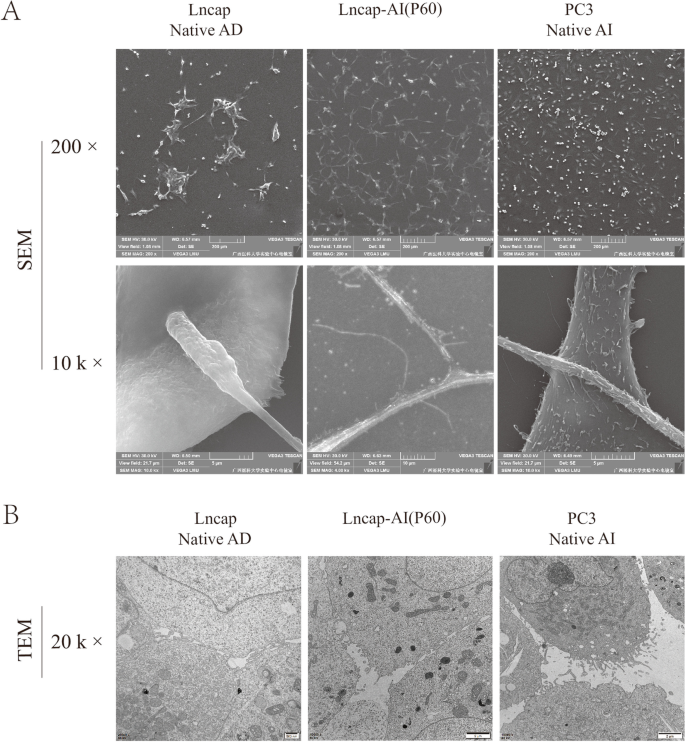
4. Biomarker研究及发现成果解析
本研究涉及的Biomarker包括AR、PSA及细胞黏附相关基因(MCAM、ICAM1、L1CAM、ALCAM),通过“数据库筛选-细胞模型验证-分子水平检测”的完整逻辑链条进行筛选与验证,明确了这些Biomarker与CRPC生物学特性的关联。
AR和PSA的样本来源为Lncap-AD、Lncap-AI及PC3细胞,AR通过实时荧光定量PCR检测mRNA表达、蛋白质免疫印迹检测蛋白表达,PSA通过蛋白质免疫印迹检测蛋白表达、酶联免疫吸附实验(ELISA)检测分泌水平;细胞黏附相关基因首先从KEGG数据库筛选26个细胞黏附通路基因,再通过CCLE数据库筛选Lncap与PC3细胞间的差异基因,最后用实时荧光定量PCR在Lncap-AD与Lncap-AI细胞中验证表达。特异性与敏感性方面,本研究未提供ROC曲线等相关数据。核心成果方面,AR在Lncap-AI细胞中呈现mRNA高表达、蛋白低表达的模式,且对AR抑制剂恩杂鲁胺不敏感,提示AR通路重构是Lncap-AD向Lncap-AI转化的核心机制之一;PSA在Lncap-AI细胞中的蛋白表达水平高于Lncap-AD细胞,但分泌水平无显著差异,说明Lncap-AI细胞仍保留PSA分泌功能;MCAM、ICAM1、L1CAM、ALCAM在Lncap-AI细胞中高表达,与细胞黏附、迁移能力增强直接相关,其中MCAM(P<0.001)、ICAM1(P<0.001)的差异具有统计学意义,这些基因可作为CRPC转移机制研究的潜在靶点。本研究的创新性在于,首次在ADT联合氟他胺诱导的Lncap-AI细胞系中系统解析了细胞黏附相关Biomarker的表达模式,为CRPC的转化研究提供了新的分子标志物。