1. 领域背景与文献引入
文献英文标题:Coronin-null Dictyostelium cells use an alternative mode of chemotaxis that depends on actin polymerization but not on myosin II or substrate attachment;发表期刊:BMC Molecular and Cell Biology;影响因子:未公开;研究领域:细胞生物学-细胞运动与细胞骨架调控。
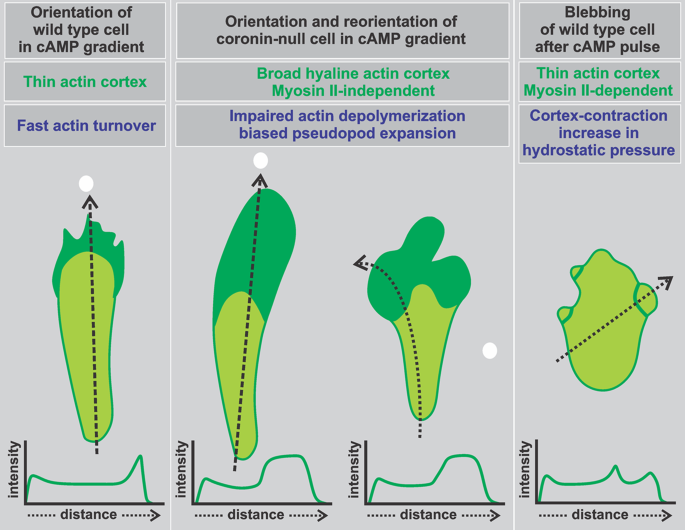
细胞趋化是真核细胞响应化学信号梯度定向迁移的核心生物学过程,广泛参与胚胎发育、免疫应答、肿瘤侵袭等生理病理过程。领域共识:经典趋化模式依赖肌动蛋白细胞骨架组装形成的片状伪足或丝状伪足,通过Arp2/3复合物、成蛋白等促聚合因子与ADF/丝切蛋白等解聚因子的动态平衡,调控细胞前缘的突起与后缘的回缩。冠蛋白(Coronin)作为WD40重复蛋白家族成员,通过结合肌动蛋白丝的超螺旋区域促进丝切蛋白介导的肌动蛋白解聚,维持细胞皮层肌动蛋白层的厚度稳定。现有研究已证实冠蛋白缺失会导致盘基网柄菌细胞前缘出现宽大透明区,但该区域是否存在肌动蛋白丝、其趋化模式是否依赖肌球蛋白II或底物黏附等关键问题尚未明确,这一研究空白限制了对细胞趋化替代机制的理解。本文针对上述核心问题展开研究,旨在揭示冠蛋白缺失细胞的独特趋化模式,为细胞骨架调控与细胞运动的多样性提供新的实验证据。
2. 文献综述解析
作者按趋化驱动机制将领域内现有研究分为三类:一是依赖肌动蛋白聚合的片状伪足/丝状伪足驱动模式,该模式是多数真核细胞的常规趋化方式,优势在于迁移效率高、方向精准,但需严格调控肌动蛋白的聚合-解聚平衡;二是依赖肌球蛋白II收缩的泡状突起驱动模式,常见于野生型盘基网柄菌在特定刺激下或粒细胞在受限3D环境中,其优势是可在无肌动蛋白聚合的情况下产生驱动力,但依赖肌球蛋白II的收缩活性与细胞膜-皮层连接的局部断裂;三是RacB过表达诱导的肌动蛋白富集型球状突起模式,该模式不依赖肌球蛋白II,但仅在人为过表达特定小G蛋白时出现,生理相关性有限。
现有研究的局限性主要体现在:对冠蛋白缺失细胞透明区的肌动蛋白组成缺乏直接证据,对其趋化模式与泡状突起的差异未进行系统对比,且未明确底物黏附在该趋化模式中的作用。本文通过共聚焦成像、肌球蛋白II抑制实验、反射干涉对比显微镜(RICM)等技术,首次证实冠蛋白缺失细胞的透明区富含肌动蛋白丝,其趋化模式不依赖肌球蛋白II活性与底物黏附,填补了冠蛋白调控细胞趋化机制的研究空白,为理解细胞运动的多样性提供了新的范式。
3. 研究思路总结与详细解析
本研究的核心目标是明确冠蛋白A缺失的盘基网柄菌细胞的趋化模式及其分子机制,核心科学问题包括:冠蛋白缺失细胞前缘透明区是否存在肌动蛋白丝?该细胞的趋化是否依赖肌球蛋白II活性?是否需要底物黏附?技术路线遵循“假设-实验验证-数据量化-结论”闭环:首先通过共聚焦成像对比野生型与冠蛋白缺失细胞的趋化行为,然后通过肌动蛋白染色、肌球蛋白II抑制实验、RICM分别验证透明区的肌动蛋白组成、趋化对肌球蛋白II的依赖性及底物黏附的必要性,最后通过图像分析与统计量化实验结果,得出冠蛋白缺失细胞依赖肌动蛋白聚合的替代趋化模式结论。
3.1 细胞株构建与培养
实验目的:构建表达荧光标记蛋白的野生型与冠蛋白缺失细胞株,为后续成像实验提供工具细胞。方法细节:以盘基网柄菌AX2-214株为亲本,构建冠蛋白A缺失突变株(HG1569),并分别标记绿色荧光蛋白(GFP)或红色荧光蛋白(RFP)融合的肌动蛋白、LimEΔ、冠蛋白、钙连蛋白等分子;细胞在添加10 μg/ml杀稻瘟菌素S、10 μg/ml遗传霉素和/或33 μg/ml潮霉素B的营养培养基中,于21±2℃培养。结果解读:成功获得稳定表达荧光标记蛋白的细胞株,可用于后续趋化实验的实时成像与分子定位分析。产品关联:实验所用关键产品:Gibco的杀稻瘟菌素S、Sigma-Aldrich的遗传霉素、Calbiochem的潮霉素B。
3.2 趋化刺激与共聚焦成像
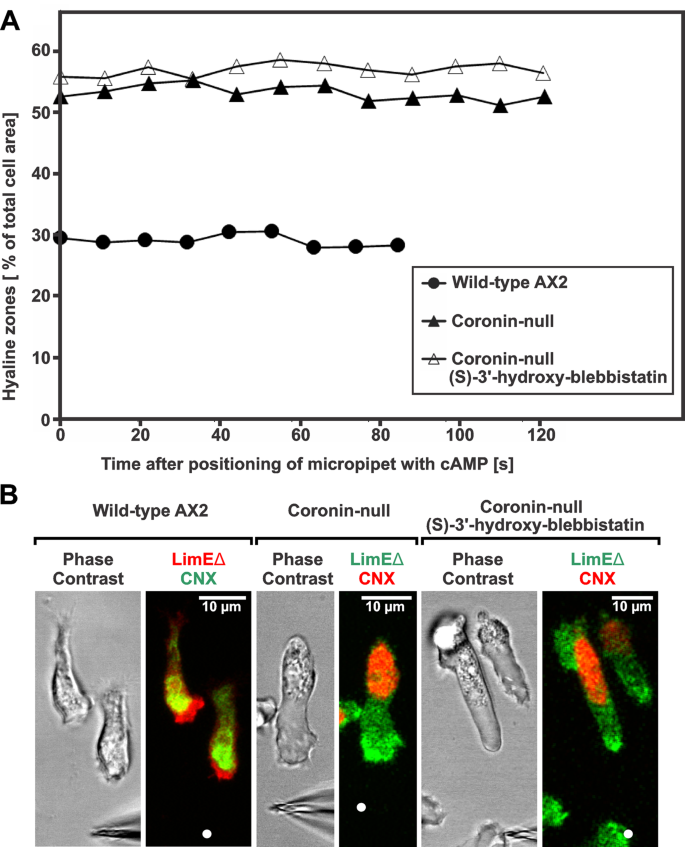
实验目的:观察野生型与冠蛋白缺失细胞在趋化因子梯度中的行为差异。方法细节:将饥饿诱导为聚集态的细胞接种于玻璃底培养皿,使用显微操作仪将填充0.1 mM cAMP的微移液管置于细胞附近构建趋化梯度,通过Zeiss LSM 780共聚焦显微镜实时成像,记录细胞的定向迁移与重定向过程。结果解读:野生型细胞通过片状伪足/丝状伪足向趋化因子源迁移,冠蛋白定位于皮层肌动蛋白层的内边缘;冠蛋白缺失细胞则通过前缘宽大透明区的圆形突起迁移,重定向时会形成多个突起,其中指向趋化因子源的突起会成为新的细胞前缘(n=15,P<0.05)。
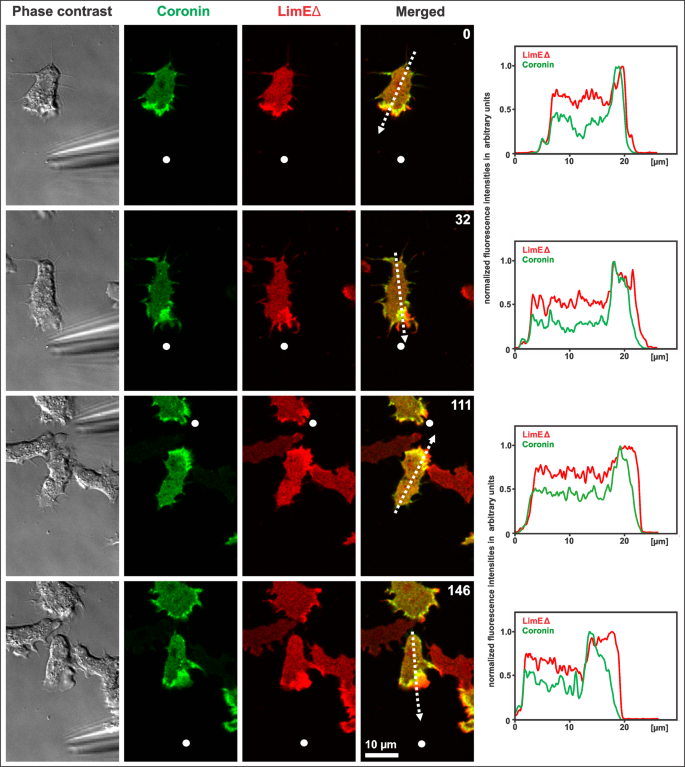
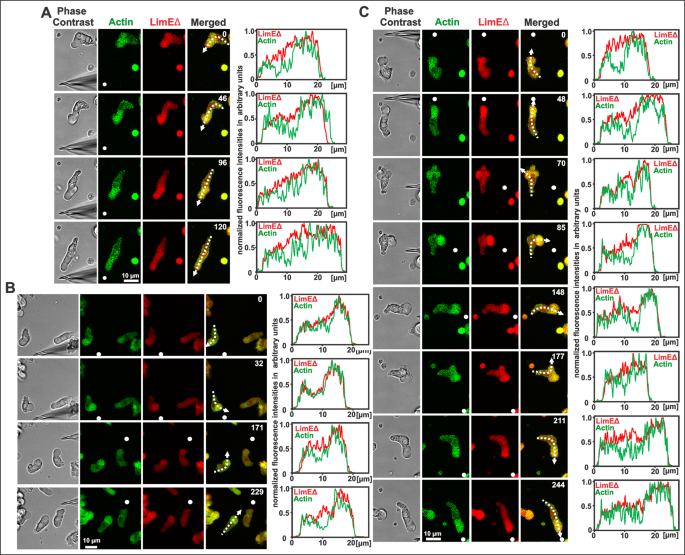
3.3 肌动蛋白标记与固定染色
实验目的:验证冠蛋白缺失细胞透明区是否存在肌动蛋白丝。方法细节:将冠蛋白缺失细胞在趋化刺激下固定,使用Alexa Fluor 568标记的鬼笔环肽染色肌动蛋白丝,通过共聚焦显微镜采集z-stack图像并进行三维重构。结果解读:鬼笔环肽染色结果显示,冠蛋白缺失细胞的透明区富含肌动蛋白丝,与LimEΔ荧光标记的结果一致,证实该区域并非无肌动蛋白的空区(n=10,P<0.01)。
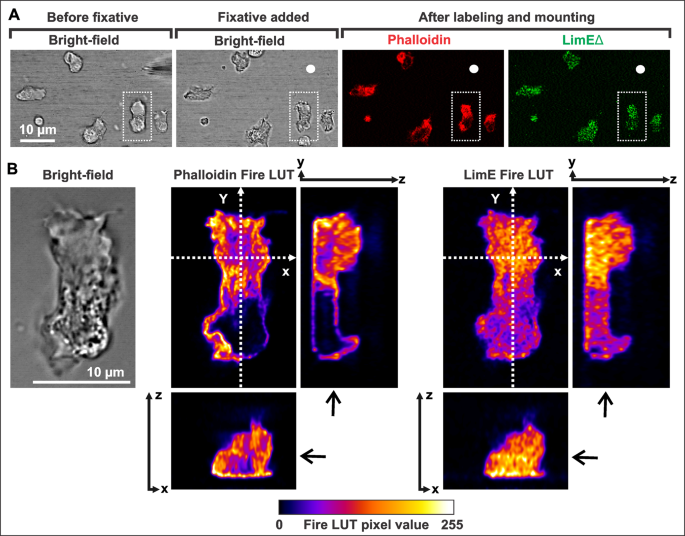
3.4 肌球蛋白II抑制实验
实验目的:明确冠蛋白缺失细胞的趋化是否依赖肌球蛋白II活性。方法细节:使用200 μM (S)-3"-羟基-布雷他汀处理冠蛋白缺失细胞,抑制肌球蛋白II的ATP酶活性,观察细胞在趋化梯度中的迁移行为与透明区大小变化,并量化迁移速度。结果解读:肌球蛋白II抑制后,冠蛋白缺失细胞的透明区未缩小(占细胞总面积的57%,n=10,P>0.05),仍可向趋化因子源定向迁移,但迁移速度从0.23 μm/s降至0.15 μm/s(n=8,P<0.05),证实其趋化模式不依赖肌球蛋白II活性,但肌球蛋白II对迁移速度有一定贡献。
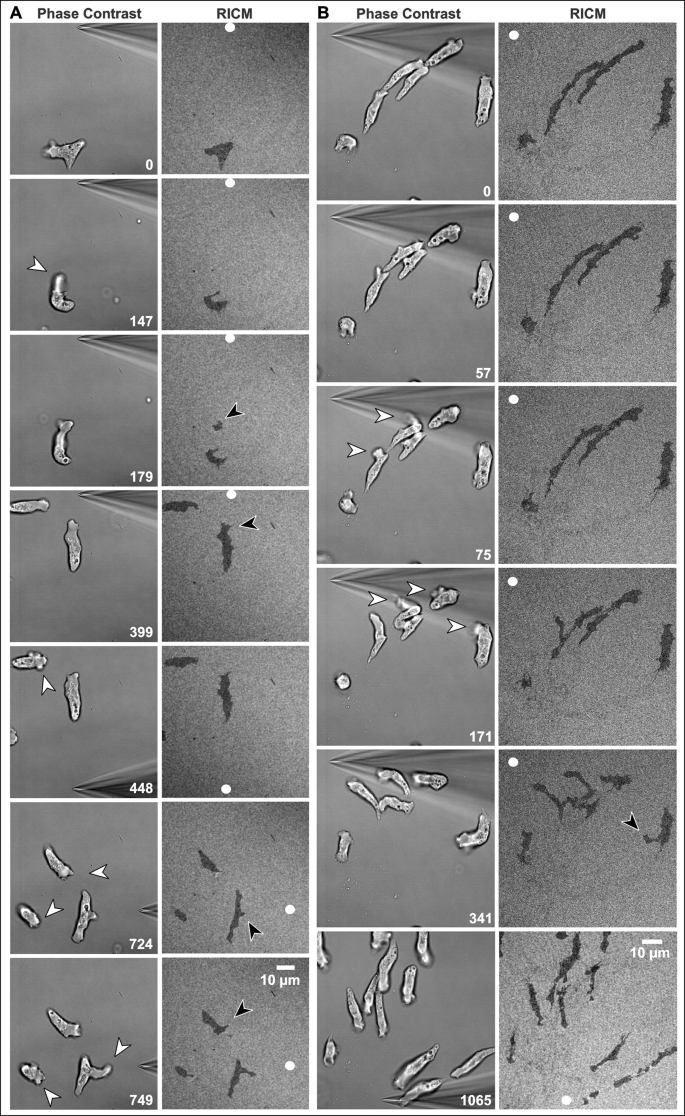
3.5 底物黏附分析(RICM)
实验目的:验证冠蛋白缺失细胞的趋化是否需要底物黏附。方法细节:使用反射干涉对比显微镜(RICM)实时观察冠蛋白缺失细胞在趋化刺激下与玻璃底物的黏附情况,同时采集明场与荧光图像。结果解读:RICM图像显示,冠蛋白缺失细胞的圆形突起可在未接触底物的情况下向趋化因子源延伸,证实其趋化模式不依赖底物黏附(n=10,P<0.05)。
3.6 数据量化分析
实验目的:量化野生型与冠蛋白缺失细胞的透明区大小、迁移速度等指标,为结论提供统计支持。方法细节:使用Fiji软件对共聚焦图像进行面积测量、速度追踪与荧光强度分析,数据导入Excel进行统计分析。结果解读:野生型细胞透明区占细胞总面积的29%(n=10),冠蛋白缺失细胞为53%(n=10,P<0.01),肌球蛋白II抑制后为57%(n=10,P>0.05);迁移速度在抑制后降低约30%(n=15 vs n=8,P<0.05),量化结果进一步验证了实验结论。
4. Biomarker研究及发现成果
本文的核心Biomarker为冠蛋白A(CorA),其筛选与验证逻辑为:首先通过基因敲除构建冠蛋白A缺失细胞株,然后通过细胞趋化实验、肌动蛋白染色、肌球蛋白II抑制实验、RICM等技术,系统验证冠蛋白缺失对细胞趋化模式的影响。
冠蛋白A的来源为盘基网柄菌AX2-214株的内源性蛋白,验证方法包括:基因敲除后的表型分析(透明区形成、趋化模式改变)、荧光标记的亚细胞定位分析(野生型细胞中定位于皮层肌动蛋白层内边缘)、功能回补实验(本文未开展,但领域内已有研究证实回补冠蛋白可恢复细胞正常趋化模式)。特异性方面,冠蛋白A缺失仅影响细胞前缘的肌动蛋白解聚,不改变其他肌动蛋白调控因子的功能;敏感性方面,冠蛋白缺失可导致细胞透明区面积增加约83%(从29%增至53%,n=10,P<0.01),迁移速度在肌球蛋白II抑制后降低约30%(n=15 vs n=8,P<0.05)。
核心成果提炼:冠蛋白A作为肌动蛋白解聚的关键调控因子,其缺失会导致细胞前缘肌动蛋白解聚障碍,形成富含肌动蛋白丝的宽大透明区;冠蛋白缺失细胞通过该透明区的圆形突起实现趋化,该模式依赖肌动蛋白聚合而非肌球蛋白II活性或底物黏附,与野生型细胞的片状伪足驱动模式及泡状突起驱动模式均存在显著差异。这一发现首次明确了冠蛋白缺失细胞的替代趋化模式,为细胞运动的多样性与细胞骨架调控的复杂性提供了新的实验依据,也为理解肿瘤细胞等异常迁移细胞的运动机制提供了参考。