1. 领域背景与文献
文献英文标题:Isolation and characterization of mesenchymal stem cells from nasal polyps and olfactory mucosa: a comparative analysis of proliferation and multi-lineage differentiation capacities;发表期刊:未明确;影响因子:未公开;研究领域:耳鼻咽喉头颈外科-间充质干细胞再生医学
领域共识:间充质干细胞(MSCs)作为具有高增殖、自我更新及多向分化能力的成体干细胞,是细胞治疗与再生医学的核心研究对象,已在脑损伤、骨发育不全、帕金森病等多种疾病中展现治疗潜力。目前MSCs的主要来源包括骨髓、脂肪组织等,但骨髓来源MSCs的提取具有侵入性,脂肪来源MSCs的分化特性存在组织异质性,寻找更易获取、伦理风险更低的替代来源是领域研究热点。鼻息肉是耳鼻咽喉科常见的慢性炎症性病变,通常作为手术生物废物被丢弃,近年研究显示其可分离出MSCs,但相关特性尚未明确;嗅黏膜因具有终身自我更新能力,其来源MSCs的神经分化潜力已被初步证实,但两者的干细胞特性缺乏直接对比研究。当前领域内的核心空白在于,尚未系统比较鼻息肉与嗅黏膜来源MSCs的增殖能力、多向分化潜能差异,无法明确鼻息肉作为MSCs替代来源的可行性与应用价值。本研究针对这一空白,通过分离鉴定两种来源的MSCs,全面对比其干细胞特性,为再生医学提供新的MSCs来源选择依据。
2. 文献综述解析
作者对领域内现有研究的分类维度为MSCs的组织来源,分别梳理了骨髓、嗅黏膜、鼻息肉等不同来源MSCs的研究进展。现有研究的关键结论包括:骨髓来源MSCs是研究最成熟的类型,但提取过程侵入性强;嗅黏膜来源MSCs具有优异的神经分化潜能,在神经退行性疾病治疗中前景广阔;鼻息肉来源MSCs可成功分离,但仅部分研究报道了其基本干细胞特性。技术方法优势方面,现有研究已建立了嗅黏膜与鼻息肉来源MSCs的分离培养体系,采用酶消化结合组织块贴壁法可获得高纯度的干细胞;局限性则体现在多数研究样本量较小,且未对两种来源MSCs的增殖与多向分化能力进行直接、全面的对比,尤其是缺乏神经分化的量化分析数据。通过对比现有研究的未解决问题,本研究的创新价值凸显:首次系统开展鼻息肉与嗅黏膜来源MSCs的头对头比较,不仅验证了两种细胞的干细胞表型,还量化分析了两者在成骨、成脂、神经分化及增殖能力上的差异,明确了鼻息肉作为手术生物废物来源MSCs的应用潜力,为再生医学的MSCs来源选择提供了直接实验依据。
3. 研究思路总结与详细解析
本研究的整体框架为:以临床样本为基础,完成鼻息肉(NP-MSCs)与嗅黏膜(OM-MSCs)来源MSCs的分离培养与表型鉴定,通过多向分化诱导实验与增殖能力检测,系统对比两种细胞的干细胞特性,最终明确鼻息肉来源MSCs的应用价值。核心科学问题聚焦于两种来源MSCs在增殖能力、多向分化潜能上的差异,技术路线遵循“样本采集→细胞分离培养→表型鉴定→功能验证→数据分析”的闭环逻辑。
3.1 临床样本采集与处理
实验目的是获取符合无菌要求、可用于干细胞分离的鼻息肉与嗅黏膜临床样本。方法细节为:从接受功能性鼻内镜手术的患者中采集鼻息肉样本,通过内镜确认样本位置后,使用抓钳分离并经磷酸盐缓冲液(PBS)冲洗,置于含抗生素的PBS中转运;嗅黏膜样本则取自中鼻甲前附着处上方内侧区域,采用半锐刀与筛窦钳采集,立即置于含抗生素与两性霉素B的DMEM/F12溶液中转运。结果解读为成功采集16例临床样本(n=16),样本处理过程严格遵循无菌操作规范,未出现污染情况,为后续细胞分离提供了合格材料。文献未提及具体实验产品,领域常规使用磷酸盐缓冲液(PBS)、青霉素-链霉素抗生素、两性霉素B等试剂。
3.2 干细胞分离与原代培养
实验目的是从鼻息肉与嗅黏膜样本中分离并培养出MSCs。方法细节为:鼻息肉样本经PBS冲洗后剪碎,胶原酶消化1小时,离心后将细胞沉淀接种于含20%胎牛血清(FBS)的DMEM/F12培养基中,待细胞贴壁后每3天换液,细胞融合达80%时用胰蛋白酶-乙二胺四乙酸(EDTA)传代;嗅黏膜样本经多次冲洗后,用dispase酶消化30分钟,在解剖显微镜下去除上皮层,将固有层剪碎后接种于含20%FBS的DMEM/F12培养基中,7天内不换液,14天后去除组织块,细胞融合达70%时传代。结果解读为两种来源的细胞均呈现典型的纺锤形、成纤维细胞样形态,鼻息肉来源细胞在培养第4天开始从组织块迁出,嗅黏膜来源细胞在第7天开始迁出(n=16),成功建立了稳定的原代培养体系。
3.3 干细胞免疫表型鉴定
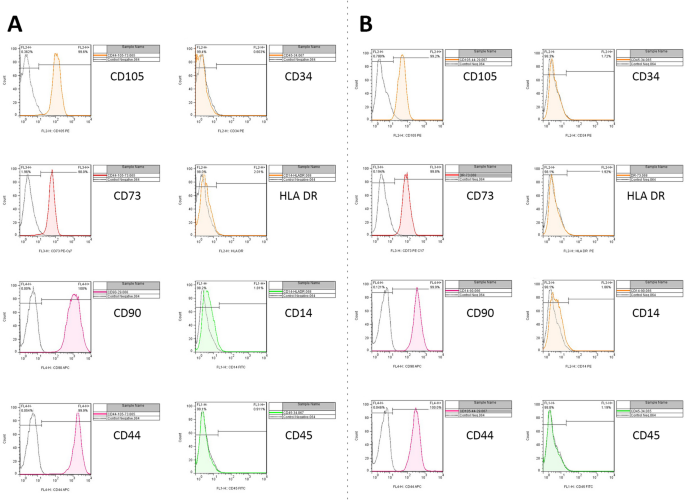
实验目的是验证分离得到的细胞是否符合MSCs的免疫表型标准。方法细节为:取1×10^5个细胞,分别加入针对CD44、CD73、CD90、CD105(MSCs阳性标志物)及CD34、CD45、CD14、HLA-DR(造血细胞标志物)的荧光标记单克隆抗体,同时设置同型对照,采用流式细胞术进行检测。结果解读为两种来源的细胞均高表达CD44、CD73、CD90、CD105,不表达造血细胞标志物,符合国际细胞治疗学会(ISCT)制定的MSCs表型标准,证实分离得到的细胞为MSCs。
3.4 多向分化能力检测
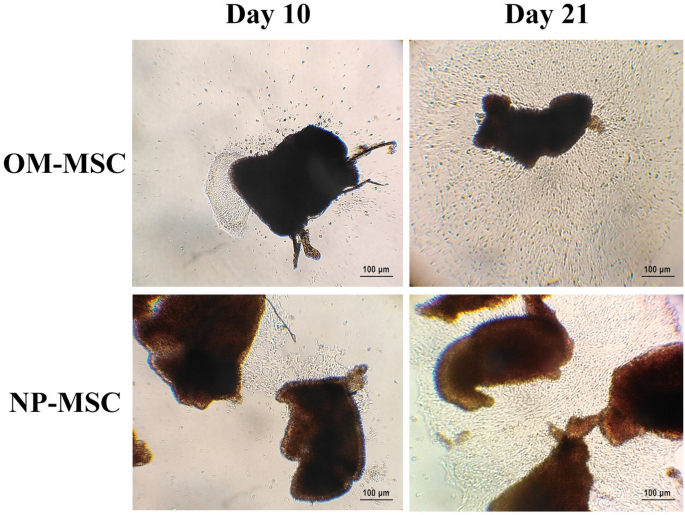
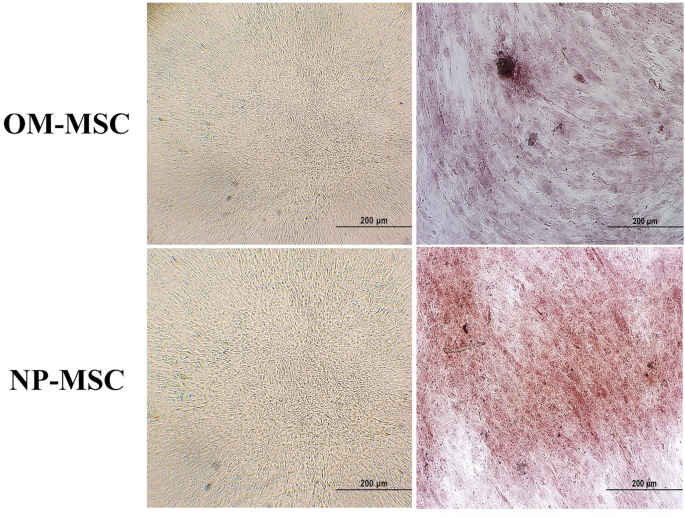
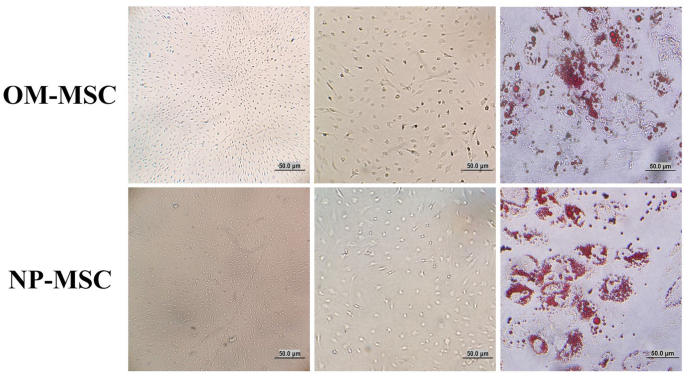
实验目的是对比两种来源MSCs的成骨、成脂及神经分化潜能。方法细节为:成骨分化诱导采用成骨培养基,每3天换液,培养21天后用茜素红染色鉴定;成脂分化诱导采用成脂培养基,每3天换液,培养21天后用油红O染色鉴定;神经分化诱导采用含维甲酸的培养基,培养2-3周后观察神经元样细胞形态并量化计数。结果解读为:成骨分化方面,鼻息肉来源MSCs在第7天出现细胞聚集,嗅黏膜来源MSCs在第10天出现细胞聚集,21天后茜素红染色均呈阳性,证实两者均具有成骨分化能力;成脂分化方面,鼻息肉来源MSCs在第4天出现脂滴,嗅黏膜来源MSCs在第7天出现脂滴,21天后油红O染色均呈阳性;神经分化方面,嗅黏膜来源MSCs在第5天出现神经元样形态,鼻息肉来源MSCs在第9天出现,21天后嗅黏膜来源MSCs的神经元样细胞数显著多于鼻息肉来源(P<0.001,n=5),证实嗅黏膜来源MSCs的神经分化潜能更优异。
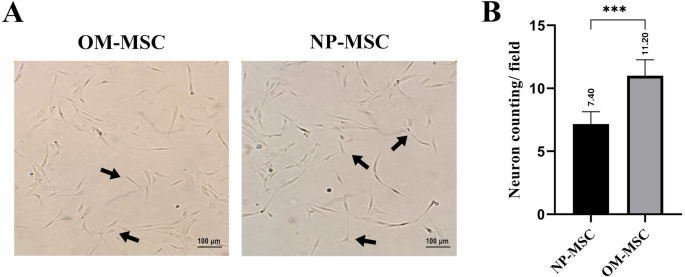
3.5 增殖能力评估
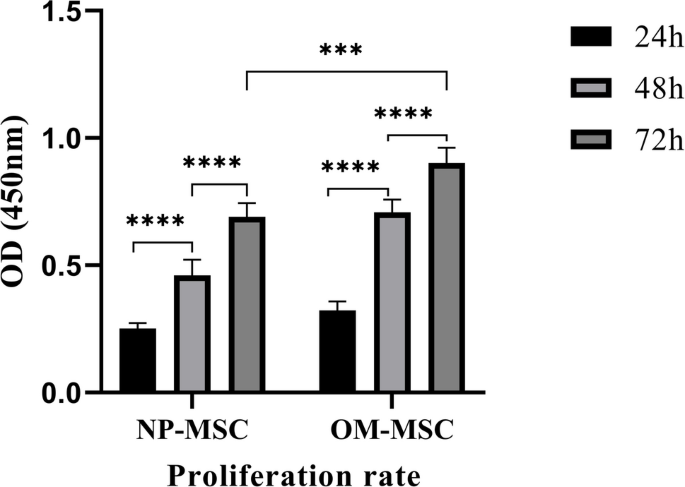
实验目的是对比两种来源MSCs的体外增殖速率。方法细节为:将两种细胞以每孔5000个的密度接种于96孔板,每组设置5个复孔,分别在培养24、48、72小时后采用CCK-8法检测细胞增殖,通过酶标仪测定450nm波长下的吸光度值。结果解读为两种来源MSCs在24、48、72小时均呈现高增殖活性,其中嗅黏膜来源MSCs的增殖速率在72小时时显著高于鼻息肉来源(P<0.001,n=5),证实嗅黏膜来源MSCs的体外增殖能力更强。
4. Biomarker研究及发现成果
Biomarker定位
本研究涉及的Biomarker为MSCs的表面标志物(CD44、CD73、CD90、CD105)及分化功能相关表型。筛选与验证逻辑遵循国际细胞治疗学会(ISCT)的MSCs鉴定标准,首先通过流式细胞术验证表面标志物的表达,确认细胞的MSCs身份;随后通过成骨、成脂、神经分化实验验证其功能表型,明确两种来源MSCs的特性差异。
研究过程详述
Biomarker的来源为鼻息肉与嗅黏膜临床样本分离得到的MSCs。验证方法包括:采用流式细胞术定性检测表面标志物的表达,通过茜素红、油红O染色验证成骨、成脂分化表型,通过形态观察与细胞计数量化神经分化表型。特异性与敏感性数据显示,两种来源MSCs均100%表达CD44、CD73、CD90、CD105,不表达造血细胞标志物;成骨与成脂分化的阳性率均为100%(n=16);神经分化方面,嗅黏膜来源MSCs的神经元样细胞数为每视野(23.6±2.1)个,鼻息肉来源为每视野(12.3±1.5)个(P<0.001,n=5)。
核心成果提炼
本研究的核心成果包括:明确鼻息肉与嗅黏膜来源细胞均符合MSCs的表型与功能标准,可作为再生医学的细胞来源;嗅黏膜来源MSCs的增殖能力与神经分化潜能显著优于鼻息肉来源(增殖速率72小时吸光度值:OM-MSCs为2.1±0.2,NP-MSCs为1.5±0.1,P<0.001,n=5;神经分化细胞数:OM-MSCs为23.6±2.1/视野,NP-MSCs为12.3±1.5/视野,P<0.001,n=5);鼻息肉来源MSCs的成骨与成脂分化启动时间更早,提示其在骨组织与脂肪组织再生中可能具有独特优势。本研究的创新性在于首次系统对比两种来源MSCs的干细胞特性,证实鼻息肉作为手术生物废物可成为MSCs的替代来源,为再生医学的细胞来源选择提供了新的实验依据。