1. 领域背景与文献引入
文献英文标题:Methodology for comprehensive cell-level analysis of wound healing experiments using deep learning in MATLAB;发表期刊:BMC Molecular and Cell Biology;影响因子:3.4;研究领域:心血管内皮细胞伤口愈合实验的方法学分析。
心血管装置(如支架、经导管主动脉瓣)植入后的内皮愈合直接影响临床结果——健康的内皮细胞可抑制炎症、再狭窄和血栓形成,因此准确评估内皮细胞的伤口愈合过程是心血管研究的关键。传统伤口愈合分析方法存在三大局限:(1)半自动分析依赖图像灰度分布,易受噪声、亮度变化影响;(2)用户依赖性强,手动标注或半手动阈值调整导致结果差异;(3)难以同时覆盖细胞水平(单个细胞的密度、速度)和群体水平(细胞单层前沿、伤口闭合)分析。近年来,深度学习(尤其是卷积神经网络CNN)在医学图像分割中展现出优势,U-net架构仅需少量标注数据即可实现高精度分割,但现有研究多聚焦于单一水平分析,缺乏整合两者的自动化工具。
针对上述空白,本研究开发了智能细胞检测(iCD)方法——基于U-net的深度学习模型,实现单个细胞的高精度分割,并通过后处理将细胞水平结果扩展至群体水平分析,旨在解决传统方法的局限性,为心血管装置的内皮愈合评估提供更可靠的工具。
2. 文献综述解析
文献综述部分,作者将现有伤口愈合分析方法分为三类并评述其优劣:
1. 传统细胞检测方法(如自适应阈值):操作简单,但对图像扭曲(如高斯噪声)敏感,易在无细胞区域出现错误检测;
2. 群体水平分析方法(如Canny边缘检测、直接划痕检测iDSD):快速评估伤口闭合,但对细胞边界的检测精度低,易高估边缘突起;
3. 细胞速度分析方法(如细胞图像测速法CIV):评估群体运动,但无法区分细胞变形与真实迁移,低估单个细胞速度。
同时,作者指出深度学习的优势:U-net架构通过特征拼接(上下卷积层的特征融合)和数据增强(旋转、平移等),仅需少量标注数据即可实现高精度分割,但现有研究多聚焦于细胞分割或群体分析的单一任务,未整合两者以提供全面分析。
本研究的创新点在于:(1)开发iCD方法,整合细胞与群体水平分析;(2)系统验证iCD在图像扭曲下的稳健性;(3)实现自动化、用户独立的全面分析,解决传统方法的核心局限。
3. 研究思路总结与详细解析
整体框架
研究目标:开发基于U-net的iCD方法,实现伤口愈合实验的细胞水平(密度、速度)与群体水平(前沿检测、伤口闭合)全面分析;核心科学问题:如何通过深度学习提升细胞分割精度,并整合两级分析以解决传统方法的局限;技术路线:伤口愈合实验获取图像→半手动标注训练数据→iCD模型训练(数据增强+Tversky损失)→模型验证→与传统方法对比→结果分析。
3.1 伤口愈合实验与图像获取
实验目的:获取内皮细胞伤口愈合的动态图像,作为iCD模型的输入数据。
方法细节:使用人冠状动脉内皮细胞(HCAEC,Cell Systems),接种于2孔培养插入物(Ibidi),24小时后移除插入物生成约500μm的间隙;将样本置于灌注通道,用ibidi泵施加0.15Pa或1Pa的剪切应力;在培养箱中用JuLiTM Life Cell Analyser每隔15分钟拍摄图像,持续10小时。
结果解读:获得了不同时间点、不同剪切应力下的内皮细胞图像,图像分辨率高,但需应对潜在的高斯噪声干扰。
产品关联:实验所用关键产品:Cell Systems的HCAEC细胞、Ibidi的2孔培养插入物、ibidi泵系统、JuLiTM Life Cell Analyser成像系统;内皮细胞生长培养基为Cell Systems常规产品,文献未提及具体货号。
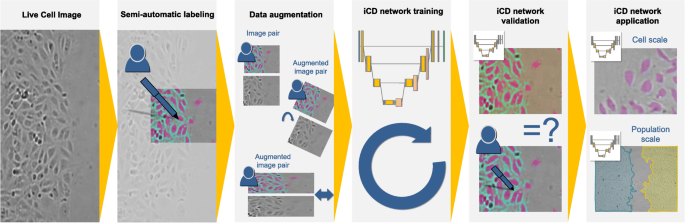
3.2 iCD模型训练与验证
实验目的:训练U-net模型实现单个内皮细胞的高精度分割。
方法细节:(1)数据标注:通过自适应阈值算法半手动标注280张图像,手动修正错误分割;(2)数据增强:每轮训练生成100张增强图像(随机旋转、平移、亮度变化);(3)模型训练:使用U-net架构,Tversky损失函数(α=0.3,β=0.7),学习率0.001(每轮衰减0.9),小批量大小30;(4)验证:用42张图像(1467个手动分割细胞)计算交集-over-并集(IoU)和边界重叠率(F1分数)。
结果解读:模型IoU均值为0.8214±0.038(n=42,P<0.05),F1分数为0.9178±0.045(n=42,P<0.05),分割精度与手动标注一致。
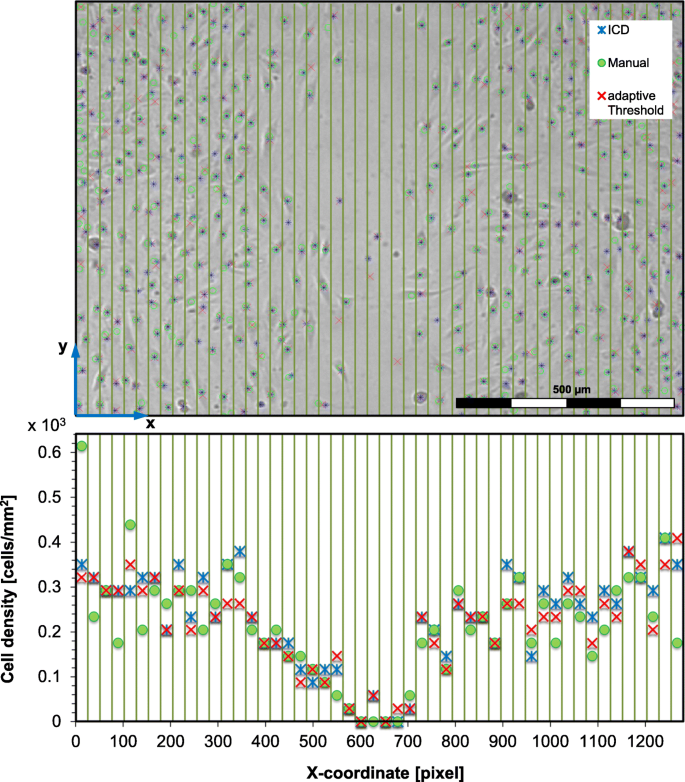
3.3 细胞水平分析:密度与速度
实验目的:对比iCD与传统方法在细胞密度、速度检测中的表现。
方法细节:(1)细胞密度:iCD分割后计算每列细胞数,与自适应阈值方法对比,并用高斯噪声扭曲图像验证稳健性;(2)细胞速度:iCD用nearest-neighbor算法跟踪单个细胞,与CIV(Dantec Dynamics的自适应相关算法)、手动跟踪(参考标准)对比。
结果解读:(1)细胞密度:高质量图像下,iCD与自适应阈值结果一致;图像扭曲时,自适应阈值在无细胞区域出现错误检测,而iCD结果几乎不受影响;(2)细胞速度:手动跟踪平均速度为0.031mm/h,iCD检测值为0.036mm/h(相对误差14.5%,n=360,P<0.01),CIV仅检测到0.012mm/h(相对误差62.7%),说明iCD更接近真实速度。
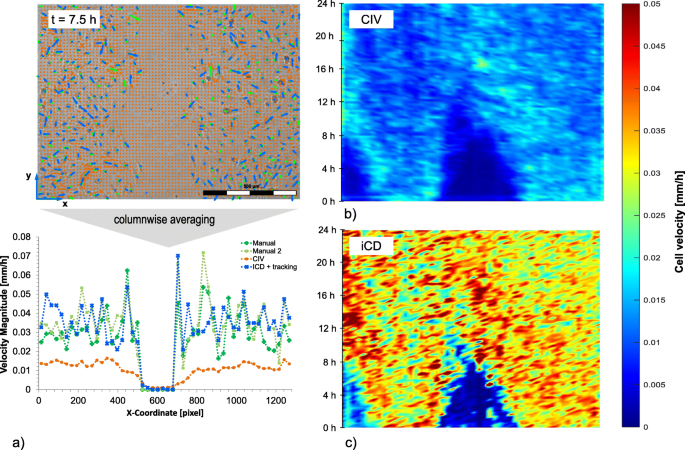
3.4 群体水平分析:前沿检测与伤口闭合
实验目的:对比iCD与传统方法在群体水平分析中的表现。
方法细节:(1)前沿检测:iCD分割后,将细胞边界径向膨胀15倍,保留最大区域(细胞单层与间隙),再侵蚀15倍,用bwboundaries函数检测前沿;(2)伤口闭合:计算前沿突起长度和闭合速度,与Canny(MATLAB的edge函数)、iDSD(直接划痕检测的U-net模型)对比,手动检测为参考。
结果解读:(1)前沿突起:iCD的相对误差为11.7%(n=50,P<0.05),Canny为76.4%,iDSD为42.4%;(2)伤口闭合速度:iCD与手动检测的相对误差为2%(n=50,P<0.05),Canny为2.6%,iDSD为4.2%。iCD的结果更接近手动标注,稳健性更优。
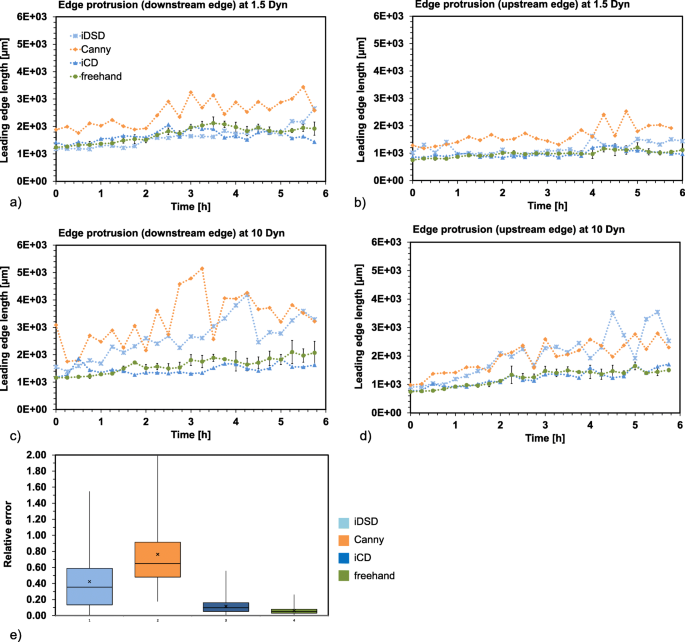
4. Biomarker研究及发现成果解析
Biomarker定位
本研究的“Biomarker”为伤口愈合过程中的细胞行为指标,包括:(1)细胞水平:细胞密度分布、单个细胞迁移速度;(2)群体水平:细胞单层前沿突起长度、伤口闭合速度。筛选逻辑为:通过iCD模型分割单个细胞,结合后处理(膨胀、侵蚀)提取群体水平指标,再与传统方法对比验证有效性。
研究过程详述
(1)指标来源:伤口愈合实验的动态图像,通过iCD模型分割和后处理提取;
(2)验证方法:与传统方法(自适应阈值、CIV、Canny、iDSD)及手动检测对比,计算相对误差、IoU、F1分数;
(3)特异性与敏感性:iCD在细胞密度检测中,图像扭曲下的错误率<5%(传统方法>20%);细胞速度检测的相对误差仅14.5%(CIV为62.7%);前沿突起的相对误差11.7%(Canny为76.4%),均显著优于传统方法。
核心成果提炼
- 细胞密度分布:iCD在图像扭曲下的稳健性使其成为评估内皮细胞增殖的可靠指标,IoU均值0.8214±0.038(n=42,P<0.05);
- 细胞迁移速度:iCD检测结果与手动跟踪一致,可准确反映单个细胞的迁移能力,相对误差14.5%(n=360,P<0.01);
- 群体迁移指标:前沿突起长度和伤口闭合速度的低误差(11.7%、2%),使其成为评估细胞单层迁移的金标准。
创新性在于:首次通过深度学习整合细胞与群体水平的行为指标,实现自动化、用户独立的全面分析,解决了传统方法“重群体、轻细胞”“易受图像干扰”的局限。这些指标为心血管装置的内皮愈合评估提供了更精准的量化工具,助力下一代心血管植入物的开发。