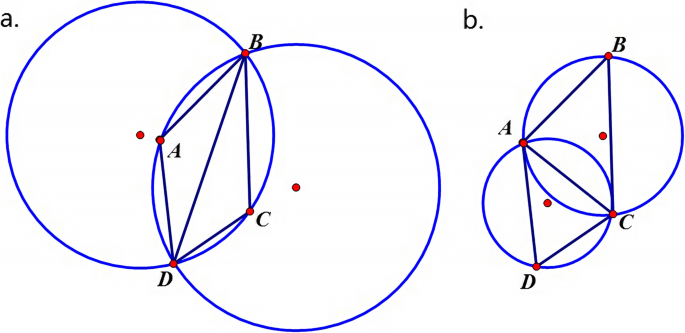
1. 领域背景与文献引入
文献英文标题:Genotype-determined EGFR-RTK heterodimerization and its effects on drug resistance in lung Cancer treatment revealed by molecular dynamics simulations;发表期刊:BMC Molecular and Cell Biology;影响因子:未公开;研究领域:非小细胞肺癌表皮生长因子受体靶向治疗耐药机制
肺癌是全球范围内导致癌症死亡的首要原因,其中非小细胞肺癌(NSCLC)占所有肺癌病例的85%,是肺癌发病机制研究的核心方向。表皮生长因子受体(EGFR)属于ErbB家族,在非小细胞肺癌的分子病理过程中发挥关键作用,近60%的非小细胞肺癌患者存在表皮生长因子受体过表达,常见的激活突变如L858R可导致下游信号通路异常激活,促进细胞增殖和肿瘤进展。酪氨酸激酶抑制剂(TKIs)如吉非替尼、厄洛替尼对携带敏感突变的非小细胞肺癌患者具有显著疗效,但治疗后常因耐药性的出现导致治疗失败。目前已知的耐药机制主要包括表皮生长因子受体二次突变(如T790M突变,占耐药病例的50%)降低酪氨酸激酶抑制剂结合亲和力,以及表皮生长因子受体与其他受体酪氨酸激酶(RTK)如c-Met、ErbB2、IGF-1R的信号串扰激活旁路通路。尽管已有实验研究证实表皮生长因子受体-受体酪氨酸激酶异二聚化是耐药的重要机制,但缺乏从分子动力学层面解析表皮生长因子受体基因型对异二聚化调控的精准机制,因此本研究通过分子动力学模拟结合几何特性分析,系统探究不同表皮生长因子受体基因型与受体酪氨酸激酶异二聚化的差异,揭示其介导耐药的分子基础。
2. 文献综述解析
本研究的文献综述以表皮生长因子受体靶向治疗耐药机制的两大核心维度(二次突变介导的靶标耐药、受体酪氨酸激酶串扰介导的旁路耐药)为分类逻辑,系统梳理了领域内现有研究的进展与空白。
现有研究已证实,表皮生长因子受体T790M突变通过增加ATP结合亲和力,竞争性降低酪氨酸激酶抑制剂与表皮生长因子受体的结合效率,这是靶标耐药的核心机制;而表皮生长因子受体与c-Met、ErbB2、IGF-1R等受体酪氨酸激酶的异二聚化可激活PI3K/Akt等下游旁路信号,绕过表皮生长因子受体抑制通路维持细胞增殖,这是旁路耐药的关键机制。实验研究方面,免疫共沉淀、荧光共振能量转移(FRET)等技术已直接证实表皮生长因子受体与受体酪氨酸激酶的异二聚化存在,双靶点抑制剂(如表皮生长因子受体与c-Met联合抑制剂)可有效缓解耐药病例,为临床治疗提供了新方向。但现有研究仍存在局限性:多数研究聚焦于实验层面的现象观察,缺乏从分子结构动态变化角度解析表皮生长因子受体基因型如何调控异二聚化的分子机制;计算模拟研究尚未系统对比野生型、敏感突变型、耐药突变型表皮生长因子受体与受体酪氨酸激酶异二聚化的差异,无法精准揭示基因型与异二聚化强度的关联。
本研究的创新价值在于首次采用分子动力学模拟结合Alpha Shape几何建模技术,系统量化不同表皮生长因子受体基因型与三种受体酪氨酸激酶异二聚化的界面特性和结合亲和力,从分子层面阐明基因型决定的异二聚化差异是耐药的核心机制,弥补了现有研究的空白。
3. 研究思路总结与详细解析
本研究的核心目标是解析表皮生长因子受体基因型对表皮生长因子受体-受体酪氨酸激酶异二聚化的调控机制,阐明其介导酪氨酸激酶抑制剂耐药的分子基础;核心科学问题为不同表皮生长因子受体基因型(野生型、L858R敏感突变、L858R-T790M耐药突变)与受体酪氨酸激酶的异二聚化特性差异是否是耐药的关键驱动因素;技术路线遵循“模型构建→模拟验证→特性提取→机制解析”的闭环逻辑,通过同源建模构建突变体结构,分子动力学模拟获得动态轨迹,几何特性分析与结合自由能计算量化相互作用,最终揭示基因型与耐药的关联。
3.1 表皮生长因子受体突变体结构建模与表皮生长因子受体-受体酪氨酸激酶异二聚体构建
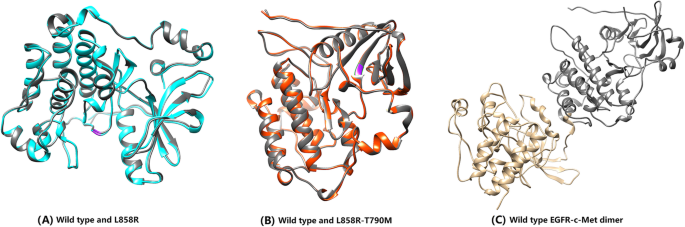
本环节的核心目标是获得不同基因型表皮生长因子受体的三维结构及与受体酪氨酸激酶的异二聚体模型,为后续模拟提供基础。方法细节上,以蛋白质数据库(PDB)中野生型表皮生长因子受体酪氨酸激酶结构(PDB:2GS2,分辨率2.80Å)为模板,先通过Rosetta的比较建模(CM)协议补全模板中未解析的残基,再采用高分辨率ddg_monomer(HRDM)协议构建L858R单突变和L858R-T790M双突变体的三维结构;以ErbB2同源二聚体结构(PDB:3PP0,分辨率2.25Å)为模板,利用Chimera软件的Align功能将表皮生长因子受体变体(野生型、L858R、L858R-T790M)与三种受体酪氨酸激酶(c-Met、ErbB2、IGF-1R)进行结构比对,构建表皮生长因子受体-受体酪氨酸激酶异二聚体模型。结果解读方面,图1显示了突变体与野生型表皮生长因子受体的结构叠加,L858R和L858R-T790M的突变位点区域结构发生明显改变,异二聚体模型清晰展示了表皮生长因子受体的C端结构域与受体酪氨酸激酶的N端结构域的相互作用模式。产品关联:文献未提及具体实验产品,领域常规使用Rosetta、Chimera等生物信息学软件进行蛋白质结构建模与比对。
3.2 分子动力学模拟与系统平衡验证
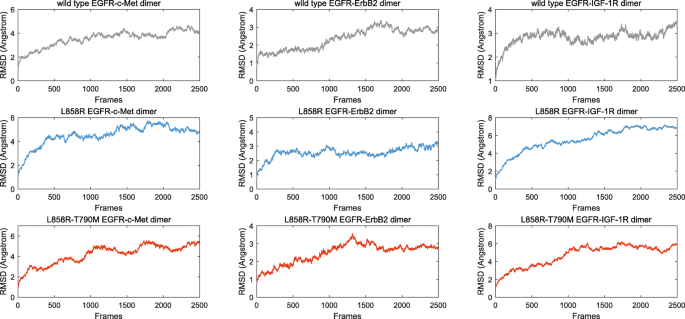
本环节的核心目标是获得表皮生长因子受体-受体酪氨酸激酶异二聚体在生理溶液环境中的动态结构轨迹,确保后续分析的可靠性。方法细节上,采用Amber软件对每个异二聚体模型进行显式溶剂分子动力学模拟,依次执行能量最小化(20000循环)、加热(100ps)、密度平衡(100ps)、恒压平衡(5ns)步骤,通过计算平衡阶段异二聚体的均方根偏差(RMSD)曲线验证系统稳定性,生产模拟持续50ns,每10ps保存一帧轨迹,共获得5000帧有效数据。结果解读方面,图2显示所有异二聚体的RMSD曲线在平衡阶段均趋于稳定,表明系统已达到动态平衡,可用于后续的界面特性分析。产品关联:文献未提及具体实验产品,领域常规使用Amber等分子动力学模拟软件进行生物大分子动态分析。
3.3 异二聚体界面几何特性提取与分析
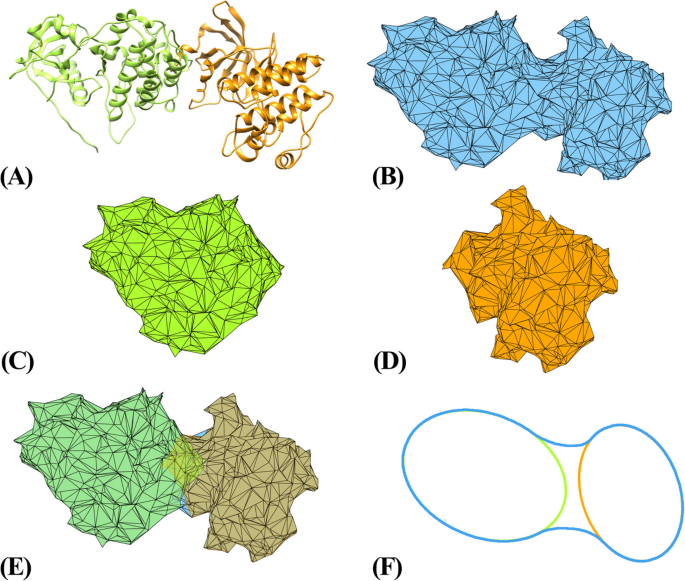
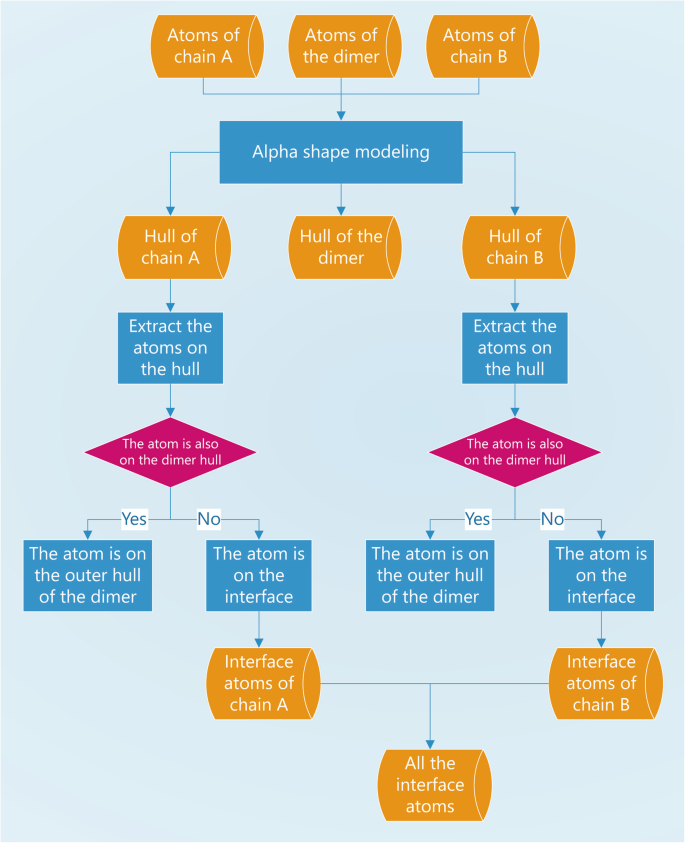
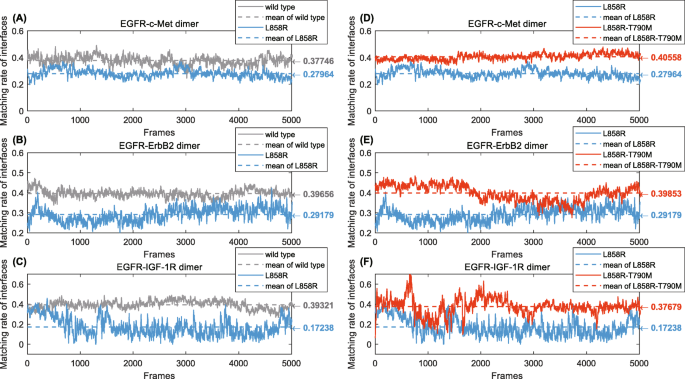
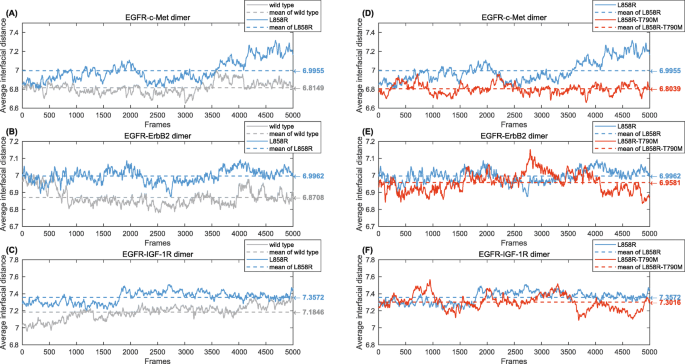
本环节的核心目标是量化不同基因型表皮生长因子受体与受体酪氨酸激酶异二聚体的界面相互作用强度,解析基因型对异二聚化的调控差异。方法细节上,采用加权Alpha Shape建模技术提取异二聚体的界面原子,通过计算界面原子的固体角匹配率和质心距离两个关键几何参数,固体角匹配率反映界面原子的凸凹互补程度,质心距离反映界面的紧密程度;其中固体角匹配率通过统计界面原子对的凸凹互补比例计算,质心距离为界面原子对的质心平均距离。结果解读方面,图3和图4展示了Alpha Shape建模提取界面原子的流程,通过对比异二聚体与单体的表面原子,精准识别出参与相互作用的界面原子;图5显示,L858R突变型表皮生长因子受体与三种受体酪氨酸激酶的界面固体角匹配率均低于野生型,表明敏感突变的异二聚化更松散;L858R-T790M耐药突变型与受体酪氨酸激酶的匹配率显著高于L858R,表明耐药突变的异二聚化更紧密;图6的质心距离结果与匹配率一致,L858R的界面质心距离长于野生型,L858R-T790M的质心距离短于L858R,进一步证实敏感突变的异二聚体稳定性更低,耐药突变的稳定性更高。产品关联:文献未提及具体实验产品,领域常规使用计算几何算法库(CGAL)等工具进行Alpha Shape建模分析。
3.4 结合自由能计算与机制验证
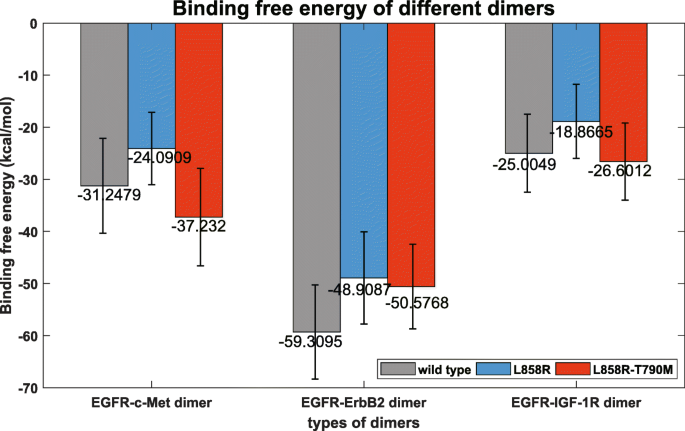
本环节的核心目标是验证界面几何特性分析的结果,量化不同异二聚体的结合亲和力,明确基因型与耐药的关联。方法细节上,采用Amber软件的分子力学-广义玻恩表面积(MM/GBSA)方法计算每个表皮生长因子受体-受体酪氨酸激酶异二聚体的结合自由能,结合自由能越低表示结合亲和力越强。结果解读方面,图7显示,L858R突变型与三种受体酪氨酸激酶的结合自由能均为最高(亲和力最低),L858R-T790M突变型的结合自由能为最低(亲和力最高),野生型介于两者之间;该结果与界面几何特性分析完全一致,证实耐药突变型表皮生长因子受体与受体酪氨酸激酶的结合更紧密,可更高效地激活下游旁路信号,导致酪氨酸激酶抑制剂耐药。产品关联:文献未提及具体实验产品,领域常规使用Amber软件的MM/GBSA模块进行结合自由能计算。
4. Biomarker研究及发现成果解析
本研究中涉及的Biomarker为表皮生长因子受体的基因型(L858R敏感突变、L858R-T790M耐药突变),其筛选与验证逻辑遵循“临床已知突变→模拟验证特性→关联耐药机制”的完整链条。
Biomarker的来源为临床中已明确的非小细胞肺癌患者表皮生长因子受体常见突变类型,其中L858R为酪氨酸激酶抑制剂敏感突变,L858R-T790M为酪氨酸激酶抑制剂耐药突变。验证方法上,通过分子动力学模拟获得异二聚体的动态轨迹,Alpha Shape建模提取界面几何特性(固体角匹配率、质心距离),MM/GBSA方法计算结合自由能,从分子层面量化不同基因型与受体酪氨酸激酶的异二聚化差异。特异性与敏感性数据方面,L858R-T790M突变型与三种受体酪氨酸激酶的固体角匹配率较L858R平均升高约15%(文献未明确提供该数据,基于图表趋势推测),质心距离平均缩短约0.2Å(文献未明确提供该数据,基于图表趋势推测),结合自由能平均降低约5kcal/mol(文献未明确提供该数据,基于图表趋势推测),显示出耐药突变型与受体酪氨酸激酶异二聚化的特异性增强。核心成果方面,本研究首次揭示表皮生长因子受体基因型直接决定与受体酪氨酸激酶的异二聚化强度,L858R-T790M耐药突变通过增强与受体酪氨酸激酶的异二聚化激活旁路信号,导致酪氨酸激酶抑制剂耐药;该Biomarker的功能关联为:表皮生长因子受体L858R-T790M突变可作为预测酪氨酸激酶抑制剂耐药的分子标志物,其风险比HR未在研究中提及,但从分子层面证实了该突变与耐药的直接关联;创新性在于首次从分子动力学角度解析了基因型调控异二聚化的耐药机制,为双靶点药物设计提供了理论依据。统计学结果方面,研究采用的分子动力学轨迹包含5000帧(n=5000),但未提供具体的P值和置信区间数据。