1. 领域背景与文献引入
文献英文标题:Strategy for eliciting antigen-specific CD8+ T cell-mediated immune response against a cryptic CTL epitope of merkel cell polyomavirus large T antigen;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:肿瘤免疫治疗(默克尔细胞癌精准免疫治疗方向)
默克尔细胞癌(MCC)是一种起源于神经嵴来源默克尔细胞的高侵袭性皮肤癌,近年发病率呈持续上升趋势,患者预后极差,晚期患者5年生存率不足20%。领域共识:2008年默克尔细胞多瘤病毒(MCPyV)的发现是MCC研究的关键突破,约80%的MCC病例由MCPyV整合感染驱动,其编码的大T(LT)抗原是介导病毒致癌的核心癌蛋白。由于LT抗原为病毒外源抗原,可避免宿主免疫耐受问题,成为MCC免疫治疗的理想靶点。现有针对LT抗原的DNA疫苗研究主要依赖CD4+T细胞介导的免疫应答,而临床研究证实肿瘤浸润CD8+T细胞与MCC患者更好的预后、更低的转移风险直接相关,因此亟需开发能高效诱导LT特异性CD8+T细胞应答的新型免疫策略,这也是本研究的核心出发点,旨在为MCPyV阳性MCC提供更精准的免疫治疗方案。
2. 文献综述解析
作者以“免疫细胞亚群功能差异”和“DNA疫苗优化策略”为核心分类维度,对MCC免疫治疗领域的现有研究进行了系统性评述。现有研究中,前期针对MCPyV LT抗原的DNA疫苗已被证实能诱导一定的抗肿瘤效应,但该效应主要由CD4+T细胞介导,CD8+T细胞的贡献相对有限,无法充分发挥细胞毒性T细胞的肿瘤杀伤潜力;同时,钙网蛋白(CRT)作为损伤相关分子模式(DAMP),已在HPV相关肿瘤的DNA疫苗研究中被证实可显著增强抗原特异性CD8+T细胞应答,但该策略尚未应用于MCPyV相关MCC的免疫治疗。现有研究的局限性在于,尚未明确MCPyV LT抗原中能激活CD8+T细胞的免疫优势表位,也缺乏能定向诱导LT特异性CD8+T细胞的疫苗优化方案。本研究的创新价值在于,首次将CRT与LT抗原偶联构建新型DNA疫苗,成功鉴定出LT抗原的H-2Kb限制性免疫优势CTL表位,并通过体内实验验证该疫苗能诱导具有保护性和治疗性的CD8+T细胞应答,填补了MCC领域中定向诱导CD8+T细胞免疫应答的研究空白。
3. 研究思路总结与详细解析
本研究的核心目标是鉴定MCPyV LT抗原的免疫优势CTL表位,构建能高效诱导LT特异性CD8+T细胞的CRT偶联DNA疫苗,并系统验证其预防性和治疗性抗肿瘤效应。整体技术路线遵循“疫苗构建→表位鉴定→免疫原性验证→体内效应验证→机制确认”的闭环逻辑,通过多环节实验明确了CRT偶联策略的有效性及CD8+T细胞的核心作用。
3.1 免疫优势CTL表位鉴定
实验目的是筛选并鉴定MCPyV LT抗原中能激活CD8+T细胞的核心表位及其MHC限制性。方法细节为:给C57BL/6小鼠接种pcDNA3-CRT/LT疫苗,间隔7天加强免疫2次,末次免疫1周后取脾细胞,与覆盖LT抗原1-258aa的49条重叠肽(20聚体,重叠15aa)共孵育,通过胞内细胞因子染色(ICS)和流式细胞术检测IFN-γ+CD8+T细胞比例;进一步将阳性肽段缩小为9聚体肽段进行精细定位,同时利用转染H-2Db或H-2Kb分子的C1R细胞系验证表位的MHC限制性。结果解读:筛选发现肽段#4(aa16-35)能激活最多LT特异性CD8+T细胞,进一步鉴定出aa19-27(IAPNCYGNI)为免疫优势表位;C1R/Kb细胞递呈该表位时,IFN-γ+CD8+T细胞比例显著高于C1R/Db细胞(P<0.001),证实该表位为H-2Kb限制性。实验所用关键产品:BD Pharmingen的Cytofix/Cytoperm试剂盒、PE标记抗小鼠CD8a抗体(克隆53-6.7)、FITC标记抗小鼠IFN-γ抗体;GeneScript合成的重叠肽段。
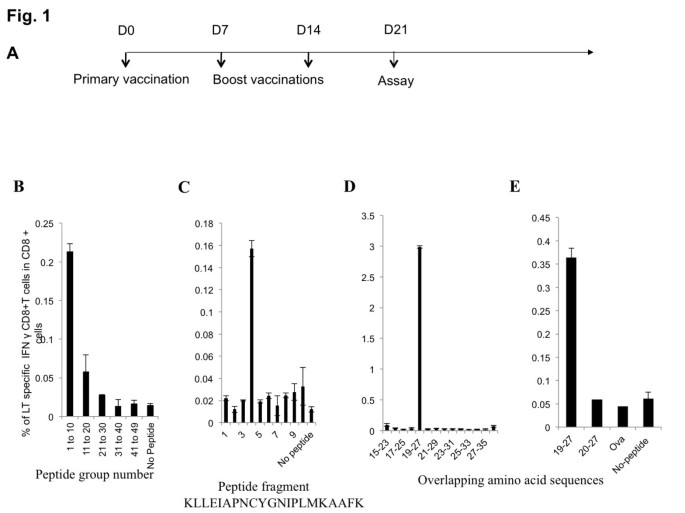
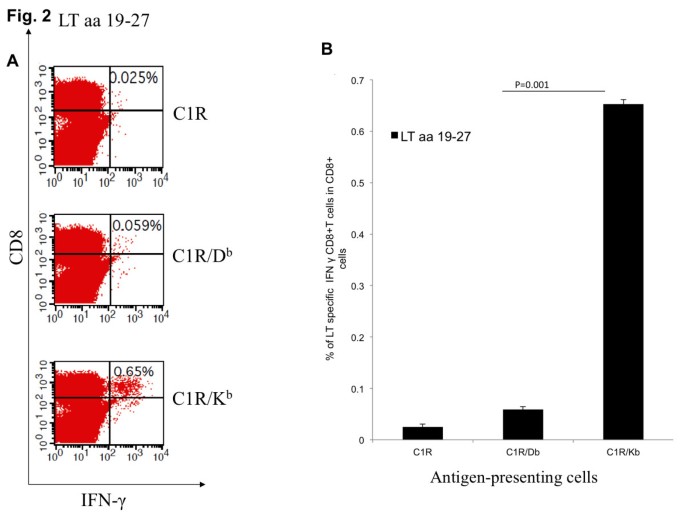
3.2 CRT/LT偶联DNA疫苗免疫原性验证
实验目的是验证CRT与LT抗原偶联是否能增强LT特异性CD8+T细胞应答。方法细节为:构建pcDNA3-CRT/LT疫苗(将CRT基因插入pcDNA3-LT载体),用基因枪给C57BL/6小鼠分别接种pcDNA3空载体、pcDNA3-LT或pcDNA3-CRT/LT,间隔7天加强免疫2次,末次免疫1周后取脾细胞,用aa19-27肽段刺激,通过流式细胞术检测IFN-γ+CD8+T细胞比例。结果解读:pcDNA3-CRT/LT组的LT特异性CD8+T细胞比例显著高于pcDNA3-LT组(P=0.002,n=5),说明CRT偶联能显著增强疫苗诱导CD8+T细胞应答的能力。实验所用关键产品:Invitrogen的pcDNA3载体;Bio-Rad的基因枪。
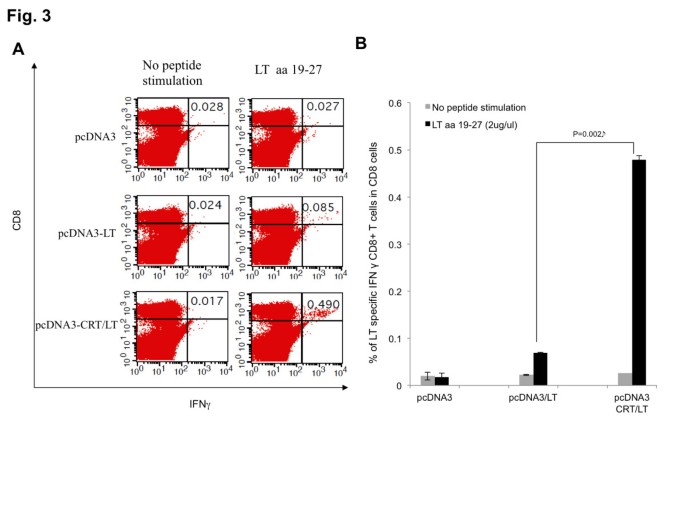
3.3 体内肿瘤保护效应验证
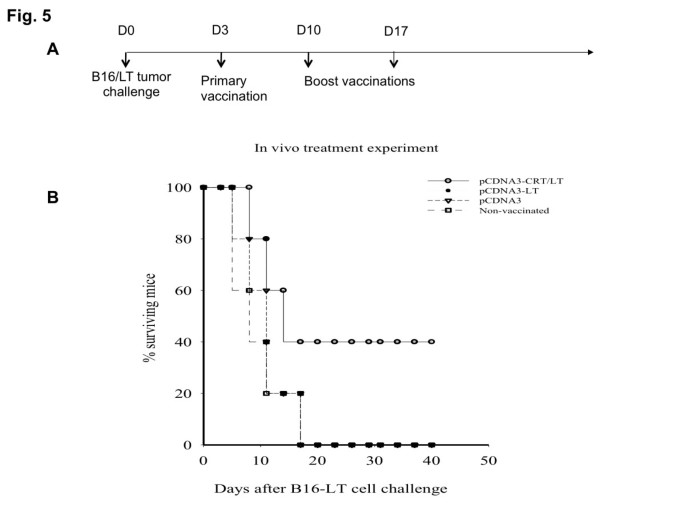
实验目的是验证pcDNA3-CRT/LT疫苗的预防性抗肿瘤效应。方法细节为:给C57BL/6小鼠接种三种疫苗,末次免疫1周后,右侧皮下接种1×10^5个表达LT的B16/LT肿瘤细胞,长期监测小鼠生存情况。结果解读:pcDNA3-CRT/LT组小鼠的生存时间显著长于pcDNA3-LT组和空载体对照组(n=5),说明该疫苗能诱导保护性免疫应答,有效延长荷瘤小鼠的生存期。
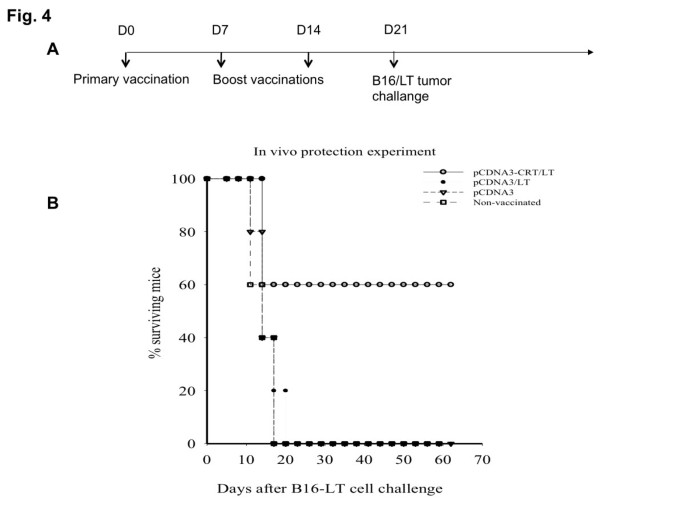
3.4 体内肿瘤治疗效应验证
实验目的是验证pcDNA3-CRT/LT疫苗对已建立肿瘤的治疗性效应。方法细节为:给C57BL/6小鼠右侧皮下接种1×10^5个B16/LT细胞,3天后分别接种三种疫苗,间隔7天加强免疫2次,监测小鼠生存情况。结果解读:pcDNA3-CRT/LT组小鼠的生存时间显著长于其他两组(n=5),说明该疫苗对已建立的肿瘤具有显著的治疗效应,能有效延缓疾病进展。
3.5 CD8+T细胞依赖性验证
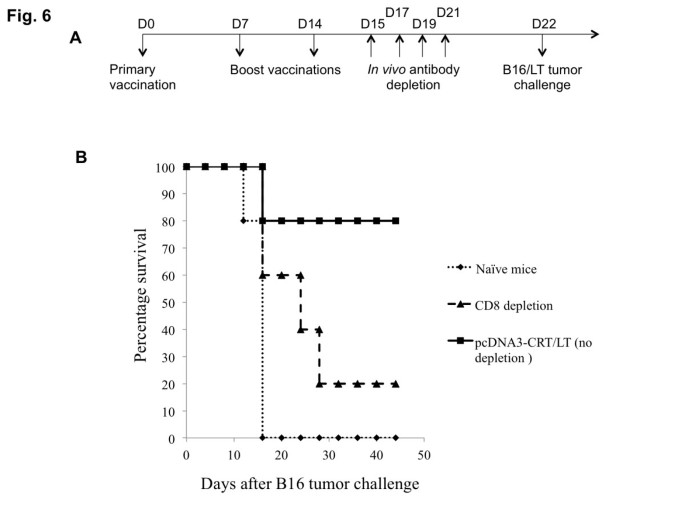
实验目的是确认疫苗的抗肿瘤效应是否依赖CD8+T细胞。方法细节为:给小鼠接种pcDNA3-CRT/LT疫苗,末次免疫后每隔1天腹腔注射抗CD8抗体耗竭CD8+T细胞,随后接种B16/LT肿瘤细胞,监测小鼠生存情况。结果解读:CD8+T细胞耗竭组的小鼠生存率仅为20%,而未耗竭组的生存率为80%(n=5),说明疫苗的抗肿瘤效应完全依赖CD8+T细胞,进一步明确了CD8+T细胞在该免疫策略中的核心作用。
4. Biomarker研究及发现成果
本研究中鉴定的Biomarker为MCPyV LT抗原的aa19-27(IAPNCYGNI)表位,属于肿瘤抗原表型生物标志物,其筛选与验证逻辑遵循“重叠肽库初筛→精细定位→MHC限制性验证→功能效应确认”的完整链条。该表位来源于MCPyV LT抗原的N端功能区域,验证方法包括胞内细胞因子染色、流式细胞术、MHC转染细胞系分析及体内荷瘤实验,特异性表现为仅能激活pcDNA3-CRT/LT疫苗免疫小鼠的CD8+T细胞,且严格依赖H-2Kb分子的递呈;敏感性方面,该表肽段能有效激活LT特异性CD8+T细胞,诱导的免疫应答能显著延长荷瘤小鼠的生存期。核心成果方面,该表位是首次被鉴定的MCPyV LT抗原免疫优势CTL表位,其功能关联表现为能作为靶点诱导具有肿瘤杀伤活性的CD8+T细胞,介导保护性和治疗性抗肿瘤效应;创新性在于,该表位的鉴定为MCC的免疫治疗提供了精准靶点,同时CRT偶联的疫苗策略为病毒相关肿瘤的免疫治疗提供了新的范式。推测:该表位经人源化MHC分子验证后,可用于MCPyV阳性MCC患者的肽疫苗开发或过继性T细胞治疗,具有较高的临床转化潜力。
