1. 领域背景与文献引入
文献英文标题:Exploring the cellular and molecular differences between ovarian clear cell carcinoma and high-grade serous carcinoma using single-cell RNA sequencing and GEO gene expression signatures;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:上皮性卵巢癌分子分型与肿瘤异质性研究
上皮性卵巢癌是全球女性第七大常见恶性肿瘤,也是致死率最高的妇科恶性肿瘤。其中高级别浆液性卵巢癌(HGSC)是最常见亚型,占所有病例的60%;卵巢透明细胞癌(OCCC)是第二常见亚型,占5-11%。领域共识:OCCC患者因对铂类化疗耐药,预后显著差于HGSC患者,成为临床治疗的难点。随着单细胞RNA测序(scRNA-seq)技术的发展,肿瘤异质性研究进入细胞水平解析的新阶段,当前领域热点聚焦于不同上皮性卵巢癌亚型的细胞组成、分子特征、化疗耐药机制及潜在治疗靶点的挖掘。然而,目前针对OCCC与HGSC的细胞异质性差异尚未得到全面解析,OCCC化疗耐药的具体细胞与分子机制仍不明确,缺乏特异性的亚型分型生物标志物及针对性治疗靶点,这也是制约OCCC临床治疗效果提升的核心问题。在此背景下,本研究旨在通过scRNA-seq结合GEO数据库的bulk RNA-seq数据,系统解析OCCC与HGSC的细胞和分子差异,阐明OCCC化疗耐药的潜在机制,筛选特异性生物标志物及潜在治疗靶点,为改善OCCC患者预后提供理论依据。
2. 文献综述解析
本文献综述部分从上皮性卵巢癌亚型的临床特征、分子特征及现有研究技术进展三个维度,系统梳理了领域内研究现状,并明确了OCCC研究的空白与不足。
现有研究已明确HGSC与OCCC在临床病理特征上的显著差异,HGSC常见TP53和WT-1基因突变,多数表达雌激素受体(ER),而OCCC以HNF1B过表达为特征,ER和孕激素受体(PR)多为阴性。在技术应用方面,scRNA-seq技术已被广泛应用于HGSC的肿瘤异质性、肿瘤微环境及化疗耐药机制研究,为HGSC的精准治疗提供了新的思路,但针对OCCC的scRNA-seq研究仍处于空白状态,缺乏两种亚型在细胞水平的全面对比分析。现有研究的局限性在于,尚未从细胞亚群层面解析OCCC化疗耐药的具体机制,且缺乏能有效区分两种亚型的特异性生物标志物,导致OCCC的临床分型与治疗靶点选择仍依赖传统病理特征,难以满足精准医疗的需求。
本研究的创新价值在于,首次利用scRNA-seq技术对OCCC与HGSC的原发肿瘤组织进行单细胞转录组分析,结合bulk RNA-seq数据的验证,全面揭示了两种亚型的细胞异质性差异,阐明了OCCC化疗耐药的细胞周期机制,鉴定了新的亚型分型生物标志物,并发现了代谢通路作为OCCC潜在治疗靶点的价值,填补了OCCC单细胞水平研究的空白,为领域内OCCC的研究提供了新的方向。
3. 研究思路总结与详细解析
本研究以解析OCCC与HGSC的细胞和分子差异、阐明OCCC化疗耐药机制、筛选特异性生物标志物及治疗靶点为核心目标,采用“样本收集-单细胞转录组分析-细胞亚群鉴定-差异标志物验证-体外功能实验-免疫微环境分析”的完整技术路线,形成了从发现问题到验证结论的研究闭环。
3.1 样本收集与单细胞RNA测序实验
本环节的核心目标是获取OCCC与HGSC的单细胞转录组数据,为后续细胞亚群分析提供基础。研究收集了5例OCCC患者和5例HGSC患者的手术切除肿瘤组织,采用胶原酶IV、透明质酸酶和DNase I联合消化的方法制备单细胞悬液,去除死细胞和红细胞后,利用10×Genomics的Chromium Next GEM Single Cell 3’ GEM Library & Gel Bead Kit v3.1构建文库,通过Illumina NovaSeq 6000平台进行测序。经过数据过滤和质量控制,最终获得101672个高质量细胞,每个细胞平均检测到2000个基因,后续通过Seurat软件进行细胞聚类分析,将细胞分为上皮细胞、免疫细胞和基质细胞三大类。
实验所用关键产品:10×Genomics的Chromium Next GEM Single Cell 3’ GEM Library & Gel Bead Kit v3.1,Illumina NovaSeq 6000测序仪,Sigma‒Aldrich的胶原酶IV、透明质酸酶,Miltenyi Biotec的红细胞裂解液、死细胞去除试剂盒。
3.2 上皮细胞亚群分析与化疗耐药机制探索
本环节旨在解析两种亚型上皮细胞的亚群差异,阐明OCCC化疗耐药的潜在细胞机制。研究对上皮细胞进行无监督亚聚类分析,鉴定出8个上皮细胞亚群,并通过细胞周期分析、转录调控网络分析和拟时间轨迹分析,解析各亚群的功能特征。结果显示,OCCC样本中Cluster4(高表达LEFTY1、MUC1等基因)的细胞比例显著高于HGSC,而Cluster7(高表达细胞周期相关基因,主要处于G2/M期)的细胞比例显著低于HGSC(n=10,P<0.05)。结合领域共识中顺铂主要诱导G2/M期细胞凋亡的机制,推测:OCCC中G2/M期上皮细胞比例较低是其化疗耐药的重要原因之一。此外,Cluster4细胞富集Hedgehog、Wnt-β-catenin、TGF-β等致癌信号通路,提示该亚群可能参与OCCC的发病过程。CNV分析显示,OCCC各上皮亚群的全基因组CNV水平显著低于HGSC,提示两种亚型的基因组不稳定性存在差异。
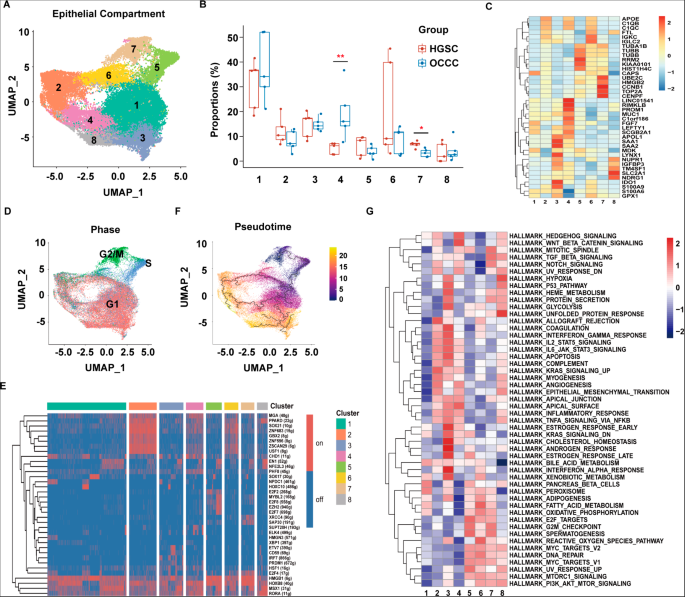
文献未提及具体生物信息学分析工具,领域常规使用Seurat、Monocle3、InferCNV、SCENIC等工具。
3.3 差异标志物鉴定与临床验证
本环节的核心目标是筛选并验证能有效区分OCCC与HGSC的特异性生物标志物,并分析其与临床预后的关联。研究首先通过scRNA-seq数据筛选出两种亚型上皮细胞的差异表达基因,结合GEO数据库中GSE189553数据集的bulk RNA-seq数据进行初步验证,初步确定AOC1、LEFTY1、GPX3在OCCC中高表达,S100A2、WFDC2、CRABP2在HGSC中高表达。随后通过实时荧光定量PCR(qRT-PCR)对8例OCCC和8例HGSC患者的组织样本进行验证,结果显示AOC1、LEFTY1、GPX3在OCCC中的表达水平分别为HGSC的2.8倍、3.2倍、2.5倍(n=8,P<0.01),而S100A2、WFDC2、CRABP2在HGSC中的表达水平显著高于OCCC(n=8,P<0.01)。Western blot实验进一步验证了上述基因的蛋白表达差异(n=4,P<0.05)。为了进行大样本验证,研究构建了包含128例OCCC和81例HGSC样本的组织芯片,通过免疫组化(IHC)染色证实了AOC1、LEFTY1、GPX3在OCCC中的高表达及S100A2、WFDC2、CRABP2在HGSC中的高表达。预后分析显示,GPX3高表达的OCCC患者无进展生存期显著长于低表达患者(P<0.05),且铂敏感OCCC患者的GPX3表达比例显著高于铂耐药患者(P<0.05)。
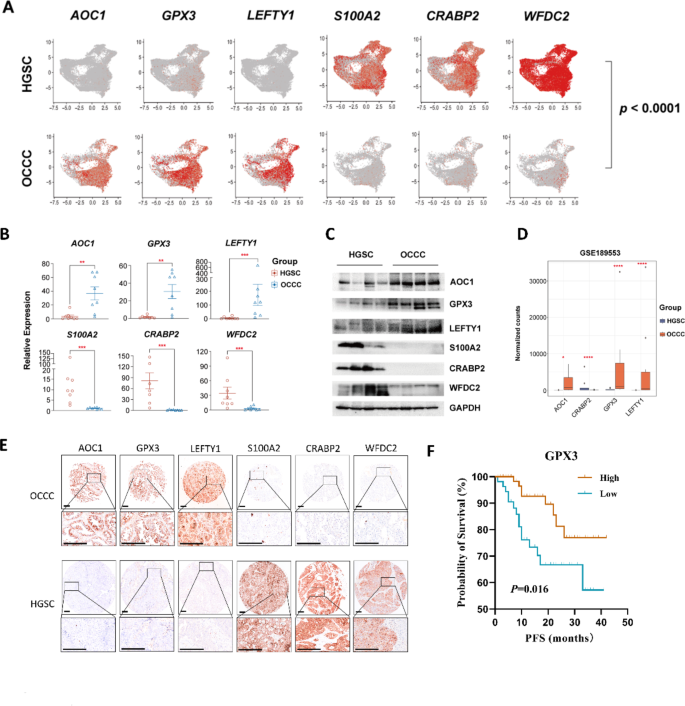
实验所用关键产品:Thermo Fisher Scientific的TRIzol试剂、PrimeScript™ RT Master Mix、Fast SYBR Green Master Mix,DAKO Autostainer Link 48免疫组化染色仪,GraphPad Prism 8.0统计分析软件。
3.4 代谢通路分析与体外功能验证
本环节旨在解析OCCC的代谢特征,并验证代谢通路作为潜在治疗靶点的可行性。通过KEGG通路富集分析,研究发现OCCC上皮细胞的差异表达基因显著富集于氧化磷酸化、谷氨酰胺代谢、糖酵解/糖异生及铁死亡等代谢通路。为了验证这些通路的治疗潜力,研究选用OCCC细胞系TOV21G和HGSC细胞系OVCAR3进行体外实验,分别处理谷氨酰胺代谢抑制剂CB-839、铁死亡抑制剂liproxstatin-1、氧化磷酸化抑制剂二甲双胍和糖酵解抑制剂2-脱氧-D-葡萄糖。结果显示,二甲双胍和2-脱氧-D-葡萄糖能显著抑制两种细胞系的细胞活力,其中二甲双胍处理72小时后,TOV21G和OVCAR3的细胞活力分别降至42.3%和38.7%(n=3,P<0.001);EdU实验和流式细胞术凋亡检测显示,二甲双胍能抑制细胞增殖并促进细胞凋亡,2-脱氧-D-葡萄糖则通过不同机制降低细胞活力。有趣的是,CB-839或liproxstatin-1与顺铂联合处理时,能显著提高TOV21G细胞的活力,降低顺铂的化疗敏感性,但对OVCAR3细胞的影响较小(n=3,P<0.05),提示抑制谷氨酰胺代谢或铁死亡仅会降低OCCC细胞的化疗敏感性。
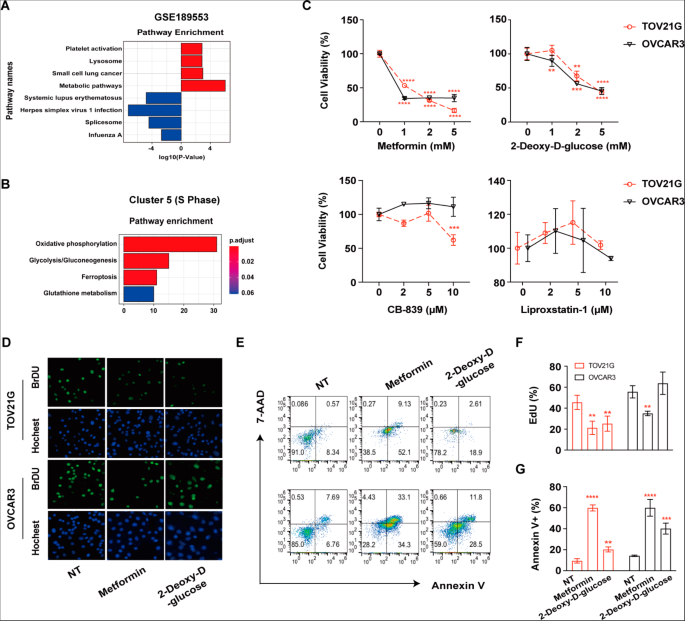
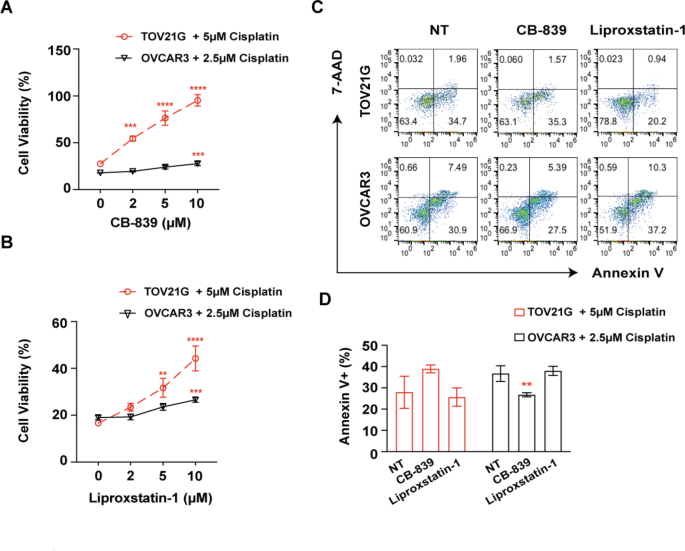
实验所用关键产品:ATCC的TOV21G细胞系,中国国家细胞库的OVCAR3细胞系,MedChemExpress的cisplatin、2-脱氧-D-葡萄糖、二甲双胍、CB-839、liproxstatin-1,Dojindo的CCK8试剂,BD的FITC Annexin V凋亡检测试剂盒,Invitrogen的Click-iT® EdU成像试剂盒。
3.5 免疫细胞亚群差异分析
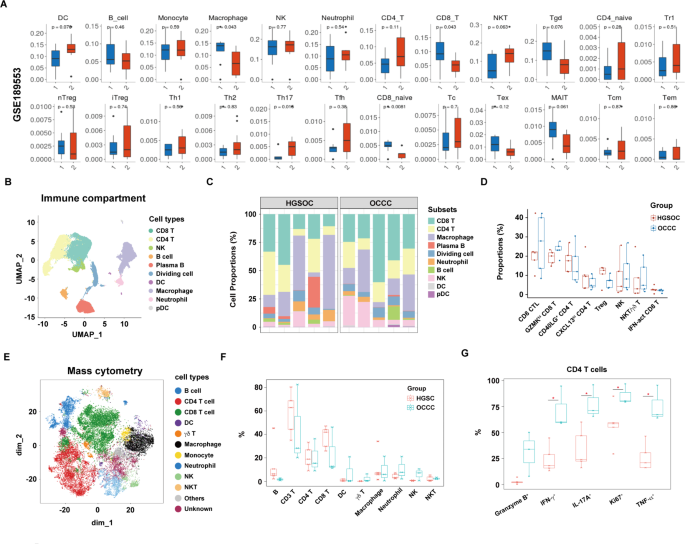
本环节旨在解析OCCC与HGSC在肿瘤免疫微环境上的差异。研究首先通过ImmunCellAI工具分析GSE189553数据集的免疫细胞丰度,发现OCCC样本中巨噬细胞和CD8+T细胞的比例显著高于HGSC,而Th17细胞和初始CD8+T细胞的比例显著低于HGSC(P<0.05)。随后对scRNA-seq数据中的免疫细胞进行亚聚类分析,鉴定出10个免疫细胞亚群,包括CD8+T细胞、CD4+T细胞、NK细胞等,进一步分析显示两种亚型的免疫细胞亚群比例无显著差异,但CD4+T细胞中增殖标志物Ki-67及炎症细胞因子IFN-γ、IL-17A、TNF-α的表达水平在OCCC中显著高于HGSC(P<0.05)。为了验证上述结果,研究采用质谱流式技术对肿瘤浸润淋巴细胞(TILs)进行分析,结果与scRNA-seq数据一致,T细胞是两种亚型TILs的主要组成部分,OCCC的CD4+T细胞中Ki-67及炎症细胞因子的表达水平显著更高。
实验所用关键产品:质谱流式检测相关试剂,ImmunCellAI在线分析工具,FlowJo流式细胞术分析软件。
4. Biomarker研究及发现成果解析
本研究共鉴定出6个能有效区分OCCC与HGSC的生物标志物,以及1个与OCCC预后相关的生物标志物,形成了从筛选到验证的完整研究链条,为上皮性卵巢癌的精准分型与预后评估提供了新的工具。
Biomarker定位方面,AOC1、LEFTY1、GPX3为OCCC的特异性标志物,S100A2、WFDC2、CRABP2为HGSC的特异性标志物,GPX3同时作为OCCC的预后标志物。筛选与验证逻辑为:首先通过scRNA-seq数据筛选两种亚型上皮细胞的差异表达基因,然后利用GEO数据库的bulk RNA-seq数据进行初步验证,接着通过qRT-PCR、Western blot在小样本临床组织中验证基因及蛋白表达差异,最后通过包含209例样本的组织芯片进行大样本免疫组化验证,并结合临床数据进行预后分析。
研究过程中,所有标志物均来自临床原发肿瘤组织样本,验证方法涵盖了转录水平、蛋白水平及组织水平的多维度验证。特异性与敏感性方面,免疫组化结果显示AOC1在OCCC中的阳性表达率为78.9%,在HGSC中的阳性表达率为22.2%(P<0.001);S100A2在HGSC中的阳性表达率为81.5%,在OCCC中的阳性表达率为31.3%(P<0.001),提示两者具有良好的分型特异性。GPX3作为预后标志物,高表达OCCC患者的无进展生存期中位数为28.5个月,低表达患者为16.2个月(HR=0.52,95% CI 0.31-0.87,P<0.05),且铂敏感患者的GPX3阳性表达率显著高于铂耐药患者(72.1% vs 45.8%,P<0.05)。
核心成果提炼:本研究首次报道AOC1和S100A2作为OCCC与HGSC的分型标志物,填补了领域内特异性分型标志物的空白;GPX3不仅能区分OCCC与HGSC,还能预测OCCC患者的预后与化疗敏感性,为OCCC的临床管理提供了新的参考指标;此外,LEFTY1高表达的上皮细胞亚群可能参与OCCC的发病机制,为OCCC的发病机制研究提供了新的方向。这些成果为上皮性卵巢癌的精准分型、预后评估及治疗靶点选择提供了重要的理论依据与实验支持。
