1. 领域背景与文献引入
文献英文标题:KLF7/VPS35 axis contributes to hepatocellular carcinoma progression through CCDC85C-activated β-catenin pathway;发表期刊:Cell & Bioscience;影响因子:7.13(2021年);研究领域:肿瘤学-肝细胞癌分子机制
领域共识:肝细胞癌是全球发病率和死亡率均位居前列的恶性肿瘤,其发生发展涉及多基因、多信号通路的异常调控,晚期患者缺乏有效的治疗手段,寻找新的驱动分子和靶向治疗靶点是当前肝癌研究的核心方向之一。Krüppel样因子(KLF)家族作为一类保守的锌指转录因子,已被证实参与多种肿瘤的发生发展,其中KLF7在神经发育及非小细胞肺癌、胃癌等实体瘤中发挥促癌作用,但目前关于KLF7在肝细胞癌中的作用及分子机制尚未见报道。空泡蛋白分选相关蛋白35(VPS35)作为retromer复合物的核心组分,此前研究发现其在肝细胞癌中高表达并通过PI3K/AKT通路促进肿瘤进展,但上游调控机制仍不明确。卷曲螺旋结构域蛋白85C(CCDC85C)此前仅在脑积水及犬乳腺肿瘤中有少量研究,其与肝细胞癌的相关性完全未知。针对上述研究空白,本研究旨在系统探究KLF7在肝细胞癌中的功能,并解析其通过调控VPS35/CCDC85C/β-连环蛋白通路促进肿瘤进展的分子机制,为肝细胞癌的诊断和治疗提供新的潜在靶点。
2. 文献综述解析
本文献综述部分按分子类型(KLF7、VPS35、CCDC85C)的维度对领域内现有研究进行分类梳理,明确了各分子的研究现状与未解决问题。
现有研究中,KLF家族成员广泛参与细胞增殖、分化、凋亡及周期调控等生物学过程,KLF7作为该家族成员,已被证实参与神经元形态发生,并在非小细胞肺癌、胃癌等实体瘤中发挥促癌作用,但缺乏其在肝细胞癌中的功能研究;VPS35主要参与内体到高尔基体或细胞膜的蛋白分选过程,此前研究发现其在肝细胞癌中作为癌基因激活PI3K/AKT通路促进肿瘤生长,但上游转录调控机制尚未阐明;CCDC85C仅在小鼠脑积水模型及犬乳腺肿瘤中有少量报道,其在肝细胞癌中的表达及功能完全未知。现有研究的局限性在于未揭示KLF7与肝细胞癌的关联,也未明确VPS35在肝细胞癌中的上游调控分子,同时缺乏CCDC85C与肝细胞癌的相关研究。
本研究的创新价值在于首次揭示了KLF7作为转录因子在肝细胞癌中高表达,并通过直接结合VPS35的启动子区域激活其转录表达,进而通过与CCDC85C相互作用激活β-连环蛋白信号通路,完善了肝细胞癌中该信号轴的调控网络;同时首次将CCDC85C与肝细胞癌的发生发展关联起来,填补了KLF7在肝细胞癌功能及VPS35上游调控机制的研究空白,为肝细胞癌的分子靶向治疗提供了新的潜在靶点。
3. 研究思路总结与详细解析
本研究的核心目标是明确KLF7在肝细胞癌中的功能及分子调控机制,核心科学问题为KLF7如何通过下游信号通路调控肝细胞癌的增殖、侵袭等恶性生物学行为,技术路线遵循“临床样本初筛→细胞功能验证→动物实验验证→分子机制解析→临床样本验证”的闭环逻辑,从临床到基础再回到临床,系统解析了KLF7/VPS35/CCDC85C/β-连环蛋白轴在肝细胞癌中的作用。
3.1 临床样本中KLF7的表达及临床相关性分析
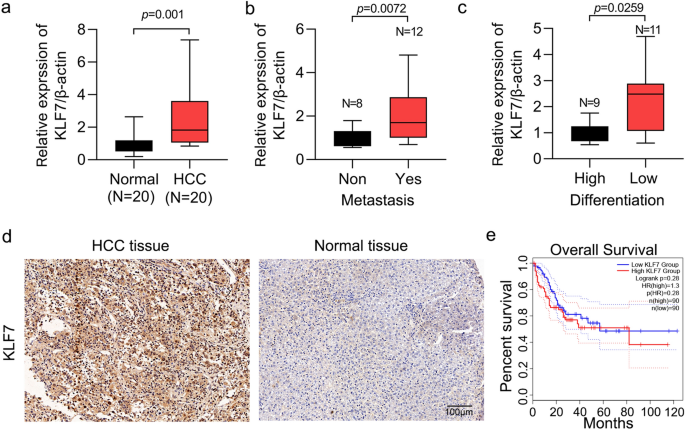
本环节的实验目的是明确KLF7在肝细胞癌患者临床样本中的表达水平,及其与患者临床病理特征的相关性。方法细节上,研究团队收集了20对肝细胞癌及癌旁正常组织样本,采用实时荧光定量PCR(qRT-PCR)检测KLF7的mRNA表达水平;同时使用包含50例肝细胞癌组织和20例正常肝组织的组织芯片进行免疫组化(IHC)染色,检测KLF7的蛋白表达;此外从TCGA数据库中提取肝细胞癌患者的基因表达及生存数据,分析KLF7表达与患者生存的相关性。结果解读显示,qRT-PCR结果表明肝细胞癌组织中KLF7的mRNA表达水平显著高于癌旁正常组织(n=20,P=0.001);有转移的肝细胞癌组织中KLF7表达水平显著高于无转移组(n=20,P=0.0072),低分化肝细胞癌组织中KLF7表达水平显著高于高分化组(n=20,P=0.0259);免疫组化染色结果显示,肝细胞癌组织中KLF7呈强阳性表达,而正常肝组织中表达水平较低;但TCGA数据库分析显示,KLF7高表达与肝细胞癌患者的总生存无显著相关性(n=90,P=0.28)。实验所用关键产品:抗KLF7抗体(货号398576,Santa Cruz);qRT-PCR试剂、免疫组化染色试剂未明确品牌,领域常规使用Takara qRT-PCR试剂盒、Dako免疫组化试剂盒等。
3.2 KLF7在肝癌细胞及动物模型中的功能验证
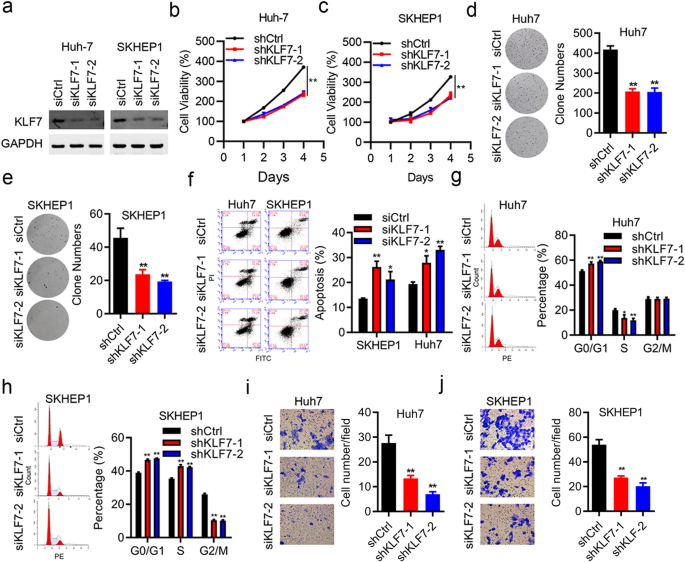
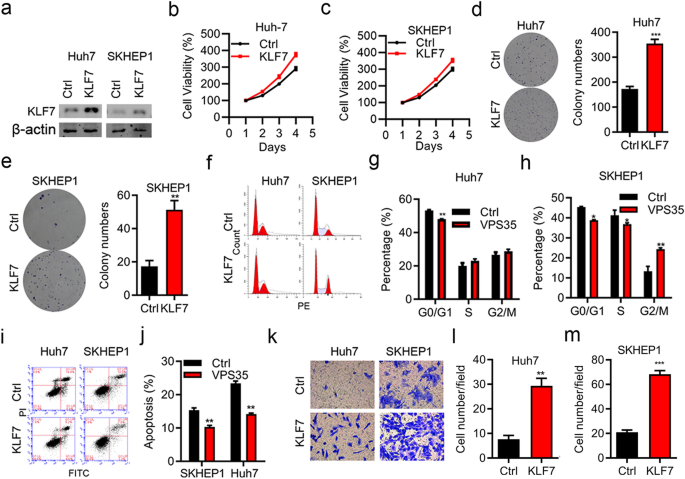
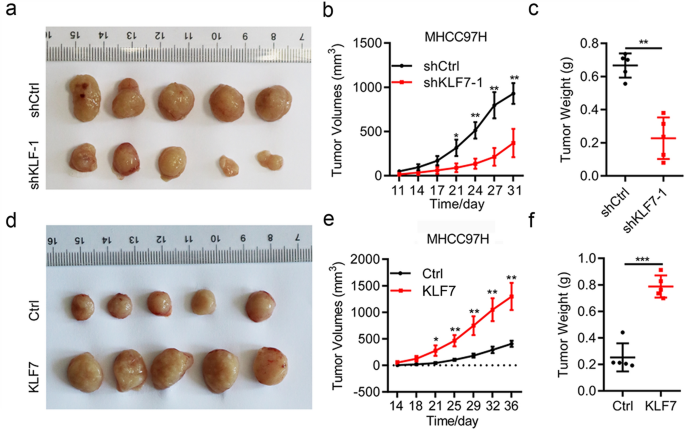
本环节的实验目的是验证KLF7对肝细胞癌细胞增殖、侵袭、细胞周期及凋亡的调控作用,以及其在体内的成瘤能力。方法细节上,在Huh-7和SKHEP1肝细胞癌细胞系中,采用siRNA技术敲低KLF7的表达,或通过pcDNA3.1质粒过表达KLF7;分别采用CCK-8实验检测细胞增殖能力,克隆形成实验检测细胞克隆形成能力,Transwell实验检测细胞侵袭能力,流式细胞术检测细胞周期分布及凋亡率;同时构建裸鼠皮下移植瘤模型,将稳定敲低或过表达KLF7的MHCC97H细胞分别注射到裸鼠右侧颈部,每3天测量肿瘤大小,30天后处死小鼠并计算肿瘤体积和重量。结果解读显示,敲低KLF7后,Huh-7和SKHEP1细胞的增殖能力显著降低(n=3,P<0.01),克隆形成率显著下降(n=3,P<0.01),细胞侵袭能力显著减弱(n=3,P<0.01),G0/G1期细胞比例显著增加,凋亡率显著升高(n=3,P<0.05);过表达KLF7则显著促进肝细胞癌细胞的增殖、侵袭能力,加速细胞周期进程,抑制细胞凋亡(n=3,P<0.01);体内实验结果显示,KLF7敲低组的肿瘤体积和重量显著小于对照组(n=5,P<0.01),KLF7过表达组的肿瘤体积和重量显著大于对照组(n=5,P<0.001),与体外实验结果一致。实验所用关键产品:FITC Annexin V凋亡检测试剂盒(BD Biosciences)、Transwell小室(Corning lnc., USA);CCK-8试剂盒未明确品牌,领域常规使用Dojindo CCK-8试剂盒。
3.3 KLF7调控VPS35的分子机制验证
本环节的实验目的是明确KLF7是否通过转录激活VPS35的表达来发挥促癌作用。方法细节上,采用蛋白质免疫印迹(Western blot)检测KLF7敲低或过表达后VPS35的蛋白表达水平;通过TCGA数据库分析KLF7与VPS35在肝细胞癌组织中的表达相关性;采用双荧光素酶报告基因实验,将VPS35的启动子序列克隆到荧光素酶报告载体中,与KLF7过表达载体共转染肝细胞癌细胞,检测荧光素酶活性;采用染色质免疫沉淀-定量PCR(ChIP-qPCR)实验验证KLF7与VPS35启动子的结合;通过rescue实验,在KLF7过表达的细胞中敲低VPS35,检测细胞增殖和侵袭能力的变化。结果解读显示,KLF7敲低后VPS35的蛋白表达水平显著降低,过表达KLF7则显著升高VPS35的蛋白表达;TCGA数据库分析显示,KLF7与VPS35在肝细胞癌组织中的表达呈显著正相关;双荧光素酶报告基因实验显示,KLF7过表达显著增强VPS35启动子的荧光素酶活性(n=3,P<0.01);ChIP-qPCR实验证实KLF7可直接结合VPS35的启动子区域;rescue实验显示,敲低VPS35可显著逆转KLF7过表达对肝细胞癌细胞增殖和侵袭的促进作用(n=3,P<0.01)。实验所用关键产品:抗VPS35抗体(货号157220,Abcam)、双荧光素酶报告基因检测系统(Promega, USA)、SimpleChIP酶促染色质IP试剂盒(Cell Signaling)。
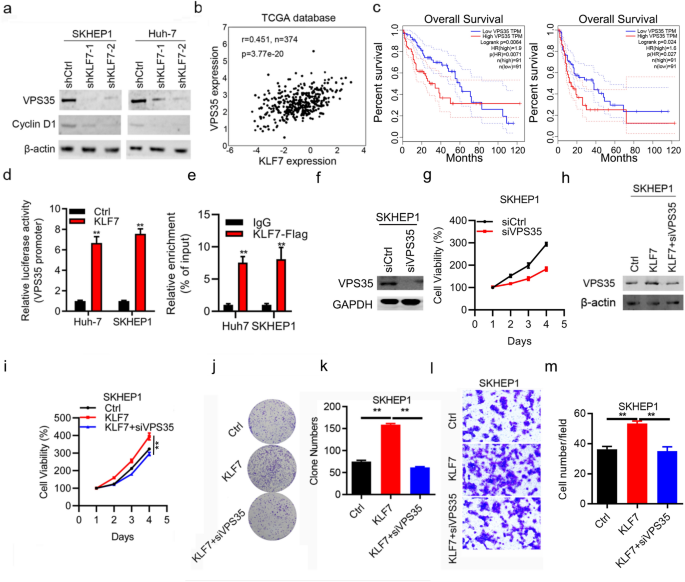
3.4 VPS35与CCDC85C的相互作用及对β-连环蛋白通路的调控
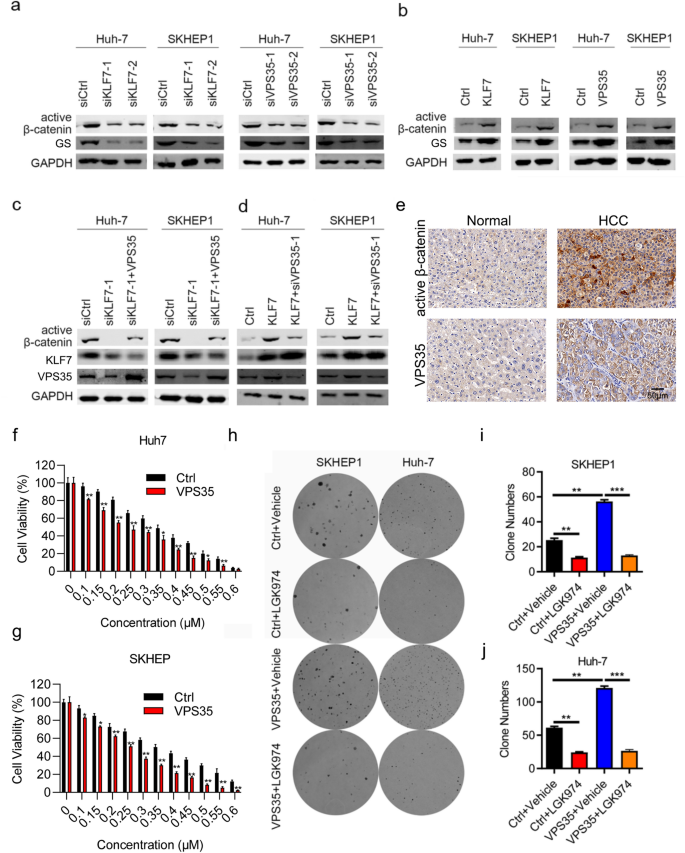
本环节的实验目的是探究VPS35下游的互作分子及KLF7/VPS35轴调控的下游信号通路。方法细节上,采用免疫共沉淀(Co-IP)实验结合质谱分析筛选VPS35的互作分子,并通过Western blot验证VPS35与CCDC85C的相互作用;通过TCGA数据库分析CCDC85C在肝细胞癌组织中的表达及与患者生存的相关性;通过rescue实验,在VPS35过表达的细胞中敲低CCDC85C,检测细胞增殖、侵袭及凋亡能力的变化;采用Western blot检测KLF7/VPS35轴对β-连环蛋白通路的影响,并使用β-连环蛋白抑制剂GK974处理细胞,验证通路功能。结果解读显示,Co-IP实验结合质谱分析证实VPS35与CCDC85C在肝细胞癌细胞中存在相互作用;TCGA数据库分析显示,CCDC85C在肝细胞癌组织中高表达,与患者总生存不良(P=0.036)及无病生存不良(P<0.027)显著相关;rescue实验显示,敲低CCDC85C可显著逆转VPS35过表达对肝细胞癌细胞增殖和侵袭的促进作用(n=3,P<0.01);Western blot结果显示,KLF7/VPS35轴可显著上调活性β-连环蛋白的表达,β-连环蛋白抑制剂GK974可显著阻断VPS35过表达对肝细胞癌细胞增殖的促进作用(n=3,P<0.001);免疫组化染色显示,肝细胞癌组织中VPS35与活性β-连环蛋白的表达呈显著正相关(n=50,P<0.05)。实验所用关键产品:抗CCDC85C抗体(货号TA330857,ORIGENE)、抗活性β-连环蛋白抗体(货号19807,Cell Signaling Technology);β-连环蛋白抑制剂GK974未明确品牌,领域常规使用Selleck GK974。
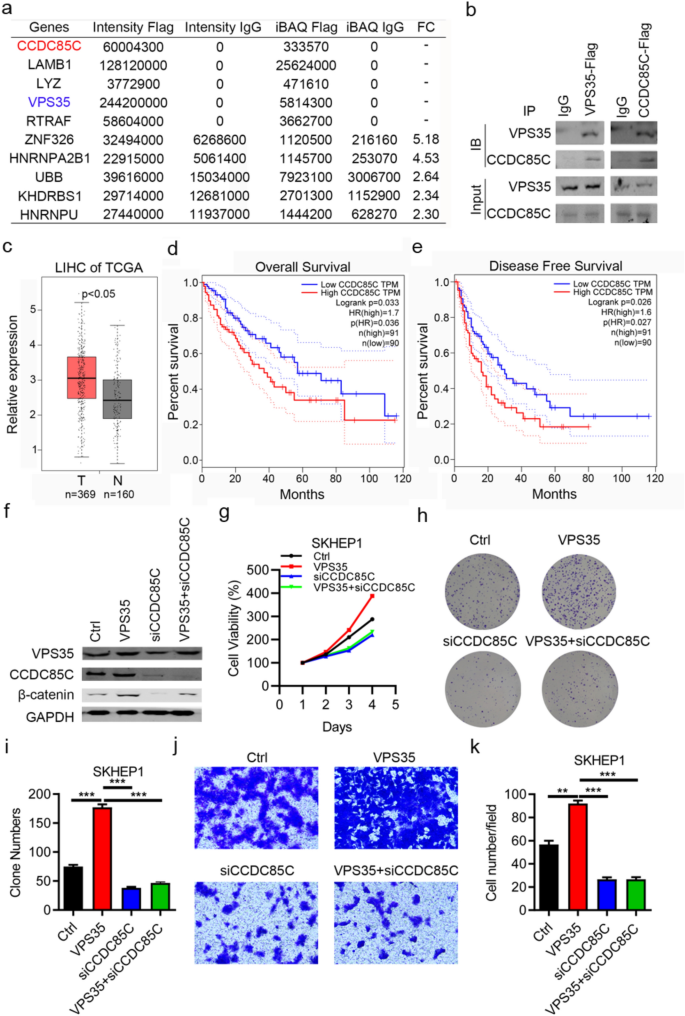
4. Biomarker研究及发现成果
本研究涉及的Biomarker包括KLF7、VPS35、CCDC85C及活性β-连环蛋白,筛选与验证逻辑遵循“临床样本初筛表达差异→细胞/动物实验验证功能→分子机制解析→临床样本验证相关性”的完整链条,系统解析了各分子作为肝细胞癌Biomarker的潜力。
研究过程中,KLF7的检测来源于20对肝细胞癌及癌旁组织样本、50例肝细胞癌组织芯片,通过qRT-PCR和免疫组化检测其表达,结果显示KLF7在肝细胞癌组织中高表达,与患者的分化程度和转移状态显著相关(n=20,P=0.001、0.0072、0.0259);VPS35通过Western blot、TCGA数据库及免疫组化检测,显示其在肝细胞癌组织中高表达,与KLF7和活性β-连环蛋白的表达呈正相关,且高表达提示患者不良生存(TCGA数据库,P<0.05);CCDC85C通过TCGA数据库分析显示其在肝细胞癌组织中高表达,与患者总生存和无病生存不良显著相关(P=0.036、P<0.027);活性β-连环蛋白通过免疫组化检测显示其在肝细胞癌组织中高表达,与KLF7、VPS35的表达呈正相关(n=50,P<0.05)。
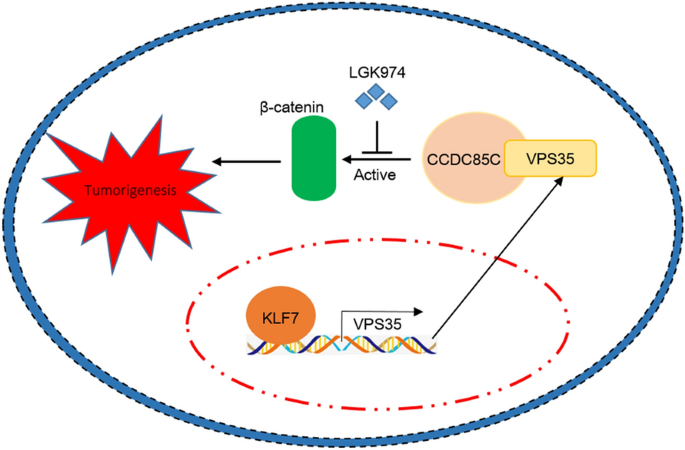
核心成果方面,KLF7作为转录因子,通过激活VPS35的转录表达,进而与CCDC85C相互作用激活β-连环蛋白通路,促进肝细胞癌细胞的增殖、侵袭和体内成瘤,是肝细胞癌的驱动分子;KLF7、VPS35、CCDC85C均可作为肝细胞癌潜在的诊断Biomarker,其中VPS35和CCDC85C可作为潜在的预后Biomarker,VPS35高表达提示患者不良生存,CCDC85C高表达与患者总生存和无病生存不良相关;KLF7/VPS35/CCDC85C/β-连环蛋白轴可作为肝细胞癌治疗的潜在靶点,β-连环蛋白抑制剂可有效阻断该信号轴的促肿瘤作用,为肝细胞癌的靶向治疗提供了新的方向。
