1. 领域背景与文献引入
文献英文标题:Evidence for a mitochondrial localization of the retinoblastoma protein;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:肿瘤抑制蛋白亚细胞定位与功能研究
领域共识:视网膜母细胞瘤蛋白(Rb)是1987年被首次克隆的人类肿瘤抑制蛋白,其功能缺失与视网膜母细胞瘤、肺癌、乳腺癌等多种恶性肿瘤的发生发展密切相关。Rb的核心生物学功能包括调控细胞周期进程、细胞分化及细胞凋亡,主要通过与E2F转录因子家族结合,抑制下游细胞周期相关基因的转录实现。当前领域研究热点集中在Rb的翻译后修饰(如磷酸化、半胱天冬酶切割)对其功能的调控,以及亚细胞定位异常在肿瘤发生中的作用——已有研究发现,在部分肿瘤细胞中Rb发生核质穿梭异常,被隔离在细胞质中失去抑癌活性,但此前尚未有研究报道Rb的线粒体定位,这一空白导致Rb在凋亡调控中的矛盾作用(既有促凋亡也有抗凋亡报道)无法得到合理解释。
针对这一研究空白,本研究通过多组细胞实验与体外验证,首次证实Rb在正常及肿瘤细胞的线粒体中存在定位,为揭示Rb的未知功能提供了新的方向。
2. 文献综述解析
作者对领域内现有研究的分类维度为Rb的功能调控机制,包括翻译后修饰调控、亚细胞定位调控两大方向。
现有研究表明,Rb的活性主要依赖于其磷酸化状态,16个潜在的丝氨酸/苏氨酸磷酸化位点的修饰决定了其与E2F的结合能力,去磷酸化形式的Rb具有抑癌活性,而过度磷酸化则会使其失去功能;在肿瘤细胞中,Rb功能失活的机制包括基因缺失、病毒癌蛋白结合、过度磷酸化,此外半胱天冬酶介导的Rb切割也参与其功能调控。亚细胞定位方面,已有研究发现Rb的核质穿梭在部分肿瘤细胞中异常,导致其被隔离在细胞质中无法发挥核内抑癌功能,但这些研究均未关注线粒体等细胞器中的Rb分布。现有技术方法的优势在于,细胞分馏、免疫印迹等经典技术为亚细胞定位研究提供了可靠手段,但局限性在于多数研究仅聚焦于核或细胞质,未覆盖线粒体,且样本多为肿瘤细胞,缺乏正常细胞的验证,导致对Rb的亚细胞分布认知不完整。
本研究通过对比现有研究的空白,首次发现Rb的线粒体定位,且在正常和肿瘤细胞中均存在,这一突破为解释Rb在凋亡调控中的矛盾作用提供了新的视角,也为Rb的功能研究开辟了线粒体相关的新方向。
3. 研究思路总结与详细解析
本研究的核心目标是验证Rb是否存在线粒体定位,并明确其在线粒体中的具体亚区室分布;核心科学问题是Rb的线粒体定位是否为普遍现象,以及其与线粒体的结合特性;技术路线遵循“初步发现→特异性验证→亚区室定位→体外验证→结合强度确认”的闭环逻辑,通过细胞实验与无细胞体系实验相互印证,确保结果的可靠性。
3.1 细胞亚分馏检测Rb的线粒体定位
实验目的是在不同类型的正常及肿瘤细胞中,检测Rb是否存在线粒体定位。方法细节:选取人原代成纤维细胞(HF)、人纤维肉瘤细胞(HT1080)、大鼠嗜铬细胞瘤细胞(PC12)、大鼠永生化成纤维细胞(FR3T3),分为未处理组和依托泊苷(50μg/ml)处理组(处理16小时诱导凋亡),采用差速离心法进行细胞亚分馏,分离得到总蛋白、核蛋白、线粒体蛋白组分,各组分取40μg蛋白进行免疫印迹(蛋白质印迹)检测,使用的标记物包括核标记物增殖细胞核抗原(PCNA)或核纤层蛋白A(lamin A)、线粒体标记物细胞色素c氧化酶II(COX II)或细胞色素c、细胞质标记物微管蛋白,以验证各组分的纯度。结果解读:免疫印迹结果显示,在所有未处理细胞的线粒体组分中均检测到Rb蛋白,与经典的核定位同时存在;依托泊苷处理后,核和线粒体中的Rb含量均有所降低,但两者的分布比例无显著变化;Image J软件定量分析显示,未处理细胞中线粒体/核的Rb含量比例显著高于PCNA(或lamin A),说明线粒体中的Rb并非核组分污染所致。实验所用关键产品:小鼠单克隆抗Rb抗体(G3-245,BD Pharmingen)、抗细胞色素c抗体(BD Pharmingen)、抗微管蛋白抗体(MAS078,Sera-Lab)等。
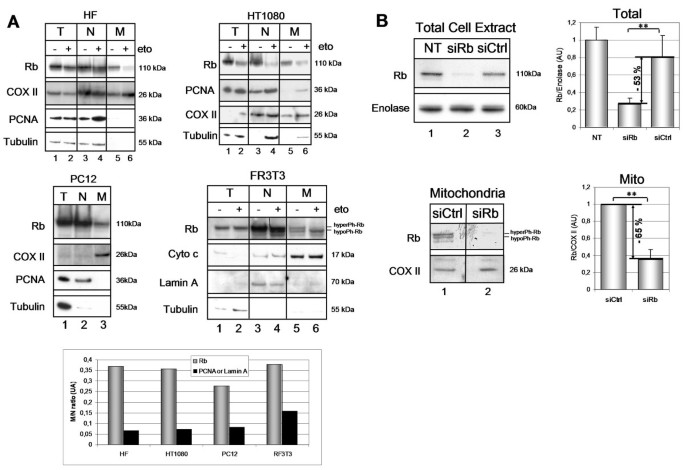
3.2 Rb siRNA验证线粒体组分中Rb的特异性
实验目的是确认线粒体组分中检测到的蛋白确实是Rb,而非交叉反应的其他蛋白。方法细节:将FR3T3细胞接种至培养皿,待细胞汇合度达50%时,分别转染Rb siRNA(Rn_Rb1_1_HP siRNA)、对照siRNA,或不进行转染,转染试剂为HiPerFect Transfection Reagent;48小时后收集细胞,进行细胞亚分馏得到线粒体组分,取20μg蛋白进行免疫印迹检测,以烯醇化酶(总蛋白)和COX II(线粒体蛋白)为内参。结果解读:免疫印迹结果显示,Rb siRNA处理后,总蛋白中的Rb含量降低53%,线粒体组分中的Rb含量降低63%(P<0.01,文献未明确提供样本量),而对照siRNA处理组无显著变化,直接证明线粒体组分中检测到的蛋白为Rb。实验所用关键产品:Rb siRNA(Rn_Rb1_1_HP siRNA,Qiagen)、HiPerFect Transfection Reagent(Qiagen)、抗烯醇化酶抗体(由N. Lamande馈赠)等。
3.3 线粒体亚分馏确定Rb的具体亚区室定位
实验目的是明确Rb在线粒体中的具体分布位置,即外膜、膜间隙、内膜或基质。方法细节:分离PC12细胞的线粒体,采用经典的线粒体亚分馏方法,将线粒体分为线粒体外膜(OM)、膜间隙(IS)、线粒体质体(MP,包含内膜和基质)三个亚组分,各组分取40μg蛋白进行免疫印迹检测,使用的亚区室标记物包括内膜/基质标记物F1-ATP酶β亚基、腺苷酸转位酶(ANT),外膜标记物电压依赖性阴离子通道(VDAC)、普遍型线粒体肌酸激酶(uMtCK),细胞质标记物肌动蛋白,核标记物TFIID,以验证各亚组分的纯度。结果解读:免疫印迹结果显示,Rb仅在线粒体质体组分中被检测到,而在外膜和膜间隙组分中均未检测到,说明Rb位于线粒体内膜或基质区,需要穿过线粒体外膜进入内部。实验所用关键产品:抗F1-ATP酶β亚基抗体(MS503,MitoScience)、抗VDAC抗体(由C. Brenner馈赠)、抗ANT抗体(由C. Brenner馈赠)等。
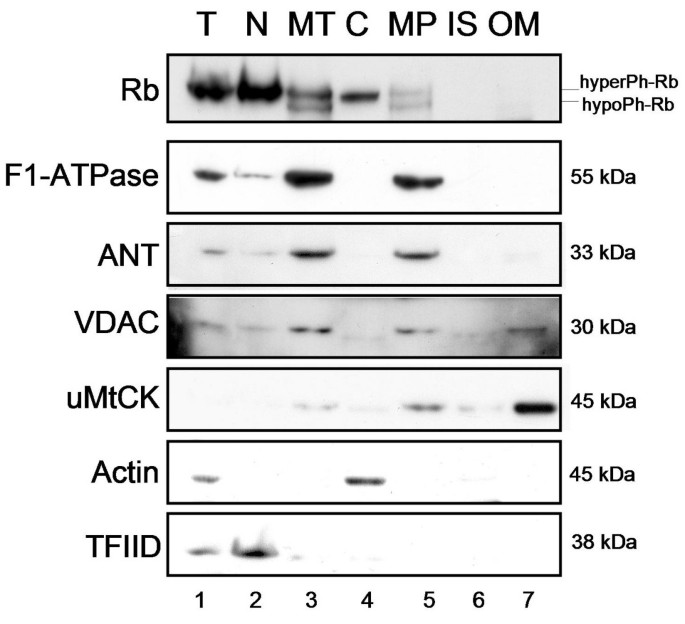
3.4 体外结合实验验证Rb与线粒体的直接结合能力
实验目的是在无细胞体系中验证Rb与线粒体的直接结合,排除细胞内其他因子的影响。方法细节:构建野生型Rb的cDNA质粒,通过体外转录翻译系统合成[³⁵S]甲硫氨酸标记的Rb蛋白,同时合成荧光素酶(阴性对照,非线粒体蛋白)和Bax(阳性对照,促凋亡蛋白,需tBid存在以结合线粒体);将8fmol标记蛋白与10mg/ml新鲜大鼠肝脏线粒体在导入缓冲液中孵育1小时(30℃),随后离心分离线粒体结合蛋白(M1)和上清中的非结合蛋白(S1),通过SDS-PAGE凝胶电泳和放射自显影检测蛋白分布。结果解读:放射自显影结果显示,Rb蛋白大量存在于线粒体结合组分中,结合强度与Bax类似,而荧光素酶几乎全部存在于上清中,说明Rb对线粒体具有较高的直接结合亲和力。实验所用关键产品:TNT偶联转录/翻译系统(Promega)、[³⁵S]甲硫氨酸(Amersham Bioscience)等。
3.5 碱性处理验证Rb与线粒体的结合强度
实验目的是确定Rb与线粒体的结合是否为强相互作用,排除弱结合或非特异性结合的可能。方法细节:将与[³⁵S]甲硫氨酸标记Rb孵育后的线粒体,用碱性缓冲液(300mM蔗糖、0.1M Na₂CO₃,pH11.3)处理30分钟(4℃),随后离心分离上清中的洗脱蛋白(S2)和线粒体结合蛋白(M2),通过SDS-PAGE凝胶电泳和放射自显影检测蛋白分布,以Bax为阳性对照(已知Bax与线粒体为弱结合,可被碱性处理洗脱)。结果解读:放射自显影结果显示,Rb蛋白几乎全部存在于线粒体结合组分中,对碱性处理具有抗性,而Bax则大部分被洗脱至上清中,说明Rb与线粒体的结合为强相互作用,进一步支持其位于线粒体内膜或基质区的结论。
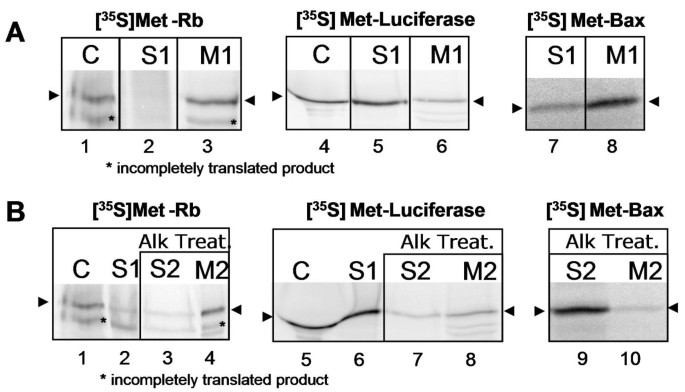
4. Biomarker研究及发现成果
本研究中涉及的Biomarker为视网膜母细胞瘤蛋白(Rb)的线粒体定位特征,属于肿瘤抑制蛋白的亚细胞分布新特征,其筛选与验证逻辑为“细胞分馏初步发现→siRNA验证特异性→线粒体亚分馏确定亚区室→体外实验验证结合能力→碱性处理确认结合强度”的完整链条。
研究过程详述:Rb为细胞内源性肿瘤抑制蛋白,来源包括人原代成纤维细胞、人纤维肉瘤细胞、大鼠嗜铬细胞瘤细胞、大鼠永生化成纤维细胞等多种正常及肿瘤细胞;验证方法涵盖细胞分馏免疫印迹、siRNA敲低验证、线粒体亚分馏、体外无细胞结合实验、碱性处理验证等多种技术;特异性方面,线粒体Rb在正常和肿瘤细胞中均存在,且不受依托泊苷诱导的凋亡影响,说明该定位是普遍存在的生理现象,而非肿瘤细胞特有的异常;敏感性方面,免疫印迹可检测到占总Rb含量1%-3%的线粒体Rb,这一比例较低可能是此前未被发现的原因。
核心成果提炼:本研究首次证实Rb的线粒体定位,且明确其位于线粒体内膜或基质区,这一发现填补了Rb亚细胞分布研究的空白;功能关联方面,结合此前研究发现的Rb调控线粒体呼吸链基因表达的结论,推测:Rb可能参与线粒体基因表达调控或线粒体生物发生,为解释Rb在凋亡调控中的矛盾作用提供了新的视角;该发现目前无直接临床预后数据,但为肿瘤治疗中靶向Rb的亚细胞定位提供了潜在的新方向,具有重要的学术价值。
