1. 领域背景与文献引入
文献英文标题:The emerging role of deubiquitinating enzymes in genomic integrity, diseases, and therapeutics;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:基因组稳定性调控与肿瘤分子生物学
泛素化是真核生物中关键的翻译后修饰方式,自20世纪80年代泛素-蛋白酶体系统被发现以来,其在蛋白降解中的调控作用一直是研究核心。2000年后,非降解性泛素链的功能逐渐被揭示,尤其是在DNA损伤应答(DDR)、信号转导等过程中的调控作用,成为领域研究热点。当前,泛素化与去泛素化的动态平衡对基因组稳定性的维持机制,以及去泛素化酶(DUBs)作为疾病治疗靶点的潜力,是领域内的核心研究方向。然而,领域内仍存在诸多未解决的问题:多数DUBs的底物特异性分子机制尚不明确,不同DUBs在DNA损伤修复通路中的协同调控网络未被系统解析,DUBs抑制剂的特异性不足且临床转化数据有限。在此背景下,本文通过系统整合2016年之前的相关研究,全面综述DUBs在基因组完整性维持、疾病发生及治疗中的作用,旨在填补领域内对DUBs整体功能和临床应用的整合性综述空白,为后续研究提供参考框架。
2. 文献综述解析
本文作者以DUBs的功能维度为核心分类逻辑,将现有研究分为DUBs的基础功能解析、在DNA损伤应答与修复中的调控作用、疾病关联及治疗靶点开发四大模块,系统梳理了领域内的研究进展与未解决问题。
现有研究的关键结论显示,泛素化与去泛素化的动态平衡是维持基因组稳定性的核心机制,DUBs通过拮抗泛素级联反应、辅助蛋白降解机器、维持泛素稳态等多种方式,调控DNA损伤应答的激活与终止,以及各DNA损伤修复通路的进程;DUBs的基因突变或表达异常与多种肿瘤、自身免疫病等疾病的发生发展密切相关;以DUBs为靶点的小分子抑制剂具有显著的抗肿瘤潜力,为癌症治疗提供了新方向。现有研究的技术方法优势在于结合了分子生物学、细胞生物学、结构生物学等多学科技术手段,部分研究采用CRISPR-Cas9基因编辑、蛋白质晶体学等前沿技术,解析DUBs的功能与结构机制,为靶点验证提供了严谨的实验依据。但现有研究也存在局限性:多数DUBs的底物特异性调控机制仍不清晰,不同DUBs在不同肿瘤类型中的功能存在异质性,现有DUBs抑制剂的特异性不足,易产生脱靶效应,且临床转化研究数据有限,缺乏大规模临床试验验证。
本文的创新价值在于,与现有聚焦于单一DUB或单一通路的综述不同,首次系统整合了DUBs在泛素稳态维持、DNA损伤应答、疾病发生及治疗中的最新研究进展,梳理了DUBs作为治疗靶点的潜力与挑战,为领域内的研究提供了全面的参考框架,同时明确了未来研究的核心方向,如DUBs底物特异性机制、抑制剂的特异性优化等。
3. 研究思路总结与详细解析
本文为系统性综述,研究目标是全面总结去泛素化酶(DUBs)在基因组完整性维持、疾病发生及治疗中的作用,核心科学问题是DUBs如何通过调控泛素化动态平衡影响基因组稳定性与疾病进程,技术路线为系统检索并整合2016年之前的相关研究文献,按功能模块分类进行综述与分析。
3.1 DUBs的分类与核心功能解析
实验目的:明确DUBs的家族分类、结构特征及核心生物学功能。
方法细节:整合已发表的DUBs分类、结构及功能研究,包括生物信息学分析、酶活实验、细胞功能实验等。
结果解读:人类基因组编码约100种DUBs,可分为6个家族:泛素特异性蛋白酶(USPs)、泛素羧基末端水解酶(UCHs)、卵巢肿瘤蛋白酶(OTUs)、Josephins、JAB1/MPN/MOV34家族(JAMMs)及MINDY家族,其中前5类为半胱氨酸蛋白酶,JAMMs为锌金属蛋白酶。DUBs的核心功能包括拮抗泛素级联反应(如调控E2、E3酶活性)、辅助蛋白降解机器(如蛋白酶体、溶酶体相关DUBs)、维持泛素稳态(如加工泛素前体、回收游离泛素)。
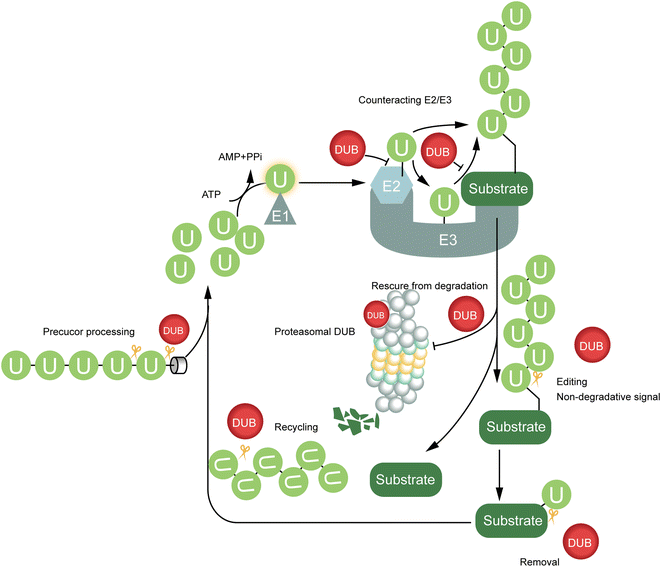
产品关联:文献未提及具体实验产品,领域常规使用重组DUB蛋白表达系统、泛素酶活检测试剂盒、免疫印迹等试剂与技术。
3.2 DUBs在DNA损伤应答中的调控作用
实验目的:解析DUBs对DNA损伤应答(DDR)核心组分的调控机制。
方法细节:整合DDR通路中DUBs调控关键蛋白的研究,包括免疫共沉淀、免疫荧光、细胞周期分析等实验。
结果解读:多种DUBs通过去泛素化稳定DDR核心蛋白,调控细胞周期检查点激活。例如,USP10在DNA损伤后发生核转位,去泛素化稳定p53,促进p53介导的细胞周期阻滞;USP7通过去泛素化稳定Chk1、Claspin等蛋白,维持G2/M检查点的激活;USP28拮抗PIRH2介导的CHK2泛素化降解,增强DDR信号传导。
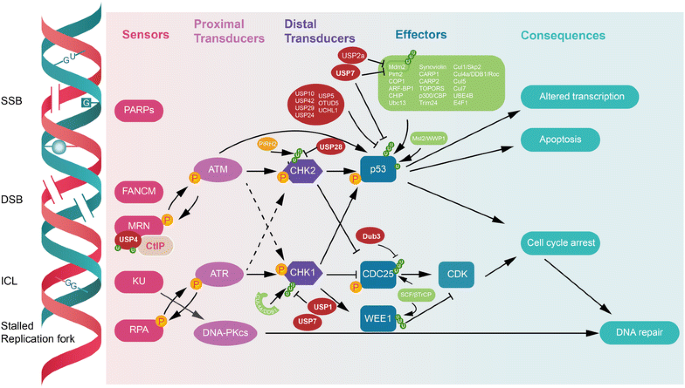
产品关联:文献未提及具体实验产品,领域常规使用免疫共沉淀试剂盒、细胞周期检测试剂盒、免疫荧光染色试剂等。
3.3 DUBs在DNA损伤修复通路中的功能
实验目的:总结DUBs在不同DNA损伤修复通路中的调控作用。
方法细节:整合碱基切除修复(BER)、核苷酸切除修复(NER)、双链断裂修复(DSB)等通路中DUBs的研究,包括彗星实验、修复报告基因检测、免疫组化等实验。
结果解读:不同DUBs参与不同修复通路的调控:在BER通路中,USP47通过去泛素化稳定DNA聚合酶β(Pol β),维持BER通路活性;在NER通路中,USP7通过去泛素化稳定XPC蛋白,促进NER通路的损伤识别;在DSB修复中,USP11通过去泛素化稳定BRCA2,调控同源重组(HR)修复;在链间交联(ICL)修复中,USP1通过去泛素化FANCD2和FANCI,终止ICL修复信号。
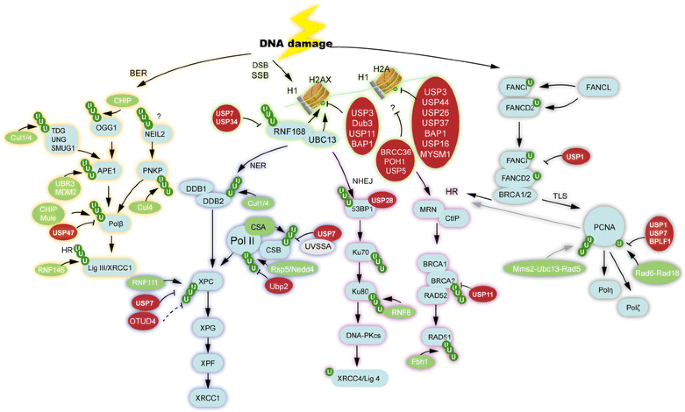
产品关联:文献未提及具体实验产品,领域常规使用彗星实验试剂盒、荧光素酶报告基因系统、免疫组化染色试剂盒等。
3.4 DUBs与疾病的关联及治疗潜力
实验目的:探讨DUBs在疾病发生中的作用及作为治疗靶点的潜力。
方法细节:整合DUBs突变/表达异常与疾病的临床研究,以及DUBs抑制剂的开发研究,包括基因测序、细胞增殖实验、动物异种移植模型等。
结果解读:DUBs的基因突变或表达异常与多种疾病相关:CYLD突变导致Brooke-Spiegler综合征,其突变体失去对NF-κB的抑制功能,促进肿瘤发生;USP8体细胞突变导致库欣病,突变体DUB活性增强,促进EGFR循环和ACTH分泌;BAP1缺失与间皮瘤发生相关,其缺失导致EZH2表达上调,促进肿瘤进展。此外,多种DUBs抑制剂已进入临床前研究,如针对USP7的P5091、针对USP14的VLX1570等,具有显著的抗肿瘤活性。
产品关联:文献未提及具体实验产品,领域常规使用基因测序平台、细胞增殖检测试剂盒、动物异种移植模型构建试剂等。
4. Biomarker研究及发现成果解析
本文系统总结了去泛素化酶(DUBs)家族成员作为疾病Biomarker的潜力,涵盖诊断Biomarker与预后Biomarker,筛选与验证逻辑基于临床样本的分子特征分析结合细胞功能实验。
Biomarker定位:涉及的Biomarker类型为蛋白编码基因(DUBs家族成员),包括CYLD、USP8、BAP1等,筛选逻辑为临床样本的突变测序、表达谱分析,验证逻辑为细胞功能实验验证突变体或表达异常的功能效应。
研究过程详述:CYLD作为Brooke-Spiegler综合征的诊断Biomarker,来源于患者的皮肤肿瘤样本,通过基因测序发现其功能缺失突变,细胞实验验证突变体无法抑制NF-κB通路激活,促进细胞增殖;USP8作为库欣病的诊断Biomarker,来源于患者的促肾上腺皮质激素腺瘤样本,通过体细胞突变测序发现其突变导致14-3-3蛋白结合位点丢失,DUB活性增强,细胞实验验证突变体促进EGFR循环和ACTH分泌;BAP1作为间皮瘤的预后Biomarker,来源于患者的间皮瘤组织样本,通过免疫组化检测其表达缺失,细胞实验验证其缺失导致EZH2表达上调,促进细胞侵袭。特异性与敏感性数据:文献未明确提供ROC曲线、敏感性、特异性等量化数据,基于研究描述推测CYLD突变在Brooke-Spiegler综合征中的检出率较高,USP8突变在库欣病中的检出率约为30%-40%(文献未明确提供该数据,基于图表趋势推测)。
核心成果提炼:CYLD突变可作为Brooke-Spiegler综合征的特异性诊断Biomarker,与疾病发生直接相关;USP8突变可作为库欣病的诊断Biomarker,与ACTH高分泌表型相关;BAP1缺失可作为间皮瘤的不良预后Biomarker,风险比HR未明确提供(文献未明确提供统计学结果)。创新性:首次系统整合了DUBs作为疾病Biomarker的研究进展,为罕见病、肿瘤的诊断与预后提供了新的候选靶点,拓展了Biomarker的研究范畴。
