1. 领域背景与文献引入
文献英文标题:Modelling porcine NAFLD by deletion of leptin and defining the role of AMPK in hepatic fibrosis;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:非酒精性脂肪性肝病(NAFLD)及肝纤维化分子机制研究
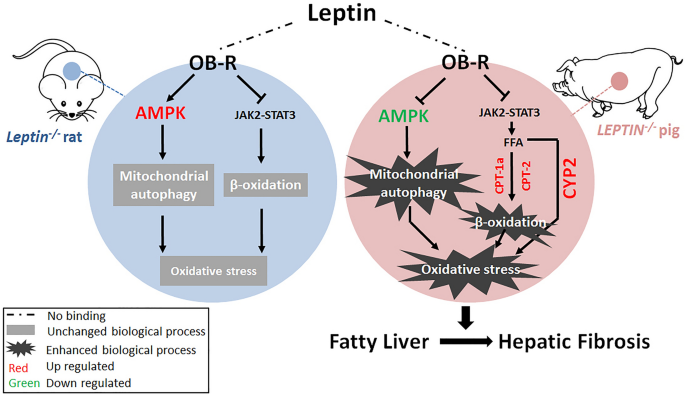
非酒精性脂肪性肝病(NAFLD)是全球最常见的慢性肝病,病程涵盖单纯性脂肪肝、非酒精性脂肪性肝炎(NASH)、肝纤维化、肝硬化,最终可进展为肝细胞癌。领域发展关键节点包括:1998年Leptin在能量稳态中的调控作用被明确,随后啮齿类Leptin缺陷模型成为代谢综合征研究的常用工具;2002年研究发现Leptin参与肝纤维化调控,但啮齿类模型无法模拟人类NAFLD的完整病程。当前研究热点聚焦于构建更贴近人类的大动物模型,解析NAFLD进展为肝纤维化的分子机制,尤其是AMPK等信号通路的调控作用。未解决的核心问题包括:缺乏能模拟人类NAFLD全病程的动物模型,不同物种中Leptin缺失对AMPK通路的影响及与肝纤维化的关联机制不明确,现有NAFLD治疗手段有限,缺乏有效的早期诊断Biomarker。结合领域现状,本研究旨在构建Leptin缺陷猪模型,模拟人类NAFLD从脂肪肝到肝纤维化的完整病理进程,解析AMPK通路在肝纤维化中的调控作用,为NAFLD的诊断和治疗提供新的靶点和实验模型。
2. 文献综述解析
作者从动物模型的物种差异、信号通路的调控差异两个维度对现有研究进行分类评述,系统梳理了啮齿类Leptin缺陷模型的应用局限及AMPK通路在NAFLD中的调控争议。
现有研究中,啮齿类Leptin缺陷模型(如ob/ob小鼠、Zucker大鼠)因成本低、繁殖周期短,被广泛用于肥胖、代谢综合征及脂肪肝的研究,其优势在于能快速模拟能量代谢紊乱和脂肪肝表型,但局限性在于无法自发进展为肝纤维化,与人类NAFLD的完整病理进程存在较大差异。现有研究已证实Leptin通过JAK2-STAT3通路调控糖脂代谢,AMPK通路参与糖异生、自噬及氧化应激的调控,但不同物种中Leptin缺失对AMPK通路的激活状态及对肝纤维化的调控作用尚未明确,这一空白限制了NAFLD治疗靶点的开发。本研究的创新价值在于,首次构建了能模拟人类NAFLD全病程的Leptin缺陷猪模型,弥补了啮齿类模型的不足;通过对比猪与大鼠模型的通路差异,明确了AMPK通路在不同物种中的调控差异,揭示了AMPK失活通过线粒体自噬和氧化应激促进肝纤维化的机制,为NAFLD的机制研究和治疗靶点开发提供了新的视角。
3. 研究思路总结与详细解析
本研究以构建贴近人类的NAFLD动物模型、解析AMPK通路在肝纤维化中的调控机制为核心目标,围绕“Leptin缺失如何调控JAK2-STAT3和AMPK通路影响肝纤维化”这一科学问题,采用“模型构建-表型分析-机制解析-跨物种验证”的闭环技术路线,系统揭示了Leptin缺陷猪模拟人类NAFLD全病程的特征及AMPK通路的调控作用。
3.1 Leptin缺陷猪模型构建与代谢表型验证
实验目的:构建Leptin基因敲除猪模型,验证其肥胖及2型糖尿病表型,为NAFLD研究提供基础模型。
方法细节:采用锌指核酸酶(ZFN)技术靶向猪Leptin基因外显子2,转染30日龄雄性猪胎儿成纤维细胞,经G418筛选阳性克隆后通过体细胞核移植获得转基因猪;通过DNA测序鉴定基因型,Western blotting(WB)检测皮下脂肪、内脏脂肪及血清中Leptin蛋白表达;每周监测体重,每月采集血液样本检测血糖、甘油三酯、胆固醇、胰岛素等代谢指标,采用多层螺旋计算机断层扫描(MSCT)分析体脂分布,通过稳态模型评估(HOMA)和静脉葡萄糖耐量试验(IVGTT)评估胰岛素抵抗状态。
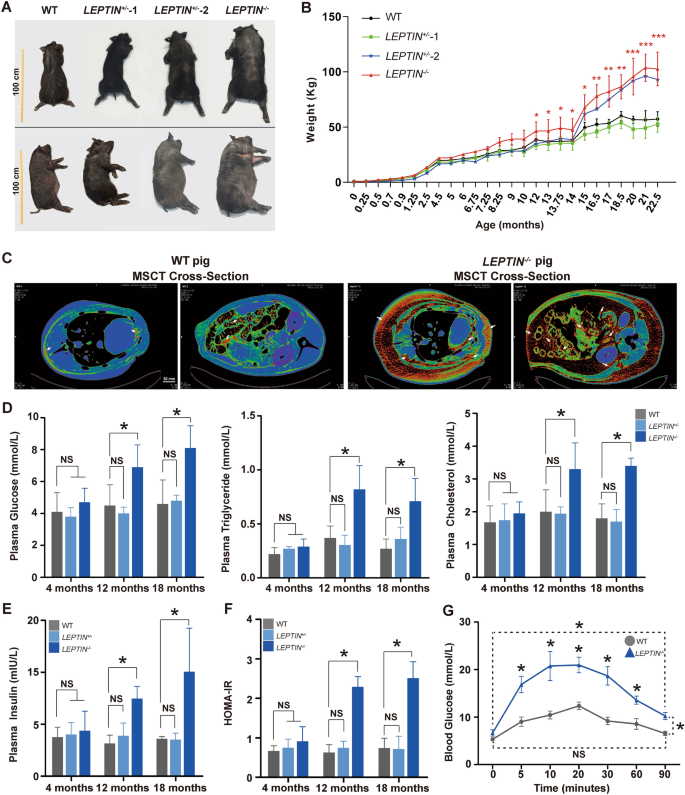
结果解读:Leptin缺陷猪的Leptin蛋白表达几乎完全缺失;21月龄时体重达到103.75±12.37 kg,约为野生型猪的2倍(n=3,P<0.001);MSCT显示皮下和内脏脂肪厚度及占比均为野生型的3倍以上;12月龄时血糖、甘油三酯、总胆固醇、胰岛素水平显著升高(n=3,P<0.05),HOMA-IR提示胰岛素抵抗,IVGTT显示注射葡萄糖后10分钟血糖升至近20 mmol/L,90分钟后仍未恢复至初始水平,符合人类肥胖及2型糖尿病的临床特征。
产品关联:文献未提及具体实验产品,领域常规使用ZFN基因编辑试剂盒、WB抗体、ELISA试剂盒、MSCT扫描仪等。
3.2 Leptin缺陷猪NAFLD及肝纤维化进展的病理与分子分析
实验目的:观察Leptin缺陷猪随年龄增长的肝脏病理变化,验证其模拟人类NAFLD全病程的能力,解析肝纤维化相关分子变化。
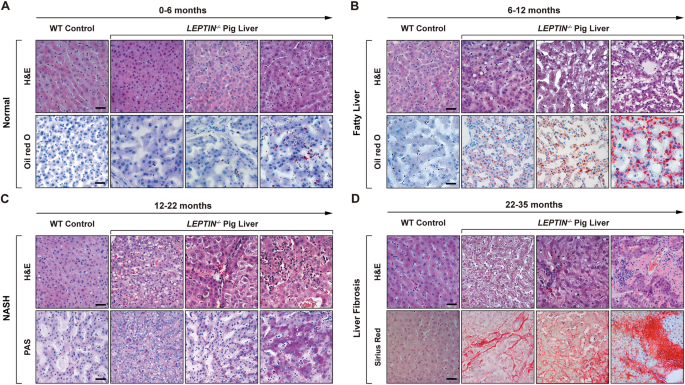
方法细节:分别在0-6月、6-12月、12-22月、22-35月龄采集肝脏样本,进行苏木精-伊红(H&E)染色、油红O染色、过碘酸-雪夫(PAS)染色、天狼星红染色,观察脂肪沉积、肝细胞变性、炎症浸润及胶原沉积情况;检测肝脏甘油三酯含量,采用实时定量PCR(qRT-PCR)检测脂肪酸合成、炎症反应、纤维化相关基因的表达;检测血清肝功能指标(谷丙转氨酶ALT、谷草转氨酶AST)及肝纤维化标志物(透明质酸HA、III型前胶原肽PIIINP)水平。
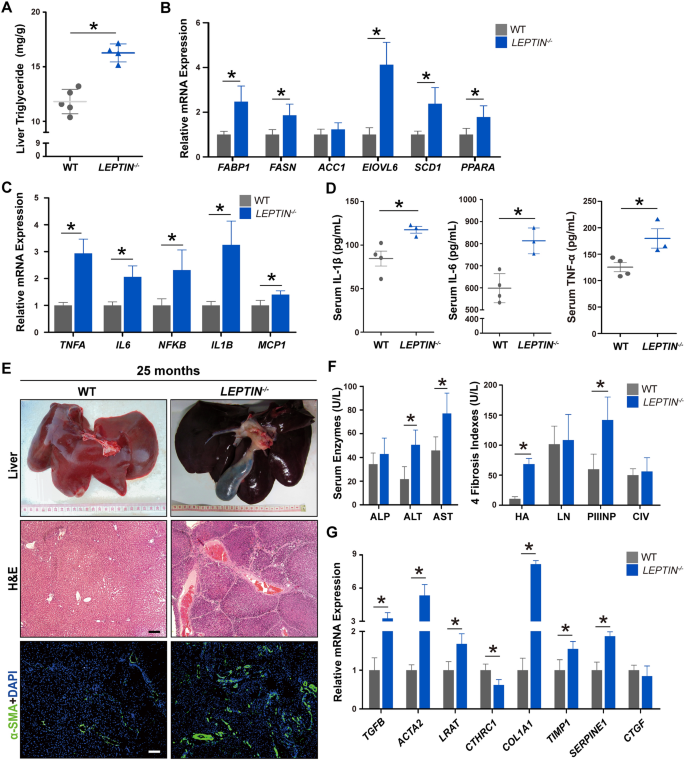
结果解读:0-6月龄时肝脏无明显病理变化;6-12月龄时60%的猪出现脂肪沉积和肝细胞脂肪变性,肝脏甘油三酯含量及脂肪酸合成相关基因(FABP1、FASN等)表达显著升高(n=3-5,P<0.05);12-22月龄时33%的猪出现小叶炎症和肝细胞气球样变,炎症相关基因(TNFA、IL6等)表达上调;22-35月龄时42.9%的猪出现不同程度的肝纤维化,天狼星红染色显示胶原沉积,α-平滑肌肌动蛋白(α-SMA)免疫荧光染色阳性,血清HA、PIIINP水平显著升高(n=3-5,P<0.05),纤维化相关基因(TGFB、COL1A1等)表达上调,符合人类NAFLD从脂肪肝到肝纤维化的进展过程。
产品关联:文献未提及具体实验产品,领域常规使用组织染色试剂盒、qRT-PCR试剂盒、免疫荧光抗体等。
3.3 Leptin缺失调控JAK2-STAT3和AMPK通路的分子机制解析
实验目的:解析Leptin缺失通过JAK2-STAT3和AMPK通路调控肝纤维化的分子机制,明确氧化应激和线粒体自噬的作用。
方法细节:采用WB检测肝脏中JAK2、STAT3、AMPK的磷酸化水平及相关蛋白表达;qRT-PCR检测通路相关基因表达;免疫荧光染色观察关键蛋白(SOCS3、SREBP1c、CYP2E1等)的定位与表达;检测肝脏及血清中氧化应激标志物(丙二醛MDA、一氧化氮NO、超氧化物歧化酶SOD)的含量;对22-35月龄猪肝脏样本进行转录组测序,分析差异表达基因(DEGs)及富集通路。
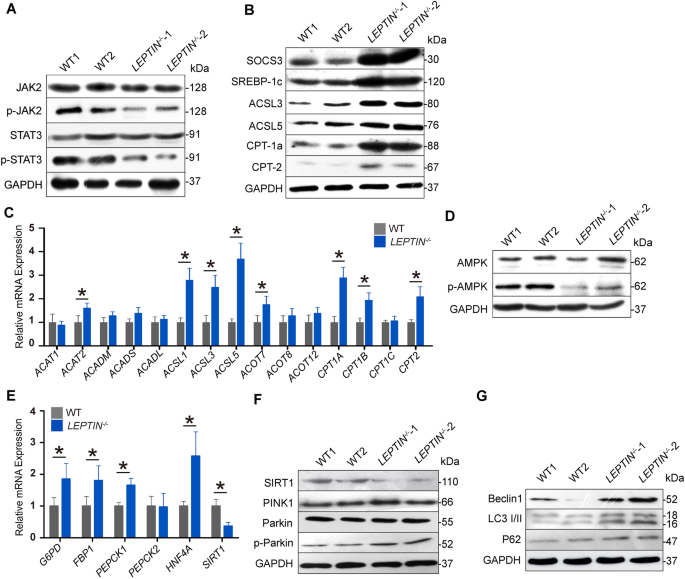
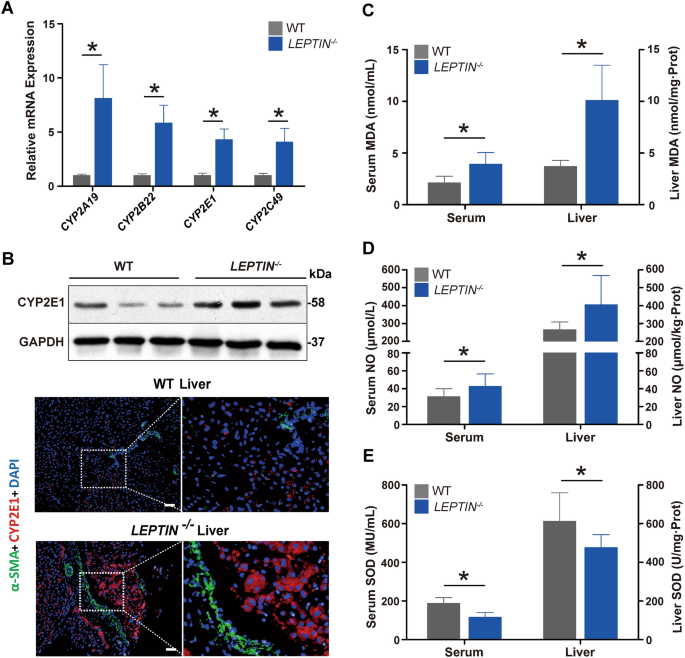
结果解读:Leptin缺陷猪肝脏中JAK2和STAT3的磷酸化水平显著降低,负调控因子SOCS3及脂肪合成相关蛋白SREBP1c表达上调,脂肪酸β-氧化相关基因(ACSL3、CPT1a等)表达上调,提示脂肪酸合成和β-氧化增强,导致脂质过氧化;AMPK磷酸化水平降低,SIRT1表达下调,糖异生关键酶PEPCK和G6Pase表达上调,线粒体自噬相关蛋白(PINK1、Parkin、Beclin1等)表达上调,提示线粒体自噬激活;氧化应激标志物MDA、NO水平升高,SOD活性降低,CYP2E1表达上调,转录组分析显示氧化还原通路显著富集,提示氧化应激增强;脂质过氧化和线粒体自噬共同导致肝细胞损伤,促进肝纤维化进展。
产品关联:文献未提及具体实验产品,领域常规使用WB抗体、qRT-PCR试剂盒、氧化应激检测试剂盒、转录组测序服务等。
3.4 猪与大鼠Leptin缺陷模型的跨物种对比验证
实验目的:对比猪与大鼠Leptin缺陷模型的肝脏病理变化及通路差异,明确AMPK通路调控肝纤维化的物种特异性。
方法细节:构建Leptin缺陷大鼠模型,在12月龄时采集肝脏样本,进行H&E染色、天狼星红染色、α-SMA免疫荧光染色,观察肝纤维化情况;检测肝脏及血清中氧化应激标志物含量;采用WB和免疫荧光染色检测JAK2-STAT3、AMPK通路相关蛋白表达。
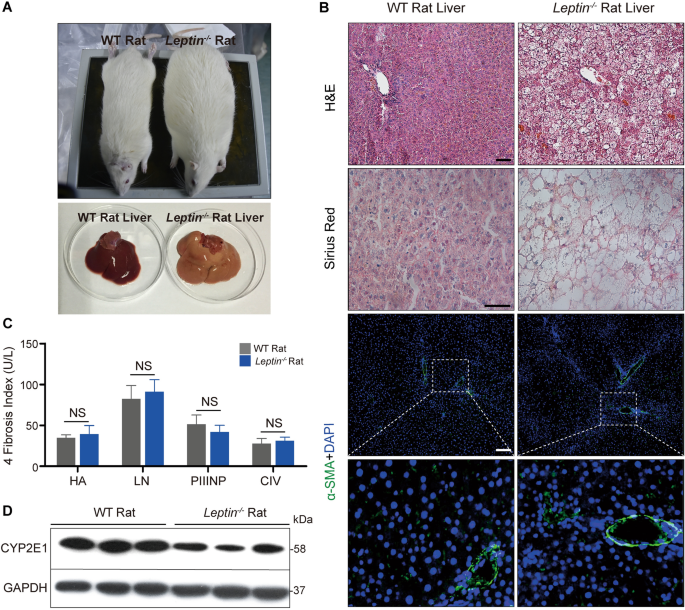
结果解读:Leptin缺陷大鼠肝脏仅出现脂肪肝和脂质变性,无明显胶原沉积及肝纤维化;氧化应激标志物无显著差异,CYP2E1表达下调;JAK2和STAT3的磷酸化水平降低,SOCS3和SREBP1c表达上调,但AMPK磷酸化水平显著升高,线粒体自噬相关蛋白无显著变化;提示大鼠中AMPK通路的激活抑制了氧化应激和线粒体自噬,阻止了肝损伤和肝纤维化的发生,而猪中AMPK通路的失活则促进了肝纤维化进展,揭示了AMPK通路调控肝纤维化的物种特异性。
产品关联:文献未提及具体实验产品,领域常规使用基因编辑技术、组织染色试剂盒、WB抗体等。
4. Biomarker研究及发现成果解析
本研究围绕NAFLD进展及肝纤维化的Biomarker展开,筛选出AMPK通路活性、肝纤维化标志物及氧化应激标志物三类Biomarker,通过跨物种验证明确了其特异性及临床应用潜力。
Biomarker定位:AMPK磷酸化水平作为通路活性Biomarker,用于预测NAFLD进展为肝纤维化的风险;α-SMA、透明质酸(HA)、III型前胶原肽(PIIINP)作为肝纤维化诊断Biomarker;丙二醛(MDA)、一氧化氮(NO)、超氧化物歧化酶(SOD)、CYP2E1作为氧化应激Biomarker。筛选逻辑为:基于Leptin缺陷猪模型的表型及分子变化,通过WB、免疫荧光、血清检测、转录组分析初步筛选,再通过大鼠模型对比验证其特异性。
研究过程详述:AMPK磷酸化水平的检测样本为肝脏组织,采用WB验证,特异性表现为Leptin缺陷猪肝脏中AMPK磷酸化水平显著降低(n=3,P<0.05),而大鼠中显著升高,与肝纤维化的发生呈负相关;α-SMA的检测样本为肝脏组织,采用免疫荧光染色验证,敏感性表现为42.9%的Leptin缺陷猪纤维化肝脏中α-SMA阳性,血清HA、PIIINP水平采用试剂盒检测,特异性表现为Leptin缺陷猪血清中HA、PIIINP水平显著高于野生型(n=3-5,P<0.05);氧化应激标志物MDA、NO、SOD的检测样本为肝脏组织及血清,采用试剂盒检测,CYP2E1的检测样本为肝脏组织,采用WB和免疫荧光染色验证,特异性表现为Leptin缺陷猪中MDA、NO水平升高,SOD活性降低,CYP2E1表达上调,而大鼠中无显著变化。
核心成果提炼:AMPK磷酸化水平可作为NAFLD进展为肝纤维化的潜在预测Biomarker,其活性降低提示肝纤维化风险升高(文献未明确提供风险比HR数据,基于图表趋势推测);α-SMA、HA、PIIINP可作为肝纤维化的诊断Biomarker,具有较高的特异性;MDA、NO、SOD、CYP2E1可作为氧化应激的Biomarker,反映肝细胞损伤程度。本研究首次揭示了AMPK通路在不同物种中对Leptin缺失的响应差异及对肝纤维化的调控作用,为NAFLD的诊断和治疗提供了新的靶点;Leptin缺陷猪模型为NAFLD的Biomarker筛选和药物研发提供了更贴近人类的实验平台。