1. 领域背景与文献引入
文献英文标题:Simultaneous stimulation of GABA and beta adrenergic receptors stabilizes isotypes of activated adenylyl cyclase heterocomplex;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:神经信号转导(G蛋白偶联受体调控腺苷酸环化酶的机制研究)
G蛋白偶联受体(GPCR)是细胞信号转导的核心调控节点,其通过偶联不同的G蛋白(Gs、Gi等)调控下游效应器腺苷酸环化酶(AC)的活性,进而控制第二信使cAMP的水平,该通路在突触可塑性、学习记忆等生理过程中发挥关键作用。领域共识:海兔缩鳃反射、果蝇学习记忆突变体等经典模型已证实,cAMP信号的精准时空调控是突触可塑性的分子基础,其中AC II亚型是同时响应Ca²+和Gs信号的关键分子,rutabaga突变体(AC II基因缺陷)会导致严重的学习记忆障碍。
1990年代后,研究人员发现一个反常现象:同时激活Gs偶联的β肾上腺素能受体和Gi偶联的GABA_B受体时,海马神经元中的cAMP水平并非如预期的相互抵消,反而出现大幅升高,且该效应主要由AC II亚型介导,但具体分子机制尚未阐明。针对这一领域空白,本研究聚焦于G蛋白亚基(Gαs、Gβγ)与AC复合物的动态相互作用,解析两种受体信号协同调控AC活性的分子基础,为突触信号整合的机制提供新的实验证据与理论见解。
2. 文献综述解析
作者以“从整体生理现象到分子亚型调控”的逻辑梳理领域研究,先总结cAMP信号在学习记忆中的核心作用,再分述不同AC亚型的调控特性,最终聚焦于同时激活Gs/Gi受体时cAMP反常升高的机制空白。
现有研究的关键结论包括:海兔和果蝇的模型明确了cAMP的精准调控是突触可塑性和学习记忆的核心,AC II亚型是同时响应Ca²+和Gs激活的关键分子;经典药理学研究证实,Gs偶联受体激活AC可升高cAMP水平,Gi偶联受体抑制AC可降低cAMP水平,但在大鼠海马神经元中同时激活两类受体会产生cAMP的反常大幅升高,且该效应依赖于AC II亚型。技术方法优势方面,早期研究通过基因敲除/突变体模型明确了AC亚型的生理功能,使用特异性激动剂、拮抗剂等药理学工具验证了受体与信号通路的关联。局限性在于,现有研究仅确定了AC II在该反常现象中的核心地位,但未阐明G蛋白亚基与AC复合物的动态相互作用机制,也未明确Gβγ对Gαs GTP酶活性的调控作用,无法解释两种相反信号如何协同提升cAMP水平。
本研究的创新价值在于,首次从G蛋白亚基与AC复合物的结合动力学和酶活性调控角度,解析了同时激活Gs/Gi受体时cAMP反常升高的分子机制,揭示了Gβγ(来自Gi)与Gαs对AC的协同调控作用,填补了该领域的机制空白,为突触信号整合的分子模型提供了新的实验依据。
3. 研究思路总结与详细解析
本研究以“同时激活GABA_B受体和β肾上腺素能受体时cAMP反常升高的分子机制”为核心科学问题,采用“药理学验证现象→分离复合物分析组成→检测酶活性解析调控”的闭环技术路线,利用大鼠脑突触体细胞膜模型,系统解析了G蛋白亚基与AC复合物的动态相互作用及对AC活性的调控机制。
3.1 突触体细胞膜制备与cAMP水平检测
本环节的核心实验目的是验证同时激活β肾上腺素能受体和GABA_B受体对cAMP合成的协同促进作用,明确该效应的受体依赖性。实验方法上,研究人员通过差速离心和密度梯度离心制备大鼠脑突触体细胞膜,分别用50 nM异丙肾上腺素(β受体激动剂)、巴氯芬(GABA_B受体激动剂)单独或同时处理细胞膜,或先使用100 nM拮抗剂(普萘洛尔、saclofen)预处理10分钟后再用激动剂联合处理,最后通过放射免疫分析(RIA)检测cAMP的合成水平。
结果显示,同时使用异丙肾上腺素和巴氯芬处理时,cAMP合成水平为340±55 pmol/min/mg(n=3,P<0.005),远高于单独使用异丙肾上腺素(105±30 pmol/min/mg,n=3,P<0.01)或巴氯芬(15±10 pmol/min/mg,n=3)的水平;使用拮抗剂预处理后,联合激动剂处理的cAMP水平恢复至单独激动剂处理的水平,证明该协同效应严格依赖于两种受体的激活。
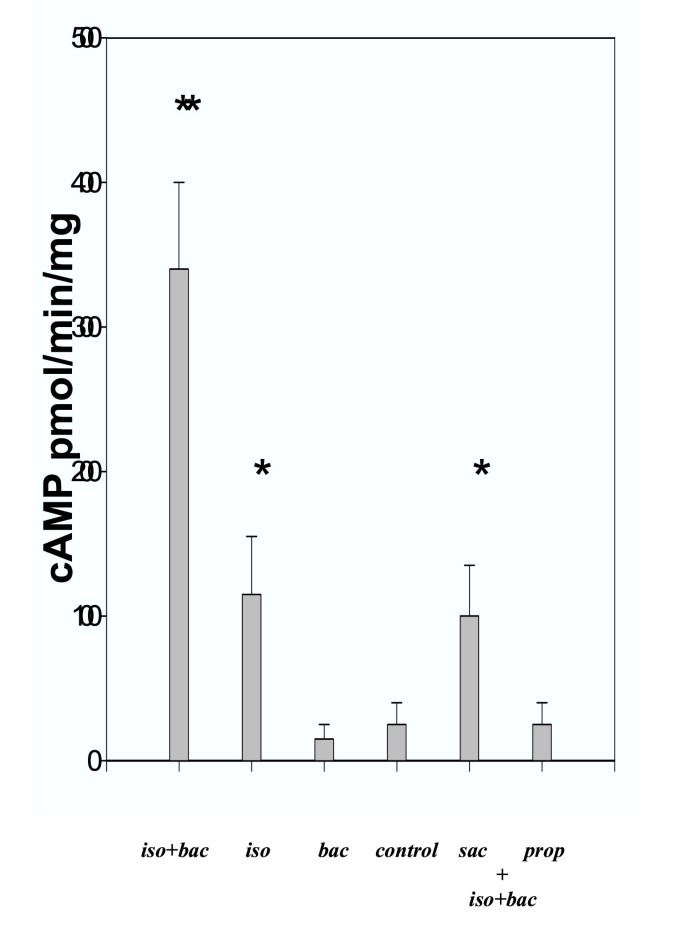
实验所用关键产品:NEN的cAMP RIA检测试剂盒,Sigma的异丙肾上腺素、巴氯芬、普萘洛尔、saclofen等药理学试剂。
3.2 AC复合物的分离与G蛋白亚基结合分析
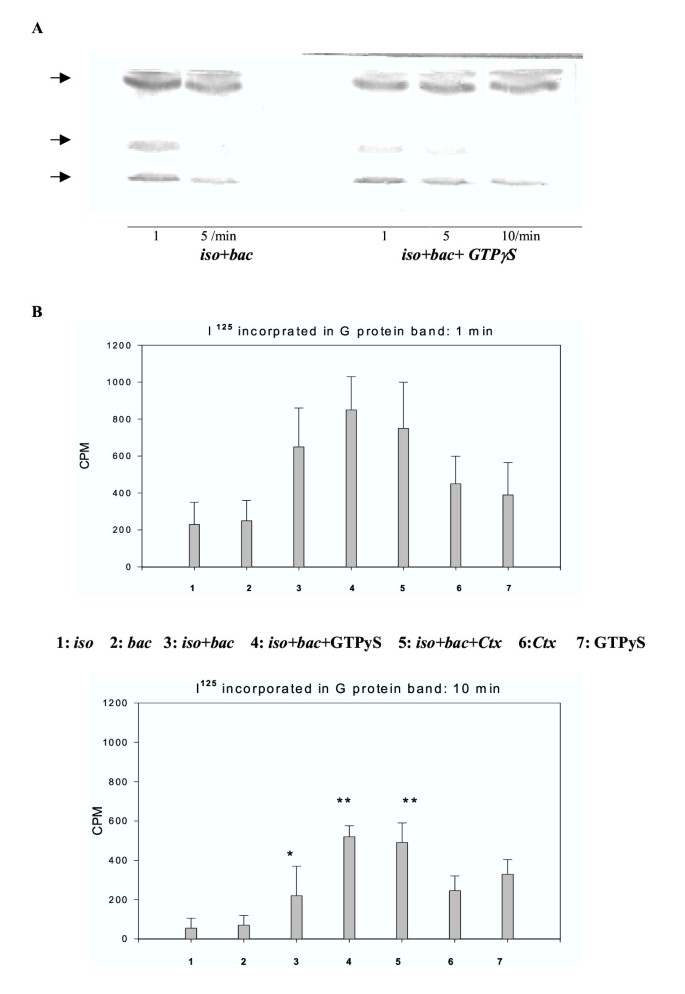
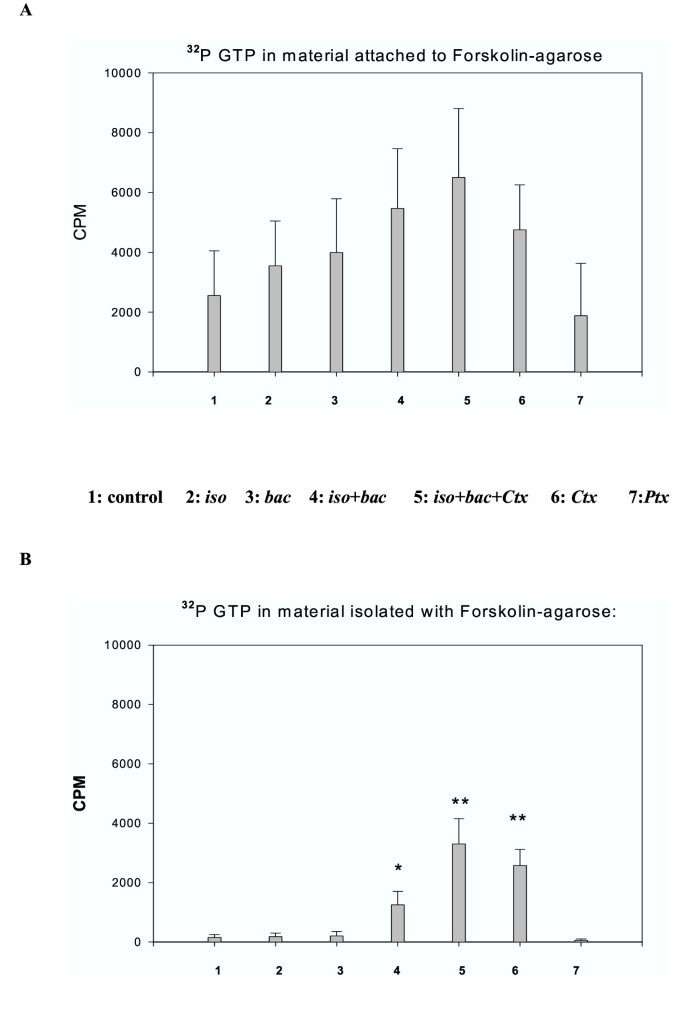
本环节的核心目的是分析Gαs和Gβγ与AC复合物的结合特性,明确同时激活两种受体对亚基结合动力学的影响。实验方法上,研究人员用非离子去垢剂溶解细胞膜,通过福斯高林-琼脂糖(Forskolin-agarose)Pull-down实验分离AC复合物;使用霍乱毒素(抑制Gαs的GTP酶活性,锁定其激活状态)和百日咳毒素(解偶联Gi与受体,阻断Gβγ释放)处理细胞膜,通过放射性ADP-核糖基化标记激活的Gαs,或通过免疫印迹(Western blot)检测Gβγ与AC的结合;同时使用Bolton Hunter碘化法量化亚基的结合水平,分析不同处理条件下的亚基结合比例。
结果显示,同时激活两种受体时,结合到AC复合物上的Gαs水平显著高于单独激活β受体的水平,如1分钟时联合处理组的放射性标记信号为300±80 cpm,单独处理组为180±50 cpm(n=3,P<0.01);Gβγ(来自Gi)与AC的结合在同时激活两种受体时更稳定,解离动力学实验显示联合处理组的Gβγ在AC复合物中的留存时间显著长于单独激活GABA_B受体的组;百日咳毒素处理后,Gβγ与AC的结合显著降低,证明Gβγ来源于Gi偶联的GABA_B受体。
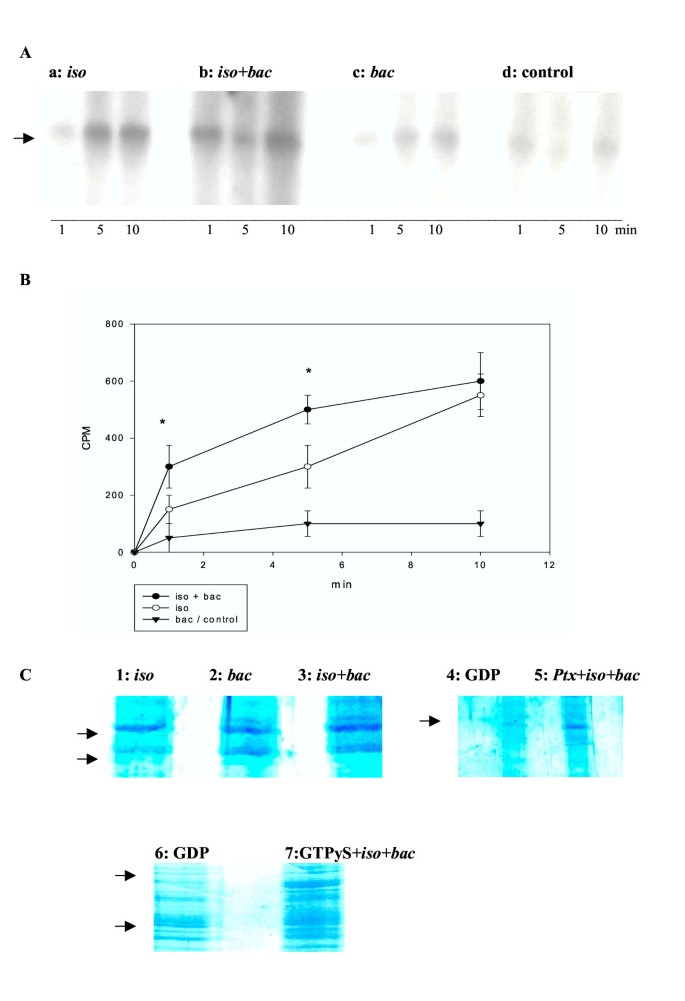
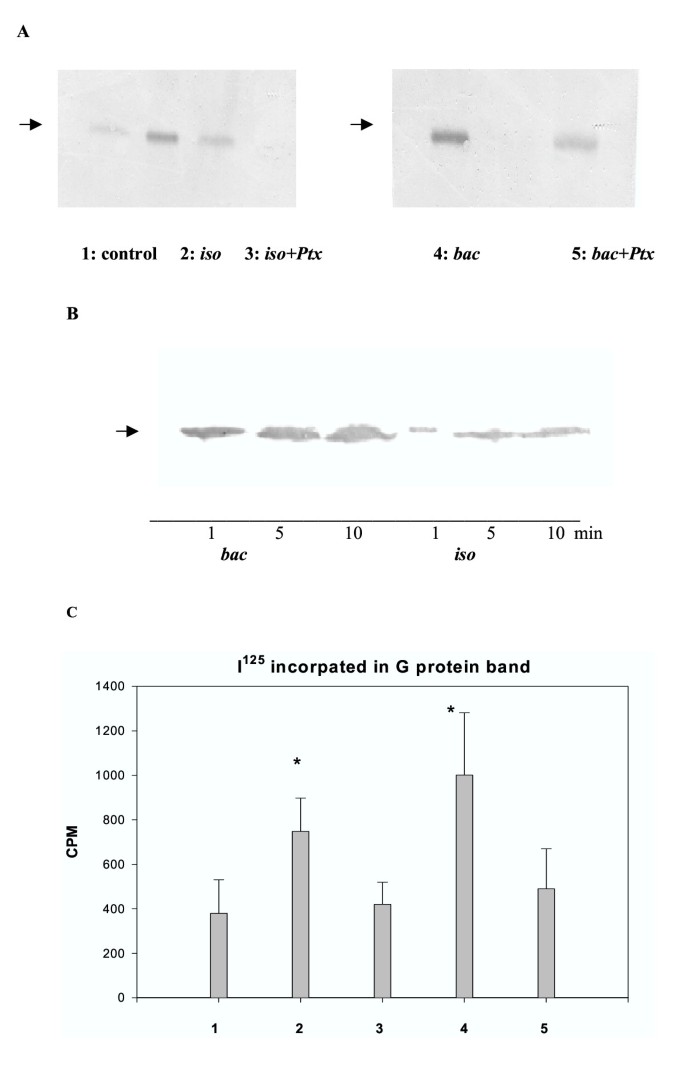
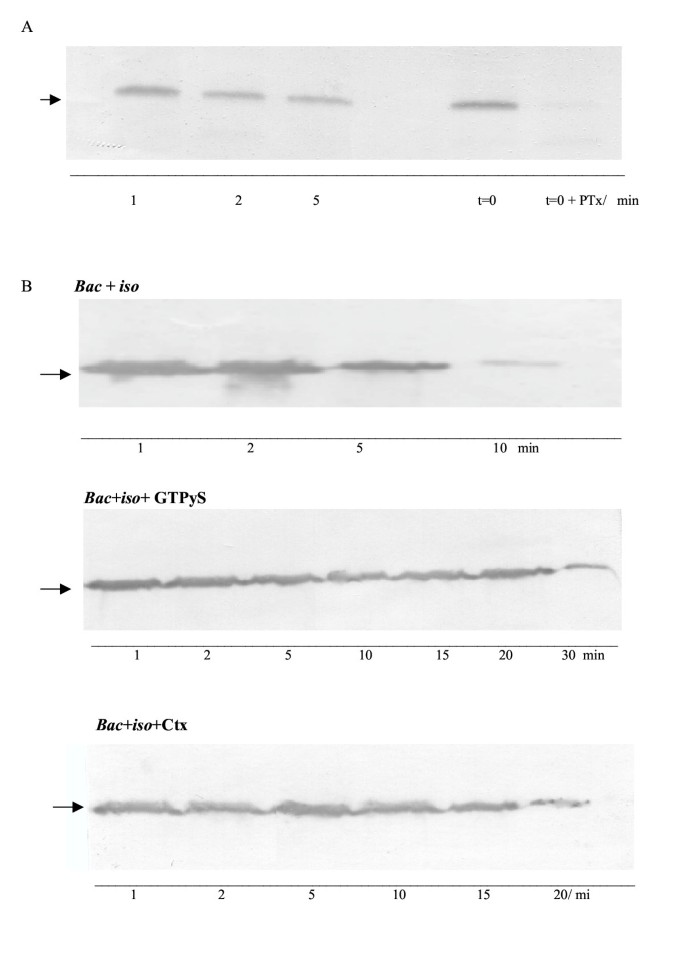
实验所用关键产品:Santa Cruz的抗Gβ多克隆抗体,Sigma的福斯高林-琼脂糖、霍乱毒素、百日咳毒素,NEN的Bolton Hunter碘化试剂。
3.3 Gαs的GTP酶活性检测
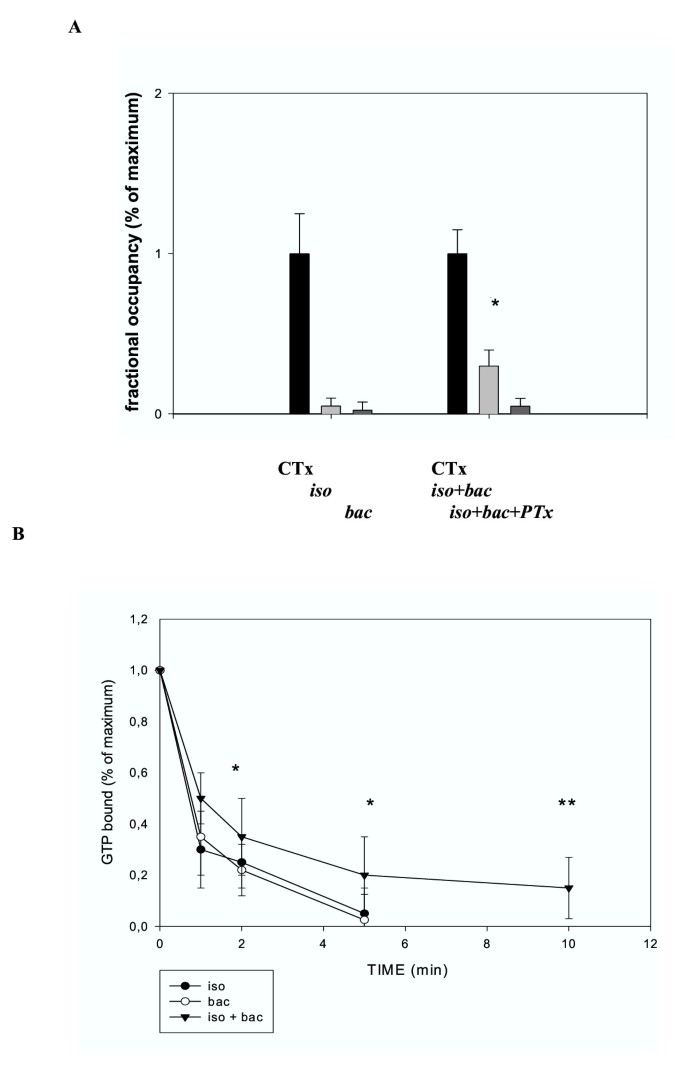
本环节的核心目的是验证Gβγ对AC结合的Gαs的GTP酶活性的调控作用,明确其对Gαs激活状态的影响。实验方法上,研究人员使用[γ-³²P]-GTP标记Gαs,通过单周转GTP酶实验检测不同处理条件下GTP的水解速率;在同时激活两种受体的条件下,检测Gαs的GTP水解分数和剩余结合的GTP水平,分析Gβγ对Gαs酶活性的调控效应。
结果显示,同时激活两种受体时,Gαs的GTP酶活性显著降低,10分钟时的GTP水解分数为0.3±0.1,远低于单独激活β受体(0.05±0.05)或GABA_B受体(0.05±0.1)的水平(n=5,P<0.01);单周转实验显示,5分钟时联合处理组剩余的[γ-³²P]-GTP水平为0.25±0.15,显著高于单独处理组的0.05(n=3,P<0.05),证明Gβγ(来自Gi)抑制了Gαs的GTP酶活性,延长了Gαs的激活状态,从而持续激活AC合成cAMP。
实验所用关键产品:NEN的[γ-³²P]-GTP,Sigma的相关试剂。
4. Biomarker研究及发现成果
本研究未涉及疾病诊断或预后相关的传统生物标志物,而是鉴定了一种参与突触信号整合的功能分子复合物——Gαs-Gβγ-AC II复合物,该复合物作为突触信号的“分子检测器”,介导了不同GPCR信号的协同调控。其筛选与验证逻辑为:从整体cAMP反常升高的生理现象出发,通过药理学工具锁定GABA_B和β肾上腺素能受体通路,再通过Pull-down实验分离复合物,结合动力学分析和酶活性检测验证其功能特性。
该功能复合物来源于大鼠脑突触体细胞膜,通过福斯高林-琼脂糖Pull-down实验分离获得,研究人员使用放射性标记、免疫印迹、单周转GTP酶实验等方法验证了其组成与功能。特异性方面,该复合物的形成严格依赖于同时激活GABA_B和β肾上腺素能受体,百日咳毒素处理可阻断Gβγ的结合,证明其特异性来自Gi偶联的Gβγ亚基;功能数据显示,该复合物可使cAMP合成水平提升约3.2倍(n=3,P<0.005),同时使Gαs的GTP酶活性降低约6倍(n=5,P<0.01)。
核心成果提炼:本研究首次发现,GABA_B受体偶联的Gi释放的Gβγ亚基,与β肾上腺素能受体偶联的Gs释放的Gαs亚基,可协同结合到AC II亚型上,Gβγ通过抑制Gαs的GTP酶活性,延长Gαs的激活状态,从而大幅提升cAMP的合成水平。该发现揭示了突触信号整合的新机制,即不同GPCR的相反信号可通过G蛋白亚基与AC复合物的动态相互作用实现协同调控,为学习记忆等依赖突触可塑性的生理过程的分子机制提供了新的理论基础。本研究未涉及疾病相关的预后或诊断数据,所有成果均聚焦于基础信号转导机制。
