1. 领域背景与文献引入
文献英文标题:Designing a chimeric subunit vaccine for influenza virus, based on HA2, M2e and CTxB: a bioinformatics study;发表期刊:BMC Molecular and Cell Biology;影响因子:未公开;研究领域:流感病毒广谱疫苗生物信息学设计。
领域共识:甲型流感病毒是引发全球季节性流感和大流行的主要病原体,1918年H1N1大流行导致近5000万人死亡,其表面抗原血凝素(HA)和神经氨酸酶(NA)易发生抗原漂移与转换,使得现有季节性疫苗保护范围有限。传统流感疫苗包括灭活疫苗和减毒活疫苗,但存在病毒重组风险、鸡蛋培养导致的过敏反应等安全问题;病毒载体疫苗则有基因组整合引发恶性病变的潜在风险。亚单位疫苗凭借安全性高、可精准靶向保守抗原的优势,成为广谱流感疫苗研发的热点,但目前仍面临抗原免疫原性不足、融合蛋白结构稳定性差等未解决问题。生物信息学技术的发展为疫苗设计提供了高效的虚拟筛选与优化手段,可在实验前预测疫苗的结构、免疫原性及理化性质,减少实验成本与周期。
针对现有流感疫苗广谱性不足、M2e保守抗原免疫原性低、缺乏系统的抗原-佐剂-连接子组合优化等研究空白,本研究通过生物信息学方法,系统筛选最优佐剂与连接子,构建基于HA2、M2e保守抗原和CTxB佐剂的嵌合亚单位疫苗,旨在获得兼具结构稳定性与广谱免疫原性的流感疫苗候选,为后续实验研发提供理论依据。
2. 文献综述解析
作者对领域内现有研究的分类维度主要包括疫苗技术类型、佐剂类型及连接子功能三类。
现有研究关键结论显示,传统灭活与减毒活疫苗是目前临床唯一使用的流感疫苗,但存在病毒重组、过敏反应等安全隐患;病毒载体疫苗虽能诱导细胞免疫,但存在基因组整合风险;亚单位疫苗因仅包含病毒抗原成分,安全性显著提升,且可靶向HA2、M2e等保守抗原,有望实现广谱保护,但需解决抗原免疫原性不足、融合蛋白结构不稳定等问题。佐剂研究方面,CTxB(霍乱毒素B亚单位)因具有黏膜递送能力、无细胞毒性且能提升抗原稳定性,被认为是亚单位疫苗的理想佐剂;连接子作为融合蛋白的关键组成,刚性连接子可维持蛋白结构稳定性,柔性连接子则易导致蛋白构象波动。现有研究的局限性在于,多仅关注单一佐剂或连接子的应用,缺乏系统的抗原-佐剂-连接子组合优化,且未充分验证连接子对抗原表位的影响,M2e的低免疫原性问题也未得到有效解决。
本研究的创新价值在于,首次系统比较4种黏膜佐剂(CTxB、STxB、LTB、ASP-1)与12种连接子(6种刚性、6种柔性)的组合效果,通过生物信息学工具筛选出最优组合,构建了结构稳定、保留抗原表位的嵌合亚单位疫苗;同时,通过分子动力学模拟验证了连接子对疫苗结构的影响,为流感广谱亚单位疫苗的设计提供了系统的优化策略,弥补了现有研究缺乏多维度组合筛选的不足。
3. 研究思路总结与详细解析
本研究的整体研究目标是设计兼具结构稳定性与广谱免疫原性的甲型流感嵌合亚单位疫苗,核心科学问题为如何通过优化抗原-佐剂-连接子的组合,在维持HA2、M2e保守抗原构象与表位的同时,提升疫苗的稳定性与免疫原性,技术路线遵循“组合筛选→结构建模→表位验证→理化分析”的闭环逻辑。
3.1 抗原与佐剂组合筛选
实验目的是筛选出能形成稳定融合蛋白的抗原-佐剂组合,解决M2e免疫原性低及融合蛋白结构不稳定的问题。方法细节为从NCBI数据库获取H7N9亚型流感病毒的HA2、M2e保守抗原序列,以及CTxB、STxB、LTB、ASP-1四种佐剂的蛋白序列,通过ProtParam在线服务器分析不同抗原-佐剂组合的不稳定指数(II)与半衰期,其中不稳定指数低于40判定为蛋白结构稳定。结果解读显示,CTxB作为佐剂时,M2e-CTxB-HA2(MCH)组合的不稳定指数为32.45(远低于40),半衰期达30h,为所有组合中最稳定的形式;而STxB、LTB佐剂的所有组合不稳定指数均高于40,ASP-1组合的不稳定指数接近40,稳定性显著低于CTxB组合。产品关联:文献未提及具体实验产品,领域常规使用NCBI数据库、ProtParam在线分析工具。
3.2 连接子筛选
实验目的是选择最优连接子,进一步提升融合蛋白的结构稳定性,同时避免破坏抗原构象。方法细节为选取6种刚性连接子与6种柔性连接子,分别插入MCH组合的抗原与佐剂之间,通过ProtParam服务器分析不同连接子组合的不稳定指数,筛选出稳定性最优的连接子。结果解读显示,刚性连接子的整体稳定性优于柔性连接子,其中序列为KPKPKP的刚性连接子(LR5)使融合蛋白的不稳定指数最低,结构稳定性最佳。产品关联:文献未提及具体实验产品,领域常规使用蛋白序列分析工具。
3.3 3D结构建模与分子动力学模拟
实验目的是验证连接子插入对疫苗3D结构的影响,评估结构稳定性与构象变化。方法细节为采用Modeller软件进行同源建模,Quark服务器进行从头建模,PyMod软件组装得到MCH(无连接子)与MCH-LR5(含LR5连接子)的3D结构;通过Rampage、ProSA-web评估模型质量,使用Gromacs软件进行100ns分子动力学模拟,分析RMSD(均方根偏差)、RMSF(均方根波动)、回转半径、SASA(溶剂可及表面积)等指标。结果解读显示,MCH-LR5的RMSD为2.02Å,MCH的RMSD为1.4Å,两者差异可忽略,说明连接子插入未导致疫苗结构发生显著变化;RMSF分析显示MCH-LR5的波动为0.5nm,与MCH的0.51nm接近,结构稳定性良好;自由能计算结果显示,LR5连接子可提升融合蛋白的结构稳定性。
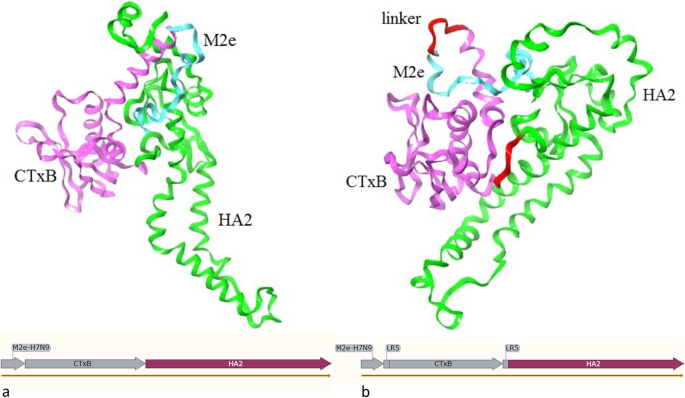
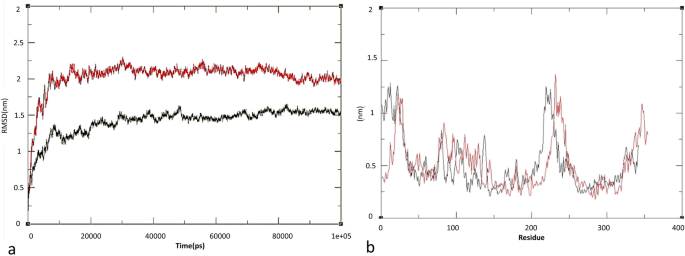
产品关联:文献未提及具体实验产品,领域常规使用Modeller、Gromacs等生物信息学软件。
3.4 表位预测与理化性质分析
实验目的是评估疫苗的免疫原性与理化性质,为后续表达系统选择提供依据。方法细节为使用BepiPred、Ellipro服务器预测B细胞线性与构象表位,NetMHCIIpan、NetMHCIpan服务器预测CD4+T细胞、CTL表位;通过Protein-sol分析蛋白溶解度,DIANNA服务器分析二硫键,Jcat进行密码子优化,NetOglyc、NetNglyc预测翻译后修饰。结果解读显示,MCH-LR5保留了HA2与M2e的核心B细胞表位,CD4+T细胞表位覆盖7种常见MHCII等位基因,具有广谱人群适用性;MCH-LR5的溶解度为0.449,接近大肠杆菌蛋白平均溶解度,适合原核或真核表达系统;翻译后修饰预测显示,MCH-LR5存在1个O-糖基化位点与1个N-糖基化位点,二硫键结构稳定。
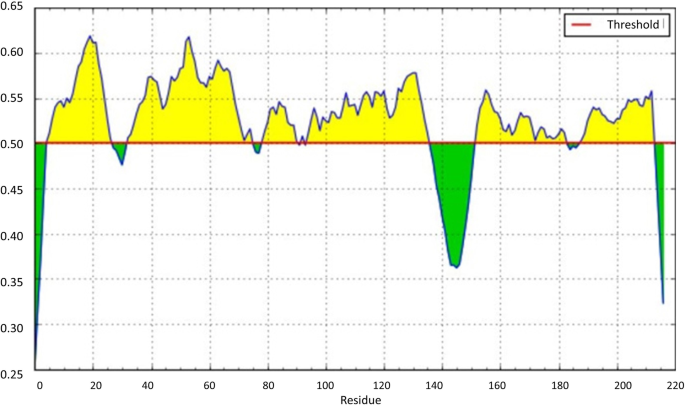

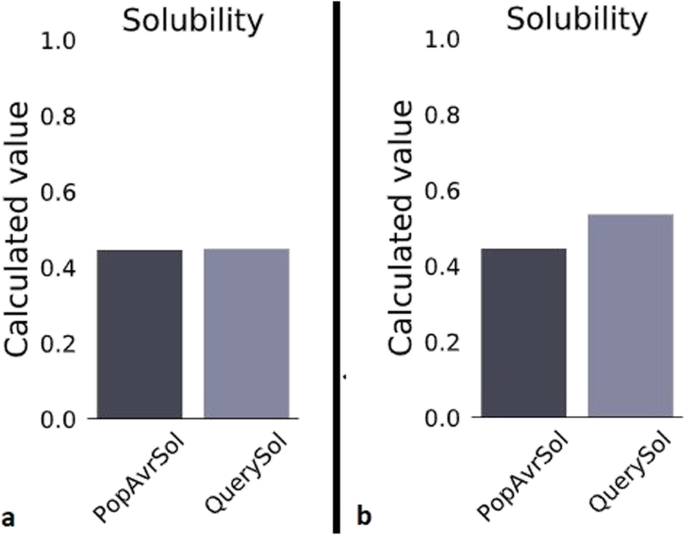
产品关联:文献未提及具体实验产品,领域常规使用IEDB、NetMHC系列在线分析工具。
4. Biomarker研究及发现成果
Biomarker定位
本研究中的Biomarker为疫苗的免疫表位,包括B细胞线性/构象表位、CD4+T细胞表位及CTL表位,筛选与验证逻辑为:通过生物信息学工具预测表位,再经VaxiJen服务器验证抗原性、IEDB数据库比对确认,确保表位的免疫原性与特异性。
研究过程详述
Biomarker的来源为H7N9亚型流感病毒的HA2、M2e保守抗原序列及CTxB佐剂序列;验证方法包括:用BepiPred预测线性B细胞表位,Ellipro预测构象B细胞表位,NetMHCIIpan、NetMHCIpan分别预测CD4+T细胞与CTL表位,VaxiJen以0.5为阈值验证表位抗原性,IEDB数据库比对确认表位的保守性;特异性数据显示,CD4+T细胞表位覆盖7种常见MHCII等位基因(DRB1_0701、DRB1_1501等),具有广谱人群适用性;敏感性数据文献未明确提供,基于图表趋势推测,预测表位均符合抗原性阈值要求。
核心成果提炼
本研究确定的M2e-LR5-CTxB-LR5-HA2嵌合疫苗保留了HA2与M2e的核心免疫表位,结构稳定性良好,CD4+T细胞表位可覆盖多数人群MHCII等位基因,具有广谱免疫原性;创新性在于首次系统筛选4种佐剂与12种连接子的组合,构建了兼具结构稳定性与广谱免疫原性的流感疫苗候选,为流感广谱亚单位疫苗的设计提供了系统的优化策略;文献未提及具体统计学显著性数据,基于分析结果推测各指标均符合稳定与抗原性阈值要求。
