1. 领域背景与文献引入
文献英文标题:A long non-coding RNA, HOTAIR, promotes cartilage degradation in osteoarthritis by inhibiting WIF-1 expression and activating Wnt pathway;发表期刊:BMC Molecular and Cell Biology;影响因子:未公开;研究领域:骨关节炎表观遗传调控与非编码RNA功能。
骨关节炎是全球范围内导致慢性致残的主要疾病之一,55-80岁以上人群中患病率超过50%,患者不仅生活质量显著下降,还因伴随心血管疾病、糖尿病等并发症增加早逝风险。遗憾的是,骨关节炎目前尚无根治方法,现有治疗仅能缓解症状,无法阻断或逆转疾病进展,其核心瓶颈在于对骨关节炎发病的复杂病理机制尚未完全阐明,涉及关节软骨、软骨下骨、滑膜等多组织的相互作用。领域共识:近年来,表观遗传调控尤其是非编码RNA的作用逐渐成为骨关节炎机制研究的热点,长链非编码RNA(lncRNA)作为长度超过200核苷酸的非编码转录本,可通过表观修饰、转录调控等方式参与疾病进程。已有研究发现部分lncRNA如GAS5、CIR、H19等在骨关节炎中存在异常表达并调控软骨细胞功能,但lncRNA在骨关节炎中的具体调控网络仍不清晰。其中,HOX反义基因间RNA(HOTAIR)在骨关节炎患者软骨中呈显著上调趋势,前期研究提示其可能参与软骨降解相关基因的表达调控,但HOTAIR在骨关节炎中的具体作用机制,尤其是与Wnt信号通路关键抑制因子Wnt抑制因子1(WIF-1)的关联尚未明确,这一研究空白限制了骨关节炎靶向治疗靶点的开发。因此,本研究旨在阐明HOTAIR调控骨关节炎软骨降解的分子机制,为骨关节炎的生物标志物筛选及治疗策略提供新的理论依据。
2. 文献综述解析
作者对领域内现有研究的分类维度包括骨关节炎临床与病理研究现状、非编码RNA尤其是lncRNA在骨关节炎中的调控作用、HOTAIR在疾病中的表观调控功能、Wnt/β-catenin通路与骨关节炎的关联四个方面,系统梳理了各方向的研究进展与未解决问题。
现有研究已明确骨关节炎是一种累及全关节的慢性退行性疾病,病理过程涉及软骨细胞代谢失衡、细胞外基质降解、炎症反应等多个环节,现有治疗手段的局限性源于对核心病理机制的认知不足。在非编码RNA领域,已有研究证实微小RNA在骨关节炎软骨稳态维持中发挥关键作用,而lncRNA的研究起步较晚,目前仅少数lncRNA如GAS5、CIR、H19等被报道参与骨关节炎的调控,其优势在于能够从表观遗传层面精准调控基因表达,为疾病机制研究提供新的视角,但局限性在于多数研究仅停留在表达关联层面,缺乏对具体调控机制的深入解析,且样本量较小,部分结论缺乏大样本临床验证。针对HOTAIR的研究,现有成果主要集中在肿瘤领域,证实其可通过招募多梳抑制复合物2(PRC2)介导组蛋白H3K27三甲基化,进而表观沉默靶基因,促进肿瘤发生与转移,但在骨关节炎等风湿性疾病中的研究较为有限,仅初步发现其在骨关节炎软骨中上调并可能调控基质金属蛋白酶(MMPs)的表达,未明确其具体作用靶点与下游通路。在Wnt/β-catenin通路方面,现有研究证实其异常激活与骨关节炎软骨降解密切相关,WIF-1作为该通路的关键抑制因子,在骨关节炎中表达下调,但WIF-1的上游调控机制尚未阐明。通过对比现有研究的未解决问题,本研究的创新价值在于首次建立了HOTAIR、WIF-1与Wnt/β-catenin通路的直接调控关联,明确了HOTAIR通过表观修饰抑制WIF-1表达,进而激活Wnt通路促进骨关节炎软骨降解的具体机制,填补了lncRNA调控骨关节炎Wnt通路的研究空白,为骨关节炎的机制研究提供了新的范式。
3. 研究思路总结与详细解析
本研究的整体研究目标是阐明HOTAIR在骨关节炎软骨降解中的调控机制,核心科学问题是HOTAIR如何通过表观遗传修饰调控WIF-1表达及下游Wnt/β-catenin通路,技术路线遵循“临床样本验证→细胞功能实验→机制探究→通路验证”的闭环逻辑,从临床现象到分子机制逐层深入解析HOTAIR的作用。
3.1 临床样本中HOTAIR及骨关节炎相关基因表达验证
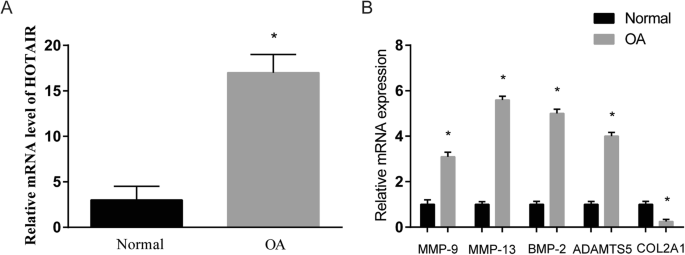
实验目的是明确骨关节炎患者软骨细胞中HOTAIR的表达特征及与骨关节炎病理相关基因的关联,为后续细胞实验提供临床依据。方法细节为收集10例因创伤行膝上截肢的正常患者和10例因骨关节炎行全膝关节置换术的患者软骨组织,通过胶原酶消化分离软骨细胞,采用实时荧光定量PCR(qRT-PCR)检测HOTAIR及骨关节炎相关基因的mRNA表达水平,以甘油醛-3-磷酸脱氢酶(GAPDH)作为内参进行标准化。结果解读显示,骨关节炎组软骨细胞中HOTAIR的相对表达量显著高于正常组(n=10,P<0.05),同时软骨降解相关基因基质金属蛋白酶9(MMP-9)、基质金属蛋白酶13(MMP-13)、聚蛋白多糖酶5(ADAMTS5)、骨形态发生蛋白2(BMP-2)的表达均显著上调,而软骨基质关键基因Ⅱ型胶原α1链(COL2A1)的表达显著下调(n=10,P<0.05),提示HOTAIR的高表达与骨关节炎软骨降解的病理过程密切相关。实验所用关键产品:TRIzol试剂(Invitrogen)、PrimeScript RT reagent Kit(Takara Bio)、SYBR Premix Ex TaqII kit(Takara Bio)、7900HT Fast Real-Time PCR System(Applied Biosystems)。
3.2 SW1353细胞中HOTAIR沉默与过表达的功能验证
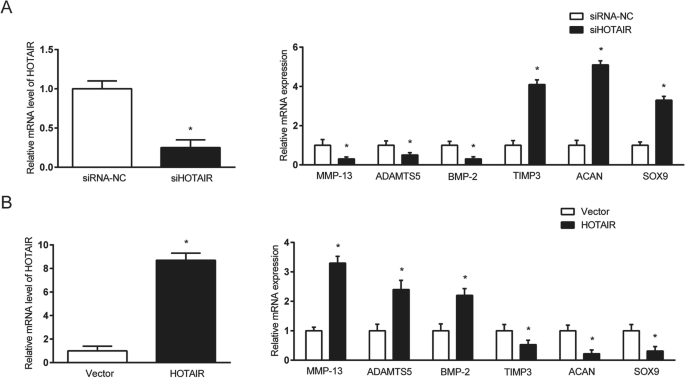
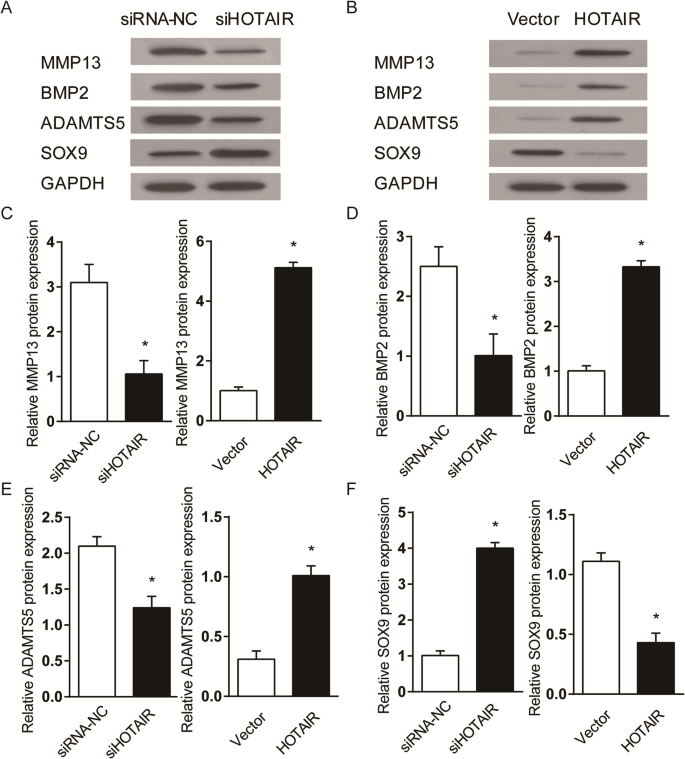
实验目的是在细胞模型中验证HOTAIR对软骨细胞代谢相关基因表达的直接调控作用,明确其在软骨降解中的功能。方法细节为采用小干扰RNA(siRNA)转染人软骨肉瘤细胞系SW1353,沉默HOTAIR的表达;同时构建HOTAIR过表达逆转录病毒载体,感染SW1353细胞实现HOTAIR的稳定过表达。转染或感染48小时后,采用实时荧光定量PCR检测HOTAIR及软骨降解相关基因、软骨合成相关基因的mRNA表达,采用蛋白质免疫印迹(Western blot)检测相关蛋白的表达水平。结果解读显示,siRNA沉默HOTAIR后,SW1353细胞中HOTAIR的mRNA表达显著降低(n=3,P<0.05),伴随软骨降解基因MMP-13、ADAMTS5、BMP-2的表达显著下调,而软骨合成相关基因金属蛋白酶组织抑制剂3(TIMP3)、聚集蛋白聚糖(ACAN)、性别决定区Y框蛋白9(SOX9)的表达显著上调(n=3,P<0.05);反之,过表达HOTAIR后,HOTAIR的mRNA表达显著升高(n=3,P<0.05),上述基因的表达变化趋势完全相反,且蛋白质免疫印迹结果显示相关蛋白的表达变化与mRNA水平一致(n=3,P<0.05),证实HOTAIR可正向调控软骨降解基因、负向调控软骨合成基因,促进软骨细胞的分解代谢。实验所用关键产品:siRNA(Sigma-Aldrich)、Lipofectamine™ RNAiMAX(Invitrogen)、pBABE逆转录病毒载体(Cell Biolabs)、polybrene(Sigma-Aldrich)、细胞裂解液(Beyotime)、BCA蛋白定量试剂盒(Thermo Fisher Scientific)、PVDF膜(EMD Millipore)、MMP-13抗体、BMP-2抗体、ADAMTS5抗体、SOX9抗体等(Sigma-Aldrich、Santa Cruz Biotechnology)。
3.3 HOTAIR调控WIF-1表达的表观机制研究
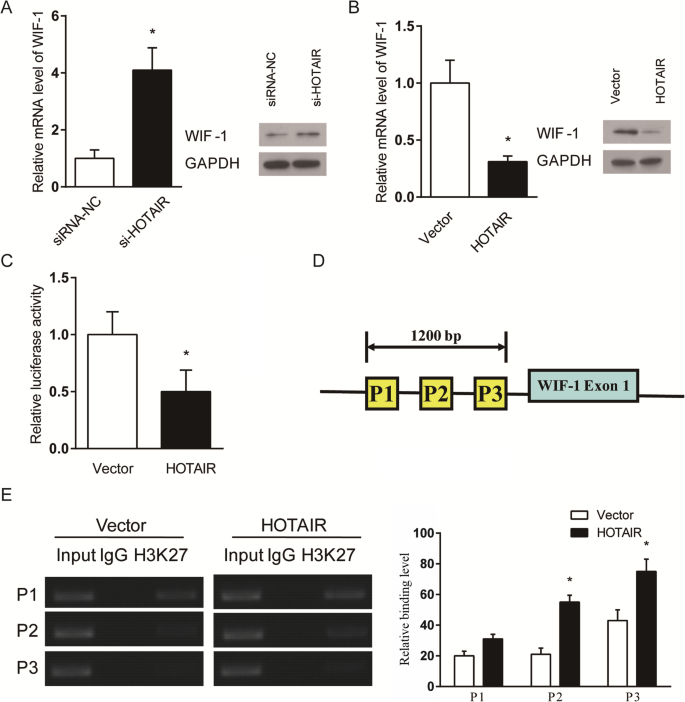
实验目的是探究HOTAIR调控软骨细胞代谢的下游靶点及具体表观调控方式,明确其与WIF-1的调控关系。方法细节为在SW1353细胞中分别沉默或过表达HOTAIR后,采用实时荧光定量PCR和蛋白质免疫印迹检测WIF-1的mRNA和蛋白表达水平;构建包含WIF-1启动子区域的荧光素酶报告载体,转染至HOTAIR过表达及对照细胞中,通过双荧光素酶报告实验检测HOTAIR对WIF-1启动子活性的影响;采用染色质免疫沉淀(ChIP)实验,检测HOTAIR过表达细胞中WIF-1启动子区域组蛋白H3K27三甲基化的富集水平。结果解读显示,沉默HOTAIR后,SW1353细胞中WIF-1的mRNA和蛋白表达均显著上调(n=3,P<0.05),而过表达HOTAIR则显著抑制WIF-1的mRNA和蛋白表达(n=3,P<0.05);双荧光素酶报告实验显示,HOTAIR过表达细胞中WIF-1启动子的荧光素酶活性显著低于对照组(n=3,P<0.05),提示HOTAIR可直接抑制WIF-1的转录;染色质免疫沉淀实验结果显示,HOTAIR过表达细胞中WIF-1启动子区域的H3K27三甲基化水平显著升高(n=3,P<0.05),证实HOTAIR通过招募表观调控复合物介导WIF-1启动子的组蛋白甲基化,进而表观沉默WIF-1的表达。实验所用关键产品:pGL3-WIF1 Promoter载体、pRL-TK内参载体(Promega)、Lipofectamine™ 2000(Invitrogen)、Dual Luciferase Reporter Assay System(Promega)、EZ-ChIP™试剂盒(Sigma-Aldrich)、抗H3K27me3抗体(Sigma-Aldrich)、WIF-1抗体(Santa Cruz Biotechnology)。
3.4 HOTAIR对Wnt/β-catenin通路的激活验证
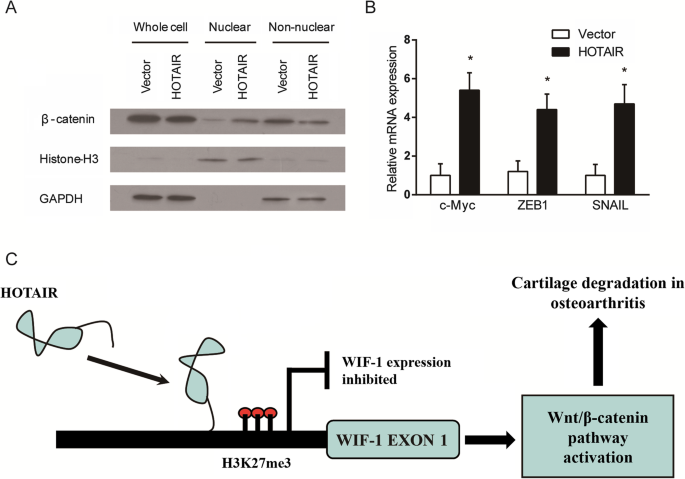
实验目的是验证HOTAIR通过抑制WIF-1表达对下游Wnt/β-catenin通路的调控作用,明确其促进软骨降解的下游信号通路。方法细节为在SW1353细胞中过表达HOTAIR后,采用核质分离试剂盒提取细胞核和细胞质蛋白,通过蛋白质免疫印迹检测β-连环蛋白(β-catenin)在细胞核和细胞质中的分布;同时采用实时荧光定量PCR检测Wnt/β-catenin通路下游靶基因c-Myc、ZEB1、SNAIL的mRNA表达水平。结果解读显示,过表达HOTAIR后,SW1353细胞中细胞核内β-catenin的含量显著升高,细胞质中β-catenin的含量显著降低(n=3,P<0.05),提示β-catenin发生核转位;下游靶基因c-Myc、ZEB1、SNAIL的mRNA表达均显著上调(n=3,P<0.05),证实HOTAIR通过抑制WIF-1表达,解除其对Wnt/β-catenin通路的抑制,导致通路异常激活,进而促进软骨降解相关基因的表达。实验所用关键产品:NE-PER™核质分离试剂盒(Thermo Fisher Scientific)、β-catenin抗体(Sigma-Aldrich)、组蛋白H3抗体(核内参)、GAPDH抗体(胞质内参)。
4. Biomarker研究及发现成果
本研究涉及的Biomarker为长链非编码RNA HOTAIR,其筛选与验证逻辑遵循“临床样本差异表达筛选→细胞功能验证→分子机制解析”的完整链条,明确了HOTAIR作为骨关节炎潜在生物标志物的基础。
HOTAIR的来源为骨关节炎患者的关节软骨组织样本,验证方法包括临床样本的实时荧光定量PCR检测、细胞模型的功能获得与缺失实验、表观机制与通路验证实验。在临床样本中,骨关节炎患者软骨细胞中HOTAIR的表达水平较正常组上调超过20倍(n=10,P<0.05),但本研究未提供其作为诊断生物标志物的特异性、敏感性数据(如ROC曲线AUC值等),需进一步大样本临床研究验证。核心成果提炼:本研究首次证明HOTAIR可通过表观遗传修饰直接调控WIF-1的表达,进而激活Wnt/β-catenin通路,促进骨关节炎软骨细胞的分解代谢与软骨降解,建立了HOTAIR-WIF-1-Wnt/β-catenin这一全新的骨关节炎调控轴。HOTAIR作为骨关节炎软骨中显著上调的lncRNA,其表达水平与骨关节炎的病理进程密切相关,具备作为骨关节炎诊断生物标志物的潜力;同时,HOTAIR介导的表观调控通路可作为骨关节炎疾病修饰治疗的潜在靶点,为开发靶向表观遗传的骨关节炎治疗策略提供了新的方向。目前本研究尚未提供HOTAIR在临床样本中的诊断效能数据,推测:后续通过大样本临床队列研究验证HOTAIR的诊断价值,并开发靶向HOTAIR的反义寡核苷酸或表观调控药物,有望为骨关节炎的精准诊断与治疗提供新的工具。
