1. 领域背景与文献引入
核心信息段:文献英文标题:Altered cellular localization and hemichannel activities of KID syndrome associated connexin26 I30N and D50Y mutations;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:皮肤遗传病与间隙连接蛋白功能机制研究。
领域共识:间隙连接是介导相邻细胞间小分子物质(如离子、代谢物)交换的关键结构,对维持细胞稳态、增殖分化等过程至关重要;连接蛋白(connexin)是间隙连接的基本组成单位,其编码基因的突变与多种人类遗传性疾病密切相关。其中,连接蛋白26(Cx26)的突变是导致非综合征性耳聋的主要原因,同时也会引发伴皮肤异常的综合征性耳聋,如角膜炎-鱼鳞病-耳聋(Keratitis-ichthyosis-deafness, KID)综合征。现有研究表明,KID综合征相关的Cx26突变多通过改变半通道活性干扰细胞功能,但这些异常半通道对细胞内钙稳态等关键过程的影响及分子机制仍未完全阐明,且针对I30N和D50Y这两个突变的功能研究较为匮乏。基于此,本研究旨在评估Cx26 I30N和D50Y突变在哺乳动物细胞系中的蛋白生物合成、细胞定位及通道功能,为KID综合征的致病机制提供新的实验依据。
2. 文献综述解析
核心信息段:作者以Cx26突变导致的疾病表型差异为分类维度,将现有研究分为非综合征性耳聋相关突变研究与综合征性耳聋伴皮肤异常相关突变研究,系统梳理了Cx26突变的致病机制及研究现状。
现有研究已明确Cx26突变通过多种机制影响间隙连接功能,包括蛋白截短、运输异常、折叠错误及通道通透性改变等,其中非综合征性耳聋相关突变多表现为间隙连接功能丧失,而KID综合征相关突变则主要导致半通道活性异常升高。现有研究的优势在于已鉴定出多个KID综合征相关Cx26突变的半通道活性异常,并初步关联了异常半通道与细胞死亡的关系,但仍存在局限性:一是针对I30N和D50Y这两个突变的细胞内定位、对钙稳态的影响等功能研究空白;二是异常半通道如何通过干扰细胞过程导致KID综合征表皮过度增殖表型的分子机制尚未明确。本研究的创新价值在于首次在HeLa和N2A细胞系中系统表征Cx26 I30N和D50Y突变的蛋白定位、半通道活性及细胞内钙水平变化,补充了KID综合征相关突变功能研究的缺失环节,为解析KID综合征的表皮表型致病机制提供了新的实验数据。
3. 研究思路总结与详细解析
核心信息段:本研究的整体研究目标为明确KID综合征相关Cx26 I30N和D50Y突变对蛋白生物合成、细胞定位及通道功能的影响,核心科学问题是这两个突变如何通过改变半通道活性干扰细胞内钙稳态,技术路线遵循“突变体构建→细胞模型建立→功能检测→抑制剂验证→机制推论”的闭环逻辑,通过多组细胞实验系统解析突变的致病功能。
3.1 突变体构建与细胞转染模型建立
实验目的是构建表达野生型(WT)及突变型Cx26的哺乳动物细胞模型,为后续功能检测提供基础。方法细节:通过定点诱变技术从人野生型Cx26 cDNA中构建I30N和D50Y错义突变体,将WT及突变体cDNA克隆至pIRES2EGFP2和pCS2+哺乳动物表达载体,测序验证突变位点;选用间隙连接通讯缺陷的HeLa细胞和N2A细胞,采用Lipofectamine 2000试剂按1:2的DNA-转染试剂比例进行转染,转染后添加3.2mM CaCl₂以预防半通道活性导致的细胞死亡,转染后24-48h用于后续实验。结果解读:成功获得稳定表达Cx26 WT、I30N及D50Y的细胞模型,为后续蛋白定位、半通道活性及钙水平检测提供了可靠的实验体系。产品关联:实验所用关键产品:Lipofectamine 2000转染试剂(Invitrogen, USA)、Dulbecco改良Eagle培养基(DMEM, Thermo Scientific HyClone, USA)、胎牛血清(Biological Industries, Israel)等。
3.2 Cx26蛋白细胞定位与运输检测
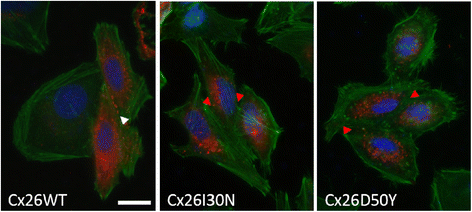
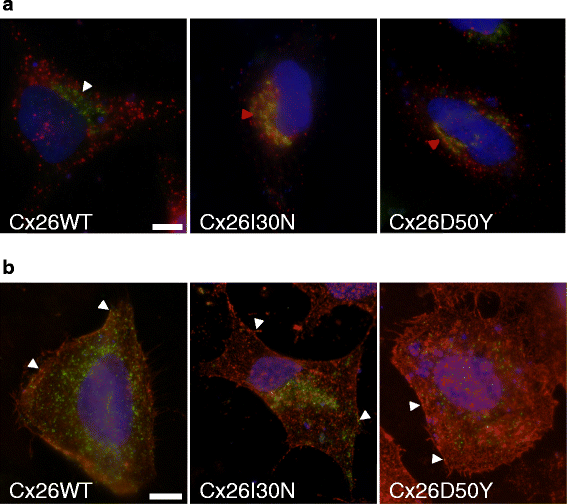
实验目的是分析I30N和D50Y突变对Cx26蛋白合成、细胞内定位及运输过程的影响。方法细节:对转染后的HeLa细胞进行免疫荧光染色,分别用Cx26特异性抗体与肌动蛋白标记物鬼笔环肽、高尔基体标记物golgin-97、细胞膜标记物麦胚凝集素(WGA)共染色,通过激光共聚焦显微镜观察蛋白定位,并采用Fiji Coloc 2插件进行共定位分析。结果解读:免疫染色结果显示,Cx26 WT在细胞间接触部位形成间隙连接斑块,而I30N和D50Y突变体无法形成该斑块,且大量滞留于高尔基体中;共定位分析显示,Cx26 WT与golgin-97的显著共定位比例仅为8%,而I30N和D50Y的比例分别为58%和50%(P<0.01),同时部分突变体蛋白可定位于细胞膜。这表明两个突变体存在蛋白运输异常,无法正常形成功能性间隙连接。
3.3 半通道活性功能验证
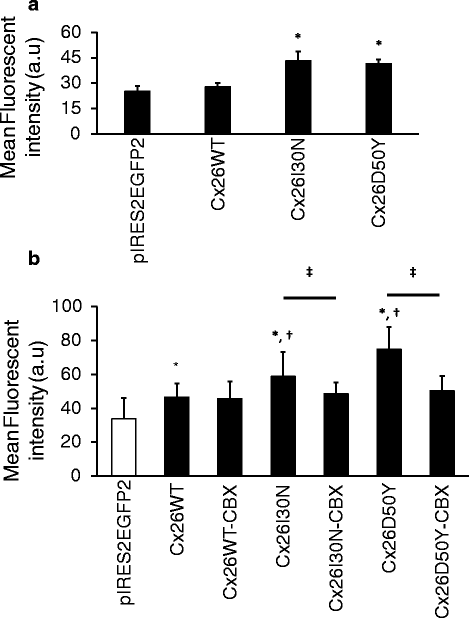
实验目的是检测I30N和D50Y突变体的半通道活性是否存在异常。方法细节:采用Neurobiotin荧光染料摄取实验,分别在生理钙浓度、无钙条件及半通道阻滞剂carbenoxolone(CBX)处理下,检测转染细胞的荧光强度;通过ImageJ软件分析GFP阳性细胞的红色荧光信号强度,采用ANOVA及Tukey’s HSD进行统计学分析。结果解读:生理钙浓度下,I30N和D50Y突变细胞的Neurobiotin摄取量比WT细胞高1.5倍(n=15,P<0.01);无钙条件下,突变细胞的摄取量分别比WT高1.3倍(n=60,P<0.01)和1.6倍(n=49,P<0.01);经100μM CBX处理后,I30N和D50Y突变细胞的荧光强度分别降低17%和35%(P<0.01),表明突变体形成的异常半通道介导了染料的异常摄取。
3.4 细胞内钙稳态影响检测
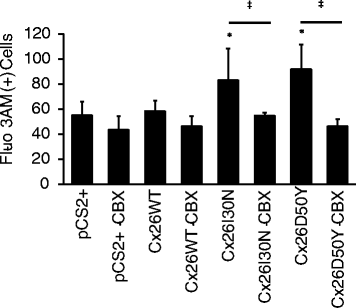
实验目的是分析I30N和D50Y突变对细胞内钙水平的影响,并验证其与异常半通道的关联。方法细节:采用Fluo-3 AM钙指示剂负载转染后的N2A细胞,通过流式细胞术检测细胞内钙荧光强度,同时设置CBX处理组验证半通道的作用;采用Student’s t-test进行组间统计学分析。结果解读:I30N和D50Y突变细胞的细胞内钙水平分别比WT细胞高1.4倍和1.6倍(P<0.01);经CBX处理后,突变细胞的钙水平分别降低34%和50%(P<0.01),表明异常半通道的活性导致了细胞内钙稳态失衡。
4. Biomarker研究及发现成果
核心信息段:本研究中涉及的Biomarker为KID综合征相关的Cx26 I30N和D50Y功能突变体,属于致病机制型Biomarker,其筛选与验证逻辑为“临床突变位点关联→细胞模型功能验证→抑制剂机制确认”,系统解析了突变体的致病功能。
该Biomarker的来源为KID综合征患者中鉴定的Cx26基因错义突变位点,验证方法包括免疫荧光染色检测蛋白定位、荧光染料摄取实验检测半通道活性、流式细胞术检测细胞内钙水平,以及半通道阻滞剂验证功能关联。特异性与敏感性数据显示,I30N和D50Y突变体与高尔基体标记物的共定位比例分别为58%和50%(显著高于WT的8%,P<0.01),突变细胞的半通道介导染料摄取量比WT高1.3-1.6倍(P<0.01),细胞内钙水平比WT高1.4-1.6倍(P<0.01),且这些异常均可被半通道阻滞剂逆转。核心成果方面,该Biomarker的功能关联为:Cx26 I30N和D50Y突变通过形成异常半通道导致细胞内钙水平升高,这一过程可能参与KID综合征表皮过度增殖表型的发生;创新性在于首次在哺乳动物细胞系中系统表征这两个突变的功能,补充了KID综合征致病突变的机制研究,为后续开发针对异常半通道的治疗靶点提供了实验依据。
