1. 领域背景与文献引入
文献英文标题:Rapamycin promoted thrombosis and platelet adhesion to endothelial cells by inducing membrane remodeling;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:血栓形成与血管内皮细胞生物学
静脉血栓栓塞症包括深静脉血栓和肺栓塞,是全球范围内导致发病和死亡的重要原因,领域共识:Virchow三联征(血管异常与内皮功能障碍、高凝状态、血流瘀滞)被认为是静脉血栓形成的核心病理机制,但具体分子机制尚未完全阐明。当前研究热点聚焦于血小板-内皮细胞相互作用的调控机制、内皮膜形态动态变化对血栓起始的影响,以及自噬通路在血管细胞生物学中的功能。雷帕霉素洗脱支架因抑制血管内膜增生的作用在临床广泛应用于冠心病介入治疗,但关于其是否增加支架内血栓风险存在显著争议,部分研究显示雷帕霉素可能通过激活组织因子、失衡纤溶系统增加血栓风险,另一部分研究则认为其安全性与裸金属支架相当。这一矛盾为领域留下了关键研究空白,亟需明确雷帕霉素对血栓形成的直接作用及潜在细胞分子机制,本研究正是针对这一问题展开,旨在揭示雷帕霉素诱导血栓形成的细胞形态学机制,为临床支架应用的安全性评估提供实验依据。
2. 文献综述解析
作者从三个核心维度梳理了领域内现有研究,一是静脉血栓形成的病理生理机制,重点围绕Virchow三联征及血小板-内皮细胞黏附的关键作用展开;二是内皮膜形态调控与血栓形成的关联,关注内皮膜粗糙度对血小板黏附的影响及环境因素对内皮膜突起的诱导作用;三是雷帕霉素的临床争议及自噬在细胞骨架重塑中的功能。
现有研究已证实Virchow三联征在血栓形成中的核心地位,血小板-内皮细胞黏附是血栓起始阶段的关键事件之一,内皮膜的动态形态变化如膜褶皱、微绒毛等可显著增加血小板黏附的有效接触面积,进而促进血栓形成;雷帕霉素作为经典的自噬激动剂,被报道可调控内皮细胞骨架结构,但关于雷帕霉素洗脱支架的血栓风险存在对立结论,部分研究通过临床数据或动物实验显示其增加支架内血栓风险,机制涉及组织因子激活、组织型纤溶酶原激活物抑制及纤溶酶原激活物抑制剂1诱导,另一部分大样本临床研究则认为其安全性与裸金属支架无显著差异。现有研究的局限性在于,尚未明确雷帕霉素是否直接通过调控内皮细胞形态影响血栓形成,且自噬通路与内皮膜重塑及血栓形成的关联机制未被系统阐明。
本研究的创新价值在于首次揭示了雷帕霉素通过诱导内皮细胞自噬依赖的膜重塑,促进血小板-内皮细胞黏附及体内血栓形成的完整机制,填补了雷帕霉素诱导血栓形成的细胞形态学机制空白,为临床关于雷帕霉素洗脱支架的血栓风险争议提供了直接的实验证据,同时拓展了自噬通路在血管血栓生物学中的功能认知。
3. 研究思路总结与详细解析
本研究的核心目标是明确雷帕霉素对体内血栓形成的直接影响及潜在细胞分子机制,核心科学问题为雷帕霉素是否通过调控内皮细胞膜重塑影响血小板-内皮细胞黏附,技术路线遵循“体内动物模型验证血栓表型→细胞水平解析血小板黏附与膜形态关联→分子通路验证自噬依赖机制”的闭环逻辑,层层递进揭示雷帕霉素诱导血栓形成的机制。
3.1 体内深静脉血栓模型构建与雷帕霉素作用验证
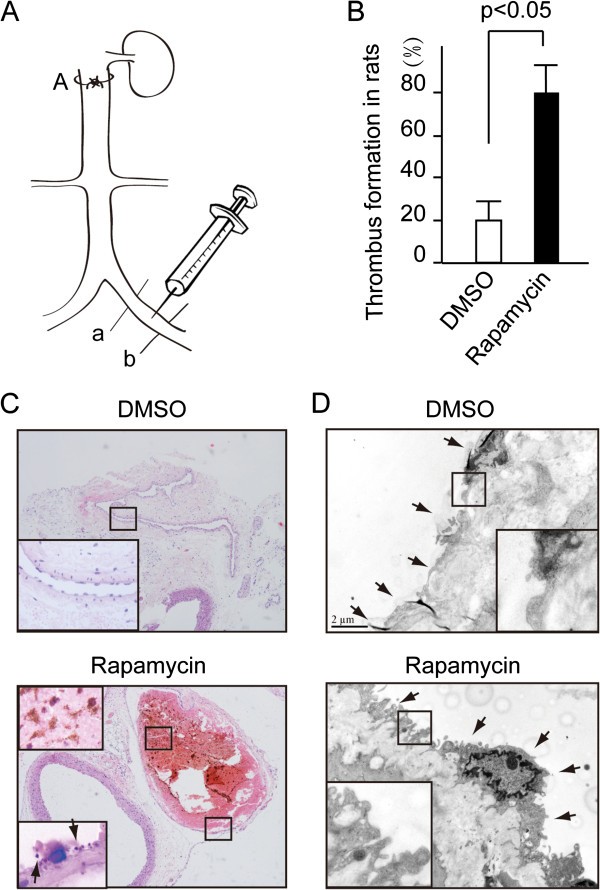
实验目的为验证雷帕霉素对体内血栓形成的直接调控作用。方法细节上,采用改良的大鼠深静脉血栓模型,选取雄性SD大鼠(180±30g),通过腹部正中切口暴露下腔静脉,在肾动脉下方分离静脉后向髂静脉注射雷帕霉素(500ng/kg)或DMSO对照,随后用丝线结扎下腔静脉40分钟以构建血流瘀滞模型,之后取静脉组织进行苏木精-伊红(HE)染色和透射电镜分析。结果解读显示,注射雷帕霉素的大鼠在40分钟时血栓形成比例为80%(n=10,P<0.05),显著高于对照组的20%;HE染色显示雷帕霉素组静脉管腔内形成闭塞性血栓,其中可见大量血小板衍生的凝块;透射电镜观察到雷帕霉素处理的大鼠内皮细胞表面出现大量微绒毛样结构,而对照组内皮表面光滑。实验所用关键产品:Sigma的雷帕霉素(货号R878)、苏木精-伊红染色试剂(文献未提及具体品牌,领域常规使用国药集团等品牌的HE染色试剂盒)、JEOL-1230透射电子显微镜。
3.2 细胞水平雷帕霉素对血小板-内皮细胞黏附的影响
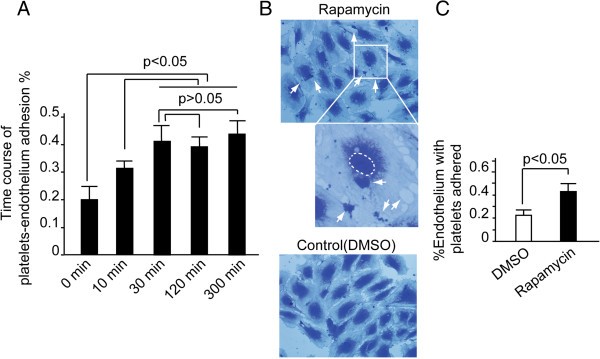
实验目的为明确雷帕霉素是否在细胞水平直接促进血小板与内皮细胞的黏附作用。方法细节上,培养人脐静脉内皮细胞(HUVECs,购自ATCC)至汇合状态,将健康志愿者分离的洗涤血小板(50×10^6/μl)与雷帕霉素(10nM)或DMSO共同加入内皮细胞培养体系,孵育30分钟(预实验确定30分钟为黏附峰值时间),之后用结晶紫染色,显微镜下计数黏附血小板的内皮细胞比例。结果解读显示,雷帕霉素处理组中黏附血小板的内皮细胞数量较对照组增加115%(n=3,P<0.05),表明雷帕霉素可显著增强血小板与内皮细胞的黏附能力。实验所用关键产品:ATCC的人脐静脉内皮细胞、Sigma的雷帕霉素(货号R878)、结晶紫染色试剂(文献未提及具体品牌,领域常规使用Sigma等品牌)。
3.3 雷帕霉素诱导内皮细胞膜重塑的验证
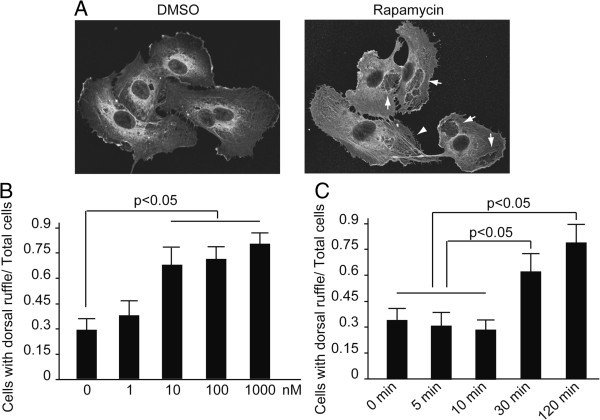
实验目的为探究雷帕霉素是否诱导内皮细胞发生膜重塑(如背侧褶皱形成)。方法细节上,用不同浓度(10nM-1000nM)的雷帕霉素处理HUVECs不同时间(10-60分钟),通过免疫荧光染色检测β-肌动蛋白的分布,观察内皮细胞背侧褶皱的形成情况,统计形成背侧褶皱的细胞比例。结果解读显示,雷帕霉素处理可显著诱导HUVECs形成背侧褶皱,10nM浓度处理30分钟时效果最显著,形成背侧褶皱的细胞比例较对照组大幅升高;浓度梯度实验显示10-1000nM的雷帕霉素均可显著增强背侧褶皱形成(n=3)。实验所用关键产品:Medical & Biological Laboratoris的抗β-肌动蛋白抗体(文献未提及具体货号,领域常规使用类似产品)、Sigma的雷帕霉素(货号R878)。
3.4 膜重塑在血小板-内皮黏附中的必要性验证
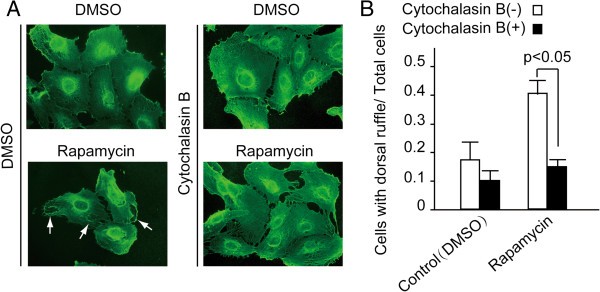
实验目的为验证内皮细胞膜重塑是否为雷帕霉素诱导的血小板-内皮黏附所必需的环节。方法细节上,用细胞松弛素B(Cytochalasin B,30μM)预处理HUVECs20分钟,通过抑制肌动蛋白聚合阻断背侧褶皱形成,之后加入雷帕霉素和血小板,检测血小板黏附情况及背侧褶皱形成比例。结果解读显示,细胞松弛素B可显著抑制雷帕霉素诱导的内皮细胞背侧褶皱形成,同时使血小板-内皮细胞黏附水平较单独雷帕霉素处理组降低约58%(n=3),表明内皮细胞膜重塑是雷帕霉素促进血小板黏附的关键环节。实验所用关键产品:Sigma的细胞松弛素B(货号C6762)、雷帕霉素(货号R878)。
3.5 自噬在雷帕霉素诱导膜重塑中的作用机制验证
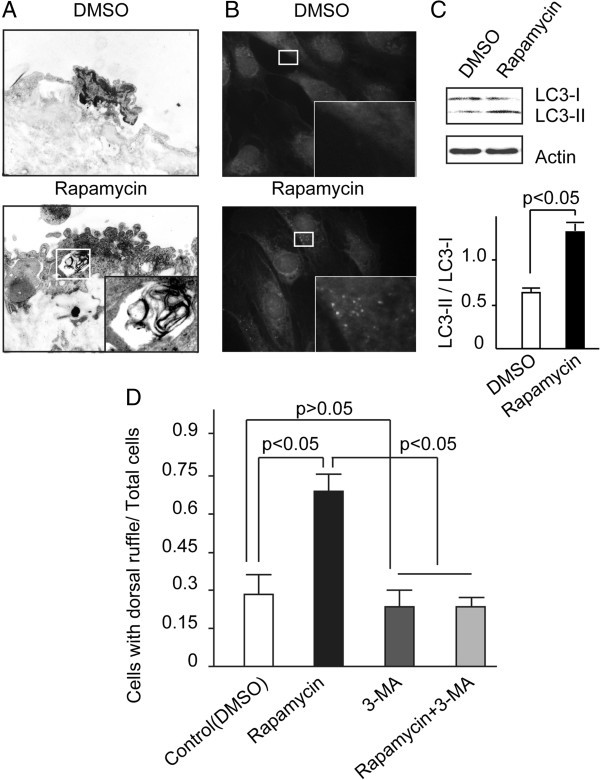
实验目的为明确雷帕霉素诱导的内皮细胞膜重塑是否依赖自噬通路。方法细节上,用自噬抑制剂3-甲基腺嘌呤(3-MA,5nM)处理HUVECs,同时加入雷帕霉素,通过透射电镜观察自噬体形成,免疫荧光检测LC3-II的聚集情况,Western blot检测LC3-II/LC3-I比例,统计背侧褶皱形成比例。结果解读显示,雷帕霉素处理可诱导HUVECs形成典型的双膜结构自噬体,LC3-II聚集显著增加,LC3-II/LC3-I比例较对照组升高;而3-MA可抑制雷帕霉素诱导的自噬激活,同时使背侧褶皱形成比例降低67%(n=3),表明雷帕霉素诱导的内皮细胞膜重塑依赖自噬通路。实验所用关键产品:Sigma的3-甲基腺嘌呤(货号M9281)、雷帕霉素(货号R878)、Medical & Biological Laboratoris的抗LC3-II抗体(货号025)。
4. Biomarker研究及发现成果
本研究未涉及传统意义上的诊断或预后生物标志物,而是鉴定了雷帕霉素诱导血栓形成的关键功能性机制节点——自噬依赖的内皮细胞膜重塑,其筛选与验证逻辑为“体内血栓表型观察→细胞水平血小板黏附与膜形态关联分析→自噬通路特异性阻断验证”的完整链条。
研究过程中,首先通过体内大鼠深静脉血栓模型观察到雷帕霉素处理后内皮细胞表面出现微绒毛样膜重塑结构,随后在细胞水平验证雷帕霉素可诱导人脐静脉内皮细胞形成背侧褶皱,且该膜重塑过程可被自噬抑制剂3-甲基腺嘌呤特异性阻断;同时,使用膜重塑抑制剂细胞松弛素B处理后,雷帕霉素诱导的血小板-内皮细胞黏附作用被显著抑制,证明膜重塑是血小板黏附及后续血栓形成的关键环节。
核心成果方面,本研究首次揭示了雷帕霉素通过激活自噬通路诱导内皮细胞膜重塑,进而促进血小板-内皮细胞黏附及体内血栓形成的完整机制,创新性地将自噬通路、内皮膜形态调控与血栓形成过程系统关联起来,为雷帕霉素洗脱支架的血栓风险争议提供了细胞分子层面的实验依据。本研究未提供传统生物标志物的特异性、敏感性数据,也未涉及预后相关的统计学结果如风险比HR等,未开展临床样本的验证分析。
