1. 领域背景与文献引入
文献英文标题:Identification of a functional nuclear translocation sequence in hPPIP5K2;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:细胞信号转导、肌醇焦磷酸代谢酶的核定位调控
肌醇焦磷酸(PP-InsPs)是一类高度磷酸化的细胞内信号分子,在细胞稳态、能量代谢及信号通路调控中发挥关键作用,其合成主要由PPIP5K和IP6K两类激酶催化完成。领域发展关键节点可追溯至1999年IP6K家族的首次鉴定,2007年PPIP5K家族被正式命名并明确其激酶活性;当前研究热点聚焦于肌醇焦磷酸的下游功能靶点及合成酶的调控机制,但核心未解决问题在于PPIP5K家族的亚细胞定位调控机制尚不清晰,尤其是PPIP5K2亚型的核定位功能及调控方式完全未知。现有研究仅揭示PPIP5K1可通过质膜定位参与PtdIns(3,4,5)P3信号通路的调控,而PPIP5K2的亚细胞分布特征及功能意义缺乏实验证据,因此本研究针对hPPIP5K2的核定位信号功能及调控机制展开,填补该家族核定位研究的空白,为肌醇焦磷酸的区室化合成机制提供新的理论依据。
2. 文献综述解析
作者以PPIP5K家族的亚型差异为分类维度,系统梳理了肌醇焦磷酸合成酶的研究现状,明确现有研究的核心结论、技术优势及局限性。
现有研究的关键结论显示,PPIP5K1通过质膜定位调控PtdIns(3,4,5)P3信号通路,肌醇焦磷酸的区室化合成是其实现功能特异性的核心机制;技术方法上,亚细胞定位分析、质谱鉴定等技术的应用为解析激酶功能提供了精准手段,但现有研究存在明显局限性:PPIP5K2的亚细胞定位及调控机制完全未被探索,生物信息学预测的核定位信号缺乏实验验证,翻译后修饰对其核定位的调控作用也未被揭示。通过对比现有研究的空白,本研究的创新价值凸显:首次鉴定PPIP5K2家族中存在功能性核定位信号,揭示其核定位受邻近丝氨酸磷酸化的负调控,为PPIP5K家族的共价修饰调控提供首个实验证据,完善了肌醇焦磷酸区室化合成的调控网络,同时为核定位信号的预测算法优化提供了新的实验数据。
3. 研究思路总结与详细解析
本研究的核心目标是鉴定hPPIP5K2的功能性核定位信号并解析其核定位的调控机制,核心科学问题聚焦于hPPIP5K2的核定位信号是否具备功能活性,以及其核定位是否受翻译后修饰调控,技术路线遵循“生物信息学预测→细胞模型验证→互作蛋白鉴定→突变体功能分析→修饰调控解析”的闭环逻辑。
3.1 生物信息学分析与细胞亚细胞定位验证
实验目的:通过生物信息学分析预测hPPIP5K2的核定位信号,并构建细胞模型验证其亚细胞分布特征。方法细节:采用ClustalW工具比对多物种PPIP5K2同源蛋白序列,鉴定保守结构域;构建GFP标签的hPPIP5K1、hPPIP5K2表达载体,转染HEK293T细胞后,通过共聚焦显微镜观察亚细胞定位,采用Image J软件量化核质荧光强度比(FN/FC)。结果解读:多序列比对显示,hPPIP5K2的C末端存在一段高度保守的63个氨基酸结构域,其中包含五聚精氨酸序列(RRRRR),该序列在PPIP5K1中不存在同源序列(
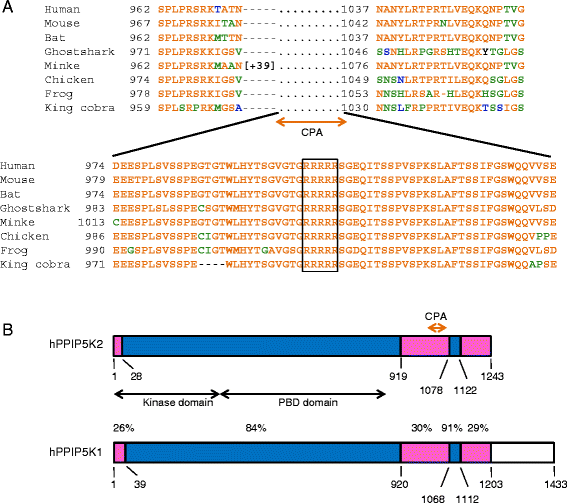
);共聚焦显微镜观察显示,hPPIP5K2存在明显的核内分布,其FN/FC比为0.28(n=15,P<0.01),显著高于hPPIP5K1的0.04(n=15,P<0.01),表明hPPIP5K2存在特异性的核内亚群(
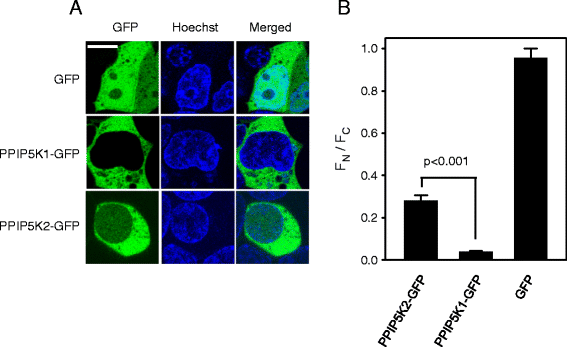
)。实验所用关键产品:Lipofectamine 3000转染试剂(Invitrogen)、Zeiss LSM 780共聚焦显微镜、Image J图像分析软件(NIH)。
3.2 核定位信号的功能验证
实验目的:验证五聚精氨酸序列作为功能性核定位信号的作用。方法细节:构建hPPIP5K2的核定位信号突变体(RRRRR→RAAAR),转染HEK293T细胞后,采用成像流式细胞术分析大量细胞的核定位水平,通过Similarity Score量化GFP与核染料DRAQ5的共定位程度,避免人工选择细胞的偏差。结果解读:野生型hPPIP5K2的中位Similarity Score为1.64(n=632),72%的细胞Score>1.2(提示显著核定位);核定位信号突变体的中位Similarity Score降至0.75(n=1195,P<0.001),仅30%的细胞Score>1.2,表明核定位信号突变显著降低了hPPIP5K2的核定位水平(
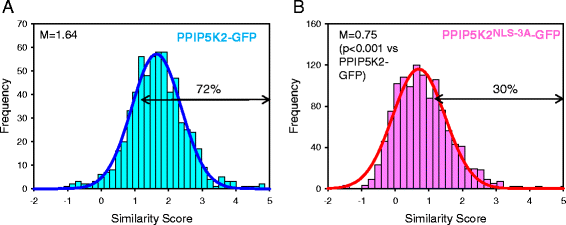
);进一步分析显示,hPPIP5K2的核定位水平与蛋白表达量无显著相关性(相关系数r≈0),排除了表达量对实验结果的干扰(
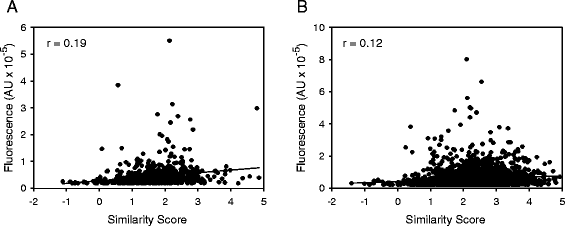
)。实验所用关键产品:ImageStream X成像流式细胞仪(Amnis Corporation)、DRAQ5核染料(Cell Signaling Technology)。
3.3 核转运互作蛋白的质谱鉴定
实验目的:鉴定与hPPIP5K2结合的核转运蛋白,验证核定位信号的功能通路。方法细节:构建FLAG标签的hPPIP5K2表达载体,稳定转染HEK293T细胞,通过FLAG亲和凝胶纯化富集互作蛋白,采用纳米液相色谱-电喷雾质谱(nanoLC-ESI-MS/MS)鉴定互作蛋白。结果解读:质谱分析鉴定到Importin-5和Importin-8与hPPIP5K2特异性结合,其中Importin-5的序列覆盖率为8.2%,Importin-8为5.9%,而对照FLAG-β-半乳糖苷酶的纯化产物中未检测到这两种蛋白,提示hPPIP5K2通过与β-importin家族蛋白结合实现核转运(

)。实验所用关键产品:ANTI-FLAG® M2 Affinity gel(Sigma)、Agilent 1100 nanoLC系统、Agilent 6340离子阱质谱仪。
3.4 丝氨酸磷酸化对核定位的调控分析
实验目的:解析hPPIP5K2核定位的翻译后修饰调控机制。方法细节:通过质谱鉴定hPPIP5K2的磷酸化位点,构建S1006A(非磷酸化模拟)和S1006D(磷酸化模拟)突变体,采用共聚焦显微镜和成像流式细胞术分析突变体的核定位水平。结果解读:质谱鉴定到hPPIP5K2的S1006位点存在磷酸化修饰(
);共聚焦显微镜显示,S1006A突变体的FN/FC比为0.41(n=15,P<0.001),显著高于野生型的0.28;成像流式细胞术分析显示,S1006A突变体的中位Similarity Score为2.58(n=1686,P<0.001),比野生型高58%,而S1006D突变体的中位Similarity Score降至1.36(n=1696,P<0.001),核定位水平降低40%,表明S1006磷酸化负调控hPPIP5K2的核定位(
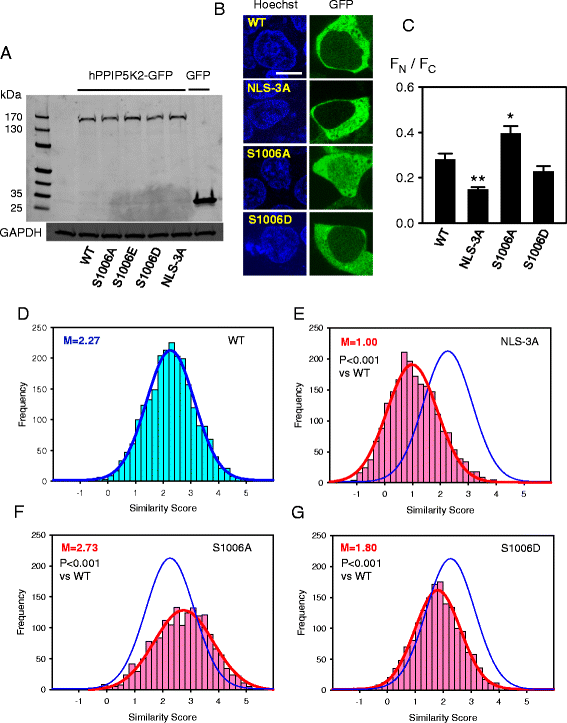
);进一步的双突变实验显示,在核定位信号失活的背景下,S1006A突变对核定位无显著影响,表明磷酸化的调控作用依赖于功能性核定位信号(
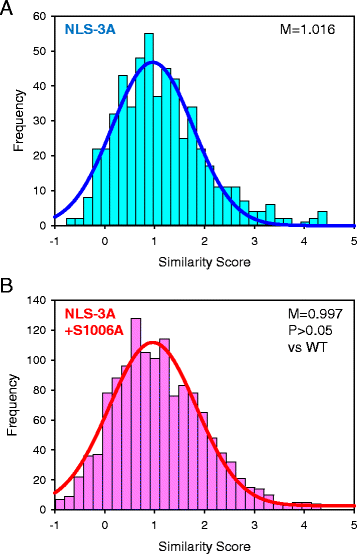
)。实验所用关键产品:TiO2磷酸肽富集tips(Glygen)、Promega胰蛋白酶。
4. Biomarker研究及发现成果
本研究中涉及的功能性生物标志物为hPPIP5K2的C末端五聚精氨酸核定位信号及邻近的S1006磷酸化位点,筛选与验证逻辑遵循“生物信息学保守性分析→细胞功能验证→翻译后修饰鉴定→突变体功能确认”的完整链条。
核定位信号的来源为hPPIP5K2的C末端保守结构域,验证方法包括共聚焦显微镜观察、成像流式细胞术量化及突变体功能分析,其特异性表现为突变后核定位水平显著降低3.6倍(P<0.001);S1006磷酸化位点通过质谱鉴定,验证方法为突变体功能分析,敏感性表现为磷酸化模拟突变使核定位水平降低40%(P<0.001)。核心成果提炼显示,该核定位信号是PPIP5K家族中首个被鉴定的功能性核定位信号,S1006磷酸化是其核定位的负调控因子,首次揭示了PPIP5K家族的共价修饰调控机制,为肌醇焦磷酸的区室化合成调控提供了新的靶点,同时为核定位信号的预测算法优化提供了实验依据;统计学结果显示,NLS突变使核定位水平显著降低(P<0.001),S1006A突变使核定位水平显著提升(P<0.001),数据具备统计学显著性。
