1. 领域背景与文献引入
文献英文标题:Requirement of Osteopontin in the migration and protection against Taxol-induced apoptosis via the ATX-LPA axis in SGC7901 cells;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:胃癌分子生物学、肿瘤信号通路与化疗耐药。
领域共识:胃癌是全球范围内高发的消化系统恶性肿瘤,发展中国家发病率显著高于发达国家,化疗耐药是临床治疗中亟待解决的核心问题之一。肿瘤信号通路研究中,自分泌运动蛋白(ATX)-溶血磷脂酸(LPA)轴和骨桥蛋白(OPN)均被证实参与胃癌细胞的存活、迁移及侵袭过程,ATX通过催化溶血磷脂酰胆碱(LPC)生成LPA,激活下游信号通路促进肿瘤进展,OPN作为多功能细胞因子,在胃癌组织中高表达并与不良预后相关。然而,现有研究多独立探讨两者的功能,尚未明确ATX-LPA轴与OPN之间的调控关系,也缺乏对两者在化疗耐药中协同作用的机制解析,这一研究空白限制了对胃癌进展分子机制的全面理解,也为开发新的治疗靶点带来阻碍。因此,本研究聚焦ATX-LPA轴与OPN的相互作用,旨在揭示其调控机制及在胃癌细胞迁移和紫杉醇耐药中的功能,为胃癌治疗提供新的理论依据。
2. 文献综述解析
作者对领域内现有研究的分类维度为ATX-LPA轴的生物学功能、OPN在肿瘤中的作用、两者作为肿瘤标志物的应用三个方向,系统梳理了各方向的研究进展与局限性,进而明确本研究的创新定位。
现有研究证实,ATX-LPA轴参与血管生成、慢性炎症及多种肿瘤的进展,其通过G蛋白偶联受体(GPCR)介导下游信号通路激活,调控细胞增殖与迁移;OPN作为细胞外基质蛋白,在胃癌、肺癌等多种肿瘤中高表达,参与细胞存活、侵袭及转移过程,部分研究将其作为肿瘤诊断与预后的潜在生物标志物。技术方法上,现有研究多采用细胞系实验、临床样本分析等手段,明确了单个分子的功能,但存在局限性:一方面,缺乏对ATX-LPA轴与OPN调控关系的机制研究,无法解释两者在肿瘤进展中的协同作用;另一方面,现有研究未涉及两者在化疗耐药中的关联,难以指导临床化疗方案的优化。
通过对比现有研究的未解决问题,本研究的创新点在于首次揭示ATX-LPA轴通过LPA2受体激活Akt和ERK信号通路调控OPN的表达,且明确OPN是ATX-LPA轴介导胃癌细胞迁移和紫杉醇耐药的必需分子,填补了两者调控机制及化疗耐药关联研究的空白,为胃癌的靶向治疗提供了新的潜在靶点组合。
3. 研究思路总结与详细解析
本研究的整体研究目标为明确ATX-LPA轴与OPN的调控关系及在胃癌细胞迁移和紫杉醇耐药中的功能,核心科学问题是ATX-LPA轴如何通过信号通路调控OPN表达,以及OPN在该轴介导的肿瘤表型中的作用,技术路线遵循“分子表达调控验证→信号通路机制解析→功能表型验证”的闭环逻辑,通过细胞系实验、分子生物学技术及功能学实验逐步验证假设。
3.1 ATX-LPA轴对OPN表达的调控验证
实验目的为确认ATX-LPA轴是否能够诱导胃癌细胞中OPN的表达,明确两者的上下游调控关系。实验方法采用人胃癌SGC7901细胞系,分别用ATX(50ng/ml)、LPC(10μM/20μM)、LPA(10μM)、ATX+LPC(两种浓度组合)处理细胞,设置未处理对照组,处理24小时后提取细胞总蛋白和RNA,通过免疫印迹(WB)检测OPN蛋白水平,实时荧光定量PCR检测OPN mRNA水平。实验结果显示,与未处理细胞相比,LPA、ATX+LPC处理组的OPN蛋白水平分别上调1.58倍、1.63倍、1.92倍(n=3,P<0.05),mRNA水平上调1.3倍(n=3,P<0.05),而ATX或LPC单独处理未引起OPN表达的显著变化,表明ATX-LPA轴是OPN表达的上游调控因素,且需要ATX催化LPC生成LPA才能发挥作用。
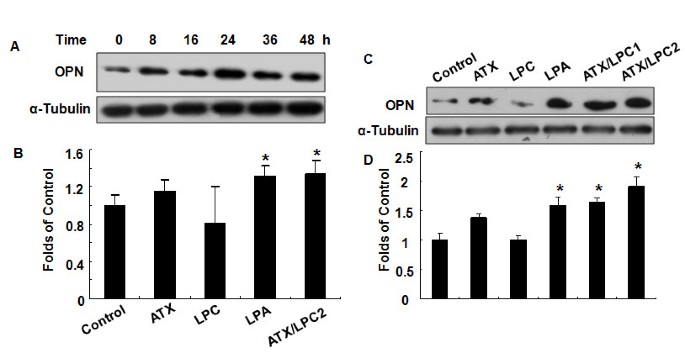
实验所用关键产品:R&D Systems的重组人ATX蛋白和OPN抗体,Sigma-Aldrich的LPA、LPC、紫杉醇等试剂,Cell Signaling Technology的磷酸化ERK和Akt抗体。
3.2 调控OPN表达的信号通路解析
实验目的为明确ATX-LPA轴调控OPN表达的特异性受体及下游信号通路,解析分子调控的具体机制。实验方法首先检测SGC7901细胞中LPA受体(LPA1-LPA4)的表达,通过实时荧光定量PCR分析ATX+LPC处理后各受体的表达变化;随后采用LPA受体抑制剂Ki16425、ERK抑制剂PD98059、Akt抑制剂LY294002预处理细胞,再用ATX+LPC处理,通过免疫印迹检测OPN蛋白水平;同时通过荧光素酶报告实验检测转录因子Elk-1的活性,明确其在调控中的作用。实验结果显示,ATX+LPC处理后LPA2受体表达显著上调,提示LPA2是介导ATX-LPA轴调控OPN的主要受体;免疫印迹结果显示,ATX+LPC处理可显著激活ERK和Akt的磷酸化,而抑制剂处理后OPN表达显著降低;荧光素酶报告实验显示,ATX+LPC处理使Elk-1的转录活性上调2.7倍(n=3,P<0.05),抑制剂处理可显著抑制该活性,表明ATX-LPA轴通过LPA2受体激活Akt和ERK通路,进而通过Elk-1转录因子调控OPN的表达。
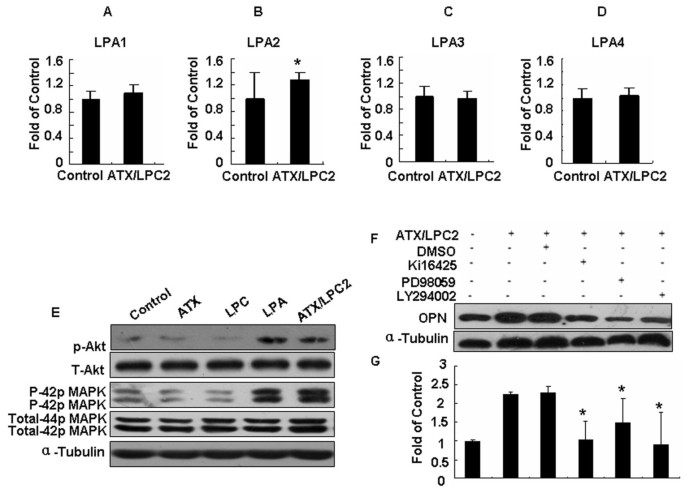
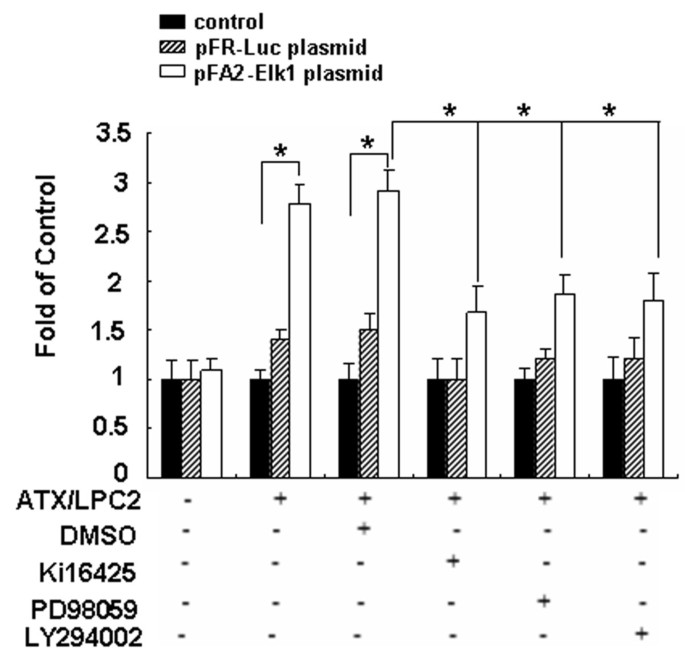
3.3 OPN在ATX-LPA轴功能中的作用验证
实验目的为确认OPN是否为ATX-LPA轴介导胃癌细胞迁移和紫杉醇耐药所必需的分子,明确其功能依赖性。实验方法首先构建OPN敲低的SGC7901细胞系,通过免疫印迹验证敲低效率;随后采用Transwell迁移实验,检测ATX+LPC处理对敲低OPN细胞和对照组细胞迁移能力的影响;同时采用流式细胞术,检测ATX+LPC处理对紫杉醇诱导的敲低OPN细胞和对照组细胞凋亡的影响。实验结果显示,OPN敲低细胞系中OPN蛋白水平显著降低;Transwell迁移实验显示,ATX+LPC处理可使对照组细胞迁移数从169个增加至670个(n=3,P<0.05),但对OPN敲低细胞的迁移能力无显著影响;流式细胞术结果显示,紫杉醇处理使对照组细胞凋亡率达64%,ATX+LPC处理可将凋亡率降至21%(n=3,P<0.05),而在OPN敲低细胞中,ATX+LPC处理仅能将凋亡率降至37.7%(n=3,P<0.05),表明OPN是ATX-LPA轴介导胃癌细胞迁移和紫杉醇耐药的必需分子。
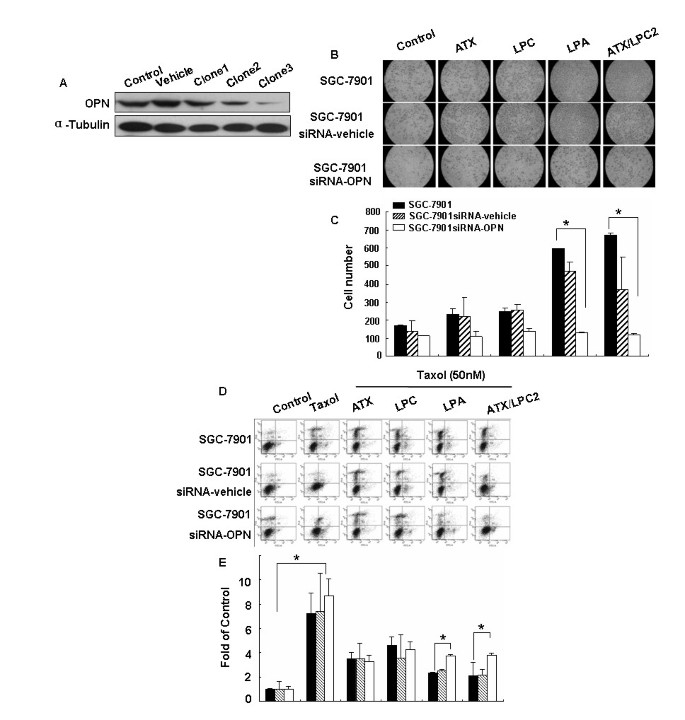
4. Biomarker研究及发现成果
本研究涉及的Biomarker为骨桥蛋白(OPN),其作为ATX-LPA轴的下游效应分子,筛选与验证逻辑为“细胞系表达调控验证→信号通路机制解析→功能表型验证”,完整明确了其在胃癌细胞迁移及化疗耐药中的功能价值。
OPN的来源为人胃癌SGC7901细胞系,验证方法包括免疫印迹、实时荧光定量PCR、Transwell迁移实验及流式细胞术。特异性方面,OPN仅在ATX-LPA轴激活时表达显著上调,未激活状态下表达水平较低;敏感性方面,ATX+LPC处理可使OPN蛋白水平上调1.92倍(n=3,P<0.05),mRNA水平上调1.3倍(n=3,P<0.05),具有显著的表达响应性。
本研究证实OPN是ATX-LPA轴介导胃癌细胞迁移和紫杉醇耐药的必需分子,其功能关联表现为:OPN表达缺失后,ATX-LPA轴无法促进胃癌细胞迁移,也无法有效抑制紫杉醇诱导的细胞凋亡;创新性在于首次揭示ATX-LPA轴通过LPA2受体激活Akt和ERK通路调控OPN表达的分子机制,明确了两者在胃癌进展中的协同作用;统计学结果显示,所有关键指标的组间差异均具有显著性(P<0.05),样本量为3次独立重复实验。此外,OPN作为潜在的胃癌化疗耐药生物标志物,其表达水平可能与紫杉醇治疗的疗效相关,为临床化疗方案的个体化调整提供了潜在参考。
