1. 领域背景与文献引入
文献英文标题:Glycosylation, transport, and complex formation of palmitoyl protein thioesterase 1 (PPT1) – distinct characteristics in neurons;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:神经退行性疾病(婴儿型神经元蜡样脂褐质沉积症)、溶酶体酶功能研究
领域共识:神经元蜡样脂褐质沉积症(NCLs)是一类最常见的隐性遗传性儿童脑病,其中婴儿型神经元蜡样脂褐质沉积症(INCL)是最严重的亚型,由CLN1基因的功能缺失突变导致棕榈酰蛋白硫酯酶1(PPT1)缺陷,进而引发新皮质神经元的特异性进行性死亡,但具体致病机制尚未完全明确。
现有研究已证实PPT1是溶酶体水解酶,通过去除蛋白质的棕榈酰化修饰参与细胞内蛋白稳态调控,且神经元中PPT1存在轴突、突触小体等溶酶体外定位,提示其可能参与神经信号传递或突触功能调控;但不同细胞类型中PPT1的翻译后修饰、细胞内转运差异,以及PPT1是否形成功能性复合物等关键问题尚未明确,这些空白限制了对INCL发病机制的理解和针对性治疗策略的开发。因此,本研究聚焦上述核心问题,通过优化实验策略深入解析PPT1的基本特性,为INCL的分子致病机制研究提供新的依据。
2. 文献综述解析
作者对领域内现有研究的分类维度包括PPT1的基本功能与疾病关联、糖基化修饰的作用、细胞类型特异性特性、疾病突变的表型关联四个方向,系统梳理了现有研究的结论、技术局限性,并明确了本研究的创新切入点。
现有研究的关键结论主要包括:PPT1的三个N-糖基化位点(N197、N212、N232)均会被翻译后修饰利用,且糖基化修饰与酶的溶酶体定位相关;INCL的临床表型(发病年龄、疾病进展速度)与CLN1突变类型相关,但基因型与表型的具体关联机制尚未明确。现有研究的技术方法优势在于建立了稳定的细胞和动物模型用于PPT1功能研究,明确了PPT1与INCL的直接因果关系;但局限性也较为明显:之前的糖基化突变策略(天冬酰胺→谷氨酰胺,N→Q)可能改变蛋白的空间结构,无法精准评估糖基化位点的功能;未系统比较神经元与非神经元细胞中PPT1的修饰和转运差异;未探究PPT1在体内的分子相互作用(如复合物形成);也未深入分析疾病突变对PPT1糖基化和复合物形成的影响。
通过对比现有研究的未解决问题,本研究的创新价值凸显:首次采用丝氨酸→丙氨酸(S→A)的糖基化位点突变策略,避免改变蛋白的主链结构,精准评估糖基化对PPT1功能的影响;首次系统揭示神经元与非神经元细胞中PPT1的翻译后修饰和细胞内转运差异;首次证实PPT1在体内能形成同源寡聚体;并分析了不同表型的疾病突变对PPT1糖基化、复合物形成等特性的影响,为INCL的发病机制研究补充了关键数据。
3. 研究思路总结与详细解析
本研究的整体研究目标是明确PPT1糖基化修饰对其酶活性和细胞内转运的调控作用,揭示神经元与非神经元细胞中PPT1的修饰、转运差异,探究PPT1的体内复合物形成特性,以及疾病突变对上述特性的影响;核心科学问题是PPT1的糖基化、转运和复合物形成在不同细胞类型中的功能意义,以及这些特性与INCL发病的关联;技术路线遵循“突变体构建→细胞模型验证→分子特性分析→突变体功能评估→结论总结”的闭环逻辑,通过多种细胞生物学和生物化学技术系统解析PPT1的特性。
3.1 PPT1糖基化位点突变对酶活性与细胞内转运的影响
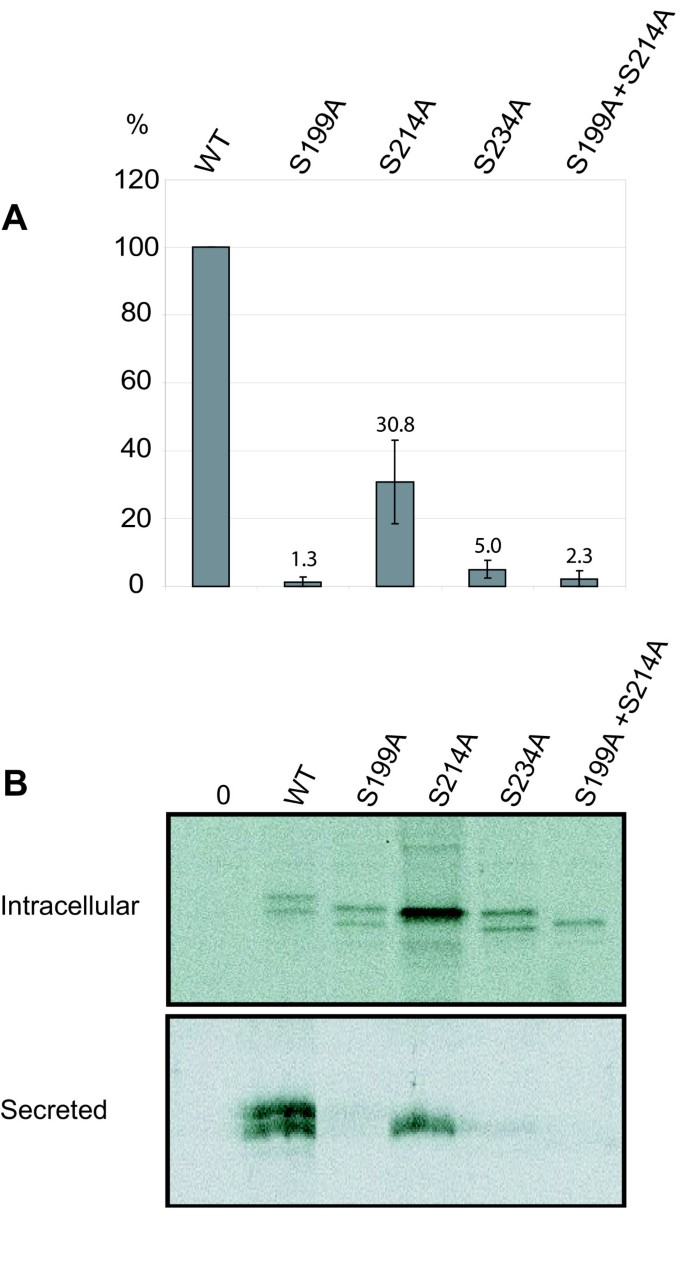
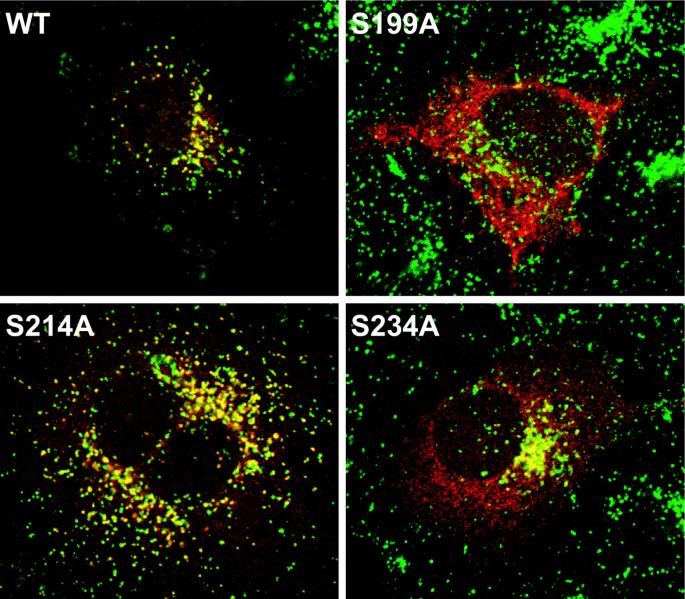
实验目的:明确PPT1的三个N-糖基化位点(N197、N212、N232)对其酶活性和细胞内转运的调控作用,避免之前突变策略对蛋白结构的干扰。方法细节:通过定点诱变将PPT1糖基化共有序列(N-X-S/T)中的丝氨酸突变为丙氨酸,构建S199A(对应N197位点)、S214A(对应N212位点)、S234A(对应N232位点)单突变体及S199A+S214A双突变体,将这些突变体及野生型PPT1转染至COS-1和HeLa细胞,转染48小时后裂解细胞,以总蛋白量标准化后检测PPT1酶活性;采用35S-半胱氨酸代谢标记1小时、 chase 2小时的方法,结合免疫沉淀分析PPT1的细胞内加工过程;通过免疫荧光染色结合溶酶体标记物LAMP-1、内质网标记物PDI,分析突变体的细胞内定位。
结果解读:酶活性检测结果显示,S214A突变体保留约31%的野生型酶活性(n=3,文献未明确提供P值),而S199A、S234A及双突变体的酶活性仅为野生型的1%-5%(n=3,文献未明确提供P值),提示N197和N232位点的糖基化对PPT1的酶活性至关重要,而N212位点的糖基化影响较小。代谢标记与免疫沉淀结果显示,野生型PPT1在细胞内和培养基中均呈现36/38 kDa的成熟形式,S199A和S234A突变体主要滞留在内质网中,无法分泌至培养基,而S214A突变体可正常分泌至培养基。免疫荧光结果显示,S214A突变体可与LAMP-1共定位于溶酶体,S199A突变体与PDI共定位于内质网,S234A突变体部分定位于溶酶体、部分滞留于内质网,进一步证实N197和N232位点的糖基化是PPT1正确转运至溶酶体的必要条件。
实验所用关键产品:文献未提及具体实验产品,领域常规使用细胞转染试剂、放射性代谢标记物、免疫荧光抗体、酶活性检测荧光底物等。
3.2 神经元与非神经元细胞中PPT1的修饰与转运差异分析
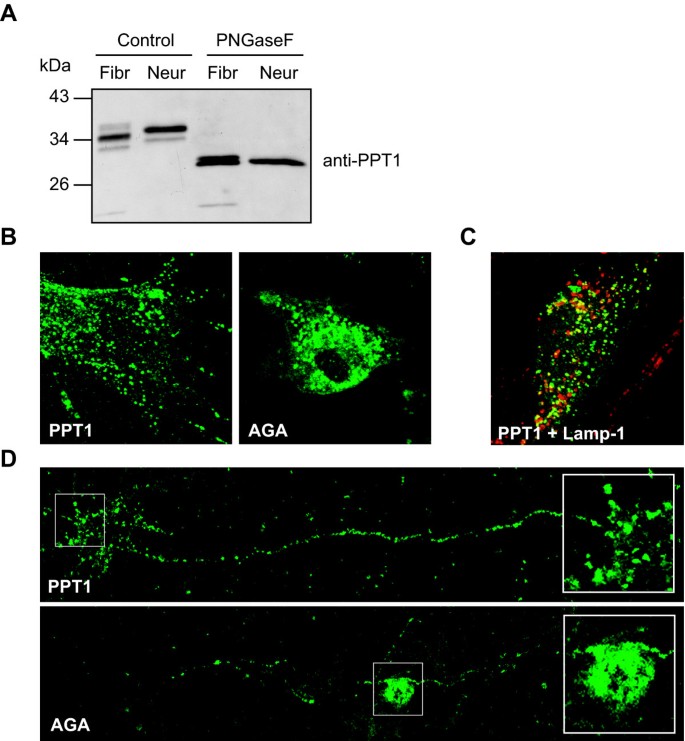
实验目的:系统比较神经元与非神经元细胞中PPT1的翻译后修饰和细胞内转运特性,明确细胞类型特异性差异。方法细节:用携带野生型PPT1的重组腺病毒感染小鼠原代成纤维细胞和神经元,培养4天后裂解细胞,取5μg总蛋白用PNGaseF处理去除N-糖链,通过SDS-PAGE和免疫印迹分析PPT1的修饰差异;采用抗体内化实验,将感染后的细胞与抗PPT1或抗天冬氨酰葡糖胺酶(AGA,经典溶酶体酶,作为对照)抗体共同孵育2小时,更换正常培养基继续培养2小时后固定,免疫荧光染色结合LAMP-1标记物分析抗体的内化定位。
结果解读:免疫印迹结果显示,小鼠成纤维细胞中PPT1呈现三种糖基化形式(单糖基化、双糖基化、三糖基化),其中双糖基化形式最为显著,而神经元中仅能检测到两种糖基化形式;经PNGaseF去除N-糖链后,神经元来源的PPT1条带迁移率仍与成纤维细胞来源的不同,提示除N-糖基化外,PPT1还存在其他细胞类型特异性翻译后修饰。抗体内化实验结果显示,在成纤维细胞中,AGA抗体内化后定位于核周的溶酶体(与LAMP-1共定位),而PPT1抗体内化后主要分布于全细胞的小囊泡中,仅少量与LAMP-1共定位;在神经元中,PPT1抗体内化后在轴突中染色强烈,广泛分布于细胞内的小囊泡中,而AGA抗体内化后主要定位于胞体的溶酶体,仅少量出现在神经突起中。上述结果提示,PPT1的细胞内转运途径与经典溶酶体酶不同,可能存在不依赖甘露糖-6-磷酸(M6P)受体的替代转运途径,且这种差异在神经元和非神经元细胞中均存在。
3.3 PPT1的体内同源寡聚化特性研究
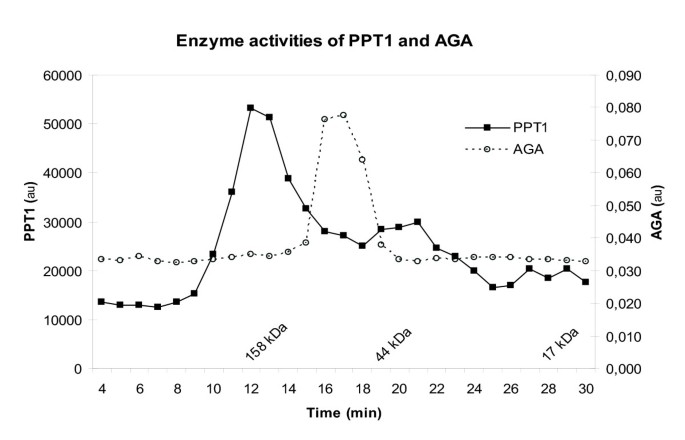
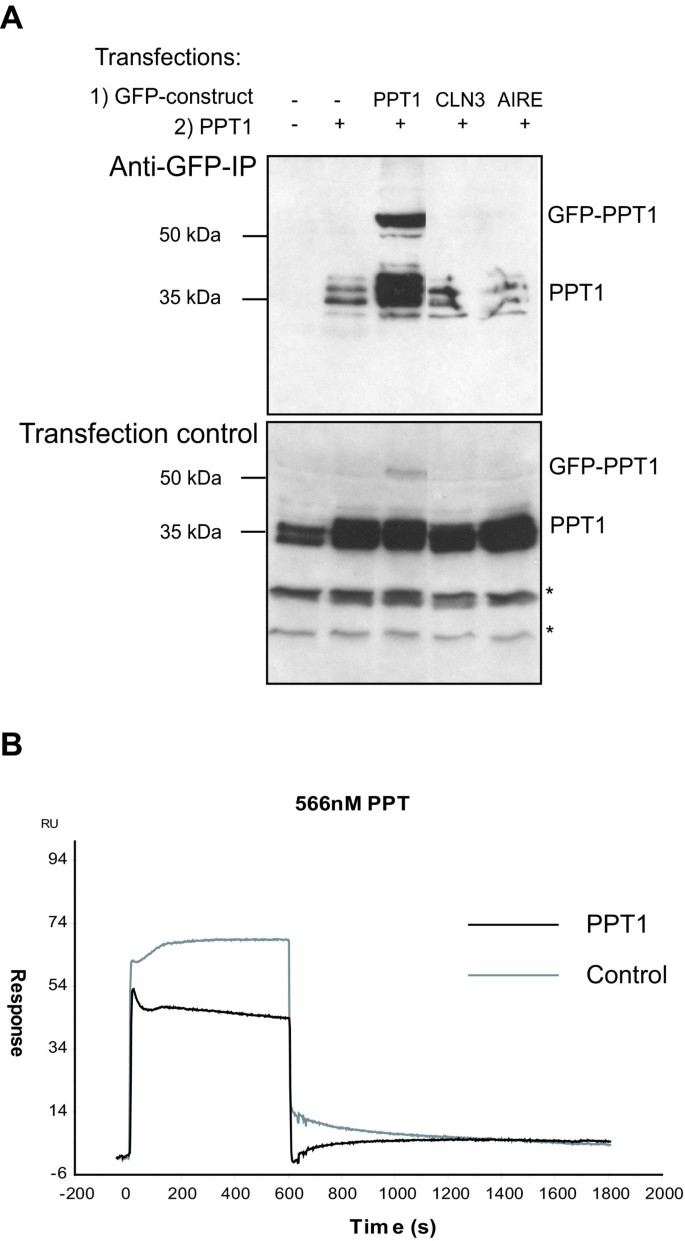
实验目的:探究PPT1在体内是否形成功能性复合物,明确其分子相互作用特性。方法细节:对PC12细胞的溶酶体富集组分进行Superose 6HR体积排阻色谱,收集各洗脱组分并检测PPT1和AGA的酶活性;在COS-1细胞中共转染GFP-PPT1与野生型PPT1、GFP-CLN3、GFP-AIRE(作为阴性对照),转染48小时后裂解细胞,用抗GFP琼脂糖珠进行免疫共沉淀,免疫印迹检测蛋白相互作用;通过Biacore表面等离子体共振技术分析纯化PPT1的直接相互作用。
结果解读:体积排阻色谱结果显示,AGA的酶活性集中在对应二聚体分子量(约80 kDa)的洗脱组分中,而PPT1的酶活性同时分布在分子量>100 kDa的复合物组分和36-38 kDa的单体组分中,提示PPT1在体内存在寡聚体形式。免疫共沉淀结果显示,GFP-PPT1可与野生型PPT1相互作用,而与GFP-CLN3、GFP-AIRE无相互作用,证实PPT1可形成同源寡聚体。Biacore实验结果显示,纯化的重组PPT1在体外条件下不发生直接相互作用,提示PPT1在体内的寡聚化可能依赖细胞内的其他分子或翻译后修饰。
实验所用关键产品:文献未提及具体实验产品,领域常规使用体积排阻色谱柱、免疫共沉淀试剂、Biacore生物传感器等。
3.4 疾病突变对PPT1特性的影响分析
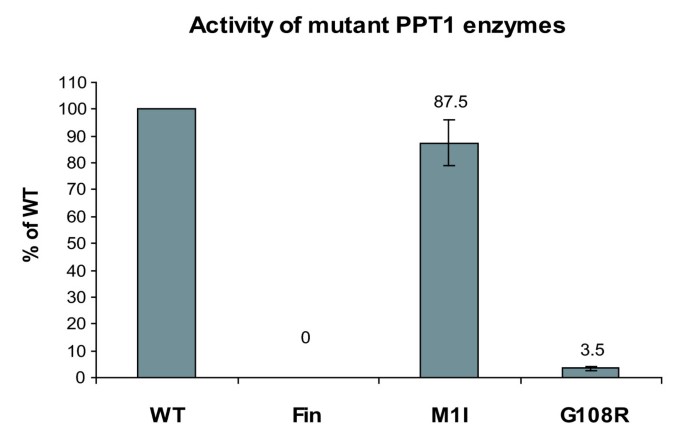
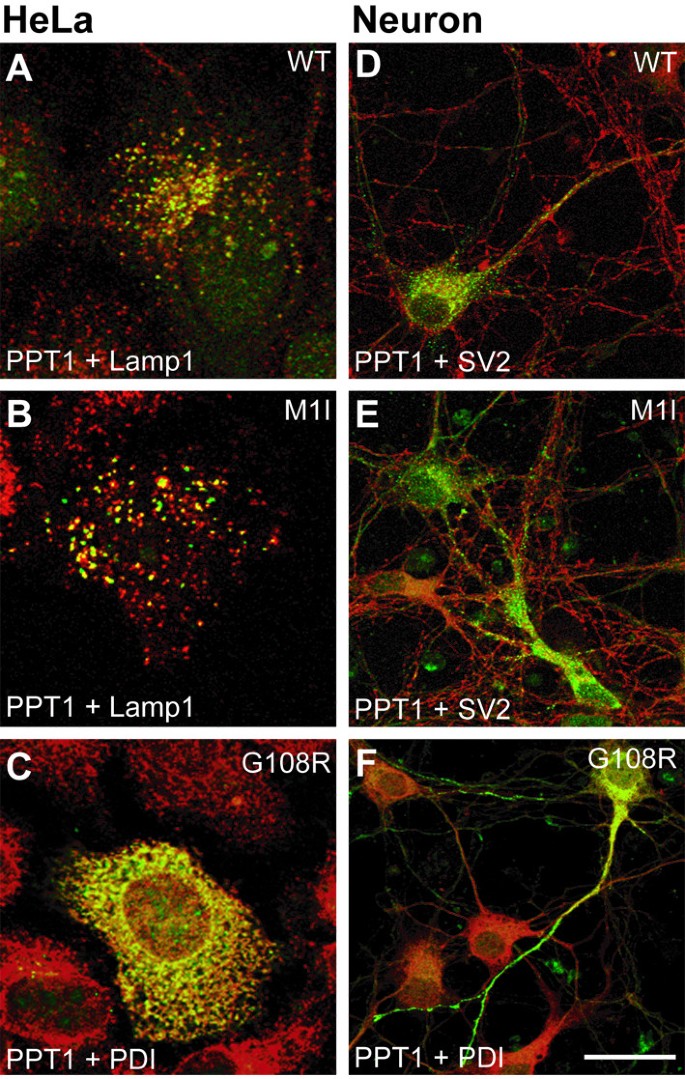
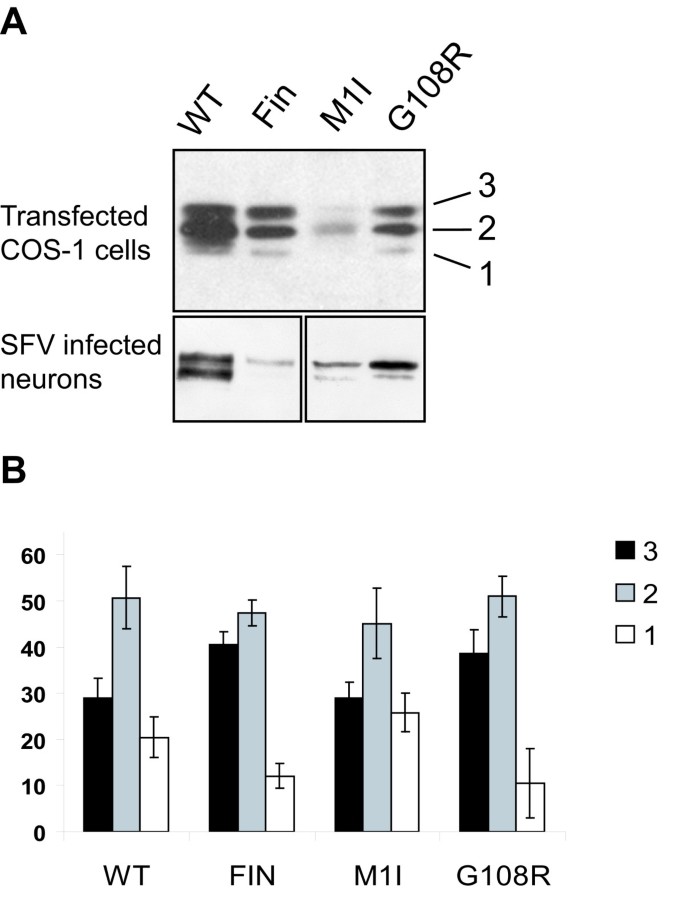
实验目的:分析不同临床表型的CLN1突变对PPT1酶活性、细胞内定位、糖基化程度及寡聚化能力的影响,明确基因型与表型的潜在关联。方法细节:构建携带M1I(晚发婴儿型)、G108R(成人型)、R122W(经典婴儿型)突变的PPT1表达载体,转染至COS-1细胞,转染48小时后裂解细胞,以蛋白表达量标准化后检测酶活性;在HeLa细胞和小鼠原代神经元中进行免疫荧光染色,结合LAMP-1、PDI、突触小体标记物SV2分析突变体的细胞内定位;提取转染细胞和病毒感染神经元的总蛋白,免疫印迹分析突变体的糖基化程度并通过密度扫描定量;在COS-1细胞中共转染突变型GFP-PPT1与对应突变型PPT1,免疫共沉淀分析寡聚化程度。
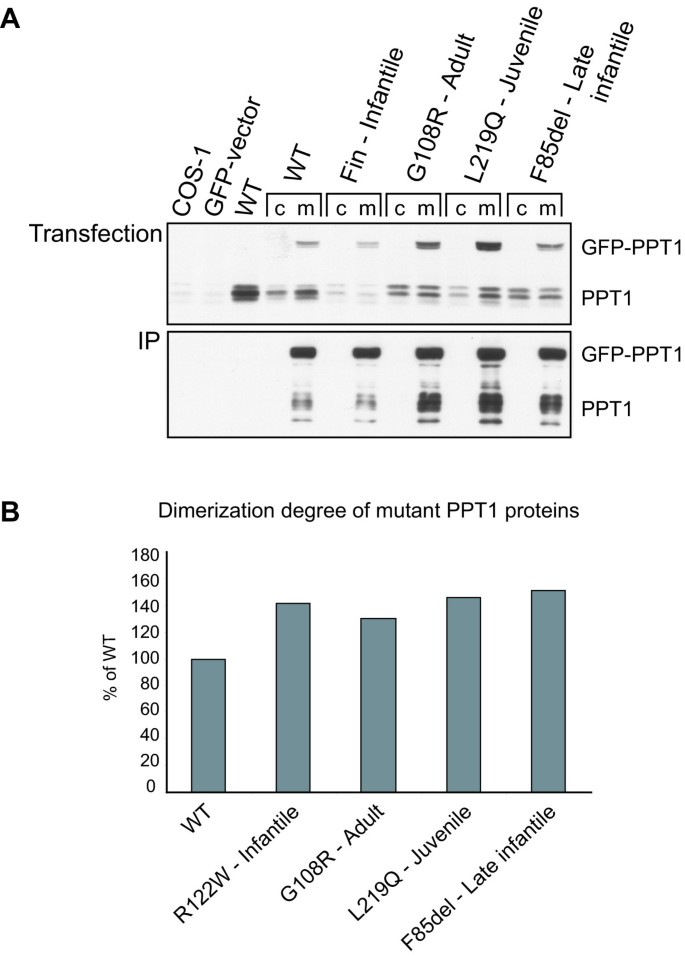
结果解读:酶活性检测结果显示,M1I突变体的酶活性接近野生型,但蛋白表达量降低;G108R突变体的酶活性仅为野生型的4%(n=3,文献未明确提供P值);R122W突变体无酶活性。免疫荧光结果显示,M1I突变体在HeLa细胞中定位于溶酶体,在神经元中定位于神经突起并与SV2部分共定位,与野生型分布一致;G108R突变体在HeLa细胞和神经元中均与PDI共定位于内质网;R122W突变体同样滞留于内质网。免疫印迹定量结果显示,G108R和R122W突变体的三糖基化形式比例为40%,而野生型和M1I突变体的三糖基化形式比例为30%(n=3,文献未明确提供P值),提示疾病突变会增加PPT1的糖基化程度;神经元中这种差异更为显著。免疫共沉淀结果显示,所有突变体的寡聚化程度均高于野生型PPT1,提示疾病突变会增强PPT1的寡聚化能力。但目前这些特性与INCL临床表型的直接关联尚未明确,需进一步研究证实。
实验所用关键产品:文献未提及具体实验产品,领域常规使用荧光底物、免疫印迹检测试剂、免疫共沉淀抗体等。
4. Biomarker研究及发现成果
本研究中,棕榈酰蛋白硫酯酶1(PPT1)作为婴儿型神经元蜡样脂褐质沉积症(INCL)的致病分子,其酶活性、糖基化程度、寡聚化能力可作为INCL的潜在诊断、预后及治疗响应标志物,研究通过细胞模型和临床突变体验证了这些特性与疾病的关联。
Biomarker定位:PPT1是INCL的核心致病分子,其功能特性(酶活性、细胞内定位)、翻译后修饰特性(糖基化程度)、分子相互作用特性(寡聚化能力)可作为INCL的潜在Biomarker,筛选/验证逻辑基于CLN1突变与PPT1功能缺陷的直接因果关系,通过构建野生型和突变型PPT1的细胞表达模型,结合临床突变体的表型特征进行系统验证。
研究过程详述:Biomarker的来源为细胞表达的野生型和不同临床表型的突变型PPT1,验证方法包括:采用荧光底物法检测PPT1的酶活性,免疫印迹结合密度扫描定量分析糖基化程度,免疫共沉淀分析寡聚化能力,免疫荧光分析细胞内定位;特异性与敏感性方面,不同突变体的酶活性差异具有显著特异性,如成人型突变G108R的酶活性仅为野生型的4%,晚发婴儿型突变M1I的酶活性接近野生型;糖基化程度方面,经典婴儿型突变R122W和成人型突变G108R的三糖基化比例比野生型高10%(n=3,文献未明确提供P值),可有效区分突变体与野生型PPT1。
核心成果提炼:PPT1的N-糖基化(N197、N232位点)和同源寡聚化是维持其酶活性和正常细胞内转运的关键特性,INCL相关的CLN1突变会显著改变这些特性:功能缺失突变会降低酶活性、增加糖基化程度、增强寡聚化能力;但目前这些特性与INCL临床表型(发病年龄、疾病进展)的直接关联尚未明确,需进一步结合临床样本验证。本研究首次揭示了PPT1的寡聚化特性,以及神经元与非神经元细胞中PPT1的修饰和转运差异,为INCL的Biomarker研究提供了新的方向,也为优化酶替代疗法等治疗策略提供了分子基础。
