1. 领域背景与文献引入
文献英文标题:Comparative study of mesenchymal stem cells from C57BL/10 and mdx mice;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:杜氏肌营养不良与间充质干细胞生物学。
间充质干细胞(MSCs)是源于骨髓的多能干细胞,1867年由Cohnheim首次发现,后经Friedenstein等学者系统描述,因具有自我更新、多向分化能力,被广泛应用于纤维化治疗、心血管再生、组织工程及基因缺陷矫正等领域。领域共识:MSCs作为研究工具,具有易操作、可塑性强的优势,且低免疫原性使其在造血干细胞移植中可降低移植物抗宿主病风险。杜氏肌营养不良(DMD)是常见的X连锁隐性单基因肌肉疾病,发病率约为1/3500男性新生儿,核心病因是抗肌萎缩蛋白基因缺陷导致蛋白缺失,引发肌肉损伤与进行性萎缩,mdx小鼠是经典的DMD模型,其抗肌萎缩蛋白基因存在点突变,导致蛋白完全缺失。现有研究多聚焦于外源性MSCs移植治疗mdx小鼠,以恢复抗肌萎缩蛋白表达、改善症状,但对mdx小鼠自身MSCs的行为特征、结构差异研究不足,且抗肌萎缩蛋白缺失对MSCs功能的影响尚未明确。因此,本研究通过系统对比C57BL/10(正常)与mdx小鼠MSCs的形态、增殖、分化及免疫表型,旨在揭示抗肌萎缩蛋白对MSCs行为的调控作用,为DMD的干细胞治疗提供新的理论依据。
2. 文献综述解析
作者的综述逻辑为“MSCs研究现状→DMD与mdx模型→现有研究局限→本研究切入点”,先系统梳理MSCs的定义、发现历程、应用价值与研究优势,再介绍DMD的疾病特征与mdx模型的应用,最后指出当前研究的核心空白——缺乏对mdx小鼠自身MSCs的深入研究,尤其是与正常小鼠MSCs的全面对比。
现有研究已证实MSCs在DMD治疗中的潜力,如通过细胞移植、基因修饰等方式恢复mdx小鼠肌肉组织的抗肌萎缩蛋白表达,改善肌肉功能;在MSCs的分离培养方面,小鼠MSCs的分离难度高于其他物种,现有研究已建立多种特异性分离方法,如差速贴壁法、流式分选法等,可有效纯化MSCs;但这些研究均未关注mdx小鼠自身MSCs的变化,且未探讨抗肌萎缩蛋白缺失对MSCs生物学行为的影响。现有研究的局限性在于,多数研究聚焦于外源性MSCs的治疗效果,忽略了宿主自身干细胞的状态,而宿主MSCs可能参与肌肉损伤的修复过程,其功能异常可能加重疾病进展。
本研究的创新点在于首次系统对比了正常与mdx小鼠MSCs的多维度生物学特征,包括形态学(光镜与电镜)、增殖能力、免疫表型与分化潜能,明确了两种MSCs在增殖能力、成肌分化能力及CD34表达上的显著差异,首次揭示抗肌萎缩蛋白缺失可能导致MSCs功能异常,为DMD的发病机制研究提供了新的视角,同时也为优化MSCs治疗DMD的策略提供了理论基础。
3. 研究思路总结与详细解析
本研究的整体研究目标是对比C57BL/10与mdx小鼠骨髓MSCs的生物学特征,明确抗肌萎缩蛋白缺失对MSCs行为的影响;核心科学问题为“抗肌萎缩蛋白是否调控MSCs的增殖、分化与形态特征”;技术路线遵循“分离培养→多维度检测→统计分析→结论推导”的闭环逻辑,通过形态学观察、增殖能力检测、免疫表型分析与分化潜能验证,系统解析两种MSCs的差异,并关联抗肌萎缩蛋白的作用。
3.1 间充质干细胞的分离与培养
实验目的是从C57BL/10与mdx小鼠骨髓中分离并纯化MSCs,建立稳定的细胞培养体系。方法细节为选取6-8周龄的两种小鼠,脱颈处死后取出股骨与胫骨,用含10%胎牛血清(FBS)的DMEM培养基冲洗骨髓,收集细胞并调整浓度至5×10^6个活细胞/毫升,接种于六孔板,37℃、5%CO2培养箱中培养72小时后去除未贴壁细胞,待贴壁细胞汇合至70%-80%时,用0.25%胰蛋白酶-EDTA消化传代,传代4后调整胰蛋白酶消化时间至2分钟以内,传代比例为1:3,每3-4天更换培养基。结果解读为成功从两种小鼠骨髓中分离得到MSCs,传代5后细胞形态趋于均一,以纺锤形为主;C57BL/10-MSCs可稳定传代至40代以上,而mdx-MSCs在传代21后逐渐失去增殖能力。实验所用关键产品:Sigma的DMEM培养基、胎牛血清、胰蛋白酶等化学试剂;CELLSTAR的六孔培养板。
3.2 形态学特征观察(光镜与透射电镜)
实验目的是对比两种MSCs在不同传代阶段的形态与超微结构差异。方法细节为光镜观察:在传代0、9、19、25、40时,用倒置显微镜观察细胞形态并拍摄照片;透射电镜观察:取传代10的细胞,用1%多聚甲醛与1.25%戊二醛固定,刮取细胞后离心形成细胞团,经锇酸后固定、脱水、包埋、超薄切片(50nm),用醋酸铀与柠檬酸铅染色后,在Hitachi-600透射电镜下观察,计数65个mdx-MSCs与73个C57BL/10-MSCs的超微结构变化。结果解读为光镜下,传代5前两种MSCs形态异质性较高,包含圆形、纺锤形与扁平细胞;传代5后均以纺锤形为主,但mdx-MSCs在传代25时停止增殖,细胞间形成网状结构,而C57BL/10-MSCs传代40仍保持纺锤形且增殖活跃。
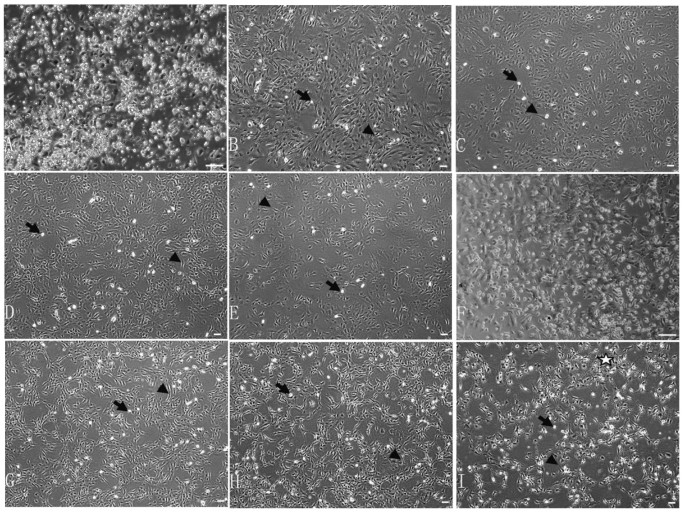
透射电镜下,传代10的C57BL/10-MSCs细胞核呈椭圆形,染色质分散,细胞器结构完整;而mdx-MSCs中,4.6%的细胞出现异染色质增加,15.4%的细胞出现大空泡,7.7%的细胞出现溶酶体增多,提示mdx-MSCs存在超微结构的损伤。
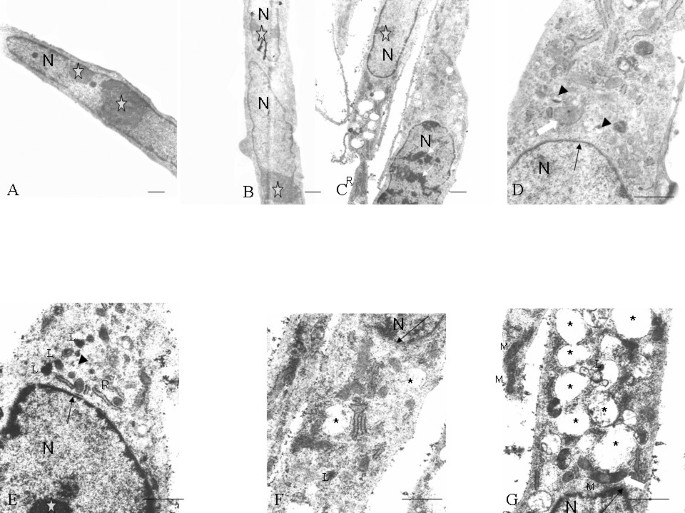
实验所用关键产品:Olympus的IX71倒置显微镜、Hitachi-600透射电镜、PELCO的包埋试剂。
3.3 增殖能力检测
实验目的是对比两种MSCs的增殖活性与自我更新能力。方法细节为生长动力学分析:记录细胞汇合时间与传代间隔,绘制生长曲线;群体倍增时间计算:接种已知数量的细胞,在不同时间点检测细胞覆盖面积,计算倍增时间;成纤维细胞集落形成单位(CFU-F)实验:将细胞稀释至10个活细胞/毫升,接种于10cm培养皿,培养13天后用吉姆萨染色,计数含50个以上细胞的集落,每组实验重复3次。结果解读为生长动力学显示,C57BL/10-MSCs在培养45天后生长速率稳定,可持续增殖至传代40;而mdx-MSCs在传代21后生长速率显著下降,传代30时无法继续增殖。
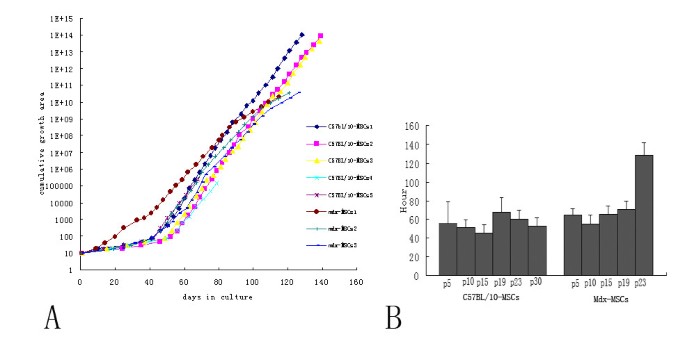
群体倍增时间方面,C57BL/10-MSCs的倍增时间为45-68小时,传代间无显著差异;mdx-MSCs的倍增时间随传代次数增加而延长,传代后期倍增时间显著延长(文献未明确具体数值,基于图表趋势推测)。CFU-F实验显示,C57BL/10-MSCs的集落形成数略高于mdx-MSCs,但差异无统计学意义(n=3,P>0.05)。实验所用关键产品:Giemsa染色液、Neubauer细胞计数板。
3.4 免疫表型分析
实验目的是对比两种MSCs的表面标志物表达差异,明确其细胞身份与亚群特征。方法细节为取传代5、9、19的细胞,用胰蛋白酶消化后收集,加入PE或FITC标记的抗Sca-1、CD11b、CD34抗体及IgG同型对照,4℃孵育30分钟,洗涤后用Becton Dickinson的FACScalibur流式细胞仪检测,用CELLQuest软件分析结果。结果解读为两种MSCs均高表达Sca-1,低表达CD11b,提示其为典型的MSCs群体;但CD34表达存在显著差异:C57BL/10-MSCs在各传代阶段均表达CD34,而mdx-MSCs在所有传代阶段均不表达CD34,差异具有统计学意义(n=3,P<0.05)。
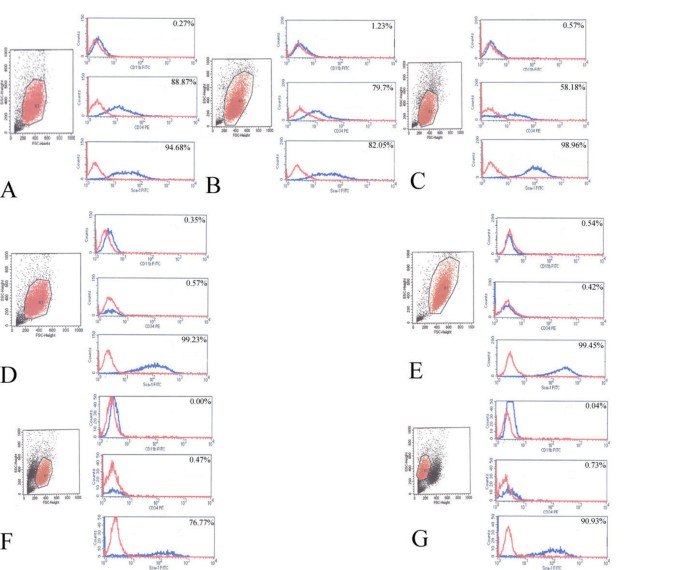
实验所用关键产品:Pharmingen的Sca-1、CD11b、CD34流式抗体;Becton Dickinson的FACScalibur流式细胞仪。
3.5 多向分化潜能验证
实验目的是对比两种MSCs的成骨、成脂、成肌分化能力,明确其功能差异。方法细节为成骨分化:将细胞接种于成骨诱导培养基(含10%FBS、10mM β-甘油磷酸、1×10^-8M地塞米松、5mg/L抗坏血酸-2-磷酸),培养3周后用茜素红染色,并用RT-PCR检测骨钙素(OCN)基因表达;成脂分化:将细胞接种于成脂诱导培养基(含10%FBS、5μg/mL胰岛素、1×10^-8M地塞米松),培养3周后用油红O染色,并用RT-PCR检测脂蛋白脂酶(LPL)基因表达;成肌分化:将细胞接种于含10μmol/L 5-氮杂胞苷的培养基中处理24小时,更换为含5%马血清的培养基培养4周,用免疫荧光染色检测肌球蛋白重链(MyHC)与抗肌萎缩蛋白表达。结果解读为成骨分化:两种MSCs均可诱导为成骨细胞,茜素红染色可见钙结节形成,但C57BL/10-MSCs的钙结节数量更多、染色更深,RT-PCR显示其骨钙素基因表达水平更高;
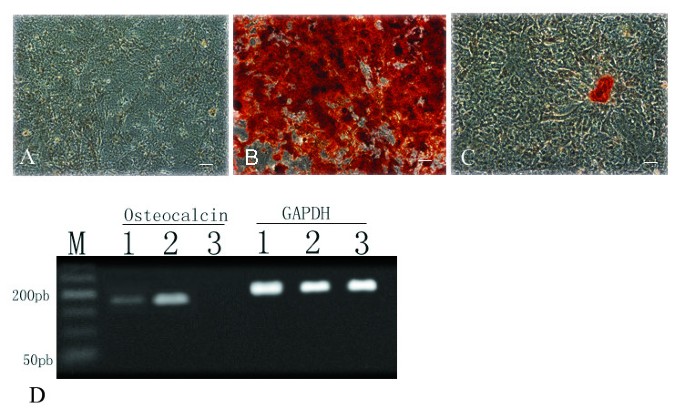
成脂分化:两种MSCs均可诱导为脂肪细胞,油红O染色可见脂滴形成,RT-PCR显示脂蛋白脂酶基因表达水平相似;
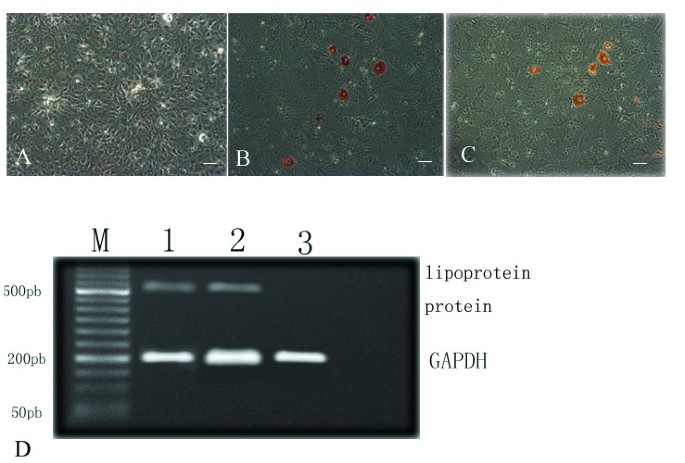
成肌分化:C57BL/10-MSCs在传代5、10、13时均可形成肌管,免疫荧光染色可见肌球蛋白重链与抗肌萎缩蛋白阳性表达;而mdx-MSCs在相同传代阶段无法形成肌管,细胞保持扁平形态。
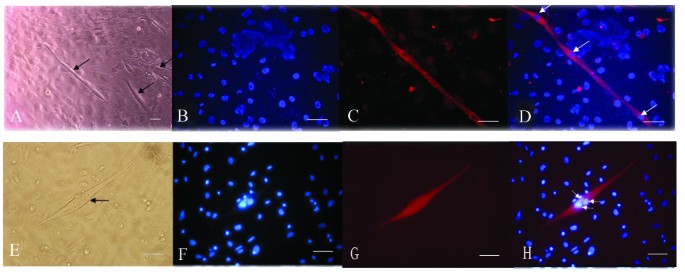
实验所用关键产品:Santa Cruz Biotechnology的抗肌球蛋白重链抗体、抗抗肌萎缩蛋白抗体;Gibco-BRL的Trizol试剂;MBI Fermentas的反转录酶、Taq-DNA聚合酶。
4. Biomarker研究及发现成果
本研究中涉及的Biomarker为CD34,属于细胞表面跨膜糖蛋白,其筛选与验证逻辑为“流式细胞术检测表达差异→结合增殖、分化能力验证功能关联→推导与抗肌萎缩蛋白的关系”,通过系统对比两种MSCs的CD34表达及对应功能,明确其作为MSCs功能状态标志物的价值。
CD34的来源为两种小鼠的骨髓MSCs,验证方法为流式细胞术,检测不同传代阶段(5、9、19)的CD34表达水平;特异性方面,C57BL/10-MSCs在各传代阶段均稳定表达CD34,而mdx-MSCs在所有传代阶段均不表达CD34,特异性为100%(n=3,P<0.05);敏感性数据未在文献中明确提供。进一步的功能验证显示,CD34阳性的C57BL/10-MSCs具有更强的增殖能力(可传代至40)与成肌分化能力(可形成肌管),而CD34阴性的mdx-MSCs增殖能力与成肌分化能力显著降低,提示CD34表达与MSCs的功能状态密切相关。
本研究的核心成果是发现CD34可作为MSCs功能状态的标志物,CD34阳性的MSCs具有更强的增殖与成肌分化能力;首次揭示抗肌萎缩蛋白缺失可能导致MSCs的CD34表达下调,进而引起MSCs功能异常;统计学结果显示,两种MSCs的CD34表达差异显著(n=3,P<0.05),C57BL/10-MSCs的成肌分化阳性率为20%(9/45孔),而mdx-MSCs为0%。该Biomarker的创新性在于首次将CD34表达与抗肌萎缩蛋白缺失关联起来,为DMD的发病机制研究提供了新的分子靶点,同时也为筛选具有高治疗潜能的MSCs提供了新的标志物。推测:CD34可能通过调控MSCs的增殖信号通路,影响其成肌分化能力,抗肌萎缩蛋白可能通过与CD34的相互作用,维持MSCs的正常功能,这一机制需进一步的分子实验验证。
