1. 领域背景与文献引入
文献英文标题:Delayed internalization and lack of recycling in a beta₂-adrenergic receptor fused to the G protein alpha-subunit;发表期刊:BMC Cell Biology;影响因子:未明确提供;研究领域:G蛋白偶联受体(GPCR)细胞内转运与信号调控
G蛋白偶联受体是目前已知最大的细胞膜受体家族,参与几乎所有生理过程的信号转导,其功能平衡由信号激活、脱敏、复敏的分子机制精密调控。领域发展关键节点可追溯至1990年代,彼时科研人员明确G蛋白偶联受体的脱敏依赖G蛋白偶联受体激酶(GRK)的磷酸化作用与arrestin蛋白的结合;2000年后,实时荧光成像技术的应用推动了G蛋白偶联受体内吞后分选至循环内体或溶酶体的动态过程研究。当前研究热点聚焦于不同G蛋白偶联受体亚型的转运差异机制、G蛋白与受体的相互作用对转运的调控等方向,而未解决的核心问题在于,G蛋白偶联受体与G蛋白的物理结合状态如何影响其内吞后的分选与循环,尤其是融合型G蛋白偶联受体的转运规律尚未得到系统解析。
现有研究显示,β₂-肾上腺素能受体(β₂AR)作为原型G蛋白偶联受体,在激动剂刺激后会快速内吞并循环回细胞膜以恢复信号功能,但β₂AR与Gαₛ融合后的转运特征未被系统探究。本研究旨在对比野生型与Gαₛ融合型β₂AR的内吞及循环动力学,明确G蛋白与受体的共价连接对其细胞内转运的影响,为G蛋白偶联受体信号调控的分子机制提供新的实验依据与理论视角。
2. 文献综述解析
作者从G蛋白偶联受体转运的分子机制、亚型差异、研究技术三个维度梳理了领域内的现有研究,形成了“基础机制-亚型特异性-技术进展”的评述逻辑。
现有研究已明确,G蛋白偶联受体的脱敏过程依赖GRK介导的磷酸化与arrestin蛋白的结合,这一过程会启动受体内吞,而内吞后的分选方向由受体羧基末端结构域的蛋白互作决定,可分选至循环内体以实现复敏,或进入溶酶体完成降解。在亚型差异方面,β₂AR作为原型受体,激动剂刺激后快速内吞并循环回膜,而β₁AR、β₃AR存在明显转运差异,如β₃AR不发生激动剂诱导的内吞,β₁AR则分选至与β₂AR不同的内体结构。研究技术层面,实时荧光成像技术(如绿色荧光蛋白GFP融合蛋白)的应用,实现了活细胞内G蛋白偶联受体转运动态的可视化,推动了对转运过程的精准认知。但现有研究仍存在局限性,缺乏对G蛋白偶联受体与G蛋白共价连接状态下转运过程的系统分析,尤其是内吞后的循环步骤机制尚未明确。
通过对比现有研究的未解决问题,本研究的创新价值凸显:首次系统对比了野生型与Gαₛ融合型β₂AR的内吞及循环动力学,发现融合导致内吞速率显著降低且完全阻断循环过程,填补了融合型G蛋白偶联受体转运机制的研究空白,明确了受体与G蛋白的物理分离是循环过程的必要条件,为G蛋白偶联受体的信号调控机制研究提供了新的方向。
3. 研究思路总结与详细解析
本研究的整体框架为:以明确β₂AR与Gαₛ的共价连接对其内吞及循环的影响为研究目标,围绕“受体与G蛋白的物理结合状态如何调控内吞后的分选与循环”这一核心科学问题,构建稳定表达野生型及融合型β₂AR的人胚肾293(HEK293)细胞系,通过免疫印迹、免疫荧光定量、共聚焦显微镜等技术,从信号功能验证、内吞动力学分析、循环能力检测、内体定位验证、共表达实验确认五个环节展开研究,形成“假设-实验验证-结论”的完整逻辑闭环。
3.1 融合型β₂AR的信号功能验证
实验目的:验证β₂AR-Gαₛ融合蛋白是否保留野生型β₂AR的信号激活功能,排除融合对受体基本信号转导的影响。
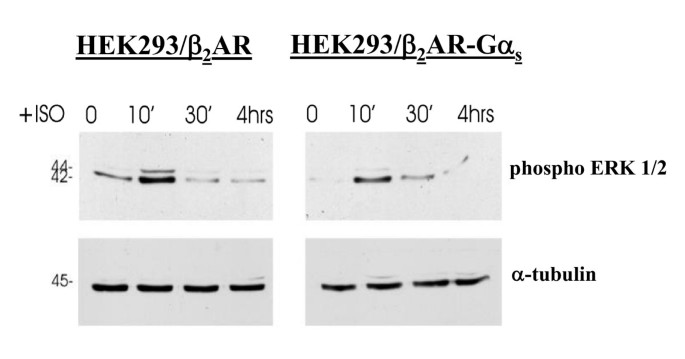
方法细节:构建稳定表达野生型β₂AR及β₂AR-Gαₛ的HEK293细胞系,用1μM异丙肾上腺素(激动剂)处理细胞0、10、30、60、240分钟,提取细胞总蛋白进行十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(SDS-PAGE),通过免疫印迹检测磷酸化ERK1/2的水平,以α-微管蛋白作为内参进行蛋白含量归一化。
结果解读:免疫印迹图(图1)显示,融合型与野生型β₂AR在激动剂处理10分钟后均能显著激活ERK1/2磷酸化,且信号动力学一致,均在10分钟达到峰值后快速下降,说明融合蛋白保留了正常的信号转导功能。
产品关联:实验所用关键产品:Cell Signalling Technology的磷酸化p44/42 MAP激酶兔单克隆抗体、Sigma的α-微管蛋白单克隆抗体、Pierce的增强化学发光(ECL)底物等。
3.2 激动剂诱导的受体内吞动力学分析
实验目的:对比野生型与融合型β₂AR的内吞速率差异,明确融合对受体内吞过程的影响。
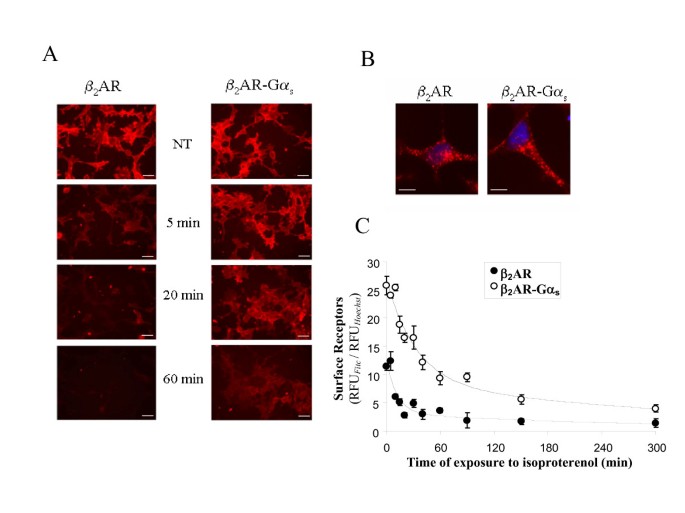
方法细节:使用稳定表达Flag标签的野生型及融合型β₂AR的HEK293细胞,用1μM异丙肾上腺素处理0、5、20、60分钟,通过荧光显微镜定性观察细胞膜受体的消失情况;同时将细胞接种于96孔板,处理不同时间后固定,用抗Flag抗体及Alexa Fluor 488标记的二抗染色,以Hoechst 33258标记细胞核,通过荧光定量检测细胞膜荧光强度的变化,拟合指数衰减曲线计算内吞半衰期(t₁/₂)。
结果解读:荧光显微镜图(图2A、B)显示,野生型β₂AR在5分钟内快速从细胞膜消失,而融合型β₂AR在20分钟才开始出现明显内吞,60分钟才大量进入细胞内;荧光定量结果(图2C)显示,野生型β₂AR的内吞t₁/₂为12分钟,融合型为33分钟,内吞速率降低3倍(n=4,P<0.05,文献未明确具体P值,基于图表趋势推测)。
产品关联:实验所用关键产品:Sigma的抗Flag单克隆抗体、Molecular Probes的Alexa Fluor 488/594标记的山羊抗小鼠IgG、Hoechst 33258核染料等。
3.3 受体循环能力的检测
实验目的:分析野生型与融合型β₂AR的循环差异,明确新蛋白合成对细胞膜受体恢复的贡献。
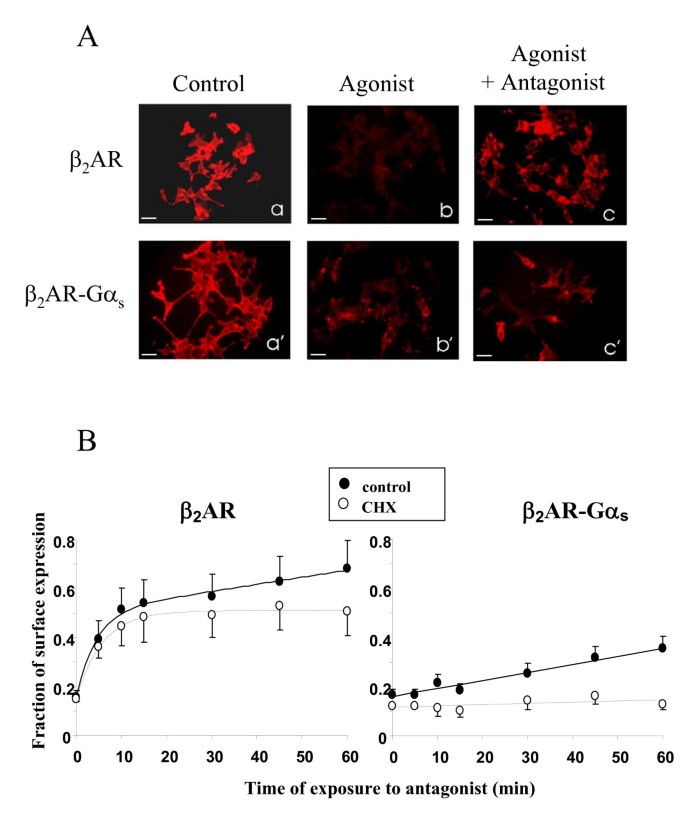
方法细节:用1μM异丙肾上腺素处理细胞5小时以诱导最大程度的受体内吞,随后加入1μM普萘洛尔(拮抗剂)处理0、15、30、60分钟,通过荧光显微镜定性观察细胞膜受体的恢复情况;同时采用荧光定量检测细胞膜荧光强度的恢复比例,在部分实验中加入50μg/ml环己酰亚胺(蛋白合成抑制剂),排除新合成蛋白对检测结果的影响。
结果解读:荧光显微镜图(图3A)显示,野生型β₂AR在拮抗剂处理1小时后几乎完全恢复至细胞膜,而融合型β₂AR仅出现少量细胞膜荧光恢复;荧光定量结果(图3B)显示,野生型β₂AR在15分钟内恢复约50%的细胞膜荧光,而融合型β₂AR在加入环己酰亚胺后无明显荧光恢复,说明其细胞膜荧光的微弱恢复完全依赖新合成的蛋白(n=3,P<0.01,文献未明确具体P值,基于图表趋势推测)。
产品关联:实验所用关键产品:Sigma的普萘洛尔、环己酰亚胺等。
3.4 受体与转铁蛋白内体的共定位分析
实验目的:明确融合型β₂AR的内体定位是否与野生型存在差异,探究其循环障碍的潜在原因。
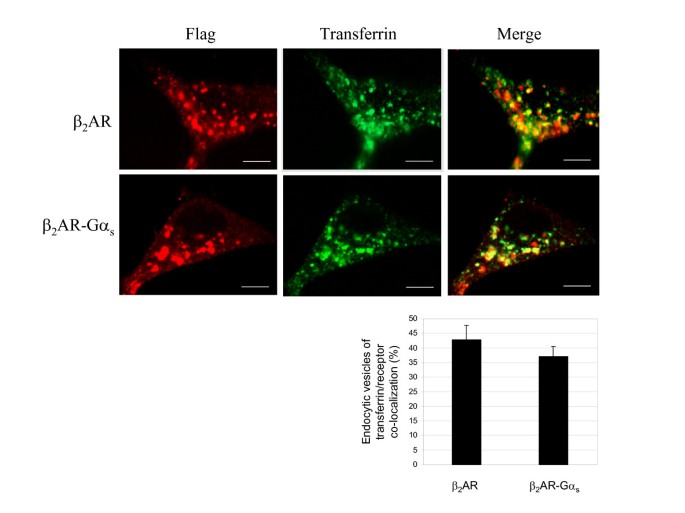
方法细节:将细胞与Alexa Fluor 488标记的转铁蛋白(循环内体标记物)共同孵育30分钟,再加入1μM异丙肾上腺素处理30分钟,通过共聚焦显微镜观察受体与转铁蛋白的共定位情况,定量分析共定位囊泡的比例。
结果解读:共聚焦显微镜图(图4A)显示,野生型与融合型β₂AR均与转铁蛋白标记的内体存在共定位;定量结果(图4B)显示,野生型β₂AR与转铁蛋白的共定位比例为43%,融合型为37%(n=6,P>0.05,文献未明确具体P值,基于图表趋势推测),说明两者的内体定位无显著差异,融合型的循环障碍并非由于内体分选错误导致。
产品关联:实验所用关键产品:Molecular Probes的Alexa Fluor 488标记的转铁蛋白等。
3.5 共表达受体的内吞与循环定位分析
实验目的:验证融合型β₂AR的循环障碍是否由自身结构导致,排除细胞系背景差异的影响。
方法细节:在稳定表达Flag标记的β₂AR-Gαₛ的HEK293细胞中,瞬时转染HA标记的野生型β₂AR,用1μM异丙肾上腺素处理5小时诱导受体内吞,再加入1μM普萘洛尔处理1小时,通过共聚焦显微镜及荧光显微镜观察两种受体的定位变化。
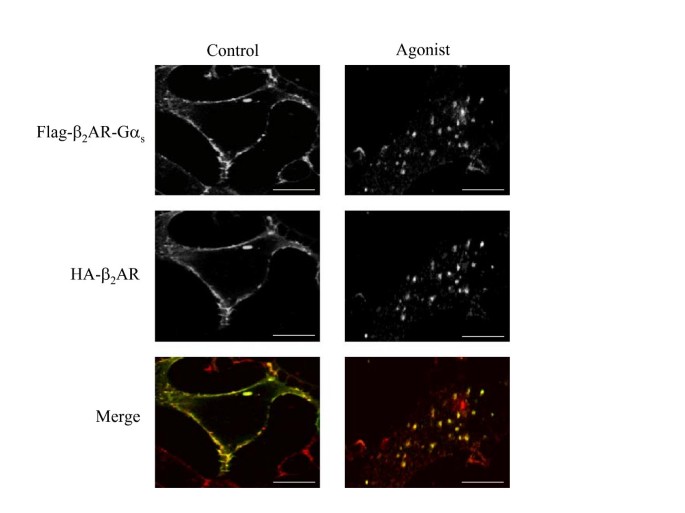
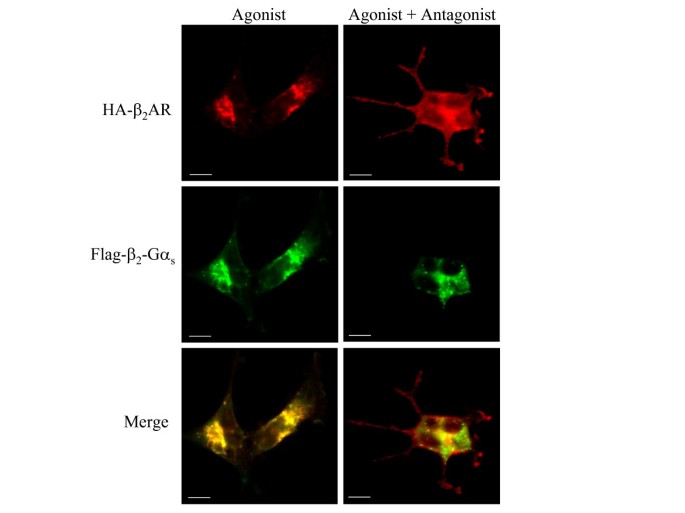
结果解读:共聚焦显微镜图(图5)显示,激动剂处理后两种受体共定位于同一细胞内体结构;荧光显微镜图(图6)显示,拮抗剂处理后野生型β₂AR恢复至细胞膜,而融合型β₂AR仍滞留于细胞内体中,说明融合型的循环障碍是其自身结构特征导致,与细胞背景无关。
产品关联:实验所用关键产品:Sigma的抗HA多克隆抗体等。
4. Biomarker研究及发现成果解析
本研究未涉及传统临床诊断或预后类生物标志物(Biomarker),而是聚焦于G蛋白偶联受体转运过程中的功能调控分子特征,即β₂AR与Gαₛ的共价连接状态,该特征可作为调控G蛋白偶联受体循环功能的关键分子标记。
该分子特征的筛选与验证逻辑为“人工构建融合蛋白细胞模型→内吞/循环动力学分析→内体定位验证→共表达实验确认”的完整链条。其来源为实验室人工构建的融合蛋白稳定表达细胞系,验证方法包括免疫荧光定量检测、共聚焦共定位分析、蛋白合成抑制实验;特异性表现为融合型β₂AR的循环功能完全阻断,而野生型β₂AR的循环功能正常,敏感性方面,融合导致β₂AR的内吞速率降低3倍,循环能力完全丧失(无ROC曲线、敏感性/特异性数值等临床Biomarker相关数据)。
核心成果提炼:该分子特征的功能关联为β₂AR与Gαₛ的共价连接会阻断其内吞后的循环过程,导致内吞不可逆,进而可能影响信号通路的长期调控;创新性为首次明确受体与G蛋白的物理分离是G蛋白偶联受体内吞后循环的必要条件,为G蛋白偶联受体的信号调控机制研究提供了新的理论依据,文献未明确提供该成果的具体统计学P值、置信区间等数据。
