1. 领域背景与文献引入
文献英文标题:Distinct expression patterns of HCN channels in HL-1 cardiomyocytes;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:心脏生理学(心肌细胞电生理与起搏机制)
心脏自主节律起源于窦房结的起搏细胞,其自发节律性动作电位触发心肌收缩,起搏电流I_f(又称I_h)是维持心脏自主节律的核心组分,由超极化激活环核苷酸门控(HCN)通道介导。领域共识:哺乳动物HCN通道包含HCN1-4四个亚型,具有不同的生物物理特性和组织表达模式,其中HCN4在小鼠窦房结起搏细胞中占主导地位,基因敲除研究证实HCN4对胚胎期心脏起搏功能至关重要,成年小鼠敲除HCN4会导致严重心动过缓或心律失常。当前领域研究热点聚焦于HCN通道在心脏节律调控中的分子机制,以及不同病理状态下HCN表达的变化,但核心问题在于,细胞层面HCN亚型的表达异质性与心肌细胞分化、收缩活性的关联尚未被系统解析。现有研究多依赖体内动物模型或胚胎干细胞衍生心肌细胞,而HL-1细胞作为唯一能在体外连续传代且保留成年心肌细胞收缩特性的细胞系,其HCN通道的表达模式尚未被全面揭示,本研究通过系统分析HL-1细胞中HCN亚型的转录和蛋白表达动态,填补了这一研究空白,为心肌细胞分化的分子调控机制提供新的实验依据。
2. 文献综述解析
作者以HCN通道的功能层级、体内外研究模型为分类维度,系统梳理了HCN通道在心脏节律调控中的研究进展,明确了现有研究的成果与局限性,进而凸显本研究的创新价值。
现有研究的关键结论包括:HCN通道是起搏电流I_f的分子基础,不同亚型的组合表达决定了起搏电流的生物物理特性;HCN4在小鼠窦房结的起搏功能中发挥核心作用,胚胎期敲除HCN4会导致心脏起搏功能丧失,成年敲除则引发严重心律失常。技术方法优势方面,体内基因敲除模型能够直接验证HCN通道的整体生理功能,胚胎干细胞衍生心肌细胞模型可模拟心肌细胞的分化过程;但现有研究存在明显局限性,体内研究难以解析细胞层面的表达异质性,胚胎干细胞衍生心肌细胞的HCN亚型表达模式存在不一致性,而HL-1细胞作为理想的成年心肌细胞体外模型,仅被报道存在HCN通道的功能活性,其转录和蛋白表达的动态变化及与细胞收缩活性的关联尚未被系统研究。本研究的创新价值在于,首次在HL-1细胞中整合转录组和蛋白组层面的分析,揭示HCN亚型随细胞密度变化的动态表达模式,以及其与细胞收缩活性的空间关联,填补了HL-1细胞作为心肌模型在HCN通道研究中的空白,为进一步解析心肌细胞分化的分子机制提供了新的切入点。
3. 研究思路总结与详细解析
本研究的核心目标是解析HL-1心肌细胞中HCN通道亚型的转录与蛋白表达模式,明确其与细胞分化状态(收缩活性)的关联;核心科学问题为HCN亚型表达是否随HL-1细胞密度动态变化,以及HCN表达细胞与收缩细胞的空间关系;技术路线遵循“细胞模型构建→转录表达定量→蛋白表达定位→功能关联分析”的闭环逻辑,通过qPCR和免疫细胞化学技术的结合,系统揭示HCN通道的表达特征。
3.1 HL-1细胞培养与样本分组
实验目的是建立不同密度和培养时间的HL-1细胞模型,为后续HCN表达分析提供标准化样本。方法细节为使用添加胎牛血清、去甲肾上腺素、L-谷氨酰胺等组分的Claycomb培养基培养HL-1细胞,接种于明胶和纤连蛋白包被的培养皿或玻璃底培养板,按视觉判定的细胞密度分为1-20%、21-40%、41-60%、61-80%、81-100%五个组别,同时设置1-4天的不同培养时间梯度样本。结果解读为成功获得不同密度和培养时间的HL-1细胞样本,其中细胞密度接近100%汇合时,部分细胞簇出现自发收缩活性,为后续分析HCN表达与收缩活性的关联提供了基础。实验所用关键产品:Claycomb培养基(SAFC Biosciences)、胎牛血清(SAFC Biosciences)、去甲肾上腺素(Sigma-Aldrich)、L-谷氨酰胺(Life Technologies)、抗坏血酸(Sigma-Aldrich)、链霉素/青霉素(Life Technologies)、明胶(Life Technologies)、纤连蛋白(Sigma-Aldrich)、Ibidi玻璃底培养皿。
3.2 HCN亚型转录表达的定量PCR分析
实验目的是检测HCN1-4四个亚型在HL-1细胞中的转录水平,分析其随细胞密度变化的动态模式。方法细节为使用Qiagen的AllPrep试剂盒提取细胞总RNA,经Oligo-dT引物和M-MLV反转录酶合成cDNA,采用SYBR Green实时荧光定量PCR技术,以gapdh为内参基因,使用经BLAST验证特异性的基因引物,在Roche LightCycler 1.5仪器上进行扩增,通过熔解曲线验证扩增产物的均一性,采用Ct法分析基因表达水平,并按细胞密度分组进行统计学分析。结果解读为在汇合的HL-1细胞中,HCN4的转录水平约为HCN1或HCN2的2倍(n=4,P<0.005),HCN3仅检测到微量转录本;随细胞密度增加,HCN1和HCN2的转录水平先升高,在60%左右密度时达到峰值,HCN1在100%汇合时回落至初始水平,而HCN2维持高表达,HCN4的转录水平则随细胞密度增加呈线性降低(方差分析显示HCN1组F_(4,27)=8.298,P<0.0002;HCN2组F_(4,28)=5.708,P<0.002;HCN4组F_(4,25)=31.22,P<0.0001)。
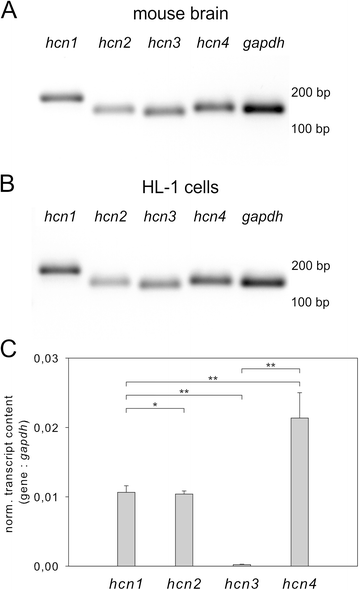

实验所用关键产品:DNA/RNA/Protein AllPrep® Kit(Qiagen)、Oligo-dT引物(Qiagen)、Moloney Murine Leukemia Virus反转录酶(Life Technologies)、LightCycler 1.5(Roche)、QuantiTect SYBR Green PCR Kit(Qiagen)、基因特异性引物(MWG Operon)。
3.3 HCN亚型蛋白表达的免疫细胞化学分析
实验目的是检测HCN1-4蛋白在HL-1细胞中的表达定位和细胞分布特征。方法细节为使用HCN1、HCN2、HCN4的亚型特异性一抗进行免疫细胞化学染色,细胞经4%多聚甲醛固定后,用含化学封闭剂和Triton-X的缓冲液封闭非特异性结合,依次孵育一抗和荧光标记的二抗,采用Leica TCS SP5II共聚焦显微镜观察,统计阳性细胞比例。结果解读为HCN1、HCN2、HCN4蛋白主要定位于细胞膜,在汇合的HL-1细胞培养中,HCN4阳性细胞约占10%,HCN1阳性细胞约占3%,HCN2阳性细胞约占1%,HCN3蛋白未被检测到;HCN1表达于单个细胞或小细胞簇,HCN2多表达于单个细胞,HCN4阳性细胞则倾向于形成大细胞簇;共染色结果显示,约0.5%的细胞共表达HCN1和HCN4,而HCN2与HCN4几乎完全在不同细胞或细胞簇中表达,这与体内小鼠心脏中HCN亚型的表达模式相似。
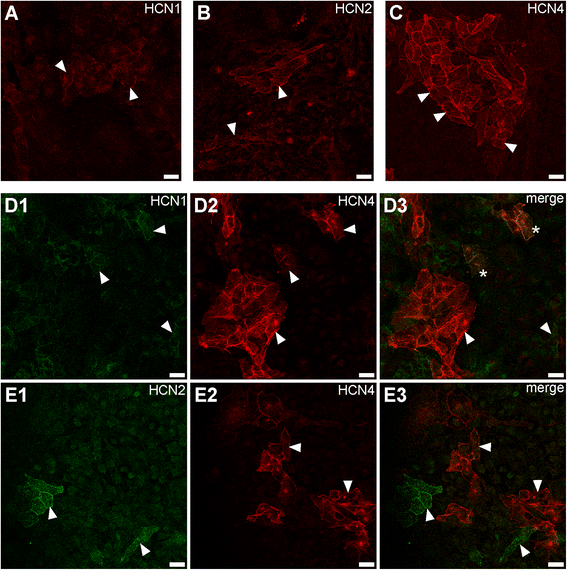
实验所用关键产品:抗mHCN1抗体(HCN1α,豚鼠)、抗mHCN2抗体(HCN2α,兔)、抗mHCN4抗体(PG2-1A4,大鼠)、抗兔-Cy2二抗(Dianova)、抗大鼠-Cy3二抗(Dianova)、抗豚鼠-A594二抗(Dianova)、4%多聚甲醛、Aqua-Poly/Mount封片剂(Polysciences)、Leica TCS SP5II共聚焦显微镜。
3.4 HCN表达与HL-1细胞收缩活性的关联分析
实验目的是明确HCN阳性细胞与具有收缩活性的细胞之间的空间关系。方法细节为首先使用Zeiss Axio Vert.A1显微镜和Nikon D200数码相机记录HL-1细胞的收缩活性,标记收缩细胞簇的位置,随后进行HCN亚型的免疫染色,通过ImageJ软件将收缩活性记录图像与免疫染色图像叠加,分析两者的空间关联。结果解读为具有收缩活性的细胞簇中未检测到HCN1、HCN2或HCN4蛋白的表达,但HCN4阳性细胞簇常位于收缩细胞簇的附近,推测:HCN阳性细胞可能通过旁分泌信号通路影响收缩细胞的活性,而非直接参与收缩细胞的起搏过程。
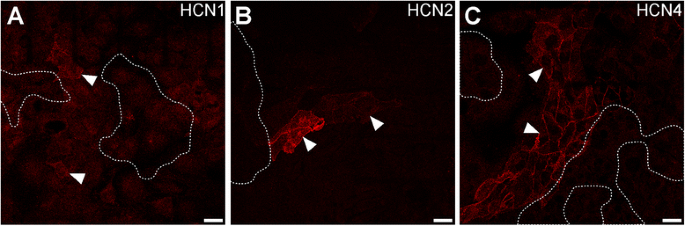
实验所用关键产品:Zeiss Axio Vert.A1显微镜、Nikon D200数码相机、ImageJ软件。
4. Biomarker研究及发现成果解析
本研究中HCN1、HCN2、HCN4通道亚型作为HL-1细胞分化状态的分子标志物,其表达模式与细胞密度、收缩活性密切相关,为心肌细胞分化的分子调控提供了新的标志物。
Biomarker定位:HCN1、HCN2、HCN4属于细胞表面离子通道类标志物,筛选与验证逻辑为:基于HCN通道在心脏起搏中的已知功能,首先通过qPCR筛选HL-1细胞中表达的HCN亚型,再通过免疫细胞化学验证蛋白表达的细胞特异性,最后结合细胞密度和收缩活性分析其与细胞分化状态的关联,形成完整的验证链条。
研究过程详述:Biomarker的来源为HL-1细胞系,验证方法包括实时荧光定量PCR(转录水平)和免疫细胞化学(蛋白水平);特异性方面,qPCR引物经BLAST验证仅靶向对应HCN亚型,抗体为亚型特异性抗体;敏感性方面,qPCR能够检测到微量的HCN3转录本,免疫细胞化学能够检测到低至1%的阳性细胞;定量数据显示,在汇合的HL-1细胞中,HCN4的转录水平是HCN1的2倍(n=4,P<0.005),HCN4阳性细胞比例为10%,HCN1为3%,HCN2为1%。
核心成果提炼:该Biomarker的功能关联在于,HCN亚型的表达模式与HL-1细胞的分化状态密切相关,HCN4在低密度未分化细胞中高表达,HCN1/2在中密度分化细胞中高表达,而收缩细胞不表达HCN亚型,提示HCN亚型可作为HL-1细胞分化阶段的分子标志物;创新性在于首次揭示HL-1细胞中HCN亚型的异质性表达模式及其与细胞收缩活性的空间关联,为心肌细胞分化的旁分泌调控机制提供了新的线索;统计学结果显示,HCN1、HCN2、HCN4的转录水平随细胞密度变化的差异均具有统计学显著性(HCN1:F_(4,27)=8.298,P<0.0002;HCN2:F_(4,28)=5.708,P<0.002;HCN4:F_(4,25)=31.22,P<0.0001)。
