1. 领域背景与文献引入
文献英文标题:Mucin 1 (MUC1) is a novel partner for MAL2 in breast carcinoma cells;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:乳腺癌分子生物学、蛋白质相互作用与肿瘤调控机制。
乳腺癌是全球女性发病率最高的恶性肿瘤,分子层面的机制研究是揭示肿瘤发生发展、开发靶向治疗的核心方向。MAL家族蛋白属于四次跨膜结构的膜蛋白,参与细胞内囊泡运输、极性建立等关键生物学过程,其中MAL2蛋白定位于染色体8q24区域,该区域在乳腺癌、卵巢癌等多种肿瘤中频繁发生扩增,导致MAL2蛋白过表达,但MAL2在肿瘤中发挥功能的具体机制长期不明确,核心原因是缺乏对其结合伴侣及下游调控靶标的研究。另一方面,粘蛋白1(MUC1)是经典的肿瘤相关生物标志物,在多种上皮来源肿瘤中过表达,通过降低细胞间粘附、调控信号通路等机制促进肿瘤侵袭转移,然而MUC1的亚细胞定位及表达水平的调控机制仍存在空白,尤其是膜蛋白对其的调控作用尚未被揭示。针对MAL2结合伴侣未知及MUC1调控机制不明确的研究空白,本研究通过酵母双杂交筛选结合细胞功能实验,首次发现MAL2与MUC1的相互作用,为解析二者在乳腺癌中的协同调控机制提供了关键依据。
2. 文献综述解析
作者在综述部分围绕MAL2的结构功能、肿瘤表达特征及MUC1的肿瘤调控作用展开,以“蛋白结构-表达特征-功能机制”为分类维度,系统梳理了领域内现有研究的进展与不足。
现有研究已明确MAL2属于MAL家族四次跨膜蛋白,定位于脂质筏结构,参与肝细胞等上皮细胞的基底侧向顶侧转运过程,且在乳腺癌、卵巢癌、胰腺癌等多种肿瘤中存在基因扩增与蛋白过表达,甚至被纳入乳腺癌不良预后基因签名,但MAL2在肿瘤中发挥功能的分子机制始终未被阐明,仅有的研究显示其与D52样蛋白家族存在相互作用,缺乏对其他结合伴侣的探索。对于MUC1的研究,现有结论已证实其在肿瘤中过表达通过多种机制促进肿瘤进展,包括抑制细胞间粘附、激活下游信号通路等,但MUC1的亚细胞定位调控机制仍不清晰,尤其是膜蛋白对其转运及表达的调控作用尚未见报道。作者通过对比现有研究的局限性,明确本研究的核心创新点在于首次发现MAL2与MUC1的相互作用,填补了MAL2结合伴侣研究的空白,同时揭示了MAL2对MUC1的调控作用,为解析二者在乳腺癌中的协同功能提供了新的方向。
3. 研究思路总结与详细解析
本研究的核心目标是筛选并验证MAL2在乳腺癌中的新型结合伴侣,明确其相互作用的结构基础及功能意义,整体技术路线遵循“酵母双杂交筛选→细胞内相互作用验证→结合结构域定位→亚细胞分布分析→功能调控验证”的闭环逻辑,围绕MAL2与MUC1的相互作用及调控关系展开系统研究。
3.1 酵母双杂交筛选MAL2结合伴侣
实验目的是从乳腺癌组织中筛选MAL2的特异性结合蛋白,明确其潜在的功能调控靶标。方法上,以全长MAL2蛋白为诱饵构建酵母双杂交诱饵载体,转染酵母细胞后筛选乳腺癌cDNA表达文库,对阳性克隆进行DNA测序鉴定,并通过缺失突变体构建验证结合结构域的特异性。结果显示,筛选获得7个阳性MUC1克隆,均为N端截短形式,包含SEA模块、跨膜域及胞质尾结构;进一步的缺失突变实验表明,MAL2的N端结构域是结合D52样蛋白的必需区域,而第一个跨膜域是结合MUC1的关键结构域,二者结合MAL2的区域相互独立。
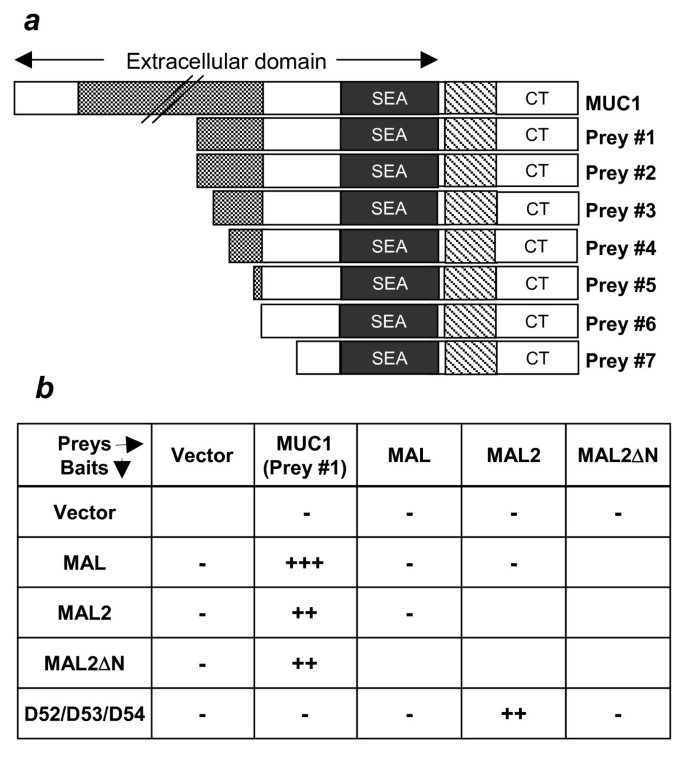
实验所用关键产品:酵母双杂交载体pAS2-1、pACT2(Clontech),乳腺癌cDNA文库(Stratagene)。
3.2 MAL2多克隆抗体制备与特异性验证
实验目的是制备能特异性识别MAL2蛋白的多克隆抗体,为后续细胞内实验提供检测工具。方法上,选取MAL2蛋白的N端(N¹³-V²⁴)和C端(C¹⁶⁵-P¹⁷⁶)多肽作为抗原,分别免疫羊和兔,通过亲和纯化获得特异性抗血清,随后利用蛋白质免疫印迹(Western blot)技术在多种乳腺癌细胞系中验证抗体的特异性。结果显示,制备的多克隆抗体可在MDA-MB-435、MDA-MB-453、MCF-10A等细胞系中检测到19kDa的MAL2蛋白,同时还能检测到更高分子量的糖基化修饰形式,与之前的研究报道一致。
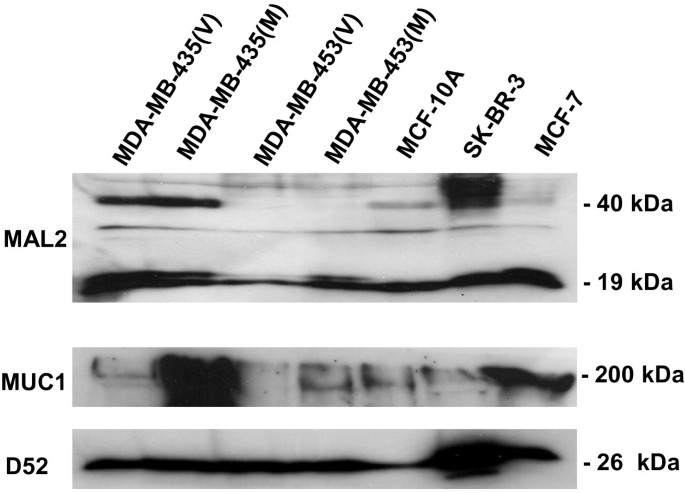
实验所用关键产品:多肽抗原,亲和纯化试剂,兔多克隆c-Myc抗体(Santa Cruz Biotechnology),兔多克隆CAV1抗体(BD Biosciences),化学发光检测试剂(Perkin Elmer)。
3.3 免疫共沉淀验证MAL2与MUC1细胞内相互作用
实验目的是在哺乳动物细胞内验证MAL2与MUC1的特异性相互作用,同时探索二者与D52蛋白的复合物形成情况。方法上,构建稳定转染Myc标签MAL2的MCF-10A细胞系,提取总蛋白后分别用MUC1单克隆抗体、c-Myc多克隆抗体、MAL2多克隆抗体进行免疫沉淀,随后通过Western blot检测共沉淀的蛋白组分,同时设置MAL2多肽封闭对照验证相互作用的特异性。结果显示,MUC1抗体可免疫沉淀MAL2蛋白,MAL2抗体也可免疫沉淀MUC1蛋白,同时D52蛋白也被共沉淀,提示三者可能形成多分子复合物;加入MAL2特异性多肽后,MAL2的免疫沉淀及MUC1、D52的共沉淀均被完全阻断,证实了相互作用的特异性,且该相互作用在MCF-7及MUC1转染的MDA-MB-435细胞中也得到了验证。
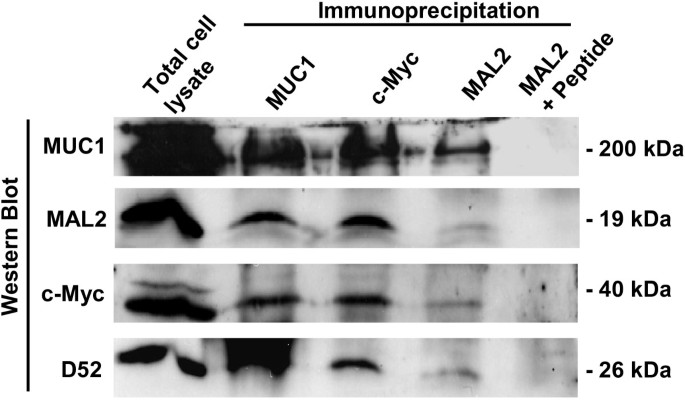
实验所用关键产品:Protein A-Sepharose、Protein G-agarose(Sigma-Aldrich),辣根过氧化物酶标记二抗(Jackson ImmunoResearch)。
3.4 缺失突变体定位MAL2与MUC1结合结构域
实验目的是明确MAL2蛋白中与MUC1结合的具体结构域,进一步解析二者相互作用的分子基础。方法上,构建一系列MAL2的N端及跨膜域缺失突变体,通过酵母双杂交系统检测各突变体与MUC1的结合能力,结合之前的D52样蛋白结合实验结果,对比分析不同结构域的结合特异性。结果显示,缺失MAL2的第一个跨膜域后,其与MUC1的结合能力完全丧失,而缺失N端结构域仅影响与D52样蛋白的结合,不影响与MUC1的相互作用,证实MAL2的第一个跨膜域是与MUC1结合的必需区域,且MUC1与D52样蛋白结合MAL2的结构域相互独立。
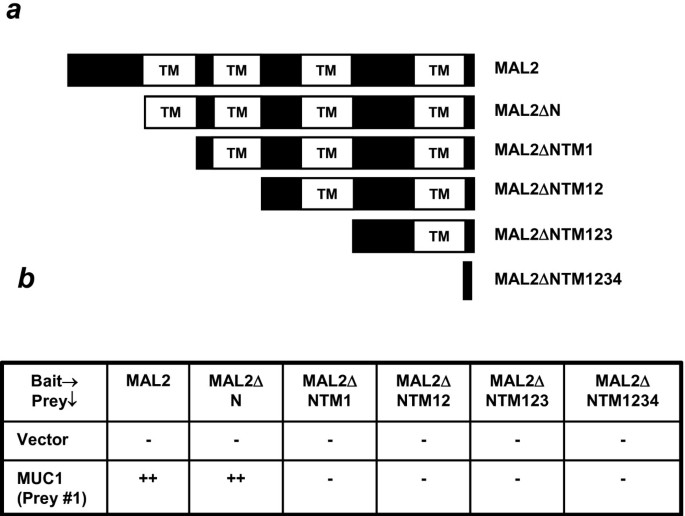
实验所用关键产品:PCR特异性引物,酵母双杂交载体。
3.5 共聚焦显微镜观察MAL2与MUC1亚细胞共定位
实验目的是在细胞内直观观察MAL2与MUC1的亚细胞定位及共分布情况,为二者的功能相互作用提供形态学依据。方法上,选取SK-BR-3、MDA-MB-435、MCF-7等乳腺癌细胞系,通过免疫荧光染色分别标记MAL2和MUC1蛋白,利用激光共聚焦显微镜观察二者的亚细胞分布及共定位情况,同时观察MUC1过表达对MAL2分布的影响。结果显示,MAL2与MUC1在多种乳腺癌细胞系的细胞质中呈现部分共定位,MUC1在SK-BR-3及过表达MUC1的MDA-MB-435细胞中呈点状分布,在MCF-7及MDA-MB-453细胞中则集中于细胞外周,但无论MUC1的主要定位如何,均与MAL2在细胞质中存在共分布,且MUC1过表达不改变MAL2的亚细胞分布。
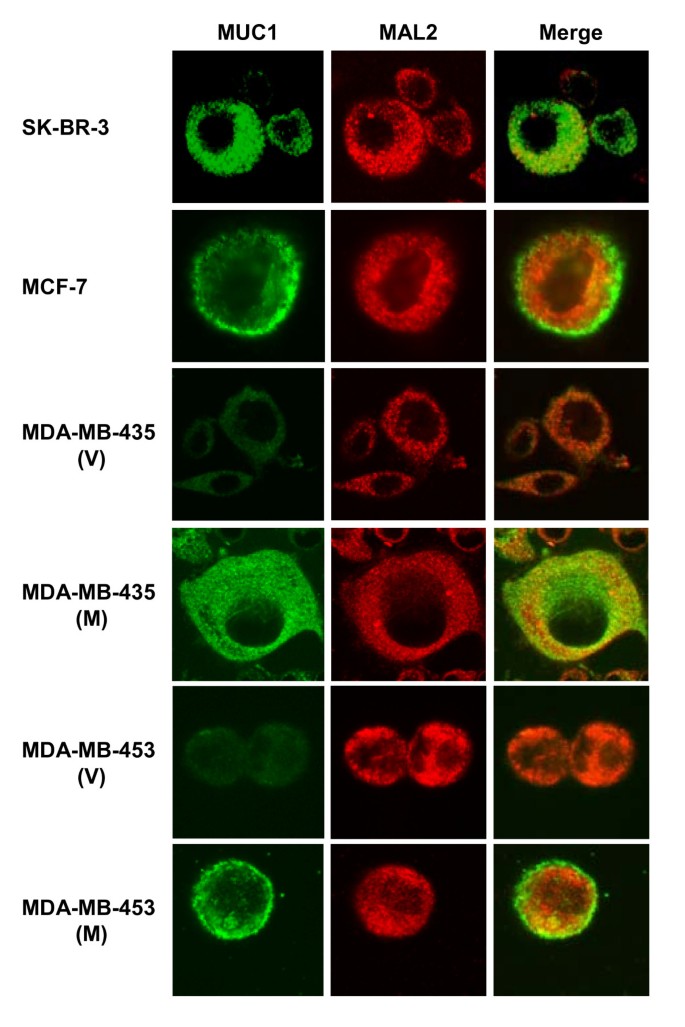
实验所用关键产品:激光共聚焦显微镜(Leica TCS SP2),FITC标记二抗、CY3标记二抗(Jackson ImmunoResearch)。
3.6 蔗糖密度梯度离心分析蛋白在脂质筏中的分布与相互作用
实验目的是分析MAL2与MUC1在脂质筏及非脂质筏组分中的分布特征,明确二者相互作用的亚细胞区域。方法上,采用Triton X-100低温裂解细胞,通过蔗糖密度梯度离心分离脂质筏(不可溶组分)与非脂质筏(可溶性组分),利用Western blot检测MAL2、MUC1及D52在各组分中的分布;同时采用甲基-β-环糊精(MβCD)处理细胞消耗胆固醇,观察蛋白分布的变化;最后对不同组分进行免疫共沉淀验证相互作用的区域特异性。结果显示,MAL2与MUC1在脂质筏及非脂质筏组分中均有分布,MβCD处理后二者从脂质筏组分转移至可溶性组分;但免疫共沉淀实验仅在可溶性组分中检测到MAL2与MUC1的相互作用,提示二者的相互作用主要发生在非脂质筏区域。
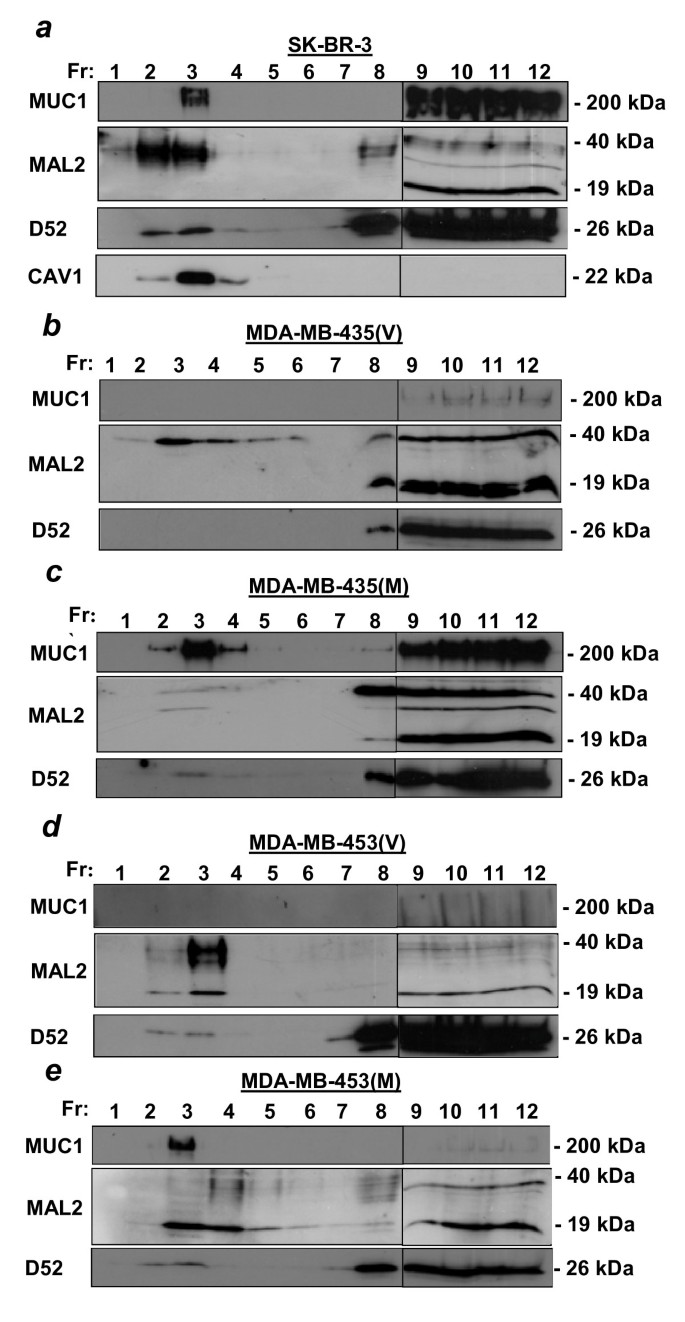
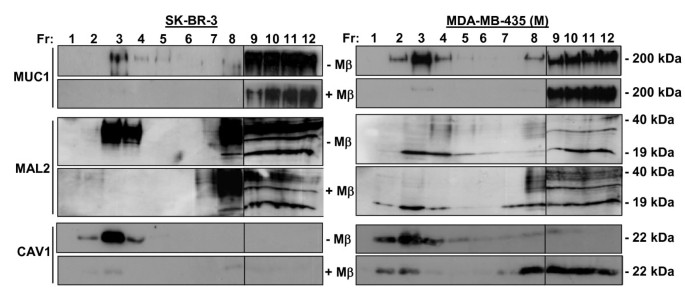
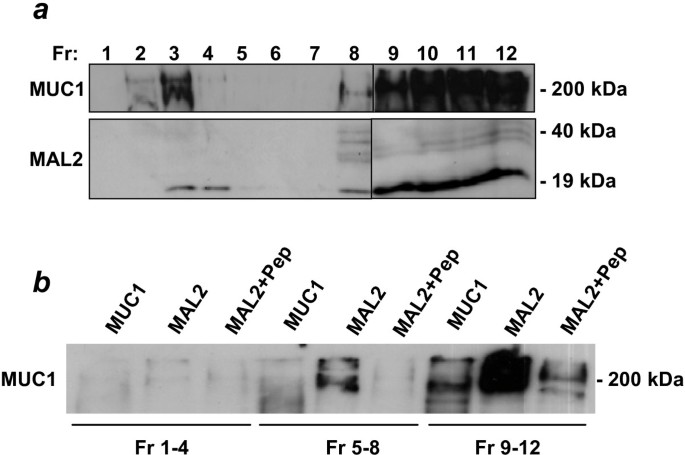
实验所用关键产品:甲基-β-环糊精(MβCD,Sigma-Aldrich),Beckman SW41离心机转子。
3.7 MAL2过表达对MUC1定位与表达的调控作用
实验目的是明确MAL2过表达对MUC1亚细胞定位及表达水平的影响,解析二者相互作用的功能意义。方法上,构建稳定转染Myc-MAL2的MCF-10A细胞系,通过光学显微镜观察细胞形态变化,利用蔗糖密度梯度离心结合Western blot检测MUC1在各组分中的表达水平,同时通过共聚焦显微镜观察MUC1的亚细胞定位变化。结果显示,MAL2过表达导致MCF-10A细胞形态发生明显伸长改变,MUC1在细胞表面的表达显著增加,且在脂质筏及非脂质筏组分中的表达水平均有所提升,共聚焦显微镜观察显示MUC1在MAL2过表达细胞的外周区域积累,提示MAL2可能通过调控MUC1的转运或表达影响其亚细胞定位。
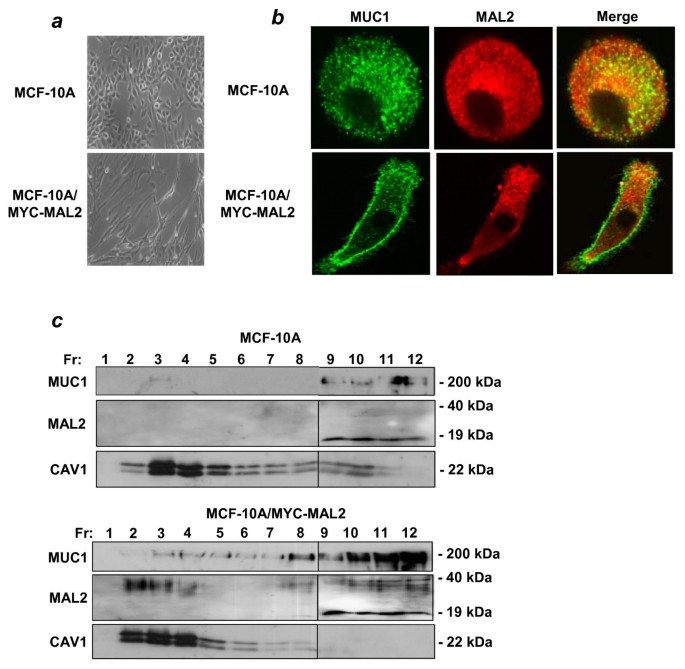
实验所用关键产品:LipofectAMINE 2000转染试剂(Life Technologies),G418筛选试剂。
4. Biomarker研究及发现成果
本研究涉及的生物标志物包括MAL2与MUC1蛋白及其相互作用复合物,二者均为乳腺癌中过表达的分子,研究通过“文库筛选→细胞验证→结构定位→功能分析”的完整逻辑链条,明确了二者的相互作用及调控关系,为乳腺癌的分子机制研究及靶向治疗提供了新的靶点。
Biomarker定位方面,MAL2是定位于染色体8q24区域的四次跨膜蛋白,在多种肿瘤中存在基因扩增与蛋白过表达;MUC1是经典的肿瘤相关粘蛋白,在上皮来源肿瘤中过表达促进肿瘤进展。本研究通过酵母双杂交筛选从乳腺癌cDNA文库中发现MUC1为MAL2的新型结合伴侣,随后通过免疫共沉淀、共聚焦显微镜观察在多种细胞系中验证了二者的相互作用,通过缺失突变体定位了结合的关键结构域,通过蔗糖密度梯度离心明确了相互作用发生在非脂质筏区域,最后通过过表达实验证实MAL2对MUC1的亚细胞定位及表达水平具有调控作用。研究过程中,在稳定转染细胞系及多种乳腺癌细胞系中均验证了二者的相互作用,实验重复3-4次结果具有一致性,但文献未提供具体的统计学P值及样本量数据。核心成果方面,本研究首次发现MAL2与MUC1的特异性相互作用,明确MAL2的第一个跨膜域是结合必需区域,且MAL2过表达可促进MUC1的细胞表面表达,推测二者的相互作用可能通过调控MUC1的定位参与乳腺癌的侵袭转移过程,为乳腺癌的不良预后机制提供了新的解释,同时为开发针对二者相互作用的靶向治疗策略提供了潜在靶点。
