1. 领域背景与文献引入
文献英文标题:Concentration-dependent effects of native and polymerised α1-antitrypsin on primary human monocytes, in vitro;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:炎症生物学、分子免疫学
α1-抗胰蛋白酶(α1-antitrypsin,AAT)是人体血浆中主要的丝氨酸蛋白酶抑制剂,传统研究认为其核心功能是抑制中性粒细胞弹性蛋白酶等蛋白酶的活性,维持蛋白酶-抗蛋白酶平衡,防止组织发生蛋白水解损伤,例如遗传性α1-抗胰蛋白酶缺乏会导致蛋白酶-抗蛋白酶失衡,是肺气肿、肝硬化等疾病的重要致病因素。领域共识:随着研究深入,α1-抗胰蛋白酶的非抗蛋白酶功能逐渐被发现,包括刺激成纤维细胞增殖与胶原合成、调控B细胞向IgE及IgG4分泌细胞分化、抑制中性粒细胞超氧阴离子产生等,这些功能拓展了α1-抗胰蛋白酶在炎症调控中的作用范畴。当前研究的核心未解决问题是:不同构象(天然活性型与聚合非活性型)的α1-抗胰蛋白酶在不同浓度下对单核细胞这一关键炎症调控细胞的作用差异及分子机制尚不明确,现有研究多聚焦单一构象或单一浓度的α1-抗胰蛋白酶作用,未系统对比不同构象在多浓度梯度下的调控差异,且对其调控免疫细胞炎症反应的分子机制解析不够深入。
针对这一空白,本研究旨在通过体外实验系统对比天然及聚合型α1-抗胰蛋白酶在多个浓度梯度下对原代人单核细胞促炎反应的影响,明确其浓度依赖性的调控规律及转录层面的机制,补充α1-抗胰蛋白酶在炎症反应中的双重功能理论,为α1-抗胰蛋白酶相关疾病的治疗提供新的理论依据。
2. 文献综述解析
本文综述部分以α1-抗胰蛋白酶的构象类型、功能属性及浓度依赖性为核心分类维度,系统梳理了领域内关于α1-抗胰蛋白酶的研究进展,明确了现有研究的成果与局限性,为自身研究的创新点奠定了基础。
现有研究已证实,天然α1-抗胰蛋白酶是循环中最丰富的蛋白酶抑制剂,其遗传性缺乏会导致蛋白酶-抗蛋白酶失衡,是肺气肿、肝硬化等疾病的重要致病因素;聚合型α1-抗胰蛋白酶因丧失蛋白酶抑制活性,与α1-抗胰蛋白酶缺乏相关疾病的病理进程密切相关,可在患者肝脏、肺部形成包涵体引发组织损伤。同时,越来越多的研究发现α1-抗胰蛋白酶具有非抗蛋白酶功能,包括刺激成纤维细胞增殖与胶原合成、调控B细胞向IgE及IgG4分泌细胞分化、抑制中性粒细胞超氧阴离子产生等,这些功能拓展了α1-抗胰蛋白酶在炎症调控中的作用范畴。现有研究的技术方法多采用细胞系、动物模型及临床样本分析,能够在体内外层面验证α1-抗胰蛋白酶的功能,但局限性在于多数研究仅关注单一构象或单一浓度的α1-抗胰蛋白酶作用,未系统对比不同构象在多浓度梯度下的调控差异,且对其调控免疫细胞炎症反应的分子机制解析不够深入。
通过对比现有研究的空白,本研究的创新点在于首次系统开展了天然与聚合型α1-抗胰蛋白酶在0.01 mg/ml至1 mg/ml多浓度梯度下的原代人单核细胞作用研究,不仅明确了两种构象α1-抗胰蛋白酶的浓度依赖性双向调控作用,还深入到转录因子NF-κB层面解析了其分子机制,证实这种调控作用不依赖于α1-抗胰蛋白酶的蛋白酶抑制活性,补充了α1-抗胰蛋白酶作为炎症信号分子的新功能理论。
3. 研究思路总结与详细解析
本研究的整体框架为“假设提出→体外细胞实验验证→分子机制解析→结论总结”的闭环逻辑,研究目标是明确天然及聚合型α1-抗胰蛋白酶对原代人单核细胞促炎反应的浓度依赖性调控作用,核心科学问题是α1-抗胰蛋白酶的浓度及构象如何影响单核细胞的炎症信号通路,技术路线为制备两种构象的α1-抗胰蛋白酶→多浓度处理原代人单核细胞→检测促炎细胞因子释放及NF-κB活性→分析浓度依赖性规律及机制。
3.1 实验材料制备与原代单核细胞模型构建
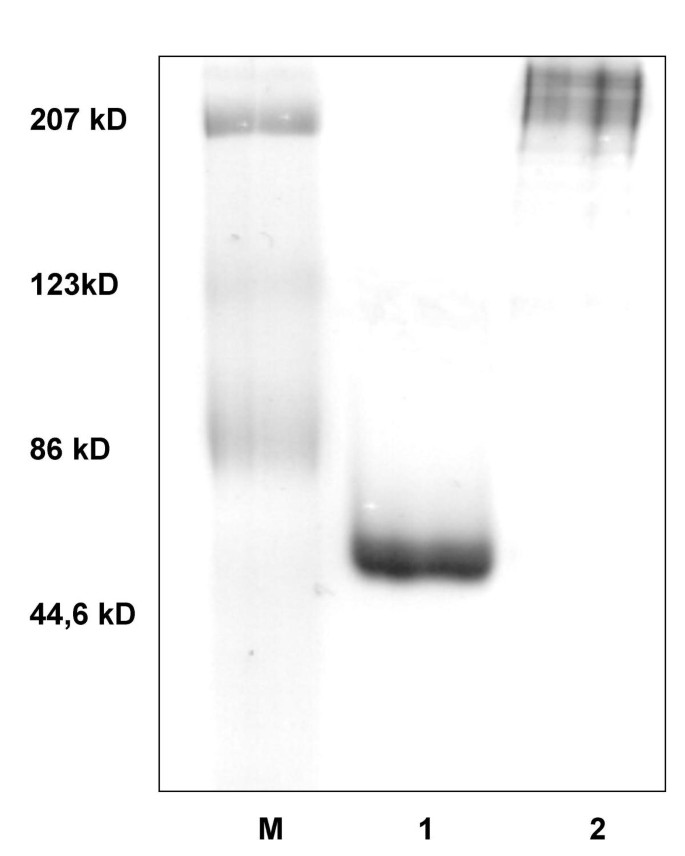
实验目的是获得高纯度、构象明确的天然及聚合型α1-抗胰蛋白酶,同时建立合格的原代人单核细胞实验模型,为后续实验提供可靠基础。方法细节:从人血浆中提取纯度>95%、抑制活性>75%的天然α1-抗胰蛋白酶,通过60℃孵育3小时的方法制备聚合型α1-抗胰蛋白酶,采用7.5%非变性聚丙烯酰胺凝胶电泳验证聚合效果;从不同供体的Buffy coat中分离原代人单核细胞,通过贴壁培养法纯化细胞,经台盼蓝染色验证细胞活力,最终获得纯度>97%的单核细胞,接种于无血清培养基中培养。结果解读:图1显示,天然α1-抗胰蛋白酶在非变性凝胶电泳中呈现单一分子量条带,而聚合型α1-抗胰蛋白酶则呈现多条不同大小的聚合物条带,证实α1-抗胰蛋白酶聚合制备成功;单核细胞的纯度与活力均符合实验要求,可用于后续处理实验。实验所用关键产品:Calbiochem的人血浆α1-抗胰蛋白酶、Pierce的内毒素去除凝胶、R&D Systems的DuoSet ELISA试剂盒、Activemotif的TransAm NF-κB检测试剂盒。
3.2 不同浓度α1-抗胰蛋白酶处理后的促炎细胞因子检测
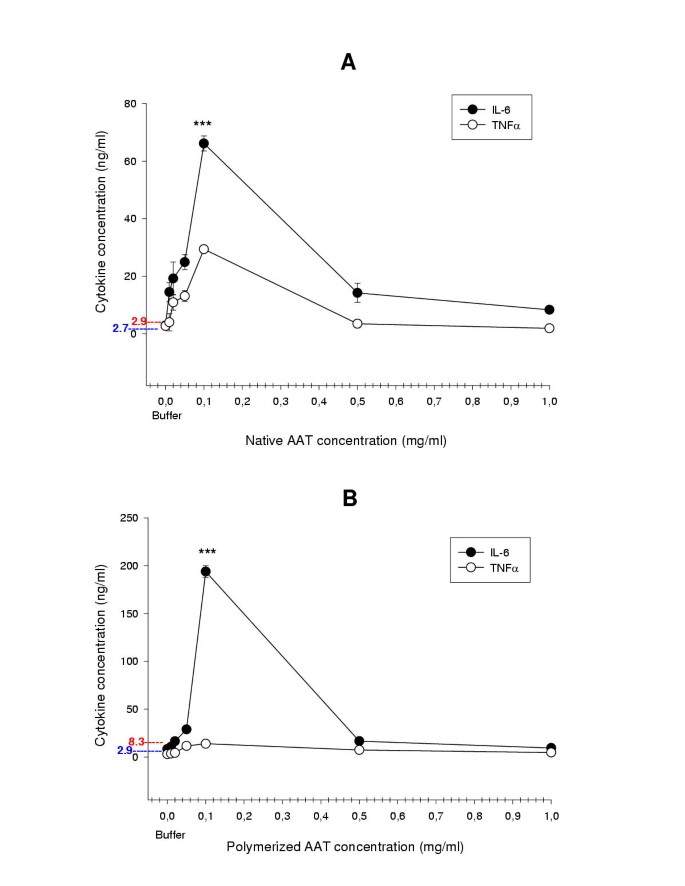
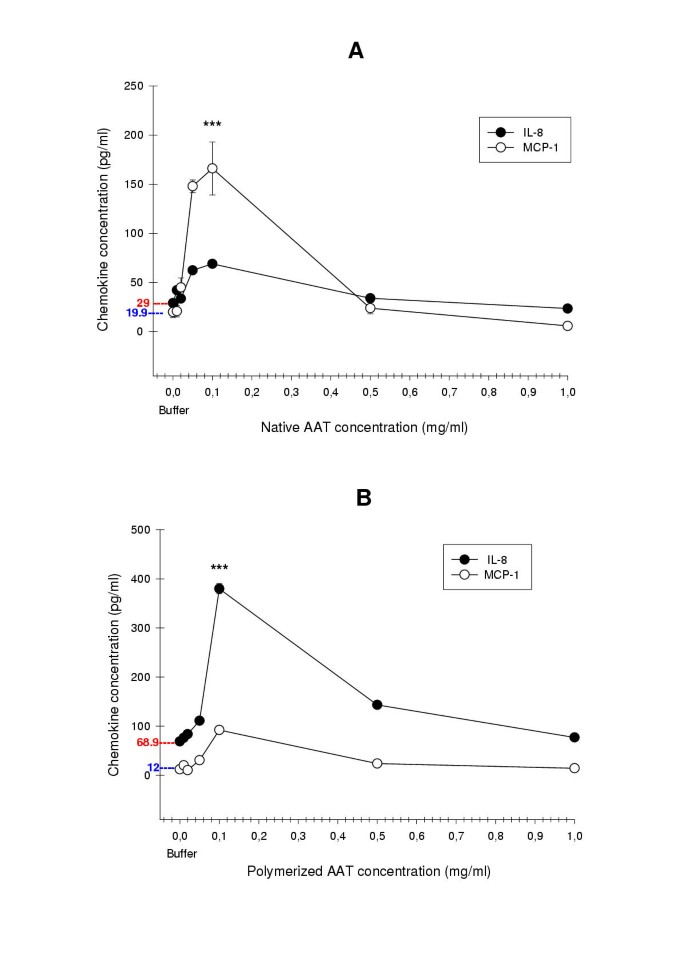
实验目的是明确天然及聚合型α1-抗胰蛋白酶在不同浓度下对原代人单核细胞促炎细胞因子及趋化因子释放的影响,验证其浓度依赖性调控作用。方法细节:将原代人单核细胞分别暴露于0.01、0.02、0.05、0.1、0.5、1 mg/ml浓度的天然或聚合型α1-抗胰蛋白酶中处理18小时,收集细胞培养上清,采用夹心ELISA法检测肿瘤坏死因子-α(TNF-α)、白细胞介素-6(IL-6)、白细胞介素-8(IL-8)、单核细胞趋化蛋白-1(MCP-1)的水平,每个浓度梯度设置至少三次重复实验。结果解读:图2和图3显示,低浓度(0.05-0.1 mg/ml)的天然及聚合型α1-抗胰蛋白酶均能显著上调单核细胞中促炎细胞因子及趋化因子的释放,其中天然α1-抗胰蛋白酶处理组的TNF-α释放量上调10.9倍、MCP-1上调8.3倍(n=6,P<0.001),聚合型α1-抗胰蛋白酶处理组的IL-6释放量上调23.4倍、IL-8上调5.5倍(n=6,P<0.001);而高浓度(0.5、1 mg/ml)的两种构象α1-抗胰蛋白酶则无明显刺激作用,其细胞因子释放水平与对照组无显著差异甚至更低。
3.3 NF-κB转录因子活性检测
实验目的是解析天然及聚合型α1-抗胰蛋白酶调控单核细胞促炎反应的分子机制,明确转录层面的调控靶点。方法细节:提取不同浓度α1-抗胰蛋白酶处理后的单核细胞核蛋白,采用TransAm试剂盒检测NF-κB p50亚基的活性,通过吸光度值反映其激活水平,设置特异性对照验证实验结果的可靠性。结果解读:图4显示,低浓度(0.05-0.1 mg/ml)的天然及聚合型α1-抗胰蛋白酶均能显著激活NF-κB p50的活性,而高浓度(1 mg/ml)的两种构象α1-抗胰蛋白酶则抑制NF-κB p50的活性,这一趋势与细胞因子释放的结果完全一致,证实NF-κB是α1-抗胰蛋白酶调控单核细胞促炎反应的关键转录因子,其活性变化介导了不同浓度α1-抗胰蛋白酶的双向调控作用。

4. Biomarker研究及发现成果
本文中涉及的Biomarker为α1-抗胰蛋白酶的浓度及构象,其作为炎症调控的功能性Biomarker,具有浓度依赖性的双向调控作用,为炎症反应的精准调控提供了新的靶点。
该Biomarker的筛选逻辑基于α1-抗胰蛋白酶在炎症中的已知作用,验证逻辑为“多浓度梯度处理→细胞因子释放检测→转录因子活性验证”的完整链条,明确了其浓度而非构象是调控单核细胞炎症反应的核心因素,两种构象的α1-抗胰蛋白酶具有相似的调控趋势。
该Biomarker的来源为从人血浆中提取的天然α1-抗胰蛋白酶及体外聚合制备的聚合型α1-抗胰蛋白酶;验证方法包括ELISA定量检测促炎细胞因子释放、TransAm试剂盒检测NF-κB活性;特异性与敏感性数据显示,低浓度(0.05-0.1 mg/ml)α1-抗胰蛋白酶对促炎细胞因子的上调倍数为2.4-23.4倍(n=6,P<0.001),NF-κB活性在低浓度时显著升高,高浓度时则被抑制至接近检测下限。
本研究首次明确α1-抗胰蛋白酶的浓度是调控单核细胞促炎反应的关键因素,而非其蛋白酶抑制活性;低浓度α1-抗胰蛋白酶通过激活NF-κB通路促进促炎细胞因子释放,高浓度则抑制该通路活性;天然与聚合型α1-抗胰蛋白酶的调控趋势一致,但对不同细胞因子的作用强度存在差异,其中天然α1-抗胰蛋白酶对TNF-α和MCP-1的刺激作用更显著,聚合型α1-抗胰蛋白酶对IL-6和IL-8的作用更强。该成果的创新性在于揭示了α1-抗胰蛋白酶作为炎症信号分子的浓度依赖性双向调控机制,为α1-抗胰蛋白酶缺乏相关疾病的治疗提供了新的思路,即通过调节α1-抗胰蛋白酶的浓度来调控炎症反应进程。
