1. 领域背景与文献引入
文献英文标题:Hypoxia-mimetic agents inhibit proliferation and alter the morphology of human umbilical cord-derived mesenchymal stem cells;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:间充质干细胞与低氧微环境调控
间充质干细胞(hMSCs)是一类具有多向分化潜能的成体干细胞,1974年由Friedenstein等首次从骨髓中分离鉴定,随后的研究证实其广泛存在于胎盘、脐带、羊膜等多种组织中。其中,人脐带来源的hMSCs因获取便捷、伦理争议少、免疫原性低等优势,成为组织工程、细胞替代治疗等领域的研究热点。低氧是体内组织微环境的重要特征,生理状态下骨髓、脐带等组织的氧浓度仅为1%-7%,远低于体外常规培养的20%氧浓度。已有研究表明,低氧可通过激活低氧诱导因子-1α(HIF-1α)通路,调控hMSCs的增殖、分化、迁移等生物学行为,但多数研究聚焦于物理低氧环境对骨髓hMSCs的影响,关于低氧模拟剂(如去铁胺DFO、氯化钴CoCl₂)对脐带hMSCs的形态及增殖的系统研究仍存在空白。因此,本文旨在分析DFO和CoCl₂对脐带hMSCs形态和增殖的影响及机制,为其在低氧缺血疾病中的治疗应用提供实验依据。
2. 文献综述解析
作者的综述分类维度为低氧对hMSCs不同生物学功能的影响,以及低氧诱导方式的差异。现有研究显示,物理低氧可促进骨髓hMSCs的克隆形成能力、增殖活性及趋化性,延长其分化潜能;低氧模拟剂通过抑制HIF-1α的降解模拟低氧效应,操作简便且效果与物理低氧相当,可用于低氧信号通路的机制研究。但现有研究存在局限性:部分研究发现物理低氧与化学模拟剂对hMSCs的增殖调控存在差异,且针对脐带hMSCs的研究较少,缺乏对其形态及超微结构的系统分析。本文的创新价值在于,首次采用原子力显微镜(AFM)和透射电子显微镜(TEM)观察低氧模拟剂处理后脐带hMSCs的超微结构变化,明确其通过阻滞细胞周期抑制增殖的机制,填补了脐带hMSCs在化学低氧条件下生物学特性研究的空白,为其临床应用提供了更全面的实验数据。
3. 研究思路总结与详细解析
本文以脐带hMSCs为研究对象,首先分离培养并鉴定细胞的干细胞特性,随后通过低氧模拟剂DFO和CoCl₂处理,从增殖、细胞周期、形态及超微结构三个层面系统分析其生物学效应,最终揭示低氧模拟剂通过影响细胞周期抑制脐带hMSCs增殖并改变其形态的机制,为低氧缺血疾病的干细胞治疗提供实验依据。
3.1 脐带hMSCs的分离培养与鉴定
实验目的:获取高纯度的人脐带来源hMSCs,并验证其干细胞特性,为后续实验提供可靠的细胞模型。
方法细节:选取健康足月剖宫产婴儿的脐带组织,用磷酸盐缓冲液冲洗后剪碎,采用0.2%Ⅱ型胶原酶37℃消化5-6小时,过滤离心后接种于含10%胎牛血清的DMEM/F12培养基中,置于37℃、5%CO₂培养箱培养,每3天更换培养基,待细胞融合至80%-90%时传代,取3-7代细胞用于实验。采用流式细胞术检测细胞表面标志物(CD29、CD44、CD105、CD106、CD40、CD34、CD45等),并通过成脂、成骨诱导验证细胞的多向分化潜能。
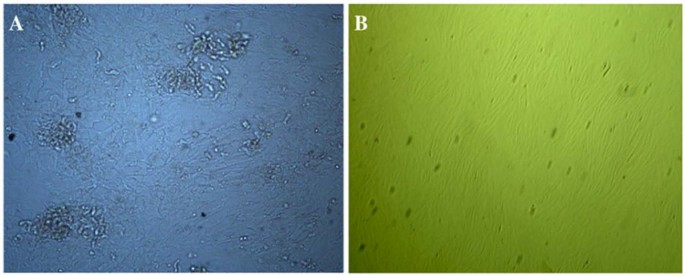
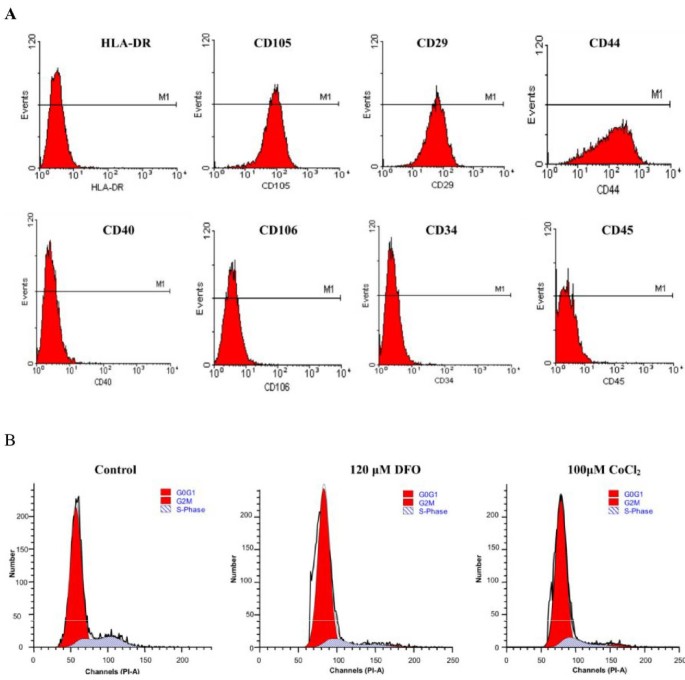
结果解读:流式细胞术结果显示,分离的细胞高表达间充质干细胞特异性标志物CD44(96.1%)、CD29(98.5%)、CD105(98.6%),低表达造血细胞标志物CD106(2.1%)、CD40(0.8%)、CD34(0.5%)、CD45(0.8%)及HLA-DR(0.7%),符合国际细胞治疗协会制定的hMSCs鉴定标准。成脂诱导后,细胞形态由长梭形变为卵圆形,油红O染色可见胞质内出现红色脂滴;成骨诱导后,细胞形成多层细胞簇,von Kossa染色可见钙结节形成,证实细胞具有向脂肪细胞和成骨细胞分化的多能性。
实验所用关键产品:Gibco的Ⅱ型胶原酶、DMEM/F12培养基、胎牛血清;BD Biosciences的流式抗体;PHILIP5 TECNAI 10透射电子显微镜。
3.2 低氧模拟剂对hMSCs增殖的影响
实验目的:明确低氧模拟剂DFO和CoCl₂对脐带hMSCs增殖的调控作用,并分析其浓度依赖性。
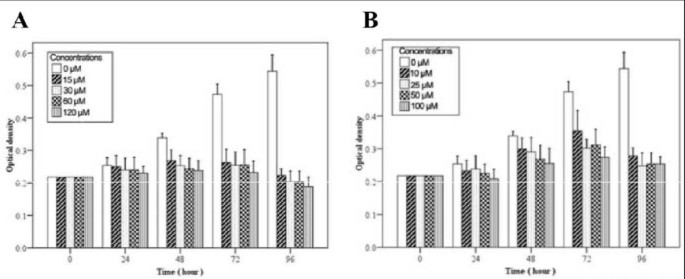
方法细节:将处于对数生长期的hMSCs接种于96孔板,分别加入不同浓度的DFO(15、30、60、120μM)和CoCl₂(10、25、50、100μM),设置不含低氧模拟剂的对照组,分别在处理24、48、72小时后采用MTT法检测细胞增殖活性,每组设置3个复孔。
结果解读:MTT检测结果显示,DFO和CoCl₂处理48小时后均显著抑制hMSCs增殖(P<0.05),且抑制作用呈浓度依赖性。其中,120μM DFO处理组的细胞增殖抑制率为29.8%(n=3,P<0.05),100μM CoCl₂处理组的抑制率为24.6%(n=3,P<0.05);随着处理时间延长,抑制作用进一步增强,但各浓度组间的差异无统计学意义。
3.3 低氧模拟剂对hMSCs细胞周期的影响
实验目的:探究低氧模拟剂抑制hMSCs增殖的细胞周期机制。
方法细节:用120μM DFO和100μM CoCl₂处理hMSCs 48小时,对照组加入等量培养基,收集细胞后用70%冷乙醇固定,RNase A消化后PI染色,采用流式细胞术检测细胞周期分布。
结果解读:流式细胞术结果显示,与对照组相比,DFO和CoCl₂处理组G0/G1期细胞比例显著升高,G2/S/M期细胞比例显著降低,提示低氧模拟剂将细胞周期阻滞在G0/G1期,从而抑制细胞增殖;不同浓度的DFO或CoCl₂处理组间细胞周期分布无显著差异,但呈剂量依赖性趋势。
3.4 低氧模拟剂对hMSCs形态及超微结构的影响
实验目的:观察低氧模拟剂处理后hMSCs的形态及超微结构变化,进一步揭示其生物学效应。
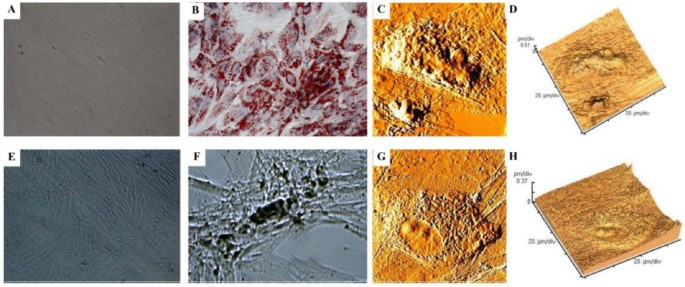
方法细节:用120μM DFO和100μM CoCl₂处理hMSCs 72小时,对照组加入等量培养基,采用原子力显微镜(AFM)观察细胞表面形态,透射电子显微镜(TEM)观察细胞超微结构。
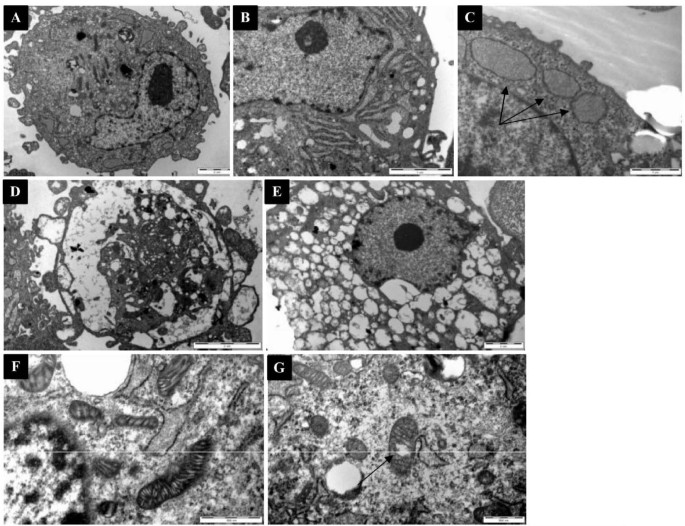
结果解读:AFM结果显示,对照组细胞呈长梭形,细胞间紧密接触形成网状结构;处理后细胞伸长至近100μm,细胞间接触减少,出现明显间隙,细胞表面的突触样结构减少。TEM结果显示,DFO处理后细胞胞质内出现大量空泡样结构,粗面内质网扩张,线粒体嵴扩张,核膜皱缩或部分解体,染色质浓缩,提示细胞出现早期凋亡迹象;CoCl₂处理组的形态变化与DFO组类似,但程度稍轻。


4. Biomarker研究及发现成果解析
Biomarker定位:本文未聚焦于特定Biomarker的筛选与验证,而是围绕低氧模拟剂对脐带hMSCs的生物学效应展开系统研究,涉及的核心调控通路为低氧诱导因子-1α(HIF-1α)介导的低氧信号通路,该通路的激活是低氧模拟剂发挥作用的关键机制,相关激活效应已被前期研究证实,但本文未直接检测HIF-1α的表达水平。
研究过程详述:本文通过低氧模拟剂DFO和CoCl₂处理脐带hMSCs,采用MTT法、流式细胞术、AFM及TEM等技术,从细胞增殖、细胞周期、形态及超微结构多个层面分析其生物学变化,未开展特定Biomarker的定量检测与临床样本验证。
核心成果提炼:本文明确了低氧模拟剂通过阻滞细胞周期在G0/G1期抑制脐带hMSCs增殖,并改变其形态及超微结构,为脐带hMSCs在低氧缺血疾病中的治疗应用提供了实验基础。其创新性在于首次采用AFM和TEM观察低氧模拟剂处理后脐带hMSCs的超微结构变化,揭示了低氧模拟剂对脐带hMSCs的潜在损伤效应,为优化脐带hMSCs的体外培养条件及治疗方案提供了参考。
