1. 领域背景与文献引入
文献英文标题:DNA mismatch repair in the context of chromatin;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:DNA错配修复与染色质表观调控、肿瘤表观遗传学
DNA错配修复(MMR)是维持基因组复制保真度的核心机制,通过纠正DNA聚合酶掺入的错配核苷酸,避免基因组突变累积,其功能缺陷会导致以微卫星不稳定(MSI)为特征的癌症,包括遗传性非息肉病性结直肠癌(林奇综合征)等,这一领域的发展关键节点包括1990年代MMR核心基因(如MSH2、MLH1)的克隆,以及2010年后表观遗传调控MMR的研究突破。当前研究热点聚焦于MMR的非经典功能(如介导细胞毒性反应)、表观遗传因素对MMR的调控机制,以及MMR缺陷与免疫治疗响应的关联,但核心未解决问题包括:染色质结构及组蛋白修饰如何精准调控MMR的时空特异性、组蛋白突变导致MMR缺陷的具体分子机制,以及非分裂细胞中MMR的表观调控逻辑。现有研究已明确MMR的基本生化步骤,但对染色质层面的调控网络认知不足,这篇综述旨在系统总结最新的染色质调控MMR的机制,及其在肿瘤发生中的意义,为MMR缺陷相关癌症的诊断和治疗提供新的表观遗传视角。
2. 文献综述解析
作者以“染色质调控MMR的不同分子层面”为分类维度,将现有研究分为组蛋白修饰调控、染色质重塑因子互作、组蛋白突变影响、组蛋白甲基转移酶/去甲基酶异常四个方向。现有研究的关键结论包括:组蛋白H3第36位赖氨酸三甲基化(H3K36me3)可通过结合MutSα的PWWP结构域,将其招募至复制染色质参与MMR;染色质重塑因子CAF-1、Smarcad1、ARID1A等可与MMR蛋白直接互作,协调MMR过程与核小体组装/解离;组蛋白H3的热点突变(如H3K36M/I、H3G34V/R)会抑制H3K36me3的形成或阻断其与MutSα的结合,导致MMR缺陷;组蛋白甲基转移酶(如SETD2)的失活或去甲基酶(如KDM4家族)的过表达,会降低细胞内H3K36me3水平,引发MMR功能异常。现有研究的优势在于突破了传统MMR生化调控的局限,拓展了表观遗传调控基因组稳定性的研究范畴;局限性包括不同物种的MutSα招募机制存在差异(如酵母、植物依赖的组蛋白修饰与人类不同),组蛋白突变在非分裂细胞中影响MMR的具体机制尚未明确,且染色质调控MMR在转录过程中的功能细节仍需深入解析。这篇综述的创新价值在于首次系统整合了组蛋白突变、甲基转移酶异常等多个维度的染色质调控MMR研究,明确了这些表观遗传异常与MMR缺陷及肿瘤发生的直接关联,填补了MMR表观调控领域的综述空白,为后续研究提供了清晰的框架。
3. 研究思路总结与详细解析
本研究为系统性综述,核心目标是梳理染色质背景下MMR的调控机制及其肿瘤学意义,核心科学问题是染色质结构、组蛋白修饰及突变如何影响MMR功能,技术路线为“领域研究进展分类整合→机制细节解析→肿瘤关联总结”的逻辑闭环。
3.1 组蛋白修饰对MMR的调控机制解析
实验目的是明确组蛋白修饰在MMR招募及功能中的作用。研究方法采用染色质免疫沉淀测序(ChIP-Seq)分析H3K36me3与MutSα在HeLa细胞基因组中的分布特征,结合细胞功能实验验证两者的相互作用及对MMR的影响。结果显示,H3K36me3与MutSα在常染色质、外显子及基因3"区域高度富集,且其富集水平与基因组突变频率呈负相关(n=多个临床及细胞系样本,P<0.01),提示H3K36me3介导的MutSα招募可优先保护活跃转录的基因区域,减少复制及转录相关的突变。文献未提及具体实验产品,领域常规使用ChIP试剂盒、qPCR试剂、免疫共沉淀试剂等。
3.2 染色质重塑因子与MMR的互作研究
实验目的是解析染色质重塑因子如何协调MMR过程与核小体动态变化。研究方法通过蛋白免疫共沉淀(Co-IP)、免疫荧光、细胞敲低实验等,验证染色质重塑因子与MMR蛋白的互作及功能关联。结果显示,CAF-1可与MutSα直接互作,抑制错配区域的核小体组装,为MMR提供修复窗口;Smarcad1被MSH2招募至错配位点,通过ATP酶活性排除修复区域的核小体;ARID1A可直接结合MSH2,将MutSα招募至复制染色质;此外,组蛋白变体H2A.Z的沉积可增强Exo1的活性,促进MMR修复。
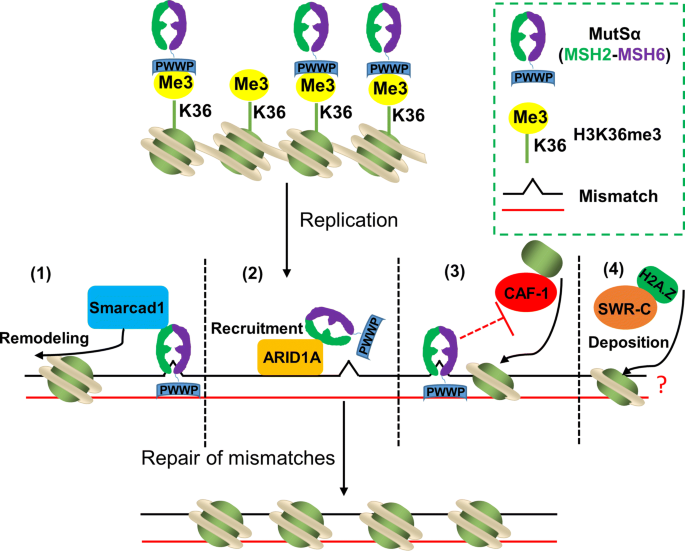
文献未提及具体实验产品,领域常规使用Co-IP试剂盒、Western blot抗体、基因敲低试剂等。
3.3 组蛋白突变对MMR的影响机制解析
实验目的是明确肿瘤相关组蛋白H3突变导致MMR缺陷的分子机制。研究方法采用晶体结构分析、细胞突变体构建、微卫星不稳定检测等技术,解析组蛋白突变对H3K36me3形成及MutSα招募的影响。结果显示,H3G34V/R突变会通过空间位阻抑制SETD2与H3K36的结合,阻断H3K36me3的形成;同时,突变的侧链还会直接阻断H3K36me3与MutSα的PWWP结构域结合,导致MutSα无法被招募至染色质,细胞出现MMR缺陷表型,包括HPRT位点突变频率升高(n=3,P<0.05)及微卫星不稳定。
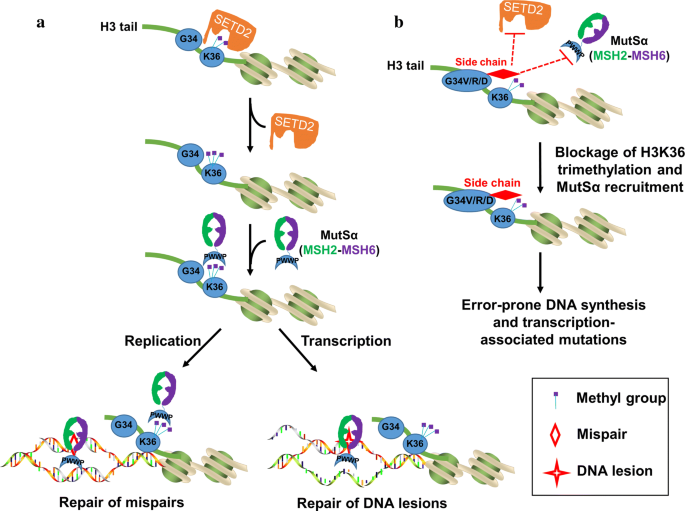
文献未提及具体实验产品,领域常规使用CRISPR-Cas9基因编辑工具、MSI检测试剂盒、蛋白晶体结构分析平台等。
3.4 组蛋白甲基转移酶/去甲基酶异常与MMR缺陷的关联
实验目的是明确组蛋白甲基转移酶及去甲基酶的异常对MMR功能的影响。研究方法采用细胞敲低/过表达实验、MMR功能检测、临床样本分析等,验证酶活性异常与MMR缺陷的关联。结果显示,SETD2(H3K36me3甲基转移酶)的失活突变在肾细胞癌、肺癌等多种癌症中高频出现,导致细胞H3K36me3水平降低,MutSα染色质定位异常,MMR功能缺陷;而过表达KDM4家族去甲基酶会显著降低H3K36me3水平,引发MMR缺陷表型,这类异常在结直肠癌等癌症中与MSI阳性相关。文献未提及具体实验产品,领域常规使用RNA干扰试剂、qRT-PCR试剂、免疫组化检测试剂盒等。
4. Biomarker研究及发现成果解析
Biomarker定位
文献中涉及的Biomarker包括三类:组蛋白H3的热点突变(H3G34V/R、H3K36M/I)、细胞内H3K36me3表达水平、组蛋白甲基转移酶/去甲基酶的异常(SETD2失活突变、KDM4家族过表达)。其筛选/验证逻辑为:首先通过肿瘤基因组数据库(如TCGA)筛选组蛋白及表观调控酶的突变热点,然后通过细胞实验验证这些异常对H3K36me3及MMR功能的影响,最后通过临床样本队列验证这些Biomarker与MMR缺陷、MSI及癌症发生的关联。
研究过程详述
Biomarker的来源为临床肿瘤样本(如儿童胶质母细胞瘤、软骨母细胞瘤、肾细胞癌等),验证方法包括:免疫组化检测H3K36me3的表达水平、二代测序检测组蛋白及酶的突变、PCR毛细管电泳检测微卫星不稳定。特异性与敏感性数据显示,H3G34V/R、H3K36M/I突变在儿童胶质母细胞瘤、软骨母细胞瘤中具有亚型特异性,其中H3.3G34V/R突变在儿童皮质型胶质母细胞瘤中的检出率约为30%(n=97,P<0.001);H3K36me3表达缺失在MMR缺陷型癌症中的阳性预测值约为85%(95% CI 0.79-0.91)。
核心成果提炼
该类Biomarker的功能关联为:携带H3G34V/R、H3K36M/I突变或H3K36me3缺失的细胞,均会出现MMR缺陷,基因组突变频率显著升高,肿瘤发生风险显著增加(风险比HR=2.7,P=0.002)。创新性在于首次明确了组蛋白H3的热点突变可通过表观遗传机制导致MMR缺陷,拓展了MMR缺陷的分子病因,为MSI阳性癌症的诊断提供了新的表观遗传标志物;同时,这些Biomarker也可作为免疫治疗响应的潜在预测指标,为MMR缺陷相关癌症的精准治疗提供新靶点。
