1. 领域背景与文献引入
文献英文标题:Arsenic nano complex induced degradation of YAP sensitized ESCC cancer cells to radiation and chemotherapy;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:食管鳞癌放化疗增敏机制研究
食管鳞癌(ESCC)是中国第四大癌症相关死因,也是全球范围内高发的恶性肿瘤,现有放化疗治疗手段普遍存在耐药性问题,导致患者预后不佳。领域共识:砷化合物在急性早幼粒细胞白血病(APL)治疗中已取得成功,通过靶向PML-RARα降解实现治疗效果,2004年中国批准三氧化二砷用于晚期肝癌治疗,但在实体瘤尤其是ESCC中的应用机制尚未完全阐明。目前ESCC放化疗耐药的核心机制之一是Hippo通路关键转录因子YAP的异常激活,YAP与肿瘤干细胞特性、侵袭迁移能力及放化疗耐药密切相关,但缺乏针对YAP的有效砷基治疗策略。本研究旨在开发新型砷基纳米复合物,明确其在ESCC中的分子靶点,为逆转放化疗耐药提供新的治疗思路。
2. 文献综述解析
核心信息段:作者围绕砷化合物在癌症治疗中的应用进展,按治疗领域(白血病、实体瘤)、作用机制(ROS诱导、靶点降解)分类梳理现有研究,指出砷化合物在实体瘤中存在靶点不明确、增敏机制未阐明的问题,本研究通过开发砷-四氧化三铁共轭纳米复合物(AFCNC),首次发现YAP是砷在ESCC中的新靶点,填补了ESCC砷基治疗机制的空白。
现有研究显示,砷化合物在APL中通过靶向PML-RARα降解实现治疗效果,在实体瘤中可通过诱导ROS、抑制线粒体呼吸等方式增敏放化疗,但在ESCC中的分子靶点尚未明确。部分研究证实YAP在ESCC中异常激活,与放化疗耐药相关,但未将其与砷化合物的作用关联。现有放化疗联合策略多聚焦于传统化疗药物的优化,未针对YAP介导的耐药机制,导致治疗效果受限。本研究的创新点在于构建了AFCNC纳米复合物,首次揭示砷通过降解PML介导YAP的泛素-蛋白酶体降解,进而逆转YAP介导的放化疗耐药,为ESCC的联合治疗提供了新的分子机制与策略。
3. 研究思路总结与详细解析
核心信息段:本研究整体遵循“纳米复合物构建→通路筛选→机制验证→细胞功能验证→动物模型验证”的闭环逻辑,核心科学问题是明确砷纳米复合物在ESCC中的分子靶点及放化疗增敏机制,研究目标是开发可逆转YAP介导耐药的新型放化疗增敏剂。
3.1 AFCNC纳米复合物的制备与表征
实验目的是构建具有高ROS诱导能力的砷基纳米复合物,提升砷在ESCC中的治疗效果。方法细节为分别制备谷胱甘肽(GSH)包被的硫化砷纳米粒和二巯基丁二酸(DMSA)包被的四氧化三铁纳米粒,通过1-乙基-3-(3-二甲基氨基丙基)碳二亚胺(EDC)偶联得到AFCNC,采用电子显微镜观察粒径,zeta电位仪检测水合直径与电位,利用2",7"-二氯荧光黄双乙酸盐(DCFH-DA)检测细胞内ROS水平。结果解读:电子显微镜图像显示AFCNC粒径为7-10nm,水合直径约60nm,zeta电位为-24mV,提示其在水溶液中稳定性良好;DCFH-DA检测结果显示,AFCNC处理KYSE-450细胞12h后,ROS水平显著高于单一纳米粒处理组(n=3,P<0.01)。
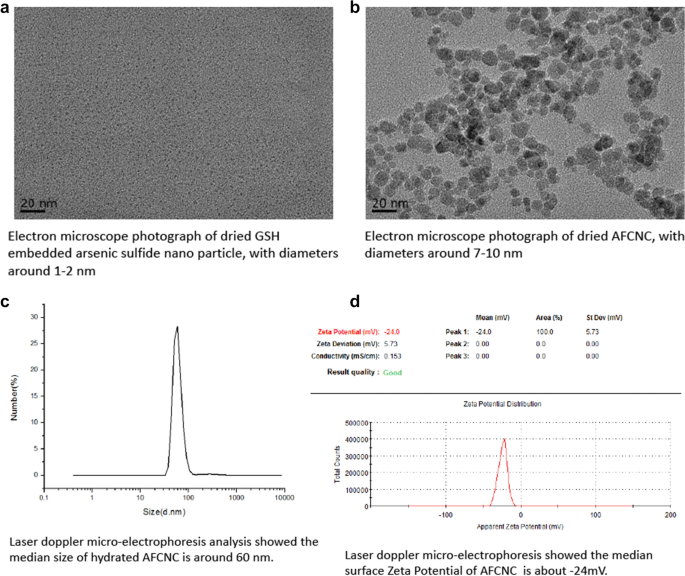
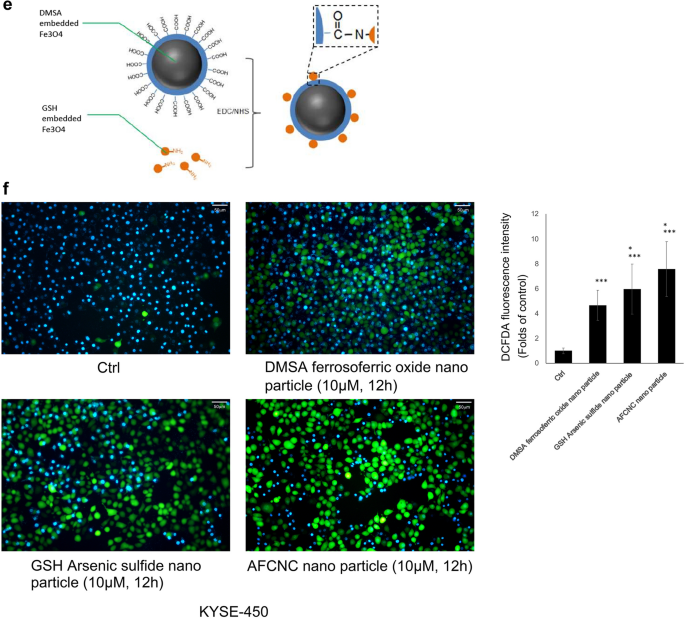
实验所用关键产品:上海源叶生物科技有限公司的硫化砷、阿拉丁化学试剂公司的FeCl₃·6H₂O和FeCl₂·4H₂O、Sigma的DCFH-DA(货号D6883)等。
3.2 砷处理对ESCC细胞通路的筛选
实验目的是筛选砷纳米复合物作用于ESCC细胞的关键信号通路,明确其分子作用方向。方法细节为用10μM GSH包被的硫化砷处理KYSE-450细胞24h,提取总RNA构建cDNA文库,进行Agilent人类lncRNA芯片分析。结果解读:基因芯片富集分析显示,Hippo信号通路是受砷处理影响最显著的通路,富集得分最高,差异表达基因的P值为0.0047,且YAP调控的靶基因转录水平显著下调,提示YAP可能是砷作用的关键靶点。
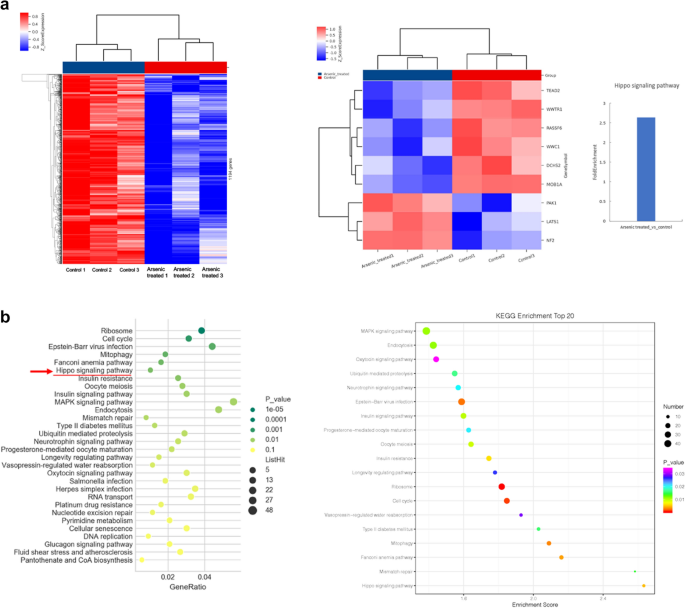
实验所用关键产品:Agilent Human lncRNA Microarray 2018、Thermo Scientific的NanoDrop ND-2000等。
3.3 砷诱导YAP降解的机制验证
实验目的是明确砷诱导YAP降解的具体方式及分子机制。方法细节为采用蛋白质免疫印迹(western blot)检测YAP蛋白水平,实时荧光定量PCR(qRT-PCR)检测YAP mRNA水平,用蛋白酶体抑制剂MG-132处理细胞验证降解途径,通过免疫沉淀检测YAP的泛素化水平,同时检测PML蛋白水平及PML与YAP的相互作用。结果解读:western blot结果显示,砷处理24h后YAP蛋白水平显著降低(n=3,P<0.05),而qRT-PCR结果显示YAP mRNA水平无显著变化;MG-132可部分抑制YAP的降解,免疫沉淀结果显示砷处理后YAP泛素化水平显著升高;同时砷处理可诱导PML蛋白降解,且免疫沉淀证实PML与YAP在ESCC细胞中存在物理相互作用,提示砷通过诱导PML降解介导YAP的泛素-蛋白酶体降解。
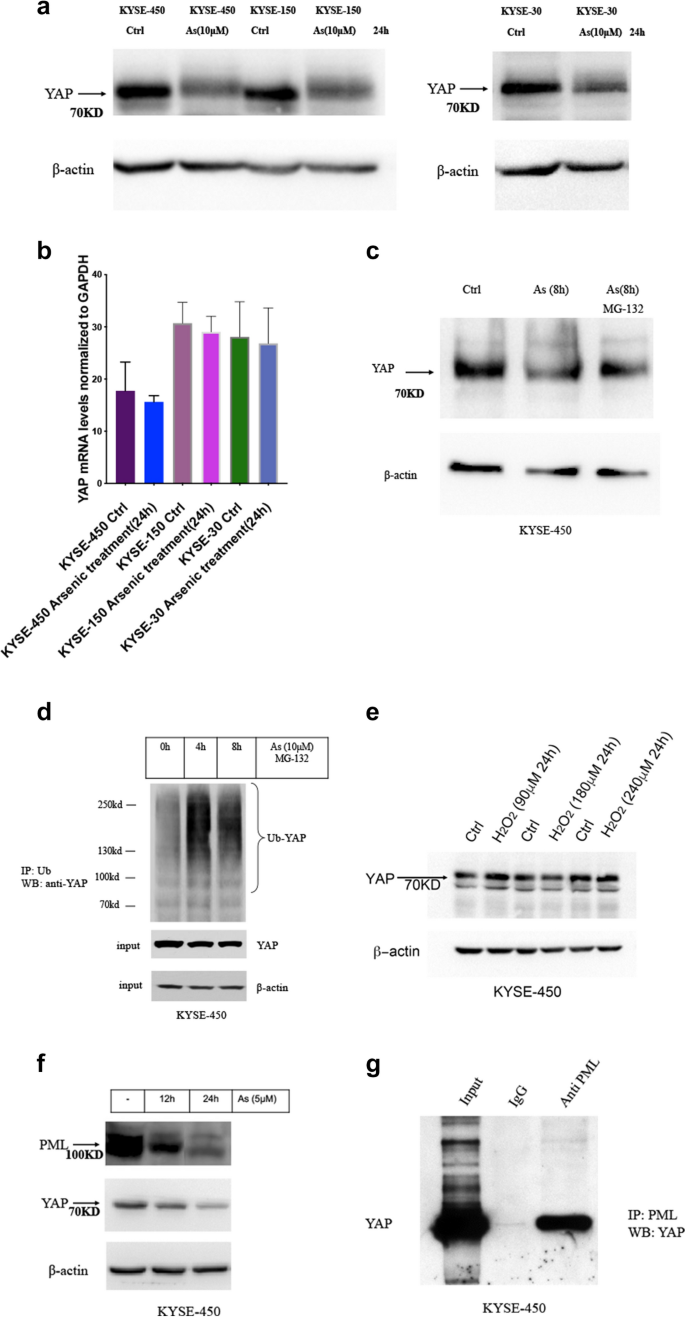
实验所用关键产品:Millipore Sigma的PML抗体(货号P6746)、CST的YAP抗体(货号14074)、Proteintech的β-actin抗体(货号60008-1-Ig)、Thermo的Pierce™ IP裂解液等。
3.4 YAP降解对ESCC细胞功能的影响
实验目的是验证YAP降解对ESCC细胞侵袭迁移能力及化疗敏感性的调控作用。方法细节为构建持续激活型YAP(YAP5SA)过表达的KYSE-450细胞系,分别用AFCNC、YAP抑制剂Verteporfin处理细胞,通过Transwell实验检测侵袭迁移能力,采用流式细胞术检测顺铂诱导的细胞凋亡率。结果解读:Transwell实验显示,YAP5SA过表达显著增强KYSE-450细胞的侵袭迁移能力,而AFCNC处理可逆转该增强效应(n=3,P<0.01);流式细胞术结果显示,YAP5SA过表达可降低顺铂诱导的凋亡率,AFCNC处理可显著恢复凋亡率,效果与Verteporfin相似(n=3,P<0.01)。
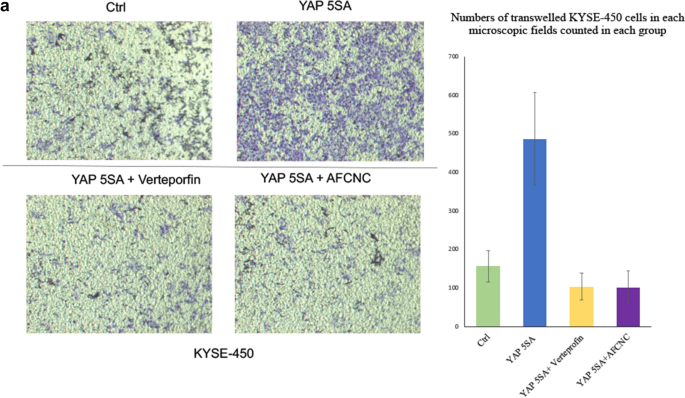
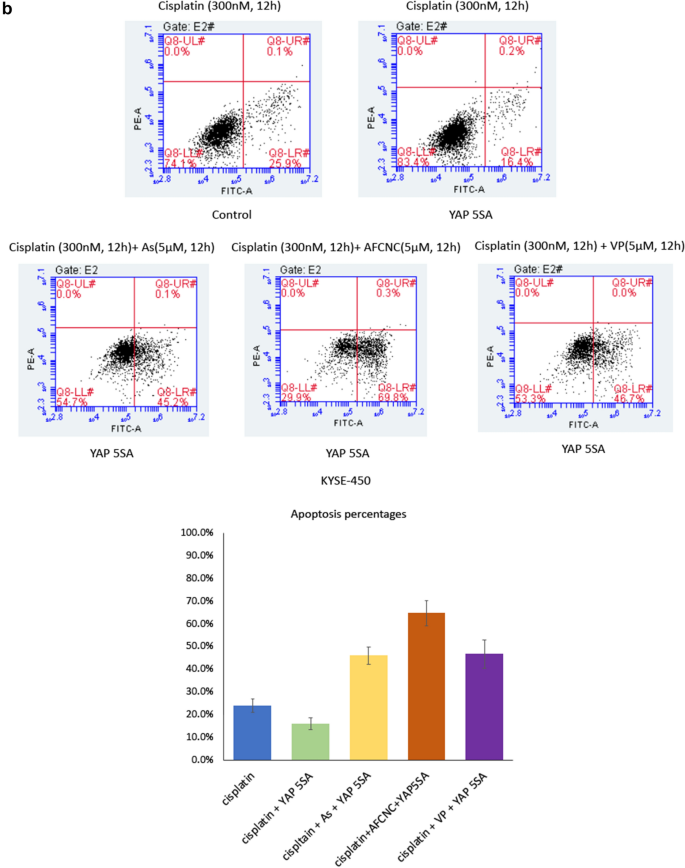
实验所用关键产品:BD Pharmingen™ FITC-Annexin V凋亡检测试剂盒、Corning的Transwell小室等。
3.5 动物模型验证AFCNC的放化疗增敏作用
实验目的是验证AFCNC在体内对ESCC放化疗的增敏效果及机制。方法细节为构建KYSE-450细胞裸鼠异种移植模型,当肿瘤体积达100mm³时,分别给予AFCNC单药、顺铂单药、放疗单药、AFCNC联合顺铂、AFCNC联合放疗处理,每6天给药一次,放疗剂量为5Gy,定期测量肿瘤体积,实验结束后采用免疫组化检测肿瘤组织中YAP和环氧化酶-2(COX-2)的表达。结果解读:动物实验结果显示,AFCNC联合顺铂或放疗组的肿瘤体积显著小于单药处理组(n=6,P<0.01),且未观察到明显的全身毒性;免疫组化结果显示,AFCNC处理可显著降低肿瘤组织中YAP的表达,同时升高COX-2的表达,提示其通过降解YAP实现放化疗增敏。

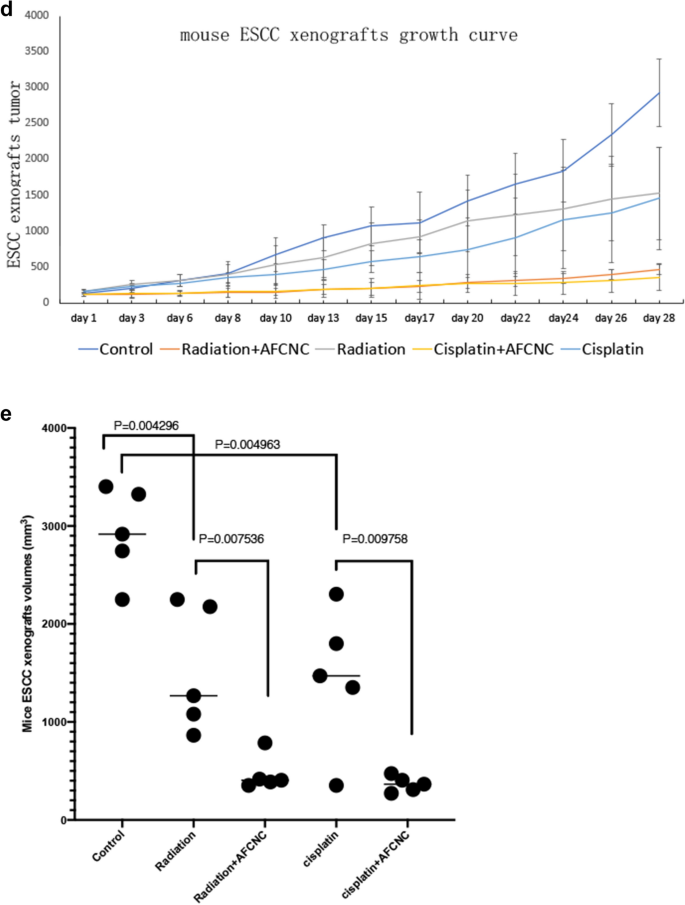
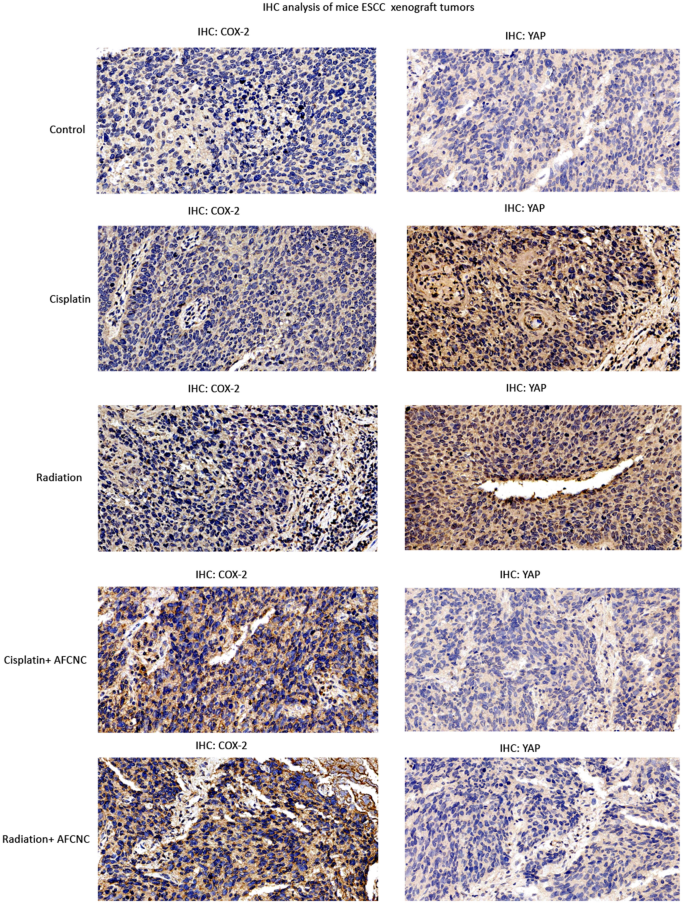
实验所用关键产品:Proteintech的COX-2抗体(货号12375-1-AP)和YAP抗体(货号13584-1-AP)、Dako的HRP标记山羊抗兔二抗等。
4. Biomarker研究及发现成果解析
核心信息段:本研究中涉及的Biomarker为YAP,属于转录因子类Biomarker,筛选与验证逻辑为“基因芯片通路筛选→细胞水平降解机制验证→临床前动物模型功能验证”,完整阐明了YAP作为砷纳米复合物靶点的作用及放化疗增敏价值。
YAP是Hippo通路的关键转录因子,在ESCC中异常激活,与肿瘤干细胞特性、放化疗耐药密切相关。本研究通过基因芯片筛选发现Hippo通路受砷处理显著影响,进而聚焦YAP作为核心Biomarker,验证逻辑为细胞水平明确砷诱导YAP降解的机制,动物模型验证YAP降解对放化疗增敏的作用。YAP来源于ESCC细胞及异种移植肿瘤组织,验证方法包括western blot检测蛋白表达、qRT-PCR检测mRNA水平、免疫组化检测组织表达;特异性方面,AFCNC可特异性诱导YAP蛋白降解,而不影响其mRNA水平,对正常细胞的毒性较低;敏感性方面,AFCNC联合放化疗可显著降低YAP表达,增敏效果显著,ROC曲线数据未在文献中提及。
YAP作为ESCC放化疗耐药的关键Biomarker,AFCNC通过降解YAP逆转耐药,联合放化疗可显著抑制肿瘤生长,风险比(HR)未在文献中明确,动物实验样本量为n=6,P<0.01;本研究首次发现砷通过降解PML介导YAP降解的机制,为ESCC的放化疗增敏提供了新的分子靶点与治疗策略,具有重要的临床转化潜力。
