1. 领域背景与文献引入
文献英文标题:RNA sequencing profiles reveal dynamic signaling and glucose metabolic features during bone marrow mesenchymal stem cell senescence;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:干细胞衰老与代谢调控
领域共识:干细胞衰老被认为是机体衰老的核心驱动因素,1956年Harman提出自由基衰老理论,2013年《Cell》杂志系统阐述了衰老的九大标志,为该领域奠定了理论基础。当前干细胞衰老领域的研究热点聚焦于代谢重编程与干细胞命运调控的关系,已有研究证实代谢在干细胞自我更新、多向分化及衰老过程中发挥关键作用,但代谢相关基因及信号通路在生理性衰老中的具体调控机制仍不明确,尤其是骨髓间充质干细胞(MSCs)作为组织修复和再生医学的核心种子细胞,其年龄相关衰老过程中的糖代谢变化及调控网络尚未得到系统解析。针对这一研究空白,本研究通过RNA测序结合功能富集分析,系统解析老年大鼠MSCs的差异表达基因谱,聚焦糖代谢通路揭示其对MSCs衰老的调控机制,为干预年龄相关表型提供新的治疗靶点。
2. 文献综述解析
作者对领域内现有研究的分类维度主要包括:按干细胞类型(骨髓间充质干细胞、造血干细胞、神经干细胞等)、代谢能量来源(糖酵解、氧化磷酸化)、衰老调控通路(p16INK4a/Rb、p53/p21等)进行分类梳理。现有研究的关键结论显示,与分化成熟细胞依赖氧化磷酸化产生ATP不同,干细胞主要通过糖酵解满足能量需求;不同类型干细胞衰老时糖代谢变化存在差异,如老年大鼠造血干细胞糖酵解水平下降,而生殖干细胞糖酵解水平升高。现有研究的技术方法优势在于多组学(转录组、代谢组、蛋白质组)技术的应用,能够从全局层面解析干细胞衰老的分子特征,但局限性在于缺乏对MSCs生理性衰老过程中糖代谢调控的系统研究,尤其是关键代谢基因与非编码RNA的调控网络尚未明确。本研究的创新价值在于,首次通过RNA测序结合功能富集分析,系统鉴定老年大鼠MSCs的差异表达基因,聚焦糖酵解通路明确其水平下降与MSCs衰老的直接关联,并构建了糖代谢关键基因的miRNA调控网络,填补了MSCs生理性衰老中糖代谢调控机制的研究空白。
3. 研究思路总结与详细解析
本研究的整体框架为:以年轻和老年大鼠MSCs为研究对象,首先验证老年大鼠MSCs的生理性衰老表型,随后通过RNA测序筛选差异表达基因,经功能富集分析聚焦糖代谢通路,进一步验证糖酵解相关基因表达及糖酵解功能水平,最后预测糖代谢关键基因的miRNA调控网络,形成“表型验证-组学筛选-功能验证-机制预测”的完整研究闭环。研究目标是明确年龄相关MSCs衰老的分子特征,揭示糖代谢对MSCs衰老的调控机制;核心科学问题是糖代谢相关基因及信号通路如何参与MSCs的生理性衰老过程。
3.1 骨髓间充质干细胞分离与衰老表型验证
实验目的是确认老年大鼠来源MSCs是否发生生理性衰老,为后续组学分析提供可靠的研究模型。方法细节为采用全骨髓贴壁法分离1-2月龄(年轻)和15-18月龄(老年)Wistar大鼠的MSCs,传至第3代(P3)后,通过形态学观察、衰老相关β-半乳糖苷酶(SA-β-gal)染色、活性氧(ROS)荧光检测、衰老标志物p16INK4a和磷酸化Rb1的mRNA及蛋白水平检测,多维度验证细胞衰老表型。结果解读显示,老年大鼠MSCs呈现不规则、扁平膨大的形态,细胞表面积显著增加(n=3,P<0.001);SA-β-gal阳性细胞比例较年轻组升高3倍以上(n=3,P<0.001);ROS荧光强度显著增强(n=3,P<0.01);p16INK4a和磷酸化Rb1的mRNA及蛋白水平均显著上调(n=3,P<0.05至P<0.001),上述结果共同证实老年大鼠MSCs发生生理性衰老。
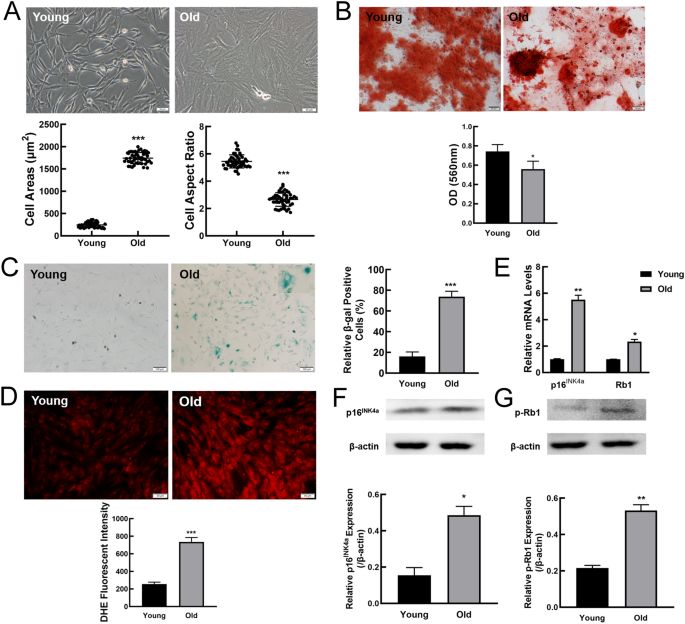
实验所用关键产品:Abclonal的抗p16INK4a抗体、抗磷酸化Rb1抗体,BD的FACSCalibur流式细胞仪,Beyotime的SA-β-gal染色试剂盒、DHE ROS检测试剂盒,OLYMPUS的荧光显微镜。
3.2 RNA测序与差异表达基因筛选
实验目的是系统筛选年轻与老年大鼠MSCs的差异表达基因(DEGs),解析年龄相关MSCs衰老的转录组特征。方法细节为提取P3代MSCs的总RNA,经琼脂糖凝胶电泳检测完整性后,用KAPA Stranded RNA-Seq Library Prep Kit构建测序文库,通过Illumina HiSeq 4000平台进行RNA测序,以FPKM≥0.5、倍数变化>1.5且P<0.05为标准筛选DEGs。结果解读显示,共鉴定出868个上调DEGs和2006个下调DEGs,上调基因主要参与细胞分化、生长因子结合等生物学过程,下调基因主要富集在细胞代谢、线粒体功能等通路;相关性分析和主成分分析显示,组间基因表达差异显著,组内样本重复性良好,表明基因表达变化与年龄效应密切相关。
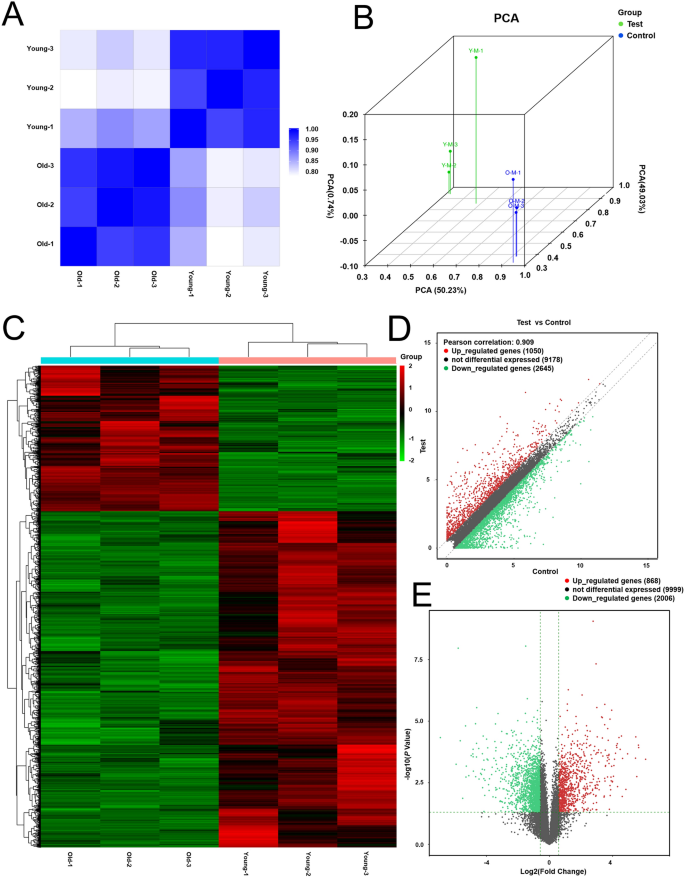
实验所用关键产品:Takara的RNAiso总RNA提取试剂、RNA PCR反转录试剂盒,Illumina的KAPA Stranded RNA-Seq Library Prep Kit、HiSeq 4000测序平台。
3.3 差异表达基因功能富集分析
实验目的是解析DEGs的功能分类及富集通路,明确与MSCs衰老相关的核心生物学过程及信号通路。方法细节为采用基因本体(GO)和京都基因与基因组百科全书(KEGG)数据库对DEGs进行功能富集分析,筛选FDR校正P<0.05的显著富集条目。结果解读显示,GO分析中上调DEGs富集在解剖结构形态发生、细胞分化等生物过程,下调DEGs富集在细胞代谢过程、线粒体等细胞组分;KEGG分析显示上调通路包括黏着斑、ECM-受体相互作用、PI3K-Akt信号通路等,下调通路包括代谢通路、糖酵解/糖异生、戊糖磷酸途径等,表明老年大鼠MSCs代谢水平显著下降,糖酵解通路是调控MSCs衰老的核心通路之一。
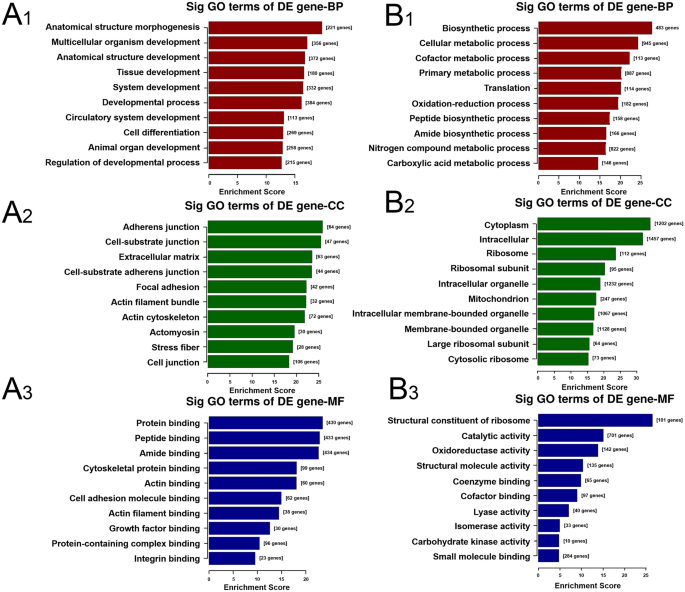
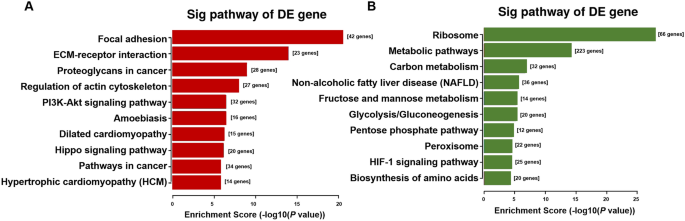
文献未提及具体分析工具,领域常规使用StringTie、R语言clusterProfiler包进行功能富集分析。
3.4 糖酵解相关基因表达与功能验证
实验目的是验证糖酵解通路关键基因的表达变化及糖酵解功能水平,明确糖酵解与MSCs衰老的直接关联。方法细节为从糖酵解/糖异生通路中筛选高表达、组间差异显著的关键基因,用实时定量反转录聚合酶链式反应(RT-qPCR)验证RNA测序结果;通过葡萄糖摄取、乳酸分泌、ATP生成、细胞外酸化率(ECAR)检测糖酵解功能水平;并用2-脱氧-D-葡萄糖(2-DG)抑制糖酵解,进一步验证糖酵解对MSCs衰老的调控作用。结果解读显示,RNA测序显示糖酵解关键限速酶(HK1、PFKM、PFKL、PK)及乳酸脱氢酶(LDHA、LDHB)等基因在老年大鼠MSCs中表达显著下调;RT-qPCR验证显示HK1、PFKM、LDHA、LDHB等基因表达与测序结果一致(n=3,P<0.05至P<0.001);老年大鼠MSCs的葡萄糖摄取、乳酸分泌、ATP生成、ECAR均显著降低(n=3,P<0.05至P<0.001);2-DG处理后,两组MSCs糖酵解水平均显著下降,且老年组变化更显著,表明糖酵解水平下降与MSCs衰老密切相关。
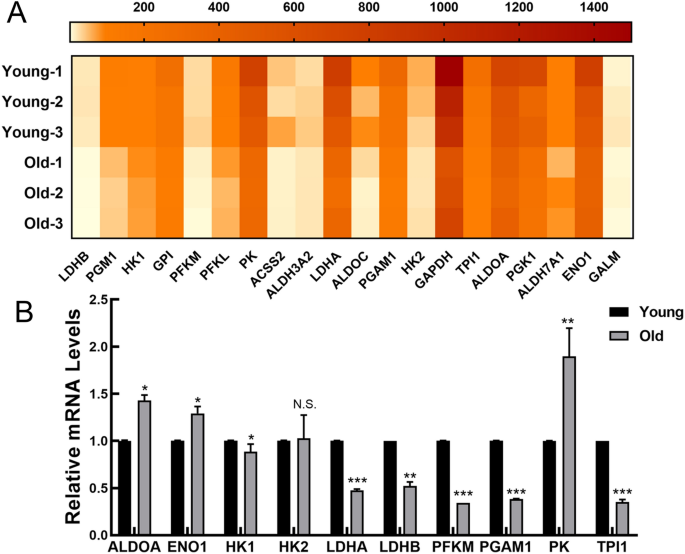
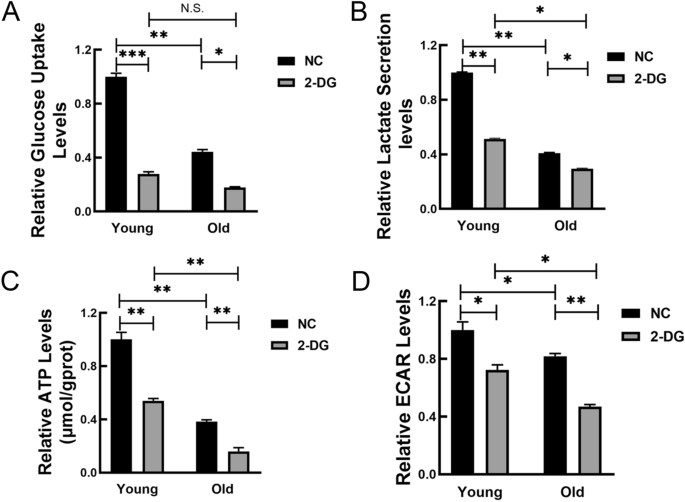
实验所用关键产品:Jiancheng Bio的葡萄糖检测试剂盒、乳酸检测试剂盒、ATP检测试剂盒,Luxcel Bioscience的pH-Xtra ECAR检测试剂,ABI的7300实时PCR系统。
3.5 糖代谢关键基因的miRNA调控网络预测
实验目的是解析糖代谢调控MSCs衰老的潜在分子机制,筛选调控糖代谢关键基因的miRNA。方法细节为利用microRNA.org数据库对糖酵解关键基因(LDHB、PGM1、GPI、PFKM、PFKL)进行miRNA预测,筛选PhastCons≥0且mirSVR≤-0.1的潜在靶向miRNA,并用Cytoscape软件构建mRNA-miRNA调控网络。结果解读显示,共构建了包含5个糖代谢关键基因和49个miRNA的调控网络,其中miR-30d与PGM1的靶向作用最显著,miR-128、miR-130a、miR-150、miR-873可能在调控网络中发挥核心作用,为后续解析miRNA调控糖代谢参与MSCs衰老的机制提供了方向。
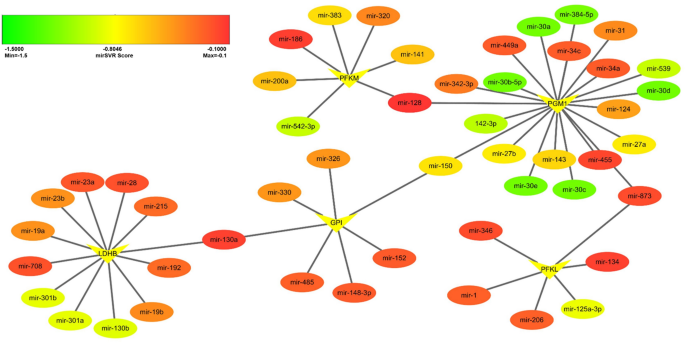
文献未提及具体实验产品,领域常规使用Cytoscape软件构建调控网络。
4. Biomarker研究及发现成果解析
Biomarker定位:本研究中涉及的潜在Biomarker包括糖酵解关键基因(HK1、PFKM、LDHA、LDHB等)及靶向调控这些基因的miRNA(miR-128、miR-30d等)。筛选与验证逻辑为:首先通过RNA测序筛选MSCs衰老过程中的差异表达基因,经功能富集分析聚焦糖酵解通路关键基因,随后用RT-qPCR验证基因表达变化,最后通过生物信息学预测靶向调控这些基因的miRNA,形成“组学筛选-实验验证-网络预测”的完整链条。
研究过程详述:这些Biomarker的来源为老年大鼠MSCs的转录组数据,验证方法包括RT-qPCR(基因表达验证)和糖代谢功能实验(葡萄糖摄取、乳酸分泌、ATP生成、ECAR检测);特异性方面,HK1、PFKM等基因在老年大鼠MSCs中的表达下调倍数为1.5-3倍(n=3,P<0.05),能够有效区分年轻与老年大鼠MSCs;敏感性数据未在文献中明确提及。
核心成果提炼:这些糖酵解关键基因可作为MSCs衰老的潜在分子标志物,其表达下调与MSCs衰老显著相关(P<0.05);本研究的创新性在于首次系统揭示老年大鼠MSCs中糖酵解水平下降的分子机制,并构建了糖代谢关键基因的miRNA调控网络,为干预年龄相关MSCs衰老、改善老年组织修复能力提供了新的潜在靶点。由于缺乏临床样本验证,这些Biomarker的临床应用价值仍需进一步研究。
