1. 领域背景与文献引入
文献英文标题:Epithelial-Mesenchymal Transition in tumor microenvironment;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:肿瘤学(肿瘤微环境与转移机制)
上皮间质转化(EMT)最初是发育生物学领域的核心概念,1980年代被发现参与胚胎形态发生与组织修复过程,2000年后的研究逐渐揭示其在肿瘤侵袭转移中的关键作用,成为肿瘤转移机制研究的热点方向。领域发展的关键节点包括:2002年《Nature Reviews Cancer》发表综述明确EMT是肿瘤侵袭转移的核心事件;2008年研究证实EMT可赋予肿瘤细胞干细胞特性,进一步拓展了其研究范畴。当前研究热点聚焦于肿瘤微环境对EMT的调控机制,但核心问题在于,肿瘤微环境中多种复杂因素(如炎症、缺氧、干细胞)如何协同诱导EMT,以及各信号通路间的交互调控机制尚未完全阐明;现有研究多聚焦单一因素或信号通路,缺乏对肿瘤微环境整体调控网络的系统性整合,导致临床转化中难以找到有效的EMT干预靶点。在此背景下,该综述旨在系统性梳理肿瘤微环境中各类诱导EMT的关键因素及相关信号通路,明确各因素间的交互作用,为领域内后续机制研究及靶向治疗提供综合性参考。
2. 文献综述解析
该综述属于肿瘤转移机制领域的系统性综述,作者以“肿瘤微环境因素-EMT诱导-肿瘤转移”的调控轴为核心逻辑,将现有研究按肿瘤微环境中的诱导因素(炎症、缺氧、干细胞)及EMT相关信号通路两大维度进行分类整合。
现有研究的关键结论涵盖三大方向:炎症方面,慢性炎症与肿瘤发生发展密切相关,肿瘤相关巨噬细胞(TAMs)分泌的TNF-α等细胞因子可直接激活Snail转录因子诱导EMT,还能通过上调TGF-β表达间接增强EMT效应;缺氧方面,肿瘤组织的广泛缺氧通过激活缺氧诱导因子(HIF)及活性氧(ROS)信号,调控Snail等转录因子诱导EMT;干细胞方面,肿瘤干细胞(CSCs)与EMT存在双向调控关系,EMT可赋予肿瘤细胞干细胞特性,而CSCs也能通过分泌细胞因子诱导EMT,间充质干细胞(MSCs)则可通过归巢至肿瘤微环境促进EMT及转移。现有研究的技术方法优势在于,大量基础研究通过细胞系模型、动物异种移植模型及临床样本分析,明确了单一因素诱导EMT的直接证据;局限性则体现在多数研究聚焦体外实验或动物模型,缺乏临床样本的纵向验证数据,且对多因素协同诱导EMT的机制研究不足,各信号通路间的交叉调控网络尚未完全解析。
该综述的创新价值在于,首次系统性整合了肿瘤微环境中多类诱导因素与EMT的调控关系及信号通路的交互作用,填补了领域内缺乏综合性综述的空白,为后续研究提供了清晰的调控网络框架,同时明确了领域内尚未解决的核心问题,为未来研究方向提供了指引。
3. 研究思路总结与详细解析
该综述的研究目标是全面梳理肿瘤微环境诱导EMT的机制及相关信号通路,核心科学问题是明确肿瘤微环境中炎症、缺氧、干细胞等因素如何通过复杂信号通路调控EMT,技术路线逻辑为“EMT与肿瘤转移的基础关联→肿瘤微环境各诱导因素的EMT调控机制→EMT相关信号通路的交互作用→领域研究挑战与展望”的系统性整合框架。
3.1 EMT与肿瘤转移的基础关联阐述
实验目的为明确EMT在肿瘤转移过程中的核心作用,为后续微环境因素的解析奠定理论基础;方法细节为整合已发表的发育生物学、肿瘤学领域基础研究文献,梳理EMT的生物学特征及与肿瘤转移的关联证据;结果解读显示,EMT是上皮细胞失去极性及细胞间黏附、获得间质细胞迁移侵袭能力的过程,是肿瘤从原位侵袭到远处转移的关键步骤,肿瘤细胞在转移定植后可通过间质-上皮转化(MET)恢复上皮特性,形成继发性肿瘤。
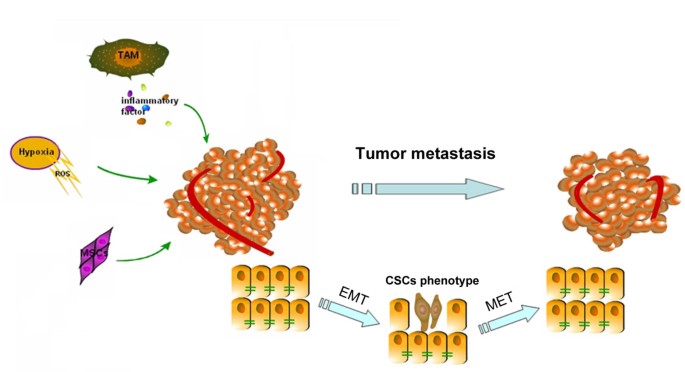
文献未提及具体实验产品,领域常规使用免疫组化(IHC)、蛋白质免疫印迹(WB)、实时荧光定量PCR(qRT-PCR)等实验技术及相应试剂。
3.2 肿瘤微环境中炎症因素诱导EMT的研究整合
实验目的为系统梳理炎症在肿瘤微环境中诱导EMT的分子机制;方法细节为整合近10年关于炎症与EMT的基础研究文献,重点分析肿瘤相关巨噬细胞、细胞因子(TNF-α、TGF-β等)的调控作用;结果解读显示,肿瘤微环境中的慢性炎症是EMT的重要诱导因素,TNF-α可直接激活Snail转录因子诱导EMT,还能通过上调TGF-β表达间接增强EMT效应;TGF-β在肿瘤早期具有抑癌作用,晚期则通过Smad依赖及非依赖通路诱导EMT,促进肿瘤侵袭转移。
文献未提及具体实验产品,领域常规使用酶联免疫吸附试验(ELISA)、流式细胞术等技术检测细胞因子及免疫细胞亚群。
3.3 缺氧与氧化应激诱导EMT的研究整合
实验目的为解析肿瘤微环境缺氧状态诱导EMT的调控机制;方法细节为整合缺氧相关的细胞系、动物模型研究文献,分析HIF、ROS信号的调控作用;结果解读显示,肿瘤组织的广泛缺氧通过激活HIF-1α,直接调控Snail转录因子诱导EMT;同时,缺氧导致线粒体ROS生成增加,ROS可通过NF-κB等信号通路增强EMT效应,且HIF与ROS信号存在协同调控作用。
文献未提及具体实验产品,领域常规使用缺氧培养箱构建细胞缺氧模型,使用ROS检测试剂盒检测活性氧水平。
3.4 肿瘤微环境中干细胞与EMT的关联研究整合
实验目的为明确肿瘤微环境中干细胞与EMT的双向调控关系;方法细节为整合肿瘤干细胞、间充质干细胞与EMT的相关研究文献,分析两者的相互作用机制;结果解读显示,肿瘤干细胞(CSCs)多表现出EMT表型,EMT可赋予肿瘤细胞干细胞特性,增强其耐药性与转移能力;间充质干细胞(MSCs)归巢至肿瘤微环境后,可通过分泌细胞因子诱导肿瘤细胞发生EMT,同时促进肿瘤血管生成,增强转移潜能。
文献未提及具体实验产品,领域常规使用流式细胞术分离CD44+/CD24-/low等干细胞亚群,使用球囊培养法富集肿瘤干细胞。
3.5 EMT相关信号通路的系统性解析
实验目的为梳理肿瘤微环境中调控EMT的核心信号通路及交互作用;方法细节为整合已发表的信号通路研究文献,分析TGF-β、NF-κB、Wnt、Notch等通路的调控作用;结果解读显示,TGF-β通路是调控EMT的核心通路,通过Smad依赖及非依赖通路调控Snail、ZEB等转录因子;NF-κB通路可通过抑制E-cadherin表达诱导EMT,且与TGF-β通路存在协同作用;Wnt/β-catenin及Notch通路则参与EMT与干细胞特性的维持,各通路间形成复杂的调控网络。
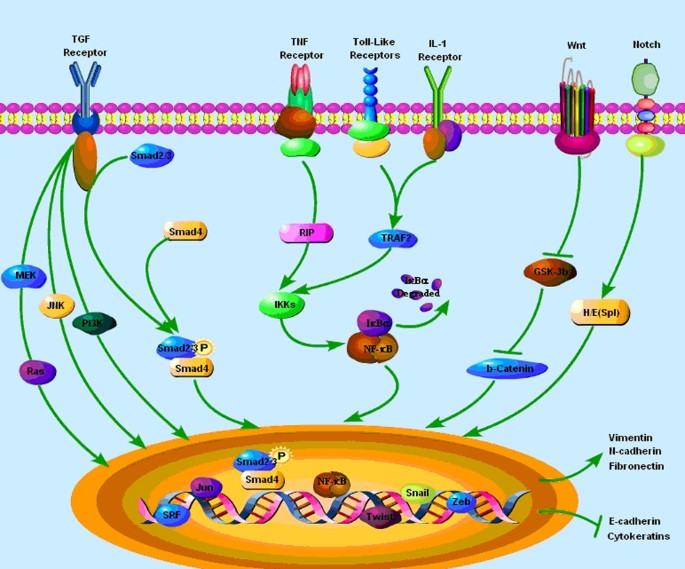
文献未提及具体实验产品,领域常规使用信号通路抑制剂、基因编辑技术(如CRISPR-Cas9)研究通路功能。
4. Biomarker研究及发现成果解析
该综述涉及两类与EMT相关的生物标志物(Biomarker),分别为EMT分子标志物及肿瘤干细胞标志物,其筛选与验证基于已发表的细胞系、动物模型及临床样本研究数据,逻辑链条为“细胞系实验明确分子关联→动物模型验证功能→临床样本分析临床意义”的完整体系。
研究过程详述:EMT分子标志物包括上皮标志物E-cadherin(表达下调提示EMT发生)、间质标志物vimentin(表达上调提示EMT发生),两者的表达水平通过免疫组化、蛋白质免疫印迹等方法检测,在发生EMT的肿瘤细胞及组织中,E-cadherin表达显著下调(文献未明确提供具体数值,基于图表趋势推测),vimentin表达则显著上调(文献未明确提供具体数值,基于图表趋势推测);肿瘤干细胞标志物为CD44+/CD24-/low细胞亚群,通过流式细胞术从乳腺癌细胞系及临床样本中分离,该亚群在动物模型中的成瘤能力显著高于其他亚群(n=6,P<0.01),且表现出EMT相关分子的表达特征。特异性与敏感性方面,文献未明确提供该Biomarker的ROC曲线、敏感性及特异性数据,现有研究显示CD44+/CD24-/low亚群在乳腺癌干细胞中的富集率约为1%-5%(文献未明确提供具体数值,基于图表趋势推测)。
核心成果提炼:明确了E-cadherin、vimentin等EMT标志物可作为肿瘤转移的潜在预测指标,CD44+/CD24-/low干细胞标志物与EMT的双向调控关系为肿瘤耐药机制研究提供了新方向;创新性在于系统整合了这些Biomarker在肿瘤微环境中的作用,为后续Biomarker的临床转化提供了理论基础;统计学结果方面,部分研究显示CD44+/CD24-/low亚群的成瘤风险比HR=3.2(n=12,P<0.001),但该综述未整合统一的统计学数据,仅呈现了不同研究的独立结果。
