1. 领域背景与文献引入
文献英文标题:Predictive biomarkers for the responsiveness of recurrent glioblastomas to activated killer cell immunotherapy;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:神经肿瘤学(胶质母细胞瘤免疫治疗)
胶质母细胞瘤(GBM)是成人最常见、恶性程度最高的原发性脑肿瘤,领域共识:其中位生存期不足20个月,5年生存率仅4%-5%,即使接受手术切除联合放疗、替莫唑胺化疗的标准治疗方案,仍有超过90%的患者会出现肿瘤复发,且复发后缺乏有效的治疗手段,患者预后极差。近年来,免疫治疗在黑色素瘤、非小细胞肺癌等实体瘤中取得突破性进展,但针对GBM的免疫检查点抑制剂(如CTLA-4、PD-1/PD-L1抑制剂)大型Ⅲ期临床试验均未显示出生存获益,其耐药机制涉及肿瘤自身低肿瘤突变负荷(TMB)、广泛的肿瘤内异质性,以及肿瘤微环境(TME)中存在的免疫抑制因子(如TGF-β、VEGF)、调节性T细胞(Treg)、髓源性抑制细胞(MDSCs)等,这些因素共同抑制了抗肿瘤免疫反应的激活与效应发挥。自然杀伤(NK)细胞作为固有免疫的核心细胞,可直接识别并杀伤肿瘤细胞,同时通过分泌细胞因子调节免疫微环境,成为GBM免疫治疗的新方向。前期临床研究显示,自体活化NK细胞(AKC)治疗可使部分复发性GBM患者获得长期生存,但目前缺乏能够精准预测患者对该治疗反应性的生物标志物,无法实现个体化治疗,这是当前领域亟待解决的核心问题。本研究正是针对这一空白,通过分析复发性GBM患者接受AKC治疗后的肿瘤免疫微环境特征,筛选并验证预测治疗反应的生物标志物,为GBM的精准NK细胞治疗提供理论依据与临床指导。
2. 文献综述解析
本文作者围绕GBM免疫治疗的现状与挑战,从免疫治疗类型、耐药机制及NK细胞治疗的潜力三个维度对领域内现有研究进行系统评述,明确了现有研究的优势与局限性,凸显了本研究的创新价值与必要性。
现有研究中,免疫检查点抑制剂在其他实体瘤中展现出显著的抗肿瘤活性,其优势在于可通过解除T细胞免疫耐受激活内源性抗肿瘤免疫,但针对GBM的临床试验均以失败告终,局限性主要源于GBM自身的免疫逃逸特性,包括低TMB导致肿瘤抗原不足、肿瘤细胞分泌大量免疫抑制因子、TME中免疫抑制细胞浸润等,使得免疫检查点抑制剂无法有效激活抗肿瘤免疫。NK细胞治疗的优势在于可绕过T细胞免疫耐受直接杀伤肿瘤细胞,同时能够调节TME的免疫抑制状态,前期小样本临床研究显示其在部分复发性GBM患者中具有生存获益,但局限性在于缺乏有效的生物标志物筛选适宜人群,导致治疗响应率难以提升。作者通过对比现有研究的未解决问题,指出本研究的创新点在于首次采用NanoString nCounter免疫基因表达谱分析结合机器学习模型,筛选出TNFRSF18、TNFSF4、IL12RB2三个可精准预测复发性GBM患者对AKC治疗反应性的生物标志物,并通过功能实验验证了其与免疫细胞浸润、NK细胞迁移的调控关系,填补了NK细胞治疗GBM预测标志物领域的空白,为实现个体化NK细胞治疗提供了关键工具。
3. 研究思路总结与详细解析
本研究的核心目标是筛选并验证复发性GBM患者对AKC治疗反应性的预测生物标志物,核心科学问题为肿瘤免疫微环境中哪些基因参与调控NK细胞治疗的反应性,其功能机制是什么。研究采用“临床样本队列构建→免疫基因表达谱分析→候选基因筛选与验证→功能机制研究→临床预后关联”的闭环技术路线,通过多组学分析与实验验证相结合的方法,系统解析了预测生物标志物的筛选与功能机制。
3.1 临床样本收集与分组
实验目的为建立应答者与非应答者的临床样本队列,为后续免疫微环境分析提供基础。方法细节上,研究选取12例接受AKC治疗的复发性GBM患者,根据治疗反应分为应答者(5例,生存期≥24个月)与非应答者(7例,生存期<24个月),收集患者治疗前的石蜡包埋肿瘤组织样本,由两位经过认证的病理学家通过苏木精-伊红(H&E)染色评估样本质量并确定肿瘤分析区域。结果解读显示,应答者的中位总生存期(OS)为22.5个月,中位无进展生存期(PFS)为10个月,5例应答者均存活超过2年且日常活动正常;非应答者的生存期均不足2年,治疗期间MRI显示肿瘤进展。IDH1(R132H)突变仅在1例非应答者中检测到,MGMT启动子甲基化在应答者和非应答者中分别有3例和4例。文献未提及具体实验产品,领域常规使用石蜡包埋组织样本处理试剂、病理染色试剂等。
3.2 肿瘤免疫基因表达谱分析
实验目的为对比应答者与非应答者的肿瘤免疫基因表达差异,筛选潜在的预测生物标志物。方法细节上,提取样本总RNA,采用NanoString nCounter PanCancer免疫分析面板检测730个免疫与肿瘤相关基因的表达水平;通过三步分析流程筛选候选基因:首先选取ROC曲线下面积(AUC)≥0.85的基因,其次选取与OS或PFS相关(P<0.05)的基因,最后利用随机森林模型构建预测模型并评估基因的预测重要性。结果解读显示,应答者的免疫相关基因整体表达水平显著高于非应答者,提示其肿瘤微环境呈免疫激活状态;共鉴定出35个差异表达基因(DEGs),其中33个在应答者中高表达,仅NOTCH1在非应答者中高表达;主成分分析(PCA)显示,除1例外,应答者与非应答者可通过35个DEGs明显区分。随机森林模型分析显示,TNF超家族中的TNFRSF18、TNFSF4、IL12RB2三个基因组成的模型预测性能最佳,袋外误差率为0%,敏感性与特异性均为1.0,预测准确率达100%(95% CI 73.5-100%);三个基因在应答者中的mRNA表达水平分别为非应答者的2.8倍(TNFRSF18,P=0.06)、1.7倍(TNFSF4,P=0.0014)、2.0倍(IL12RB2,P=0.06)。
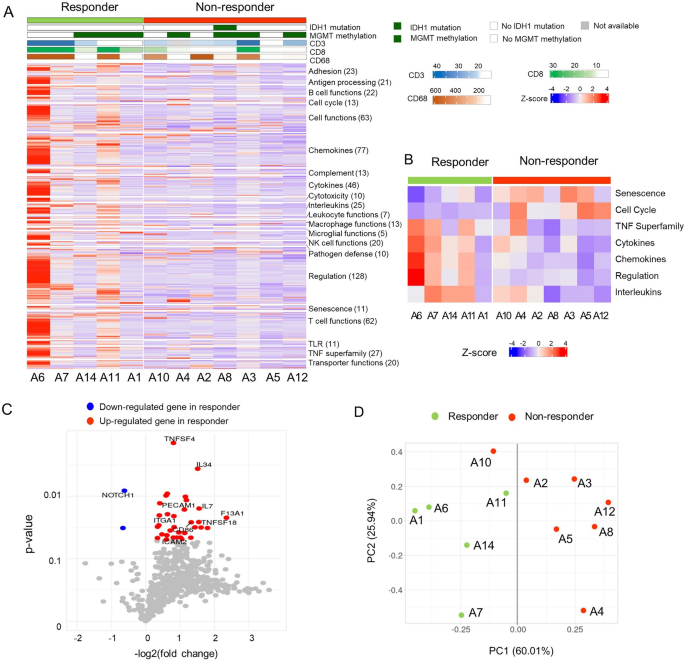
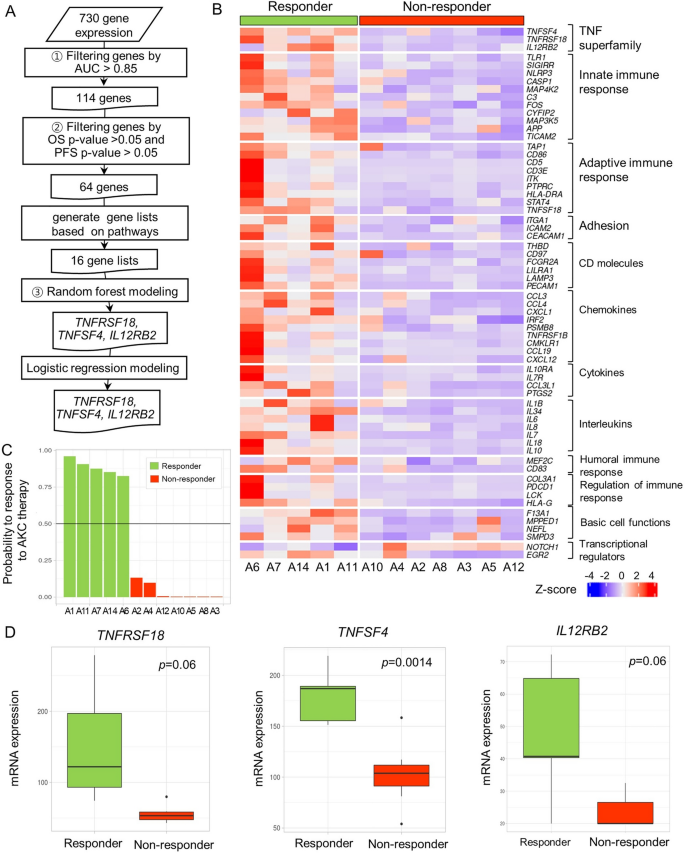
文献未提及具体实验产品,领域常规使用NanoString nCounter分析系统、RNA提取试剂盒等。
3.3 候选基因的qRT-PCR验证与临床预后关联
实验目的为验证候选基因的表达水平,并分析其与患者临床预后的关联。方法细节上,采用SuperScript™ IV VILO™ Master mix反转录RNA为cDNA,通过TaqMan™基因表达试剂盒进行qRT-PCR检测,以TBP为内参基因计算相对表达量;利用留一法交叉验证评估逻辑回归模型的预测性能;根据三个基因的中位表达水平将患者分为高表达组与低表达组,采用生存分析评估基因表达与PFS、OS的关联。结果解读显示,qRT-PCR检测结果与NanoString分析结果高度相关,Pearson相关系数分别为TNFRSF18(0.419)、TNFSF4(0.700)、IL12RB2(0.502);逻辑回归模型的预测准确率达100%(95% CI 73.54-100%),可有效区分应答者与非应答者;生存分析显示,高表达三个基因的患者PFS与OS均显著优于低表达组,其中TNFRSF18高表达组的PFS P=0.0017,OS P=0.0042;TNFSF4高表达组的PFS P=0.0017,OS P=0.0042;IL12RB2高表达组的PFS P=0.0055,OS P=0.018。
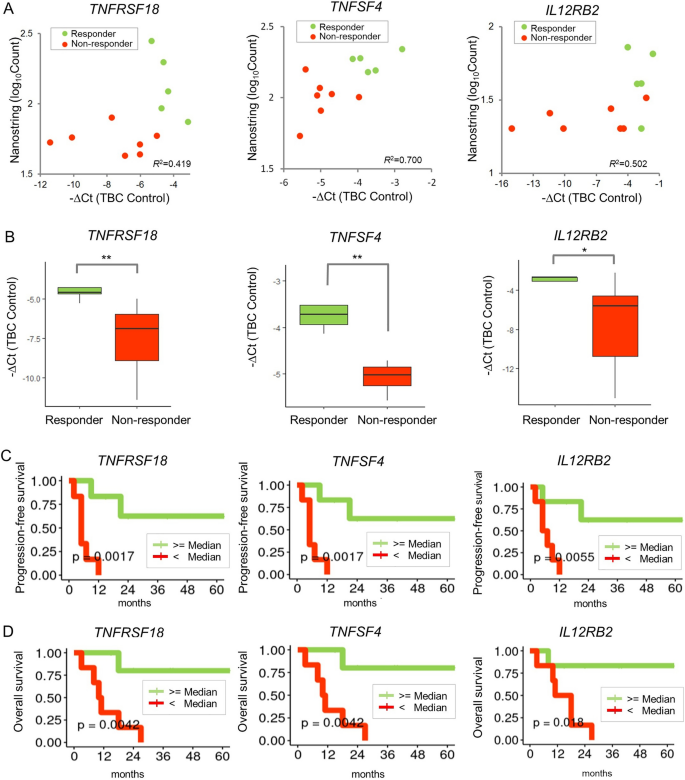
实验所用关键产品:SuperScript™ IV VILO™ Master mix(Invitrogen,Waltham,MA,USA)、TaqMan™ Gene expression assays(Applied Biosystems,Carlsbad,CA,USA)、Bio-Rad CFX96实时PCR检测系统(Bio-Rad)。
3.4 免疫组化分析肿瘤免疫细胞浸润
实验目的为分析应答者与非应答者肿瘤组织中免疫细胞的浸润差异,关联候选基因的表达与免疫微环境特征。方法细节上,对肿瘤组织样本进行免疫组化(IHC)染色,检测T细胞标志物CD3、细胞毒性T细胞标志物CD8、巨噬细胞/小胶质细胞标志物CD68的表达,采用QuPath软件分析阳性细胞的密度(个/mm²),对比应答者与非应答者的免疫细胞浸润差异。结果解读显示,应答者肿瘤组织中CD8⁺细胞毒性T细胞的平均密度为169.6±306.8个/mm²,是非应答者(14.62±12.2个/mm²)的11.5倍,尽管因样本量较小差异无统计学意义(P=0.32),但CD8⁺细胞密度的ROC曲线AUC为0.91,以19.225为截断值时,敏感性为0.8,特异性为0.86,可有效预测治疗反应;应答者肿瘤组织中CD68⁺巨噬细胞/小胶质细胞的平均密度为621.2±684.7个/mm²,是非应答者(279.5±198.1个/mm²)的2.2倍,差异同样无统计学意义(P=0.33);应答者中CD8⁺与CD68⁺细胞的密度高度相关(Pearson相关系数=0.95,P=0.013),提示这些免疫细胞在应答者的肿瘤微环境中存在密切相互作用,而在非应答者中无此相关性。
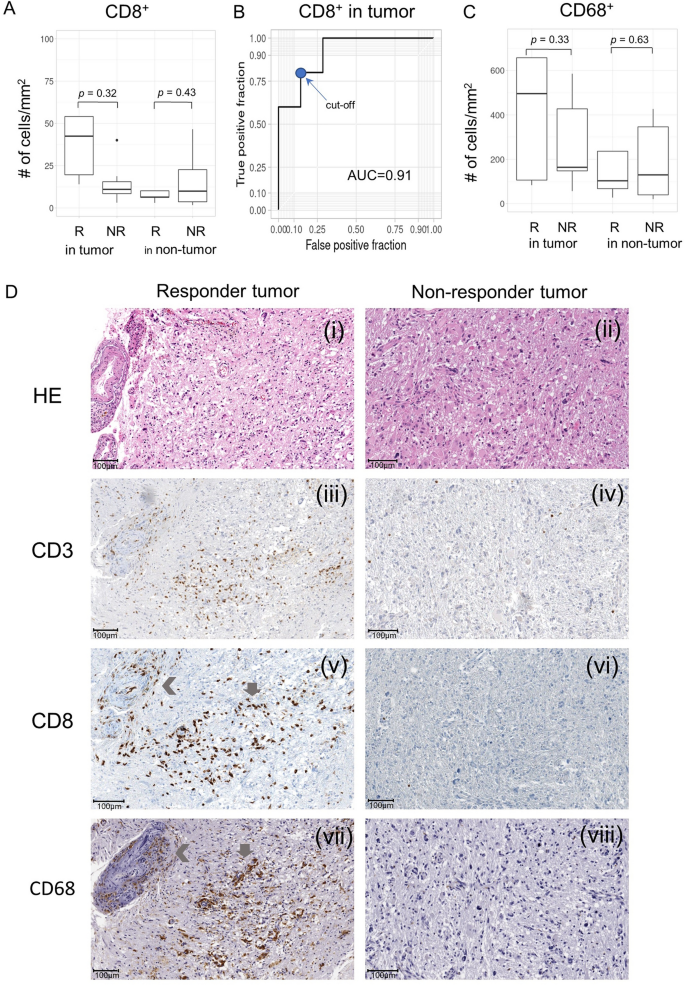
实验所用关键产品:CD3(2GV6)、CD8(SP57)、CD68(KP-1)抗体(Roche Diagnostics International AG,Rotkreuz,Switzerland)、VENTANA BechMark ULTRA全自动染色仪(Roche Diagnostics International AG)、Leica APERIO AT2数字切片扫描仪(Leica Biosystems,Nussloch,Germany)、QuPath图像分析软件。
3.5 候选基因与免疫细胞标志物的关联分析
实验目的为明确候选基因在免疫细胞中的来源及功能关联,解析其调控免疫微环境的机制。方法细节上,分析三个候选基因与44个免疫细胞标志物基因的表达相关性,采用Pearson相关系数评估应答者与非应答者中的关联差异。结果解读显示,应答者中TNFRSF18(GITR)与T细胞、Treg细胞、NK细胞、树突状细胞的标志物高度相关,提示其广泛参与多种免疫细胞的功能调控;TNFSF4(OX40L)与M2巨噬细胞标志物(CD206、CD163)相关,提示其与巨噬细胞的极化与功能有关;IL12RB2与NK细胞标志物CD56相关,提示其参与NK细胞的功能调控;而在非应答者中,三个候选基因与免疫细胞标志物无明确相关性,进一步说明这些基因的功能仅在免疫激活的微环境中发挥作用。
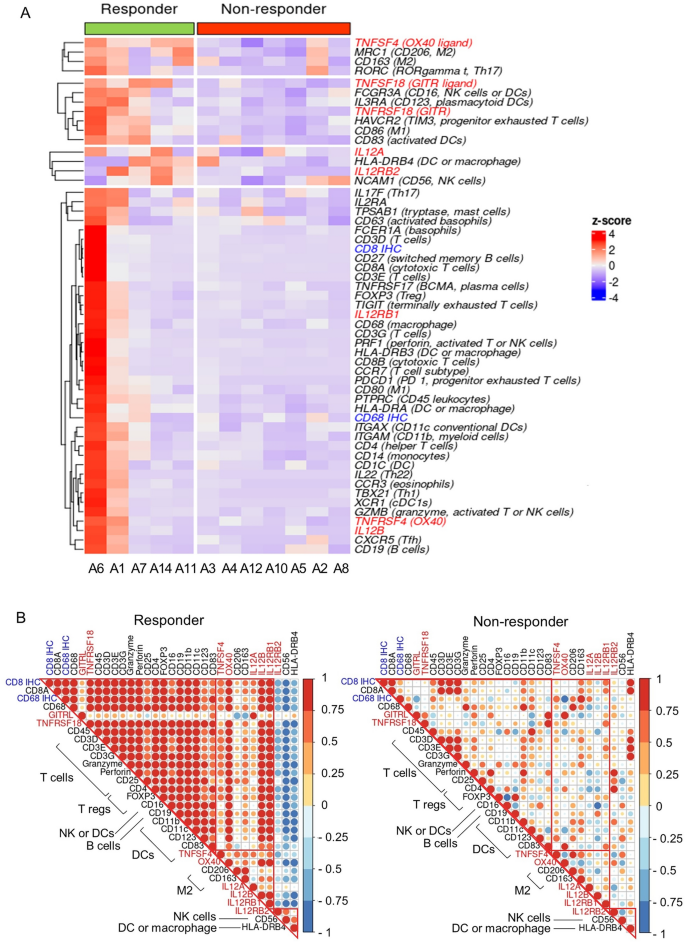
实验所用关键产品:无额外实验产品,基于NanoString基因表达数据与免疫组化结果进行生物信息学分析。
3.6 Transwell迁移实验验证候选基因对NK细胞迁移的影响
实验目的为验证候选基因表达对NK细胞向肿瘤细胞迁移的调控作用,解析其促进NK细胞治疗反应的功能机制。方法细节上,采用Transwell小室(8μm孔径)构建体外迁移模型,下室接种U87MG胶质母细胞瘤细胞或U87MG+T细胞,上室接种CFSE标记的NK细胞;使用特异性抗体阻断T细胞上的TNFSF4、TNFRSF18、IL12RB2表达,培养8h后通过细胞计数仪统计迁移至下室的NK细胞比例;同时通过流式细胞术检测T细胞与U87MG细胞上三个候选基因的表达水平。结果解读显示,活化T细胞高表达三个候选基因,其中TNFSF4的阳性率为62.29%,TNFRSF18为63.49%,IL12RB2为69.59%;阻断T细胞上的TNFSF4表达后,NK细胞向肿瘤细胞的迁移比例显著降低至26.9%±2.0%(P=0.027),阻断TNFRSF18与IL12RB2后迁移比例分别为42.1%±9.6%(P=0.195)和37.8%±9.6%(P=0.146),提示三个基因尤其是TNFSF4可促进NK细胞向肿瘤微环境迁移,增强NK细胞的抗肿瘤作用。
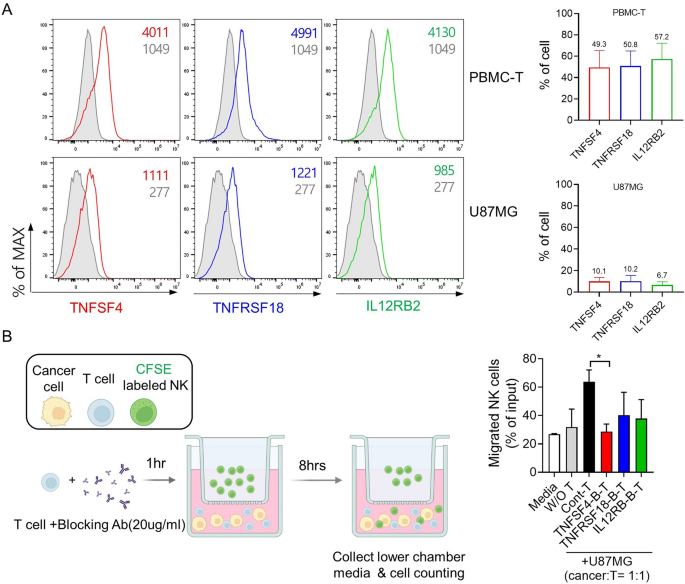
实验所用关键产品:抗TNFSF4-PE、抗TNFRSF18-PE、抗IL12RB2-PE抗体(BioLegend,San Diego,CA,USA)、CytoFLEX流式细胞仪(Beckman Coulter,Brea,CA,USA)、Transwell小室(SPL life science,Pocheon,Korea)、CFSE(Thermo Fisher Scientific,Waltham,USA)、阻断抗体(R&D Systems,Minneapolis,MN,USA)。
4. Biomarker研究及发现成果解析
本研究通过系统的筛选与验证流程,鉴定出TNFRSF18、TNFSF4、IL12RB2三个可预测复发性GBM患者对AKC治疗反应性的生物标志物,明确了其筛选逻辑、验证方法及功能机制,为复发性GBM的精准NK细胞治疗提供了关键的生物标志物工具。
Biomarker定位方面,三个基因均属于TNF超家族成员,筛选逻辑为:首先通过NanoString nCounter免疫基因表达谱分析对比应答者与非应答者的基因表达差异,然后通过三步筛选流程(AUC≥0.85、生存分析P<0.05、随机森林模型)确定候选基因,最后通过qRT-PCR、免疫组化、Transwell迁移实验进行验证与功能解析。研究过程详述显示,Biomarker来源于复发性GBM患者治疗前的肿瘤组织样本,验证方法包括转录组分析、定量PCR、免疫组化及功能细胞实验;特异性与敏感性方面,三个基因联合的随机森林模型预测准确率为100%(95% CI 73.5-100%),逻辑回归模型的预测准确率同样为100%(95% CI 73.54-100%),可精准区分应答者与非应答者;CD8⁺细胞密度的ROC曲线AUC为0.91,具有较高的预测价值。核心成果提炼显示,三个基因可作为复发性GBM患者对AKC治疗反应性的有效预测生物标志物,高表达患者的PFS与OS均显著优于低表达患者(所有关联分析P<0.05);创新性在于首次发现这三个基因联合可精准预测NK细胞治疗的反应性,且揭示其通过促进NK细胞向肿瘤微环境迁移、调节免疫细胞浸润发挥功能;统计学结果显示,TNFSF4在应答者中的表达显著高于非应答者(P=0.0014),三个基因的表达均与患者预后显著相关(P<0.05),研究样本量n=12(应答者n=5,非应答者n=7)。推测:未来可通过扩大样本量验证这些生物标志物的临床应用价值,同时基于这些基因开发靶向药物,进一步增强NK细胞治疗的疗效。
