1. 领域背景与文献引入
文献英文标题:Zinc ferrite nanoparticle-induced cytotoxicity and oxidative stress in different human cells;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:纳米毒理学、生物材料安全性评价
领域共识:磁性纳米颗粒自20世纪末起成为生物医学领域研究热点,2000年后磁铁矿(Fe₃O₄)纳米颗粒的磁共振成像(MRI)造影、肿瘤热疗应用技术逐渐成熟;2010年左右,尖晶石型铁氧体纳米颗粒(如锌铁氧体)因更优的磁性能被开发为新型MRI造影剂与自旋电子器件材料,但这类材料的生物安全性数据严重不足。当前研究热点集中在纳米颗粒的功能化修饰与临床应用转化,未解决的核心问题是多数铁氧体纳米颗粒的细胞毒性机制未明确,且缺乏不同组织来源细胞的毒性差异对比研究。本文针对锌铁氧体纳米颗粒在人类肺、皮肤、肝脏上皮细胞中的毒性效应空白,开展系统的细胞毒性与活性氧(ROS)介导机制研究,为其临床应用的安全性评估提供关键实验依据。
2. 文献综述解析
作者围绕磁性纳米颗粒的生物医学应用与安全性研究现状,按纳米颗粒类型及研究局限性的维度梳理领域进展。现有研究中,磁铁矿纳米颗粒的细胞毒性研究已证实其可通过活性氧诱导细胞凋亡,但尖晶石铁氧体纳米颗粒的研究多集中在镍、钴铁氧体,锌铁氧体的毒性数据仅见单一细胞系的初步报道,且未涉及多细胞模型的敏感性对比。现有研究的技术方法优势在于利用人类肿瘤细胞系开展高通量毒性筛选,可快速获取初步安全性数据,但局限性在于多数研究未系统解析毒性的分子机制,且缺乏对不同组织靶细胞的毒性差异分析。本文通过在三种人类上皮细胞系中同步开展细胞毒性、氧化应激及凋亡通路的多维度检测,填补了锌铁氧体纳米颗粒多细胞模型毒性机制研究的空白,明确了不同细胞的敏感性差异,为纳米材料的安全性评价提供了更全面的实验范式。
3. 研究思路总结与详细解析
本文以“锌铁氧体纳米颗粒的理化特性-细胞毒性效应-氧化应激介导机制-凋亡通路验证”为闭环研究逻辑,核心研究目标是明确锌铁氧体在不同人类上皮细胞中的毒性效应及分子机制,解决的科学问题是锌铁氧体是否通过活性氧依赖的线粒体凋亡通路诱导细胞死亡,技术路线涵盖纳米颗粒表征、细胞模型构建、多维度毒性指标检测及机制验证四个核心阶段。
3.1 锌铁氧体纳米颗粒表征
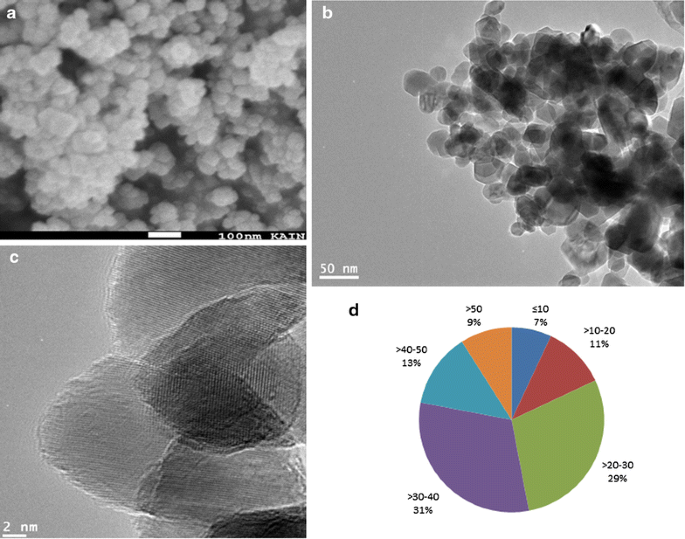
实验目的:明确锌铁氧体纳米颗粒的理化特性,为后续毒性实验提供基础参数;方法细节:采用场发射扫描电子显微镜(FESEM)、场发射透射电子显微镜(FETEM)观察颗粒形貌与晶体结构,通过动态光散射(DLS)检测其在去离子水及细胞培养基中的流体力学粒径与zeta电位,其中FETEM样品需制备为1mg/ml水悬液并超声分散15分钟;结果解读:FESEM与FETEM图像显示颗粒呈近球形,表面光滑,平均粒径为44.3nm(n=120,P<0.05),高分辨率TEM证实其晶体结构;DLS检测显示去离子水中流体力学粒径为312nm,培养基中为289nm,zeta电位分别为-18mV和-23mV,表明颗粒在培养基中易形成蛋白冠,分散性略优于水相;产品关联:实验所用关键产品:Sigma-Aldrich的锌铁氧体纳米颗粒(货号633844)、JEOL的场发射扫描电子显微镜(JSM-7600F)、场发射透射电子显微镜(JEM-2100F)、Malvern的纳米粒度电位分析仪(Nano-ZetaSizer-HT)。
3.2 细胞培养与纳米颗粒暴露处理
实验目的:构建标准化的细胞模型,实现纳米颗粒的可控暴露;方法细节:将A549(肺上皮)、A431(皮肤上皮)、HepG2(肝上皮)细胞培养于含10%胎牛血清的DMEM培养基中,在37℃、5%CO₂条件下培养至85%汇合度,用0.25%胰酶消化传代;将锌铁氧体纳米颗粒制备为1mg/ml的培养基悬液,超声分散15分钟后稀释为10、20、40μg/ml的工作浓度,细胞贴壁24小时后暴露于纳米颗粒,部分实验中细胞预先用10mM N-乙酰半胱氨酸(NAC)处理1小时;结果解读:三种细胞系在标准化培养条件下生长状态稳定,纳米颗粒悬液经超声处理后无明显团聚,可实现均匀的细胞暴露;产品关联:实验所用关键产品:ATCC的A549、A431、HepG2细胞系、Invitrogen的DMEM培养基与胎牛血清、Sigma-Aldrich的N-乙酰半胱氨酸(NAC)。
3.3 细胞毒性与细胞膜损伤检测
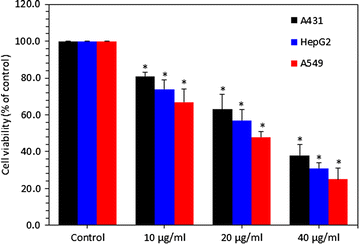
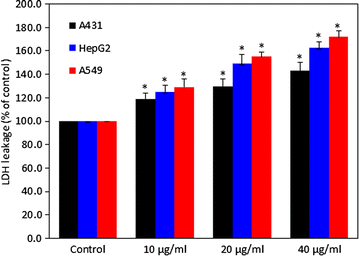
实验目的:评估锌铁氧体纳米颗粒对三种细胞的细胞毒性及细胞膜损伤程度;方法细节:采用MTT法检测细胞活力,将10000个细胞/孔接种于96孔板,暴露24小时后加入MTT溶液孵育3小时,溶解甲瓒产物后检测570nm吸光度;采用乳酸脱氢酶(LDH)漏出实验检测细胞膜损伤,收集培养上清后用试剂盒检测LDH活性;结果解读:MTT实验显示锌铁氧体以剂量依赖方式降低细胞活力,40μg/ml剂量下A549细胞活力降至25%(n=3,P<0.05),HepG2为31%(n=3,P<0.05),A431为38%(n=3,P<0.05);LDH实验显示40μg/ml剂量下A549细胞LDH漏出率达172%(n=3,P<0.05),HepG2为163%(n=3,P<0.05),A431为143%(n=3,P<0.05),表明A549细胞对锌铁氧体的敏感性最高;产品关联:实验所用关键产品:Sigma-Aldrich的MTT试剂、Bio-Vision的LDH细胞毒性检测试剂盒、BioTek的Synergy-HT酶标仪。
3.4 氧化应激指标测定
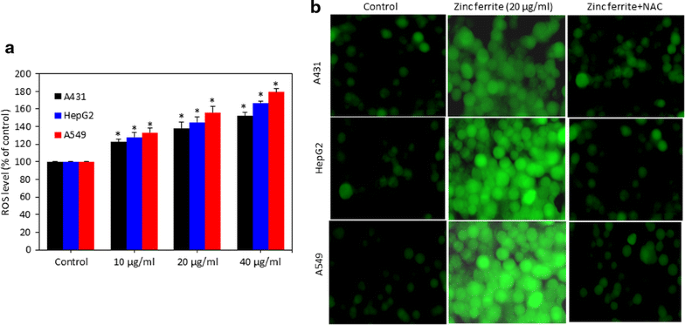
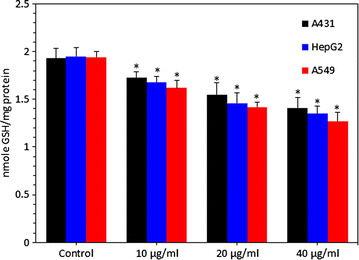
实验目的:验证锌铁氧体纳米颗粒是否诱导细胞氧化应激;方法细节:采用2",7"-二氯荧光素二乙酸酯(DCFH-DA)荧光法检测细胞内活性氧水平,分为酶标仪定量检测与荧光显微镜成像;采用Ellman法检测细胞内谷胱甘肽(GSH)含量,制备细胞裂解液后检测412nm吸光度;结果解读:活性氧水平随纳米颗粒剂量升高而显著增加,40μg/ml剂量下A549细胞活性氧水平为对照组的210%(n=3,P<0.05);谷胱甘肽水平呈剂量依赖降低,40μg/ml剂量下A549细胞谷胱甘肽含量降至对照组的42%(n=3,P<0.05),表明锌铁氧体诱导细胞内氧化-抗氧化系统失衡;产品关联:实验所用关键产品:Sigma-Aldrich的DCFH-DA与Ellman试剂、OLYMPUS的CKX41荧光显微镜。
3.5 线粒体功能与凋亡通路分析
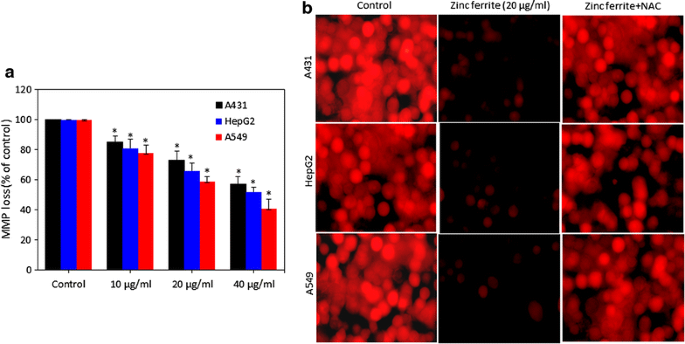
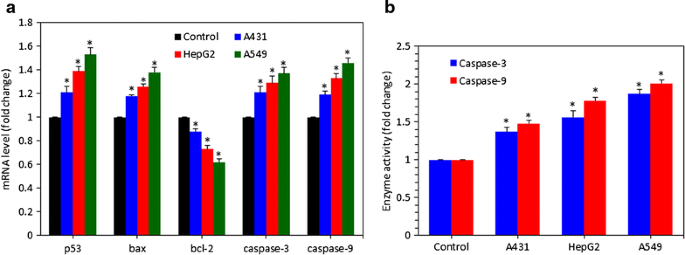
实验目的:解析锌铁氧体诱导细胞凋亡的分子通路;方法细节:采用罗丹明123(Rh123)荧光法检测线粒体膜电位(MMP),通过荧光显微镜与酶标仪定量分析;采用实时荧光定量PCR检测凋亡相关基因(p53、bax、bcl-2、caspase-3、caspase-9)的mRNA表达水平,以β-肌动蛋白为内参;采用试剂盒检测caspase-3与caspase-9的酶活性;结果解读:线粒体膜电位随纳米颗粒剂量升高而显著降低,20μg/ml剂量下A549细胞线粒体膜电位降至对照组的58%(n=3,P<0.05);实时PCR显示20μg/ml剂量下p53、bax、caspase-3、caspase-9的mRNA表达水平分别上调至对照组的2.3、2.7、3.1、2.9倍(n=3,P<0.05),bcl-2表达下调至对照组的45%(n=3,P<0.05);caspase-3与caspase-9酶活性分别升高至对照组的2.6、2.4倍(n=3,P<0.05),表明锌铁氧体通过线粒体依赖的内源性凋亡通路诱导细胞死亡;产品关联:实验所用关键产品:Sigma-Aldrich的罗丹明123、Qiagen的RNeasy RNA提取试剂盒与QuantiTect SYBR Green PCR试剂盒、Applied Biosystems的ABI PRISM 7900HT实时PCR系统、Bio-Vision的caspase活性检测试剂盒。
3.6 活性氧介导毒性机制验证
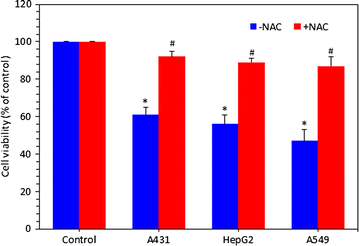
实验目的:确认活性氧是锌铁氧体诱导细胞毒性的关键介导因子;方法细节:细胞预先用10mM N-乙酰半胱氨酸(活性氧清除剂)处理1小时,再暴露于20μg/ml锌铁氧体纳米颗粒24小时,采用MTT法检测细胞活力;结果解读:N-乙酰半胱氨酸预处理可显著逆转锌铁氧体诱导的细胞活力下降,A549细胞活力从52%恢复至91%(n=3,P<0.05),HepG2从57%恢复至89%(n=3,P<0.05),A431从63%恢复至92%(n=3,P<0.05),表明活性氧生成是锌铁氧体诱导细胞毒性的核心机制;产品关联:实验所用关键产品:Sigma-Aldrich的N-乙酰半胱氨酸、Sigma-Aldrich的MTT试剂。
4. Biomarker研究及发现成果
本文涉及的Biomarker属于纳米毒理学领域的毒性效应Biomarker,涵盖氧化应激与凋亡通路相关分子,通过多维度检测明确了锌铁氧体纳米颗粒毒性的关键介导因子与效应分子。
Biomarker定位:包括氧化应激指标(活性氧、谷胱甘肽)、线粒体功能指标(线粒体膜电位)、凋亡相关基因(p53、bax、bcl-2、caspase-3、caspase-9)及酶活性,筛选逻辑为“细胞毒性初筛→氧化应激指标验证→凋亡通路分子确认→活性氧介导机制验证”的完整链条。研究过程详述:Biomarker来源为三种人类细胞系的细胞裂解液或培养上清,验证方法包括荧光定量检测、比色法、实时荧光定量PCR与酶活性检测;特异性与敏感性数据显示,活性氧在40μg/ml剂量下的诱导倍数在A549细胞中最高(2.1倍,n=3,P<0.05),谷胱甘肽的降低幅度也最为显著(58%,n=3,P<0.05),线粒体膜电位的下降率达42%(n=3,P<0.05);凋亡基因中bax/bcl-2比值在A549细胞中升高至6.0(n=3,P<0.05),远高于HepG2的4.3与A431的3.8。核心成果提炼:这些Biomarker共同证实锌铁氧体纳米颗粒通过活性氧介导的线粒体内源性凋亡通路诱导细胞毒性,其中A549细胞对该毒性效应的敏感性最高;创新性在于首次在三种人类上皮细胞系中系统解析锌铁氧体的毒性Biomarker谱,明确了不同组织来源细胞的毒性差异,为纳米材料的安全性评价提供了多维度Biomarker检测体系;统计学结果显示所有检测指标均具有显著差异(P<0.05),样本量均为3次独立重复实验。
