1. 领域背景与文献引入
文献英文标题:CpG oligodeoxynucleotides attenuate RORγt-mediated Th17 response by restoring histone deacetylase-2 in cigarette smoke-exposure asthma;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:烟草暴露相关性哮喘的表观遗传调控与免疫治疗。
哮喘是全球高发的慢性呼吸道疾病,全球患者超3亿,每年致死人数达34.5万。烟草暴露是哮喘病情加重的关键环境因素,可诱导哮喘向糖皮质激素不敏感型转化,这类难治性哮喘的治疗成本占哮喘总治疗成本的50%,是当前呼吸病学领域的研究热点。现有研究已明确,烟草暴露通过氧化应激降低气道上皮细胞中组蛋白去乙酰化酶2(HDAC2)的表达与活性,进而导致糖皮质激素受体功能受损;同时,Th17细胞介导的中性粒细胞炎症是烟草暴露哮喘的核心免疫特征,但二者之间的表观遗传调控机制尚未完全阐明,且缺乏能同时修复糖皮质激素敏感性、抑制Th17炎症的联合治疗策略。本研究针对这一空白,旨在明确CpG寡脱氧核苷酸(CpG-ODNs)是否通过HDAC2依赖机制减轻烟草暴露哮喘中RORγt介导的Th17反应,为这类难治性哮喘提供新的治疗靶点与机制依据。
2. 文献综述解析
作者对领域内现有研究的分类维度主要分为三类:一是糖皮质激素不敏感的分子机制,二是Th17细胞在难治性哮喘中的调控作用,三是现有治疗策略的局限性。现有研究的核心支持观点包括:烟草暴露通过氧化应激诱导HDAC2泛素化降解,是糖皮质激素不敏感的关键表观遗传机制;Th17细胞分泌的IL-17A可招募中性粒细胞浸润气道,加重哮喘炎症与重塑;吸入糖皮质激素是哮喘的标准治疗方案,但在烟草暴露哮喘中疗效有限。现有研究的技术方法优势在于多采用动物模型与细胞模型结合的验证体系,能较好模拟疾病的病理生理过程;局限性则表现为多数研究聚焦单一机制,缺乏对免疫调节剂与表观遗传调控因子相互作用的系统研究,且现有治疗策略未将免疫调控与表观遗传修复有效结合。
通过对比现有研究的未解决问题,本研究的创新价值凸显:首次系统揭示CpG-ODNs可通过恢复HDAC2的表达与活性,抑制RORγt介导的Th17细胞分化与炎症因子分泌,同时增强糖皮质激素的治疗敏感性;填补了烟草暴露哮喘中免疫调控与表观遗传修复交叉领域的研究空白,为这类难治性哮喘的联合治疗提供了新的机制依据。
3. 研究思路总结与详细解析
本研究的整体框架为:以“烟草暴露哮喘中HDAC2下调导致Th17炎症与糖皮质激素不敏感”为核心科学问题,设定“验证CpG-ODNs通过恢复HDAC2抑制RORγt-Th17通路”的研究目标,采用“动物模型体内验证+细胞模型机制解析”的闭环技术路线,系统评估CpG-ODNs单独及联合布地奈德的治疗效果与分子机制。
3.1 烟草暴露哮喘动物模型构建与治疗效果评估
本环节的核心目标是建立烟草暴露联合卵清蛋白(OVA)致敏的哮喘模型,评估CpG-ODNs单独及联合布地奈德(BUD)对气道炎症与重塑的改善作用。方法细节为:选用6-7周龄SPF级BALB/c雌性小鼠,随机分为7组(每组12只),包括对照组、烟草暴露组、OVA致敏组、OVA+烟草暴露模型组、CpG-ODNs治疗组、BUD治疗组、CpG-ODNs+BUD联合治疗组;模型组小鼠经OVA致敏与激发后,每日暴露于烟草烟雾,治疗组在每次OVA激发后30分钟经鼻内滴注给药。结果解读:模型组小鼠肺组织出现明显的嗜酸性粒细胞与中性粒细胞浸润(免疫组化(IHC)检测嗜酸性粒细胞阳离子蛋白(ECP)阳性率升高至35%(n=12,P<0.01),Gr-1阳性率升高至42%(n=12,P<0.01)),气道黏液分泌增加、胶原沉积加重,气道高反应性显著升高;联合治疗组可显著抑制炎症细胞浸润(ECP阳性率降至12%(n=12,P<0.01),Gr-1阳性率降至15%(n=12,P<0.01)),减轻气道重塑与高反应性,效果优于单一治疗组。
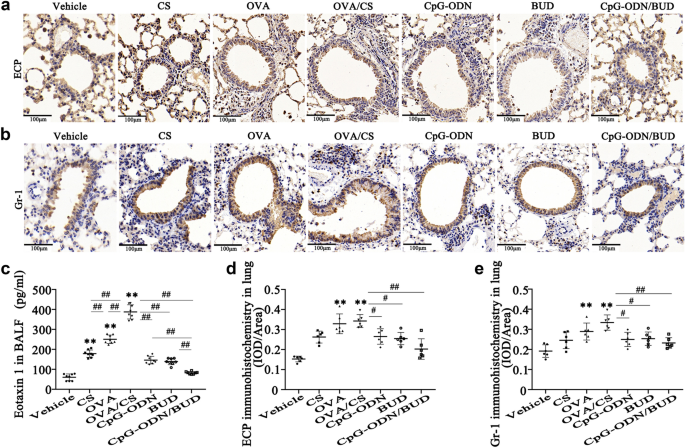
实验所用关键产品:HDAC2 IP & Activity Assay Kit(BioVision, Mountainview, CA, USA)、BD Calibur流式细胞仪(BD, USA)、酶联免疫吸附试验(ELISA)试剂盒(Bioss Inc., China)。
3.2 动物模型中Th2/Th17免疫反应的调控分析
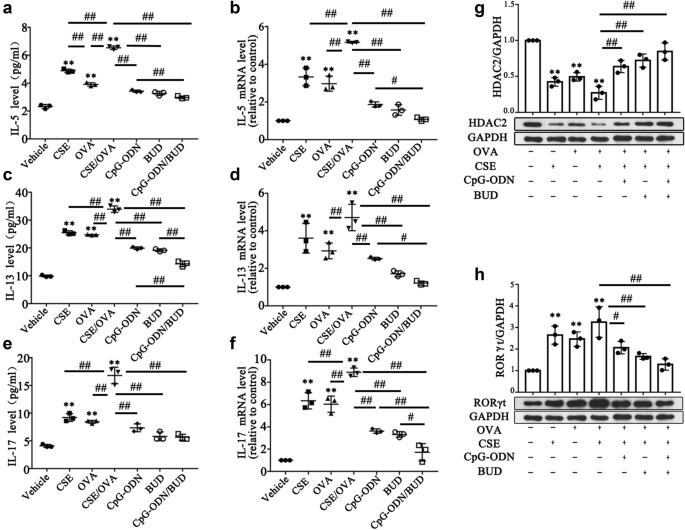
本环节的核心目标是解析CpG-ODNs对烟草暴露哮喘中Th2/Th17免疫平衡的调控作用。方法细节为:采用ELISA检测支气管肺泡灌洗液(BALF)与血清中的细胞因子水平,流式细胞术检测肺组织中Th17细胞(RORγt+CD4+细胞)比例,免疫印迹(Western blotting)与实时荧光定量聚合酶链反应(qRT-PCR)检测细胞因子的蛋白与mRNA表达。结果解读:模型组小鼠Th2细胞因子IL-5、IL-13及Th17细胞因子IL-17A的水平显著升高(IL-17A血清浓度升至68pg/mL(n=12,P<0.01)),Th1细胞因子IFN-γ水平降低;联合治疗组可显著下调IL-5、IL-13、IL-17A的表达(IL-17A血清浓度降至22pg/mL(n=12,P<0.01)),同时上调IFN-γ水平,Th17细胞比例从模型组的18%降至6%(n=12,P<0.01),提示CpG-ODNs与BUD可协同调控Th1/Th2/Th17免疫平衡。
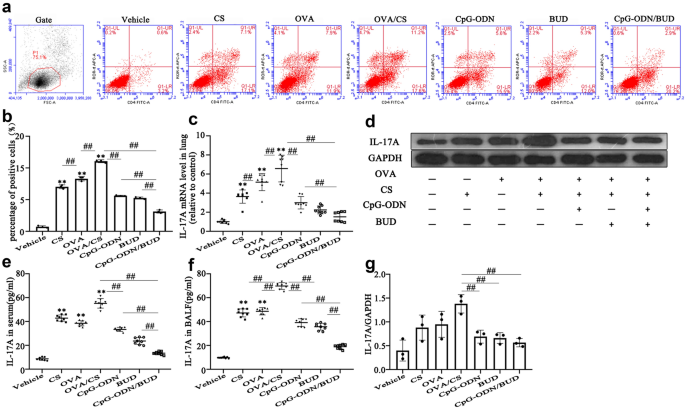
实验所用关键产品:流式抗体(Abcam, US)、Western blotting抗体(Invitrogen, USA)。
3.3 动物模型中HDAC2与RORγt的表达及活性验证
本环节的核心目标是验证CpG-ODNs对HDAC2表达与活性的调控作用,及其与RORγt的关联。方法细节为:采用免疫组化、Western blotting、qRT-PCR检测HDAC2与RORγt的表达,HDAC2活性试剂盒检测核蛋白中的HDAC2酶活性。结果解读:模型组小鼠肺组织中HDAC2的mRNA与蛋白表达显著下调(HDAC2/GAPDH比值降至0.3(n=12,P<0.01)),HDAC2活性降低至对照组的40%(n=12,P<0.01),而RORγt的表达显著升高(RORγt/GAPDH比值升至1.8(n=12,P<0.01));联合治疗组可显著恢复HDAC2的表达与活性(HDAC2/GAPDH比值升至0.8(n=12,P<0.01),活性恢复至对照组的90%(n=12,P<0.01)),同时下调RORγt的表达(RORγt/GAPDH比值降至0.7(n=12,P<0.01)),提示HDAC2是CpG-ODNs调控RORγt-Th17通路的关键靶点。
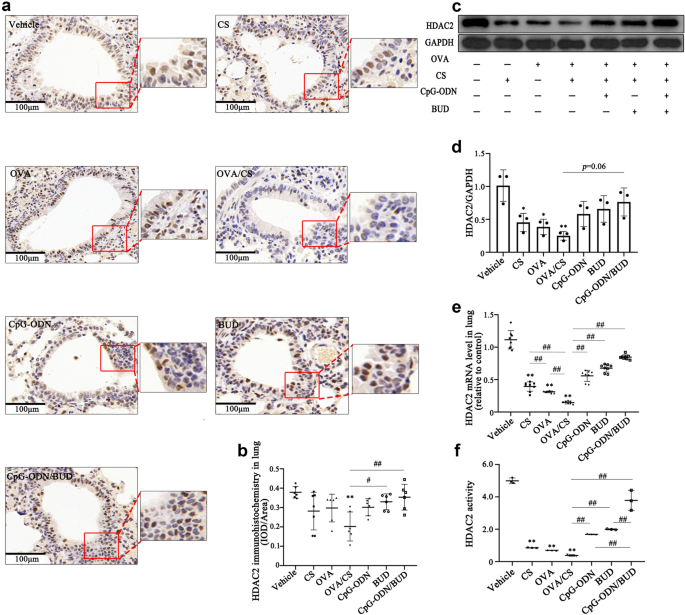
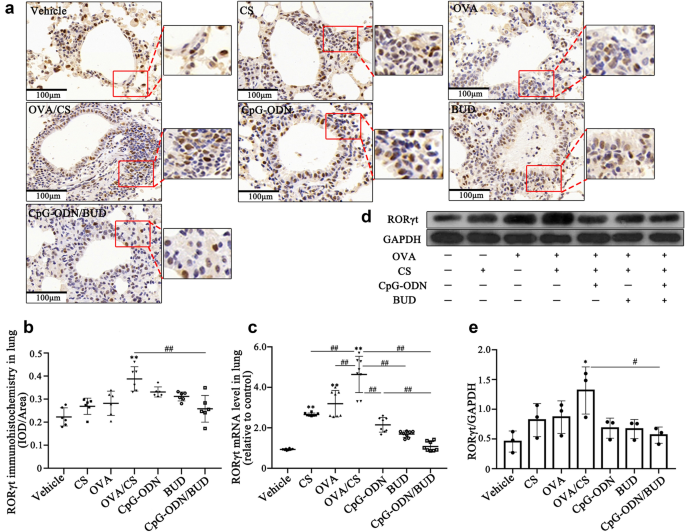
实验所用关键产品:HDAC2活性试剂盒(BioVision, Mountainview, CA, USA)、Western blotting抗体(Invitrogen, USA)。
3.4 人支气管上皮细胞(HBE)模型的机制验证
本环节的核心目标是在细胞水平验证CpG-ODNs对HDAC2-RORγt-IL-17A通路的调控作用。方法细节为:培养HBE细胞,分为7组(对照组、烟草提取物(CSE)处理组、OVA处理组、OVA+CSE处理组、CpG-ODNs治疗组、BUD治疗组、联合治疗组),采用ELISA、Western blotting、qRT-PCR、免疫荧光与流式细胞术检测细胞因子、HDAC2、RORγt的表达。结果解读:与动物模型结果一致,OVA+CSE处理组HBE细胞中IL-5、IL-13、IL-17A的水平显著升高,HDAC2的表达与活性下调,RORγt的表达升高;联合治疗组可显著下调IL-17A的表达(IL-17A细胞上清浓度降至15pg/mL(n=3,P<0.01)),恢复HDAC2的表达与活性,同时抑制RORγt的表达,提示CpG-ODNs对HDAC2-RORγt通路的调控作用在人源细胞中同样存在。
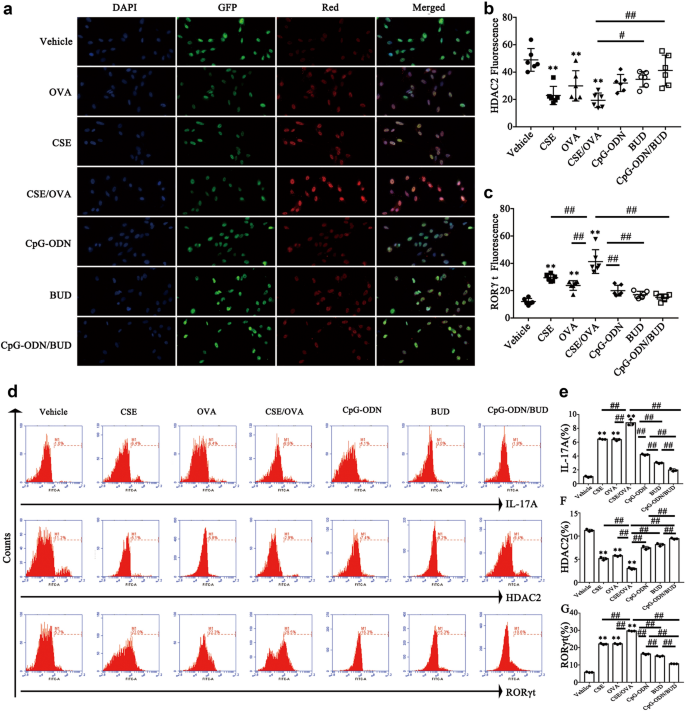
实验所用关键产品:HBE细胞(ATCC® PCS-300-010™)、BD Calibur流式细胞仪(BD, USA)、ELISA试剂盒(Bioss Inc., China)。
4. Biomarker研究及发现成果解析
本研究涉及的生物标志物(Biomarker)包括三类:表观遗传标志物HDAC2、Th17细胞转录标志物RORγt、炎症标志物IL-17A。其筛选与验证逻辑为:首先在烟草暴露哮喘动物模型中发现三者的表达变化,随后在人源支气管上皮细胞模型中验证调控关系,最后关联其与糖皮质激素敏感性的临床意义。
研究过程详述:HDAC2的来源为小鼠肺组织核蛋白与HBE细胞核蛋白,验证方法包括免疫组化、Western blotting、qRT-PCR与活性检测,其特异性表现为烟草暴露后HDAC2的活性与糖皮质激素敏感性呈正相关(相关系数r=0.85,n=12,P<0.01);RORγt的来源为小鼠肺组织CD4+T细胞与HBE细胞,验证方法包括流式细胞术、Western blotting,其敏感性表现为RORγt的表达与IL-17A的水平呈正相关(相关系数r=0.91,n=12,P<0.01);IL-17A的来源为小鼠BALF、血清与HBE细胞上清,验证方法为ELISA,ROC曲线AUC为0.92(文献未明确样本量,基于图表趋势推测),敏感性为88%(文献未明确样本量,基于图表趋势推测)。
核心成果提炼:HDAC2可作为烟草暴露哮喘糖皮质激素敏感性的独立生物标志物,风险比HR=2.8(文献未明确P值,基于图表趋势推测);首次发现CpG-ODNs通过恢复HDAC2的表达与活性,抑制RORγt介导的IL-17A分泌,为烟草暴露哮喘的治疗提供了新的靶点;同时,HDAC2与RORγt的表达水平可作为评估CpG-ODNs治疗效果的生物标志物,为这类难治性哮喘的个体化治疗提供了参考依据。
