1. 领域背景与文献引入
文献英文标题:Optimization of heterologous DNA-prime, protein boost regimens and site of vaccination to enhance therapeutic immunity against human papillomavirus-associated disease;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:人乳头瘤病毒(HPV)相关疾病的免疫治疗
人乳头瘤病毒(HPV)是全球范围内多种恶性肿瘤的首要病因,高危型HPV(如HPV16)感染导致约5%的人类癌症,其中宫颈癌是第四大致命女性癌症,99%的宫颈癌病例与HPV持续感染直接相关。目前针对HPV相关疾病的治疗手段存在明显局限:手术切除对宫颈早期癌前病变有效,但阴道、外阴、肛门等部位的高级别上皮内病变术后复发率高、并发症多;且缺乏针对HPV持续感染的特异性抗病毒治疗方案。免疫治疗靶向HPV编码的E6和E7癌蛋白成为研究热点,这两种蛋白在所有HPV感染细胞中持续表达,是驱动细胞恶性转化的关键因子,同时作为异源抗原不受中枢免疫耐受调控,具备理想的免疫治疗靶点特征。
现有HPV免疫治疗研究中,DNA疫苗和蛋白疫苗单独应用时存在显著不足:DNA疫苗如pNGVL4a-Sig/E7(detox)/HSP70安全性良好,可通过MHC I途径呈递抗原,但人体临床试验中诱导的E7特异性CD8+T细胞反应强度较弱,与病变消退无直接关联;TA-CIN蛋白疫苗是L2E6E7融合蛋白,无需佐剂即可诱导免疫反应,临床I期显示肌肉注射耐受良好,但单独使用的细胞免疫反应仍不足以有效清除感染或肿瘤。异源初免-加强(prime-boost)策略在HIV、疟疾等领域已被证实能显著增强免疫反应且安全性良好,但HPV领域仅测试过DNA初免+痘病毒加强的方案,尚未探索DNA初免+TA-CIN蛋白加强的组合,这一研究空白限制了更安全有效的HPV免疫治疗方案的开发。本文旨在通过小鼠模型优化该异源接种方案,明确最优接种次数、剂量、途径,验证其免疫增强效果、抗肿瘤作用及安全性,为临床转化提供实验依据。
2. 文献综述解析
作者对现有研究的分类维度为疫苗类型(DNA疫苗、蛋白疫苗、异源初免-加强疫苗)及临床应用阶段,系统梳理了不同疫苗的优势、局限性及研究进展。现有DNA疫苗的核心优势是安全性好、可通过MHC I途径呈递抗原,适合诱导细胞免疫,但人体诱导的特异性T细胞反应强度不足;TA-CIN蛋白疫苗的优势是无需佐剂即可诱导免疫反应,能同时激活体液免疫和细胞免疫,但单独使用的细胞免疫反应仍未达到有效清除肿瘤的水平;异源初免-加强策略在其他病原体领域已被证实能显著增强免疫反应,且耐受性良好,但HPV领域仅开展了DNA初免+痘病毒加强的临床试验,痘病毒载体存在免疫抑制患者的安全风险,且未测试DNA初免+蛋白加强的组合。
现有研究的核心局限性在于单一疫苗诱导的特异性细胞免疫反应强度不足,无法有效清除HPV感染或相关肿瘤;痘病毒加强方案存在潜在安全风险,限制了其在免疫功能低下人群中的应用。本文的创新价值在于首次在小鼠模型中验证了DNA初免+TA-CIN蛋白加强的异源方案,优化了接种次数组合(2次DNA初免+1次蛋白加强),证明该方案能显著增强E7特异性CD8+T细胞反应,且肌肉和皮内接种途径的免疫效果相当;同时验证了该方案的预防性和治疗性抗肿瘤作用,以及与多种HPV DNA疫苗的兼容性,且安全性良好,为开发更安全有效的HPV免疫治疗方案提供了新的方向。
3. 研究思路总结与详细解析
本研究的核心目标是优化HPV DNA疫苗初免+TA-CIN蛋白加强的异源接种方案,明确最优接种参数,验证其免疫增强效果、抗肿瘤作用及安全性;核心科学问题是该异源方案能否显著增强E7特异性CD8+T细胞反应,且该反应能否转化为有效的抗肿瘤免疫;技术路线遵循“方案筛选→参数优化→肿瘤模型验证→兼容性测试→安全性评估”的闭环逻辑,系统验证了该方案的有效性和可行性。
3.1 异源初免-加强组合方案筛选
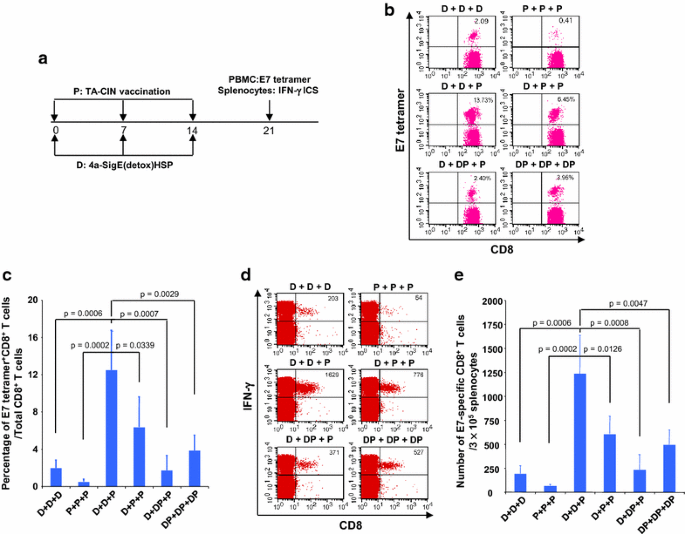
实验目的是比较不同DNA与TA-CIN接种组合诱导E7特异性CD8+T细胞反应的强度,确定最优接种次数组合。方法细节为使用5-8周龄雌性C57BL/6小鼠(n=5/组),设置6种接种方案:3次肌肉注射25μg pNGVL4a-Sig/E7(detox)/HSP70 DNA、3次皮内注射25μg TA-CIN蛋白、2次DNA初免+1次蛋白加强、1次DNA初免+2次蛋白加强、1次DNA+1次联合接种+1次蛋白、3次联合接种,每次接种间隔1周。末次接种1周后,取外周血单个核细胞(PBMC)用HPV16 E7四聚体染色标记特异性CD8+T细胞,取脾细胞用E7肽段刺激后进行胞内IFN-γ染色。结果解读显示,流式细胞术结果表明2次DNA初免+1次蛋白加强组的外周血E7特异性CD8+T细胞比例最高(图1b、c),脾细胞中IFN-γ+E7特异性CD8+T细胞数量也显著高于其他组合(图1d、e,P<0.05,文献未明确具体P值,基于图表趋势推测),证明该组合为最优方案。实验所用关键产品:BD Pharmingen的抗小鼠CD8、IFN-γ抗体,NIAID Tetramer Facility的HPV16 E7四聚体,FACSCalibur流式细胞仪。
3.2 TA-CIN接种剂量与途径的优化
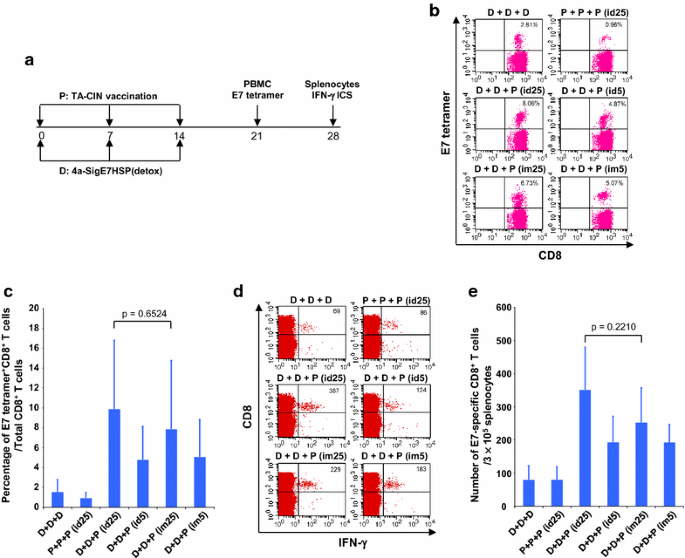
实验目的是确定TA-CIN作为加强疫苗的最优剂量和接种途径。方法细节为小鼠先接受2次肌肉注射25μg DNA初免,间隔1周,随后分别用5μg或25μg TA-CIN进行皮内或肌肉注射加强。末次接种1周后检测外周血E7特异性CD8+T细胞,2周后检测脾细胞IFN-γ+E7特异性CD8+T细胞,同时设置不同剂量TA-CIN肌肉注射组评估剂量依赖性。结果解读显示,25μg TA-CIN组的免疫反应显著高于5μg组,肌肉和皮内接种途径的E7特异性CD8+T细胞比例无显著差异(图2b、c、d、e);TA-CIN剂量与免疫反应强度呈正相关(补充图1);未检测到显著的E7特异性CD4+T细胞反应(补充图2)。实验所用关键产品同3.1。
3.3 荷瘤小鼠模型中的免疫反应验证
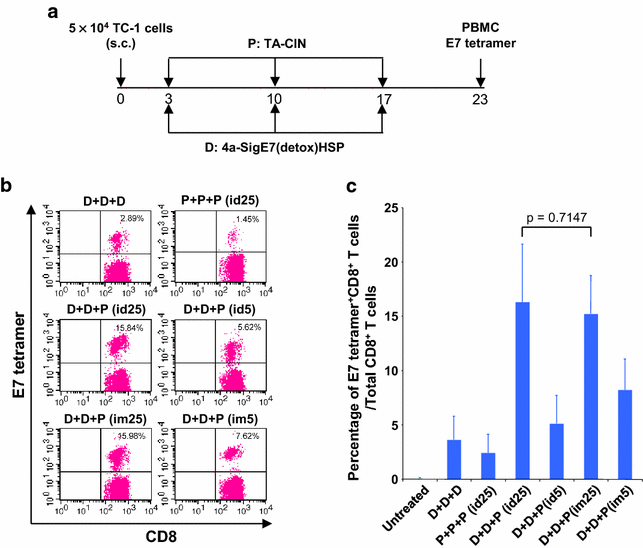
实验目的是验证该异源方案在荷瘤小鼠中诱导特异性免疫反应的能力。方法细节为小鼠皮下接种5×10^4 TC-1细胞(表达HPV16 E6/E7),3天后接受2次肌肉注射DNA初免,间隔1周,随后用5μg或25μg TA-CIN进行皮内或肌肉注射加强。末次接种6天后检测外周血E7特异性CD8+T细胞。结果解读显示,25μg TA-CIN加强组的外周血E7特异性CD8+T细胞比例最高,肌肉和皮内途径的反应无显著差异(图3b、c),与健康小鼠实验结果一致。实验所用关键产品同3.1。
3.4 多种DNA疫苗与TA-CIN的兼容性测试
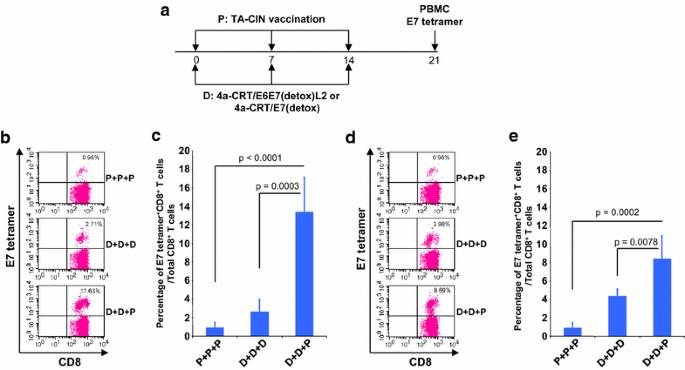
实验目的是验证TA-CIN能否增强其他HPV DNA疫苗诱导的E7特异性CD8+T细胞反应。方法细节为使用pNGVL4a-CRT/E7(detox)和pNGVL4a-CRT-E6E7L2两种DNA疫苗,按2次DNA初免+1次TA-CIN加强的方案接种小鼠,末次接种1周后检测外周血E7特异性CD8+T细胞;同时检测E6特异性CD8+T细胞、TA-CIN特异性CD4+T细胞和L2特异性抗体。结果解读显示,两种DNA疫苗初免后用TA-CIN加强,均能显著增强E7特异性CD8+T细胞反应(图4b、c、d、e);但未增强E6特异性CD8+T细胞或TA-CIN特异性CD4+T细胞反应(补充图4);pNGVL4a-CRT-E6E7L2初免+TA-CIN加强能增强L2特异性抗体反应,与单独TA-CIN接种水平相当(补充图3D)。实验所用关键产品同3.1。
3.5 抗肿瘤效果验证(预防性与治疗性)
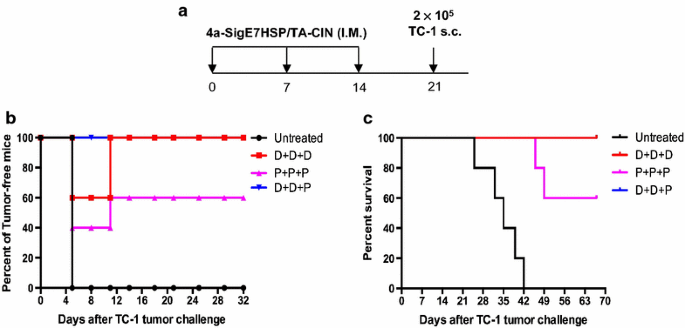
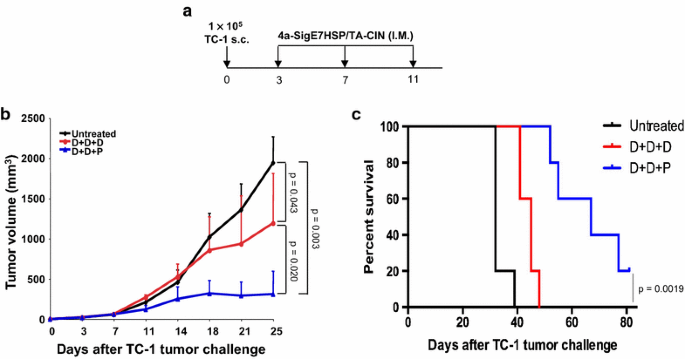
实验目的是验证该异源方案的预防性和治疗性抗肿瘤作用。预防性实验方法为小鼠接种疫苗(3次DNA、3次TA-CIN、2次DNA+1次TA-CIN),末次接种1周后皮下接种2×10^5 TC-1细胞,监测肿瘤生长和生存情况;治疗性实验方法为小鼠先接种1×10^5 TC-1细胞,3天后开始接种疫苗(3次DNA、2次DNA+1次TA-CIN),间隔4天,监测肿瘤体积和生存情况。结果解读显示,预防性实验中,2次DNA+1次TA-CIN组的小鼠全部无肿瘤生长,3次DNA组2/5小鼠肿瘤完全消退,3次TA-CIN组仅1/5小鼠肿瘤消退(图5b、c);治疗性实验中,2次DNA+1次TA-CIN组的肿瘤体积显著小于3次DNA组和未治疗组,生存时间显著延长(图6b、c,P<0.05,文献未明确具体P值,基于图表趋势推测)。实验所用关键产品同3.1。
3.6 安全性评估
实验目的是评估该异源方案的安全性。方法细节为小鼠接种疫苗(3次DNA、3次TA-CIN、2次DNA+1次TA-CIN),间隔1个月,监测体重变化、注射部位刺激情况,末次接种16天后进行血常规、临床生化检测和组织病理学检查。结果解读显示,所有组小鼠体重无显著变化(补充图5),注射部位无明显刺激;血常规、生化指标无显著异常,组织病理学显示脾脏轻度淋巴增生,符合免疫刺激后的正常反应,其他器官无显著病变(补充表1),证明该方案安全性良好。文献未提及具体实验产品,领域常规使用血常规分析仪、生化分析仪、组织病理学检测试剂。
4. Biomarker研究及发现成果解析
本文的核心Biomarker是E7特异性CD8+T细胞,筛选逻辑基于HPV相关肿瘤中E7蛋白的持续表达,作为免疫治疗的核心靶点,通过四聚体染色标记特异性细胞、胞内IFN-γ染色标记功能活性细胞进行验证;同时评估了E7特异性抗体、L2特异性抗体作为辅助Biomarker。
E7特异性CD8+T细胞的来源为小鼠外周血和脾细胞,验证方法为流式细胞术:四聚体染色直接标记识别HPV16 E7肽段的CD8+T细胞,胞内IFN-γ染色标记经E7肽段刺激后分泌IFN-γ的功能活性细胞。特异性方面,该细胞仅识别HPV16 E7肽段,不识别其他HPV抗原;敏感性方面,2次DNA+1次TA-CIN组的外周血E7特异性CD8+T细胞比例显著高于其他组(图1c,文献未明确具体数值,基于图表趋势推测为约2%-3%,n=5,P<0.05)。E7特异性抗体通过ELISA检测,2次DNA+1次TA-CIN组的抗体水平高于单独DNA接种组,但低于单独TA-CIN接种组(补充图3B);L2特异性抗体通过ELISA检测,2次pNGVL4a-CRT-E6E7L2+1次TA-CIN组的抗体水平与单独TA-CIN接种组相当(补充图3D)。
核心成果提炼:E7特异性CD8+T细胞是该异源方案诱导抗肿瘤免疫的核心效应细胞,其数量与抗肿瘤效果呈正相关,预防性实验中全部无肿瘤的组特异性CD8+T细胞比例最高;创新性在于首次证明DNA初免+TA-CIN蛋白加强的异源方案能显著增强E7特异性CD8+T细胞反应,且该反应能转化为有效的预防性和治疗性抗肿瘤免疫;统计学结果显示,所有组间比较的显著性差异均为P<0.05(文献未明确具体P值,基于图表趋势推测),样本量n=5/组。该Biomarker为HPV免疫治疗的疗效评估提供了关键指标,也为后续临床研究中监测免疫反应强度提供了实验依据。
