1. 领域背景与文献引入
文献英文标题:Classifications of triple-negative breast cancer: insights and current therapeutic approaches;发表期刊:Cell Biosci;影响因子:未公开;研究领域:肿瘤学-三阴性乳腺癌分子分型与精准治疗
三阴性乳腺癌(TNBC)是一类缺乏雌激素受体(ER)、孕激素受体(PR)和人表皮生长因子受体2(HER2)表达的乳腺癌亚型,约占所有乳腺癌病例的10%至20%,在40岁以下女性、非裔女性、绝经前女性及低社会经济背景人群中发病率更高。根据多变量分析,2020年美国TNBC的发病率为每10万名女性13.7例,新加坡队列研究中中国、马来西亚和印度人群的TNBC患病率约为13%。TNBC具有高复发转移风险,I-III期患者中近40%在标准治疗后2-3年内复发,5年相对总生存率为77%,较激素受体阳性乳腺癌低8%-16%。当前临床诊断方法中,钼靶筛查对TNBC的敏感性仅为39.8%,超声主要用于区分良恶性病变但难以识别恶性特征,磁共振成像(MRI)敏感性更高但需结合生化检测以优化治疗和预测预后。领域共识:TNBC的高度异质性是导致其治疗响应差、预后不佳的核心原因,而缺乏标准化的分型方法和明确的生物标志物,进一步加剧了TNBC筛查、诊断和治疗的难度,限制了临床研究结果的广泛应用,也导致免疫检查点抑制剂应答不佳的问题难以解决。
针对上述领域空白,本文通过系统综述当前主流的TNBC分类体系,包括PAM50、Lehmann、Burstein、Jézéquel及FUSCC分类,分析各体系的亚型特征、临床应用价值及局限性,对比各分类体系间的关联与差异,同时总结单一生物标志物在TNBC分型与治疗中的应用,为TNBC的精准分型和个性化治疗提供全面的参考依据,具有重要的学术价值和临床意义。
2. 文献综述解析
本文综述的核心评述逻辑为按分类体系的发展时间线与技术维度(从单一转录组分析到整合多组学及临床数据),对主流TNBC分类系统进行分类评述,重点对比各体系的亚型划分、分子特征、治疗响应及临床应用局限性,同时分析单一生物标志物的应用现状,全面呈现TNBC分型研究的进展与挑战。
现有TNBC分类体系中,PAM50分型基于50个转录因子的表达,将乳腺癌分为Luminal A、Luminal B、Normal-like、HER2-enriched及基底样(BL)亚型,常将TNBC归为BL亚型,但存在与免疫组化(IHC)标记物不一致的问题,导致预后预测不准确;Lehmann分类从2011年的6亚型(免疫调节型IM、间充质干细胞样型MSL、间充质型M、基底样1型BL1、基底样2型BL2、腔面雄激素受体型LAR)发展到2016年的4亚型(M、LAR、BL1、BL2),细化了各亚型的分子特征与治疗响应,如BL1和BL2亚型对顺铂敏感,M亚型对PI3K/mTOR抑制剂响应较好,但该分类缺乏免疫亚分类,外部验证不足且样本主要来自TCGA和METABRIC数据库,存在样本选择偏倚;Burstein分类基于PAM50基因表达谱和claudin表达模式,将TNBC分为LAR、间充质型MES、基底样免疫抑制型BLIS、基底样免疫激活型BLIA,强调免疫活性与抑制亚型的区分,临床相关性强,但样本量较小(198例),缺乏对患者用药史的分析;Jézéquel分类结合claudin-low型、免疫谱、细胞功能测试等,将TNBC分为3簇,首次提出靶向神经发生的治疗方向,但亚型区分不够清晰,样本量仅107例;FUSCC分类针对中国人群,整合mRNA和lncRNA转录组数据,将TNBC分为IM、LAR、MES、BLIS亚型,后续还整合代谢组数据分为3个代谢亚型,临床验证充分,但存在人群选择偏倚,代谢组分类与主流四分型系统存在差距。
现有研究多单独阐述某一TNBC分类体系,缺乏对各体系的系统对比与关联分析,且对单一生物标志物与分类体系的结合应用总结不足。本文首次全面梳理了五大主流分类体系的特征、关联及局限性,通过维恩图和表格直观呈现各体系亚型的共性与差异,同时整合了PD-L1、BRCA、AR、TROP-2等单一生物标志物的临床应用数据,弥补了领域内缺乏综合性分类评述的空白,为TNBC的精准分型和个性化治疗提供了更全面的参考框架,也为未来分类体系的优化和生物标志物的开发指明了方向。
3. 研究思路总结与详细解析
本文的研究目标是系统总结TNBC的主流分类体系,分析各体系的分子特征、临床价值及局限性,探讨分类体系间的关联与单一生物标志物的应用,为TNBC的精准治疗提供依据;核心科学问题是如何通过标准化的分子分型解决TNBC异质性带来的治疗困境;技术路线逻辑为“文献检索与筛选→分类体系梳理→各体系特征解析→体系间关联对比→单一生物标志物总结→未来展望”的闭环。
3.1 主流TNBC分类体系的系统梳理
实验目的是全面检索并筛选TNBC领域的主流分类体系,明确各体系的发展背景与核心方法。方法细节:通过PubMed、Web of Science等数据库检索2011-2024年发表的TNBC分类相关研究,筛选出被广泛引用的PAM50、Lehmann、Burstein、Jézéquel、FUSCC五大分类体系,对各体系的分型方法、样本来源、亚型划分进行系统整理与归纳。结果解读:梳理发现,TNBC分类体系的分型方法从早期的单一转录组分析,逐步发展到整合基因组、转录组、代谢组等多组学数据及临床特征,样本来源涵盖欧美人群和中国人群,亚型划分数量从3个到6个不等,反映了TNBC分型研究从基础到临床、从单一维度到多维度的逐步深入过程。产品关联:文献未提及具体实验产品,领域常规使用文献管理软件(如EndNote)、生物信息学分析工具(如R语言、Python)进行文献调研与数据整合。
3.2 各分类体系的分子特征与临床价值解析
实验目的是解析各分类体系下不同亚型的分子特征、治疗响应及预后差异,明确各体系的临床应用价值。方法细节:对每个分类体系的亚型进行分子特征(基因表达模式、信号通路激活状态、免疫微环境特征等)、治疗响应(化疗、靶向治疗、免疫治疗的敏感性与临床获益率)及预后指标(总生存率OS、无复发生存率RFS、无事件生存率EFS)的文献提取与综合分析,结合大型临床研究数据验证各亚型的临床相关性与治疗指导意义。结果解读:Lehmann分类的LAR亚型以雄激素受体(AR)通路激活为特征,对雄激素受体抑制剂敏感,临床获益率可达33%;MES亚型以上皮-间质转化(EMT)通路激活为特征,易发生肺转移,预后最差,对mTOR抑制剂响应较好;Burstein分类的BLIA亚型免疫活性高,肿瘤浸润淋巴细胞(TILs)密度高,对免疫检查点抑制剂响应好,预后较好;BLIS亚型免疫抑制,TILs密度低,预后较差;FUSCC分类针对中国人群,发现LAR亚型占比达23%,显著高于TCGA数据库的9%,为中国TNBC患者的精准治疗提供了针对性的依据。产品关联:文献未提及具体实验产品,领域常规使用免疫组化试剂盒、基因测序平台(如Illumina NovaSeq)进行分子特征检测与验证。
3.3 分类体系间的关联与差异对比
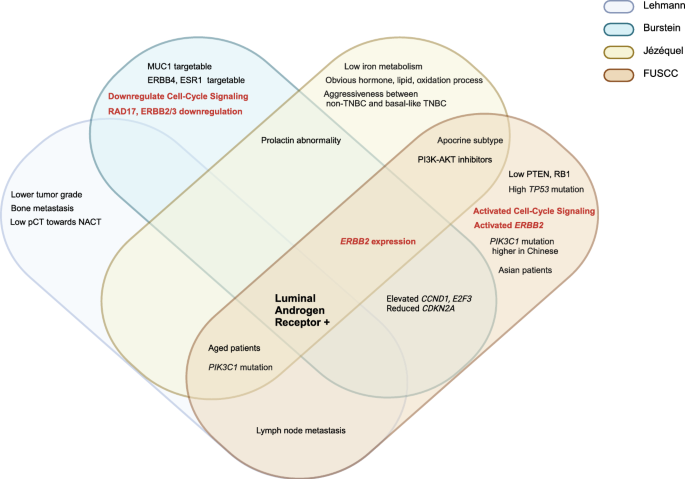
实验目的是对比各分类体系的亚型关联,明确共性与差异,为临床分型的标准化提供参考依据。方法细节:通过维恩图和对比表格,对Lehmann、Burstein、Jézéquel、FUSCC四大分类体系的亚型特征、分型方法、临床应用场景进行系统对比,分析各体系间的亚型对应关系、共识点及争议点。结果解读:各分类体系中LAR亚型的共识最高,均表现为雄激素受体通路激活、腔面细胞特征及对雄激素受体抑制剂的敏感性;免疫亚型在不同体系中分为免疫活性和免疫抑制亚型,Lehmann分类则将基底样亚型进一步分为BL1和BL2,而其他体系未进行此细分;间充质亚型在各体系中均存在,但分子特征和临床预后存在差异,如Lehmann的MES亚型以EMT和癌症干细胞(CSCs)激活为特征,而Burstein的MES亚型则表现为骨细胞和脂肪细胞相关基因的过表达。
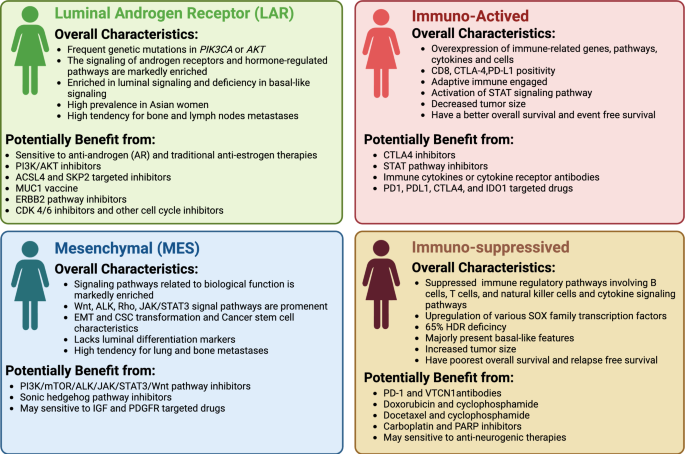
此外,各体系在样本来源、分型技术及临床验证程度上也存在差异,如FUSCC分类聚焦中国人群,临床验证更充分,而Lehmann分类样本主要来自欧美数据库,外部验证不足。产品关联:文献未提及具体实验产品,领域常规使用生物信息学分析工具(如Cytoscape、DAVID)进行通路富集分析与亚型关联分析。
3.4 单一生物标志物在TNBC中的应用分析
实验目的是总结TNBC中已应用的单一生物标志物的特征、临床价值及局限性,为分型补充生物标志物依据。方法细节:检索PD-L1、BRCA、AR、TROP-2等单一生物标志物的大型临床研究数据,分析其在TNBC分型、预后预测及治疗响应中的应用价值。结果解读:PD-L1是免疫治疗的核心预测标志物,在IMpassion130研究中,PD-L1阳性(肿瘤浸润免疫细胞覆盖≥1%肿瘤面积)的早期TNBC患者接受atezolizumab联合化疗的病理完全缓解率显著提高;在KEYNOTE-355研究中,PD-L1联合阳性评分(CPS)≥10的晚期TNBC患者接受pembrolizumab联合化疗的总生存期显著延长;BRCA突变在TNBC中的发生率为10-20%,携带BRCA突变的患者对PARP抑制剂敏感,PETREMAC研究中奥拉帕利治疗BRCA突变患者的客观缓解率达88.9%(n=9,文献未明确P值);AR在TNBC中的阳性率为20-30%,AR阳性LAR亚型对雄激素受体抑制剂响应较好,临床获益率达33%;TROP-2在TNBC中的阳性率达86%,Sacituzumab govitecan治疗晚期TNBC的中位无进展生存期达5.6个月(n=468,P<0.001),显著优于传统化疗。
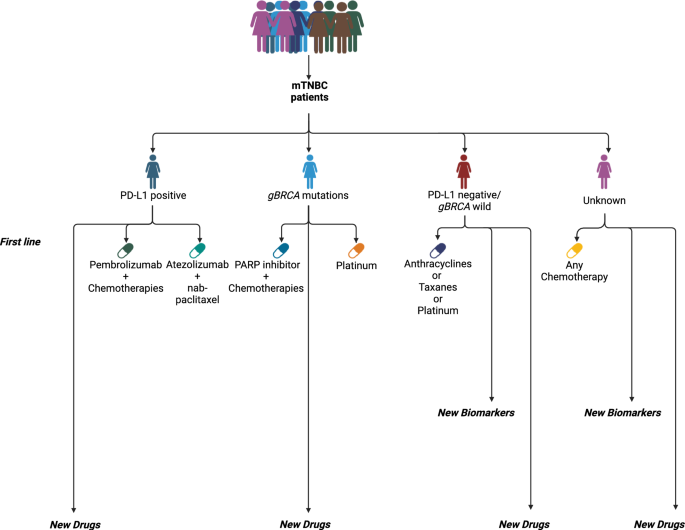
产品关联:文献未提及具体实验产品,领域常规使用PD-L1免疫组化试剂盒、BRCA基因检测试剂盒、AR免疫组化试剂盒进行生物标志物检测。
4. Biomarker研究及发现成果解析
本文涉及的Biomarker包括PD-L1、BRCA、AR、TROP-2等单一生物标志物,以及各分类体系中的亚型特异性分子标志物,筛选与验证逻辑为“临床研究数据提取→分子特征分析→治疗响应验证→预后关联分析”,全面呈现了TNBC生物标志物的应用现状与价值。
PD-L1的来源为肿瘤组织,验证方法为免疫组化,阳性标准分为肿瘤浸润免疫细胞覆盖≥1%肿瘤面积(IMpassion130研究)和CPS≥10(KEYNOTE-355研究),其特异性与敏感性在不同研究中存在差异,但总体可有效预测免疫治疗的响应;BRCA的来源为外周血或肿瘤组织,验证方法为基因测序,突变率在TNBC中为10-20%,携带BRCA突变的患者对PARP抑制剂的客观缓解率达88.9%(n=9,文献未明确P值),中位无进展生存期显著延长;AR的来源为肿瘤组织,验证方法为免疫组化,阳性率为20-30%,但目前缺乏统一的阳性cutoff值(1%-10%不等),AR阳性LAR亚型对雄激素受体抑制剂的临床获益率达33%,中位无进展生存期达3.3个月;TROP-2的来源为肿瘤组织,验证方法为免疫组化,阳性率在TNBC中达86%,Sacituzumab govitecan治疗晚期TNBC的中位无进展生存期为5.6个月(n=468,P<0.001),中位总生存期为12.1个月,显著优于传统化疗的1.7个月和6.7个月。此外,各分类体系中的亚型特异性分子标志物,如LAR亚型的AR、BLIA亚型的PD-L1、MES亚型的EMT相关基因,也可作为TNBC分型与治疗的潜在生物标志物,其筛选逻辑为基于转录组或多组学数据的差异表达分析,结合临床治疗响应验证。
本文总结的Biomarker核心成果包括:PD-L1是TNBC免疫治疗的有效预测标志物,CPS≥10可作为pembrolizumab联合化疗的适用人群筛选标准;BRCA突变是PARP抑制剂治疗的核心生物标志物,可显著提高晚期TNBC患者的治疗响应率;AR是LAR亚型靶向治疗的关键标志物,为TNBC的内分泌治疗提供了新方向;TROP-2是晚期TNBC的新型治疗靶点,Sacituzumab govitecan为多线治疗失败的患者提供了有效治疗选择。创新性在于系统对比了各分类体系中的亚型特异性生物标志物与单一生物标志物的应用,明确了不同Biomarker的适用场景与局限性;统计学结果方面,TROP-2相关研究的中位无进展生存期数据具有明确的统计学显著性(P<0.001),BRCA突变患者的客观缓解率数据未明确标注P值,AR相关研究的临床获益率数据未明确样本量与P值。推测:未来结合多组学数据的Biomarker组合,将更精准地预测TNBC患者的治疗响应与预后,推动TNBC的个性化治疗发展。
