1. 领域背景与文献引入
文献英文标题:Genetic labeling reveals spatial and cellular expression pattern of neuregulin 1 in mouse brain;发表期刊:Cell Bioscience;影响因子:未公开;研究领域:神经科学-神经精神疾病相关分子表达与神经回路研究
神经调节蛋白1(Nrg1)是一类关键的神经营养因子,其编码基因与精神分裂症、双相情感障碍、抑郁症等多种神经精神疾病的遗传易感性密切相关,同时在缺血性卒中、癫痫、阿尔茨海默病等神经系统疾病中具有明确的神经保护作用。Nrg1通过与ErbB家族受体结合激活下游信号通路,参与神经发育(如髓鞘形成、GABA能回路构建)、突触传递与可塑性(如GABA释放、长时程增强)等核心生理过程。领域共识:Nrg1的细胞内结构域还可与LIM激酶1、钠通道Nav1.1相互作用,分别调控谷氨酸能传递与神经元兴奋性。然而,现有研究对Nrg1在啮齿类动物脑中的细胞与回路水平表达模式尚未完全阐明,不同研究方法(如原位杂交、免疫组化)得到的结果存在争议,且缺乏对Nrg1阳性神经元轴突投射的系统解析,这极大限制了对其生理功能及相关疾病机制的深入研究。
针对这一核心研究空白,本研究利用CRISPR/Cas9技术构建Nrg1-Cre敲入小鼠,结合Cre报告系统与腺相关病毒(AAV)轴突追踪技术,系统解析了Nrg1在小鼠全脑不同区域的细胞类型特异性表达及轴突投射模式,为后续研究Nrg1的神经回路功能及相关疾病机制提供了关键基础数据。
2. 文献综述解析
作者对领域内现有研究的分类维度主要为研究方法(原位杂交、免疫组化、翻译核糖体亲和纯化(TRAP))及研究结论的争议点,重点围绕Nrg1的表达模式与功能研究展开评述。
现有研究已明确Nrg1与神经精神疾病的遗传关联,以及其ErbB信号通路在神经发育、突触可塑性中的核心作用;原位杂交技术可检测Nrg1 mRNA的分布,但对不同剪接体的特异性检测存在局限,且无法精准定位细胞类型;免疫组化技术能检测Nrg1蛋白表达,但结果易受抗体特异性影响;TRAP技术可富集正在翻译的Nrg1 mRNA,反映细胞的活性翻译状态,但无法实现空间定位。然而,现有研究存在明显局限性:不同研究对Nrg1在大脑皮层的表达层定位结果不一致,部分研究显示Nrg1在皮层5层表达,而另一些研究则显示在浅层表达;同时,现有研究未系统揭示Nrg1阳性神经元的轴突投射模式,无法从回路层面理解其功能。
本研究通过构建遗传标记的Nrg1报告小鼠,突破了传统方法的局限性,首次实现了在细胞和回路水平对Nrg1表达模式的精准解析。与原位杂交等方法相比,遗传标记技术能更精准地标记所有表达Nrg1的细胞,且可通过AAV追踪轴突投射,揭示Nrg1阳性神经元参与的神经回路;同时,本研究解决了之前研究中关于Nrg1表达定位的争议,明确了其在不同脑区的细胞类型特异性,为后续功能研究提供了可靠的基础。
3. 研究思路总结与详细解析
本研究的整体研究目标是系统解析Nrg1在小鼠脑中的空间与细胞表达模式及轴突投射回路;核心科学问题是明确Nrg1在不同脑区的细胞类型特异性分布,以及Nrg1阳性神经元的轴突投射路径;技术路线遵循“模型构建→验证→分脑区解析→回路追踪”的闭环逻辑:首先构建Nrg1-Cre敲入小鼠与报告小鼠模型,验证模型的特异性与可靠性,然后依次对嗅球、大脑皮层、纹状体、海马、下丘脑、丘脑、小脑等脑区的Nrg1表达模式进行解析,最后通过AAV轴突追踪技术揭示Nrg1阳性神经元的投射回路。
3.1 Nrg1-Cre敲入小鼠与报告小鼠的构建与验证
实验目的:构建能精准、特异性标记Nrg1阳性细胞的小鼠模型,确保标记结果能真实反映Nrg1的内源性表达。方法细节:利用CRISPR/Cas9基因编辑技术,在小鼠Nrg1基因的第9外显子终止密码子前插入P2A-Cre表达盒,构建Nrg1^{Cre/+}敲入小鼠;将Nrg1^{Cre/+}小鼠与Ai14(Rosa26^{LSL-tdTomato/+})报告小鼠杂交,获得Nrg1报告小鼠(Nrg1^{Cre/+}; Rosa26^{LSL-tdTomato/+}),其中tdTomato仅在Nrg1阳性细胞中表达;通过Southern blot验证基因插入的正确性,利用双荧光原位杂交(dFISH)检测tdTomato与Nrg1 mRNA的共定位,通过蛋白免疫印迹(Western blot)比较野生型与Nrg1报告小鼠纹状体中Nrg1蛋白的表达水平。结果解读:Southern blot结果显示,Spel酶切后靶向等位基因产生6.9kb片段,Ndel酶切后野生型与靶向等位基因分别产生5.5kb与6.6kb片段,证实P2A-Cre盒正确插入Nrg1基因座;dFISH结果显示,Nrg1报告小鼠伏隔核中94±1.2%的tdTomato阳性细胞同时表达Nrg1 mRNA,表明tdTomato能精准标记Nrg1阳性细胞;Western blot结果显示,野生型与Nrg1报告小鼠纹状体中Nrg1蛋白水平无显著差异(NS,n=3,非配对t检验),表明基因编辑未影响Nrg1的正常表达。
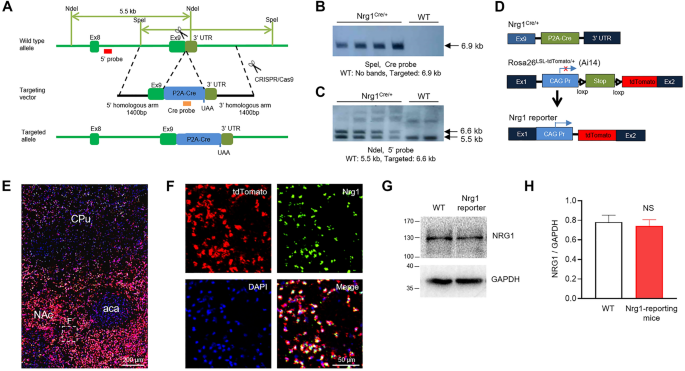
实验所用关键产品:RNAscope Multiplex Fluorescent Reagent Kit v2(Advanced Cell Diagnostics,Inc.)、抗NRG1抗体(Cell Signaling Technology,#2573)、抗GAPDH抗体(Arigo,ARG10112)、Cre报告AAV(Obio Technology (Shanghai) Corp., Ltd.)。
3.2 嗅球中Nrg1的表达模式分析
实验目的:解析Nrg1在嗅球中的细胞类型特异性分布及成年表达状态。方法细节:利用Nrg1报告小鼠,结合Gad67-GFP小鼠标记GABA能中间神经元,通过免疫荧光染色标记NeuN(泛神经元标记),采用无偏体视学方法计数嗅球不同层的Nrg1阳性细胞密度;为验证成年嗅球中Nrg1的表达,向2月龄Nrg1^{Cre/+}小鼠嗅球颗粒细胞层注射Cre报告AAV,4周后检测tdTomato表达。结果解读:嗅球中Nrg1阳性细胞主要分布在颗粒细胞层(GCL),占总Nrg1阳性细胞的73.4±2.3%,其次是mitral细胞层(ML)与肾小球层(GL),分别占23.6±3.0%与7.27±2.8%,而嗅神经层、外丛状层等区域几乎无Nrg1阳性细胞分布(P<0.0001,n=3,单因素ANOVA);共定位分析显示,Nrg1阳性细胞与Gad67-GFP共定位,表明其主要为GABA能中间神经元,包括肾小球周围(PG)细胞与颗粒细胞;AAV注射结果显示,成年小鼠嗅球颗粒细胞层能检测到tdTomato表达,证实Nrg1在成年嗅球中持续表达。
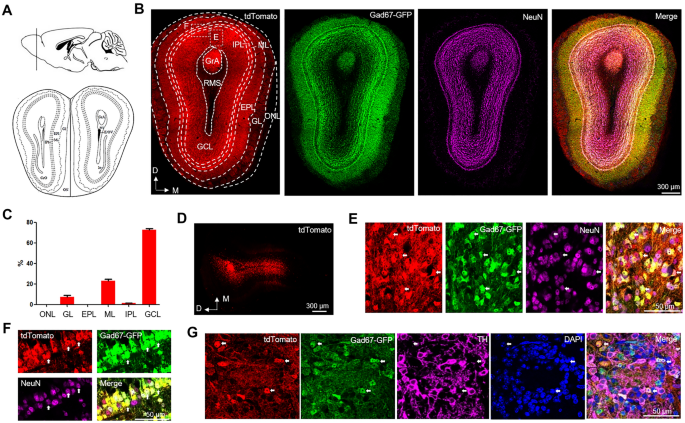
文献未提及具体实验产品,领域常规使用共聚焦显微镜、免疫组化(IHC)试剂、体视学分析软件等。
3.3 大脑皮层中Nrg1的表达模式分析
实验目的:解析Nrg1在大脑皮层不同区域的细胞类型特异性表达及层分布特征。方法细节:利用Nrg1报告小鼠,分析不同皮层区域(如听觉皮层、retrosplenial皮层、扣带回1区、初级体感皮层等)的Nrg1阳性细胞密度;通过免疫荧光染色标记NeuN、Neurogranin(NRGN,锥体神经元标记),结合Gad67-GFP小鼠标记GABA能中间神经元,明确Nrg1阳性细胞的类型。结果解读:大脑皮层中Nrg1阳性细胞密度在扣带回1区(Cg1)、retrosplenial皮层(RS)、梨状皮层(Pir)、听觉皮层(Au)显著高于初级运动皮层、初级体感皮层等区域(P<0.0001,n=3,单因素ANOVA);Nrg1阳性细胞主要分布在皮层浅层2-3层,占比显著高于深层(P<0.0001,n=3,双因素ANOVA);共定位分析显示,Nrg1阳性细胞与NeuN、NRGN共定位,表明其主要为浅层锥体神经元,几乎不与Gad67-GFP共定位,提示在皮层中Nrg1极少表达于GABA能中间神经元。

文献未提及具体实验产品,领域常规使用免疫组化(IHC)试剂、共聚焦显微镜等。
3.4 纹状体中Nrg1的表达模式与轴突投射分析
实验目的:解析Nrg1在纹状体的细胞类型特异性表达及轴突投射路径。方法细节:利用Nrg1报告小鼠结合Gad67-GFP小鼠标记中型多棘神经元(MSNs);向2月龄Nrg1^{Cre/+}小鼠伏隔核(NAc)注射Cre报告AAV,4周后检测轴突投射;通过双荧光原位杂交(dFISH)检测Nrg1与多巴胺D1受体(Drd1)mRNA的共定位,明确Nrg1阳性MSNs的通路类型。结果解读:纹状体中Nrg1阳性细胞主要分布在NAc壳区与嗅结节,而NAc核心区与尾状壳核(CPu)分布极少;共定位分析显示,所有Nrg1阳性细胞均与Gad67-GFP共定位,表明其为GABA能MSNs;AAV注射结果显示,NAc中的Nrg1阳性神经元轴突投射到黑质网状部(SNr);dFISH结果显示,大部分Nrg1阳性细胞表达Drd1 mRNA,表明其属于基底神经节的直接通路。
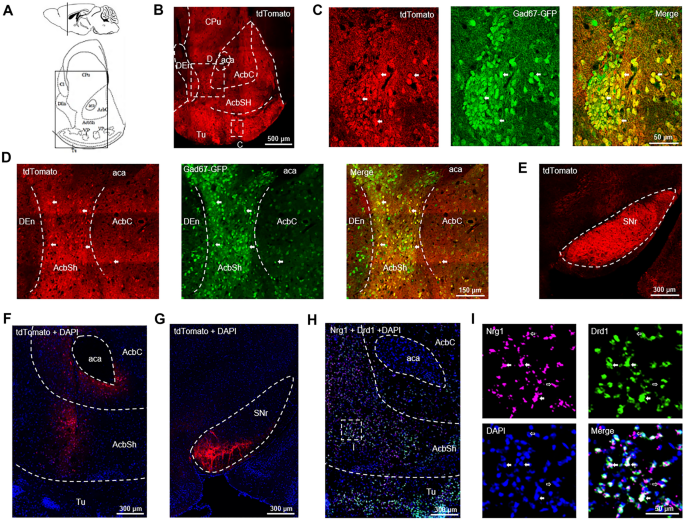
文献未提及具体实验产品,领域常规使用原位杂交试剂、立体定位注射系统、共聚焦显微镜等。
3.5 海马中Nrg1的表达模式与轴突投射分析
实验目的:解析Nrg1在海马的细胞类型特异性表达及轴突投射回路。方法细节:利用Nrg1报告小鼠,通过免疫荧光染色标记NeuN、GABA、GFAP(星形胶质细胞标记)、S100β(星形胶质细胞标记),明确Nrg1阳性细胞的类型;向2月龄Nrg1^{Cre/+}小鼠齿状回(DG)与下托(Sub)分别注射Cre报告AAV,4周后检测轴突投射;通过系列冠状切片分析Nrg1阳性神经元的投射路径。结果解读:海马中Nrg1阳性细胞主要分布在DG颗粒细胞层与下托,而CA1-3区分布极少(P<0.0001,n=6,单因素ANOVA);共定位分析显示,Nrg1阳性细胞与NeuN共定位,与GABA、GFAP、S100β无共定位,表明其主要为兴奋性神经元,且几乎不表达于星形胶质细胞;AAV注射结果显示,DG中的Nrg1阳性神经元轴突投射到CA3区的苔藓纤维,下托中的Nrg1阳性神经元轴突投射到retrosplenial颗粒皮层(RSG)与乳头体核(MM),参与Papez回路。
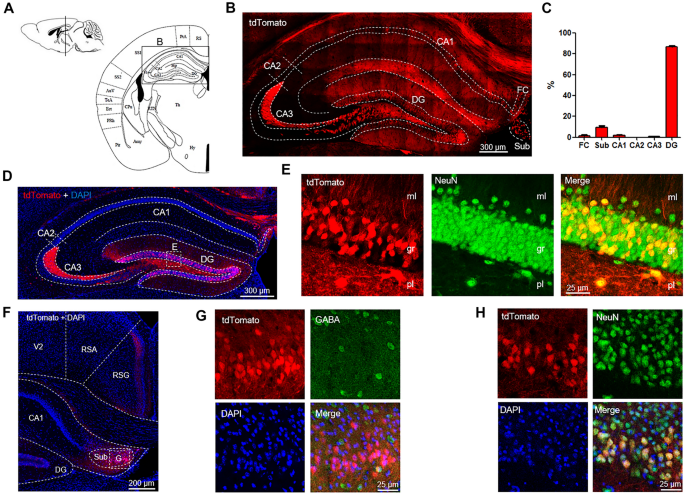
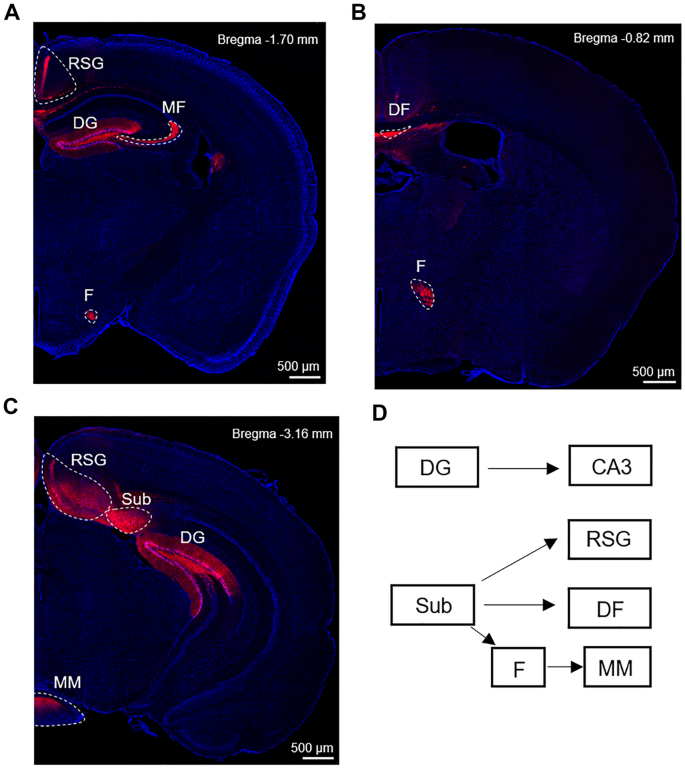
文献未提及具体实验产品,领域常规使用免疫组化(IHC)试剂、立体定位注射系统、共聚焦显微镜等。
3.6 下丘脑、丘脑与小脑的Nrg1表达模式分析
实验目的:解析Nrg1在丘脑、下丘脑与小脑的细胞类型特异性表达。方法细节:利用Nrg1报告小鼠结合Gad67-GFP小鼠,通过免疫荧光染色标记NeuN、GABA、Parvalbumin(PV,小脑浦肯野细胞标记),明确Nrg1阳性细胞的类型。结果解读:下丘脑Nrg1阳性细胞主要分布在腹内侧核(VM)、弓状核(ARC)、正中隆起(ME);VM中Nrg1阳性细胞与NeuN共定位,与Gad67-GFP无共定位,表明其为兴奋性神经元;ARC中约2/3的Nrg1阳性细胞与Gad67-GFP共定位,提示可能为AgRP神经元;ME中Nrg1阳性细胞几乎全为GABA能神经元;丘脑上丘(SC)中Nrg1阳性细胞主要为GABA能中间神经元;小脑Nrg1阳性细胞主要分布在浦肯野细胞层与分子层,与PV共定位,表明其主要为浦肯野细胞,同时在分子层的GABA能中间神经元中也有表达。
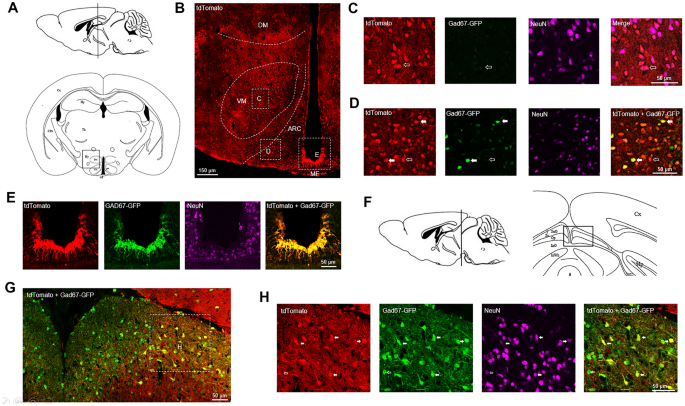
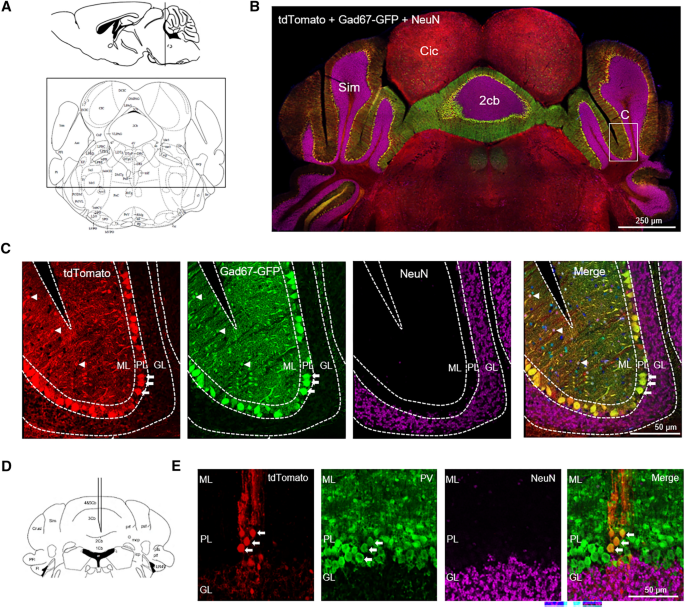
文献未提及具体实验产品,领域常规使用免疫组化(IHC)试剂、共聚焦显微镜等。
4. Biomarker研究及发现成果
本研究中,Nrg1作为神经精神疾病的易感基因,其细胞与回路水平的表达模式可作为潜在的疾病相关神经回路Biomarker,为神经精神疾病的机制研究与靶点开发提供新的方向。
Nrg1属于分子类Biomarker,其筛选与验证逻辑为:首先通过遗传标记技术构建报告小鼠,系统解析其在全脑的细胞类型特异性表达,然后通过AAV轴突追踪技术验证其神经回路投射,结合现有研究的疾病关联,明确其作为疾病相关回路Biomarker的价值。
Biomarker来源为小鼠脑组织,验证方法包括遗传标记小鼠的荧光成像、免疫荧光共定位、原位杂交、AAV轴突追踪等;特异性方面,Nrg1在不同脑区具有严格的细胞类型特异性,如皮层浅层锥体神经元、纹状体直接通路MSNs、海马DG与下托兴奋性神经元等;敏感性方面,遗传标记技术能精准标记所有表达Nrg1的细胞,tdTomato与Nrg1 mRNA的共定位率达94±1.2%(n=3)。
本研究明确了Nrg1在小鼠脑中的广泛但区域特异性的表达模式,主要表达于神经元,且在基底神经节直接通路、DG到CA3通路、Papez回路中高度富集;创新性在于首次通过遗传标记技术系统揭示了Nrg1的细胞与回路水平表达模式,解决了现有研究的争议;这些成果为后续研究Nrg1在神经精神疾病中的作用机制提供了关键基础,例如嗅球中Nrg1阳性GABA能中间神经元的ErbB4信号通路可能与精神分裂症患者的嗅觉障碍相关,纹状体直接通路的Nrg1表达异常可能导致运动与社交障碍;目前尚未开展临床样本验证,后续可进一步探索Nrg1表达模式在人类脑组织中的保守性,以及其作为疾病Biomarker的临床应用价值。
