1. 领域背景与文献引入
文献英文标题:RasG signaling is important for optimal folate chemotaxis in Dictyostelium;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:细胞生物学(盘基网柄菌趋化性与Ras信号通路调控)
细胞定向运动是多细胞生物胚胎发育、神经轴突导向及成体损伤修复等生理过程的核心基础,领域共识:盘基网柄菌(Dictyostelium discoideum)因生命周期依赖定向细胞运动,成为研究趋化信号调控的经典模式生物。在生长阶段,盘基网柄菌通过感知细菌释放的叶酸实现定向运动以捕获猎物;饥饿状态下则通过环腺苷酸(cAMP)信号介导细胞聚集形成多细胞结构。此前大量研究表明,Ras GTPase家族成员RasG和RasC是调控盘基网柄菌趋化性的关键分子,但近期有研究提出Ras信号对其叶酸趋化性无重要作用,这一结论与经典研究存在显著矛盾,导致领域内对Ras信号在趋化调控中的核心地位产生争议。本研究旨在通过系统对比不同实验条件,明确RasG在盘基网柄菌叶酸趋化性中的作用,并解析其功能关键区域,解决现有研究的结论冲突,为Ras亚型功能特异性的研究提供新的实验依据。
2. 文献综述解析
作者以实验方法学差异(细胞培养条件)和Ras蛋白亚型功能为核心维度,对领域内现有研究进行分类评述,梳理了Ras信号调控盘基网柄菌趋化性的研究进展与争议点。
现有研究主要分为两类,一类基于无血清(axenic)培养模型,证实RasG或RasG/RasC双敲除会导致盘基网柄菌叶酸趋化性完全丧失,明确了RasG在趋化信号通路中的核心调控作用,这类研究的优势是利用基因敲除模型精准定位分子功能,但局限性是未考虑细胞培养环境对生理状态的影响;另一类基于细菌共培养模型,提出Ras信号对叶酸趋化性无关键作用,这类研究的优势是模拟了盘基网柄菌的自然生长环境,但局限性是未控制趋化因子梯度强度对实验结果的干扰。两类研究因实验条件的差异得出矛盾结论,且均未深入解析RasG分子中参与趋化调控的具体结构域,导致领域内对Ras信号的作用机制缺乏统一认知。
本研究通过直接对比两种培养条件下的细胞趋化性,结合趋化源距离对梯度强度的影响,明确了RasG在不同环境下的功能需求,解决了现有研究的方法学缺陷;同时通过构建RasG与同源蛋白RasD的嵌合分子,首次发现RasG的非经典结构域(N端和C端保守区域)参与趋化调控,弥补了现有研究对Ras分子功能区域解析的不足,为理解Ras亚型的功能特异性提供了新的视角。
3. 研究思路总结与详细解析
本研究的整体研究目标是明确RasG在盘基网柄菌叶酸趋化性中的调控作用及分子基础,核心科学问题是解决不同研究中Ras信号作用的结论矛盾,技术路线遵循“矛盾溯源→变量控制→机制解析”的闭环逻辑:首先对比不同培养条件下的细胞趋化性,定位结论冲突的来源;然后排除同源蛋白代偿作用的干扰;接着分析趋化因子梯度强度对RasG需求的影响;最后通过嵌合蛋白实验解析RasG的功能关键区域。
3.1 不同培养条件下RasG对叶酸趋化性的调控作用
实验目的是验证细胞培养条件是否为导致现有研究结论矛盾的关键变量;方法细节为分别采用无血清培养基(axenic)和细菌共培养体系培养JH10野生型细胞、rasG-/rasC-双敲除细胞,将细胞接种于培养板后,用装载25mM叶酸的微量移液器置于细胞视野内,通过延时显微镜以30秒间隔捕获细胞运动轨迹,利用ImageJ软件的mTrackJ插件追踪细胞运动,计算趋化指数(细胞运动方向与趋化源方向夹角的余弦值);结果解读显示,rasG-/rasC-双敲除细胞在细菌培养条件下的平均趋化指数较无血清培养条件显著升高,平均差异为0.227(n=40,95% CI [0.092, 0.362],P<0.0001),但仍显著低于同期培养的野生型细胞,平均差异为-0.183(n=80,95% CI [-0.066, -0.3],P<0.001);而无血清培养的敲除细胞趋化指数几乎为0,与野生型细胞的平均差异为-0.336(n=80,95% CI [-0.219, -0.452],P<0.00001),说明RasG是盘基网柄菌最优叶酸趋化性所必需的,且培养条件会影响其功能需求。
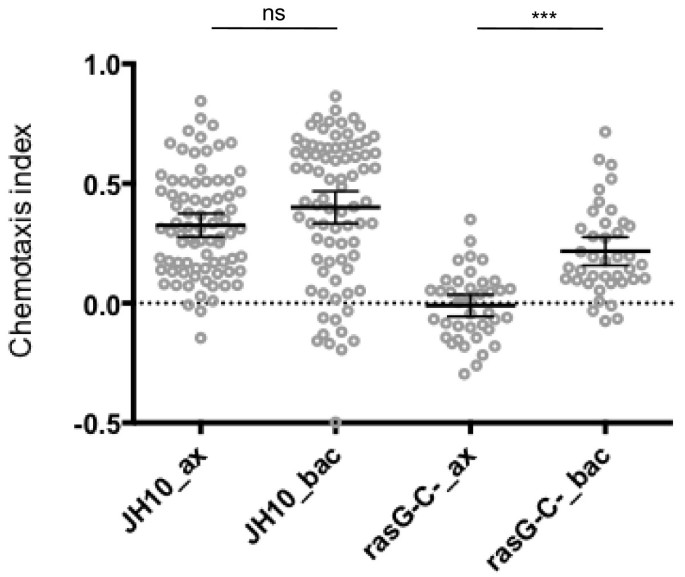
实验所用关键产品:Sigma的链霉素、氨苄青霉素、胸苷,Invitrogen的G418,ImageJ软件mTrackJ插件。
3.2 RasD代偿作用的排除验证
实验目的是明确细菌培养条件下敲除细胞趋化性部分恢复是否由同源RasD蛋白的上调表达介导;方法细节为收集不同培养条件下的细胞,提取总蛋白后进行十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(SDS-PAGE),通过免疫印迹(Western Blot)检测Ras蛋白的表达水平,其中采用泛Ras(Pan-Ras)抗体检测总Ras蛋白,特异性RasG、RasD抗体分别检测对应亚型的表达;结果解读显示,细菌培养的rasG-/rasC-细胞中RasD蛋白表达水平较无血清培养显著升高,但外源性表达RasD无法恢复敲除细胞的趋化缺陷,且未检测到新的Ras亚型表达,说明RasD的上调表达并非细菌培养细胞趋化性改善的原因,排除了同源蛋白代偿的可能。
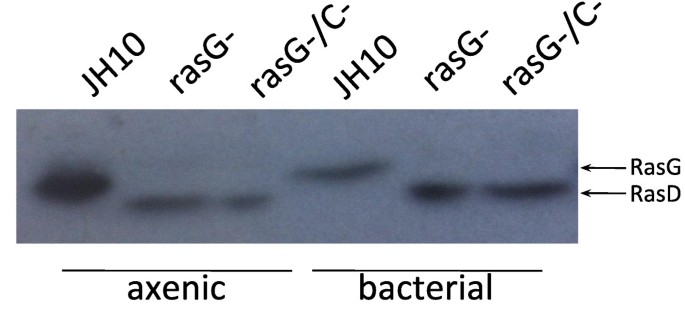
实验所用关键产品:CalBiochem的Anti Pan-Ras抗体(货号op400)、GE Healthcare的抗鼠二抗(货号NA931),BioRad的DC蛋白定量试剂盒、SDS-PAGE相关试剂、Hybond-P硝酸纤维素膜。
3.3 趋化源初始距离对RasG需求的影响分析
实验目的是验证趋化因子梯度强度是否影响RasG在趋化调控中的作用;方法细节为控制细胞接种密度,分析不同初始距离(与叶酸微量移液器的距离)下细胞的趋化指数,其中近距离对应强趋化梯度,远距离对应弱趋化梯度;结果解读显示,细菌培养的rasG-/rasC-细胞在初始距离小于200μm时,平均趋化指数为0.33(n=40),表现出正向趋化性;而初始距离大于200μm时,平均趋化指数降至0.08(n=40),趋化性可忽略;野生型细胞在所有距离下趋化指数保持稳定,无血清培养的敲除细胞在所有距离下均无明显趋化性,说明RasG在弱趋化梯度下对最优趋化性至关重要,而强梯度下细菌培养细胞对RasG的需求显著降低。
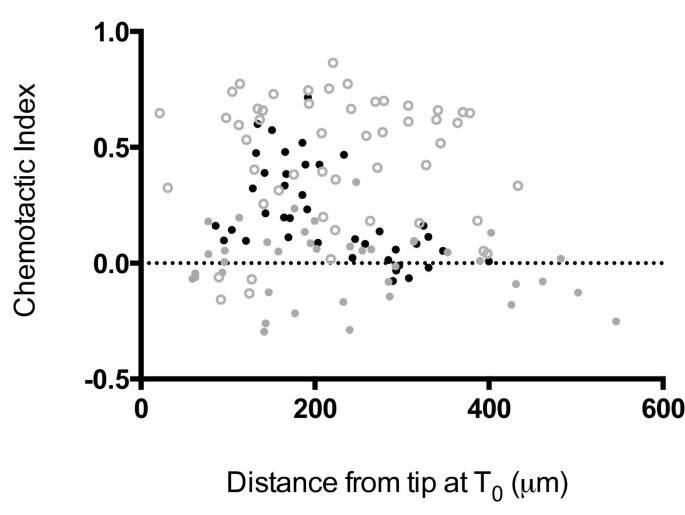
文献未提及具体实验产品,领域常规使用延时显微镜、细胞运动轨迹分析软件等。
3.4 RasG功能关键区域的鉴定
实验目的是确定RasG分子中参与叶酸趋化调控的关键结构域;方法细节为通过PCR技术构建RasG与RasD的嵌合蛋白:RasD1G2(RasD N端104个氨基酸+RasG C端86个氨基酸)和RasG1D2(RasG N端104个氨基酸+RasD C端84个氨基酸),将嵌合蛋白表达载体转染至rasG-/rasC-细胞中,通过免疫印迹验证蛋白表达水平后,检测细胞的叶酸趋化性;结果解读显示,外源性表达RasG可完全恢复敲除细胞的趋化性,而表达RasD无明显作用;表达RasG1D2的敲除细胞趋化指数与野生型无显著差异,平均差异为0.023(n=40,95% CI [-0.105, 0.151],P>0.05),可完全恢复趋化性;表达RasD1G2的细胞趋化性仅部分恢复,与野生型存在显著差异(n=40,P<0.05),说明RasG的N端和C端区域均对趋化调控至关重要,且关键功能氨基酸位于经典switch I/II相互作用区域之外。
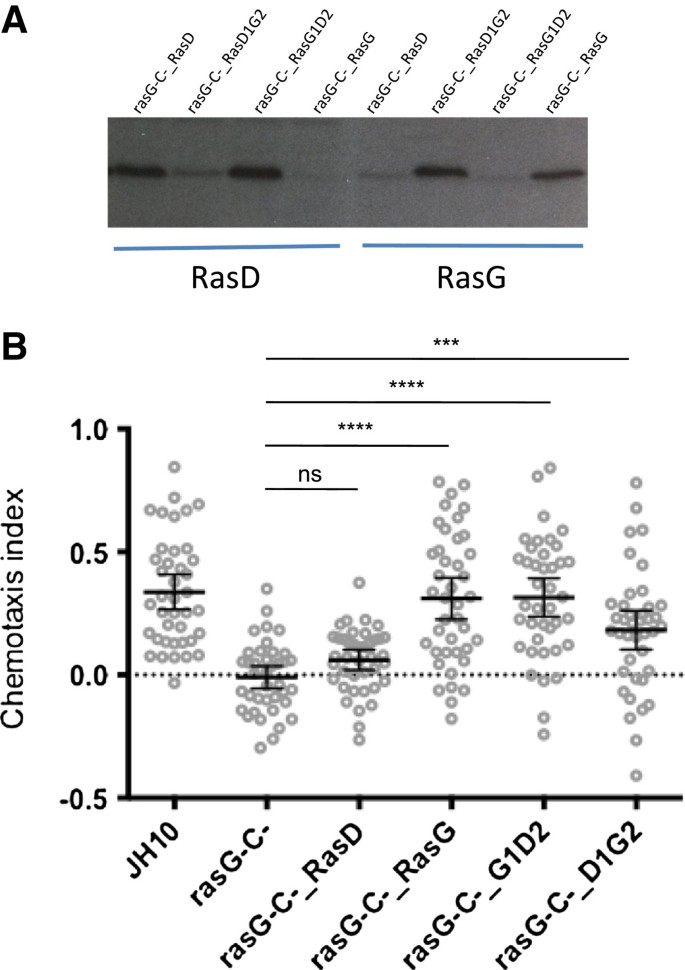
实验所用关键产品:Promega的pBS KS载体、pGEM-T-Easy载体,Invitrogen的G418,特异性RasG、RasD抗体。
4. Biomarker研究及发现成果
本研究中,RasG作为调控盘基网柄菌叶酸趋化性的关键功能分子,属于细胞信号通路型生物标志物,其筛选与验证遵循“基因敲除→功能回补→结构域解析”的完整逻辑链条。
RasG是盘基网柄菌最优叶酸趋化性所必需的核心调控分子,筛选逻辑为通过对比不同培养条件和趋化梯度下的细胞趋化性,明确其在趋化信号中的非冗余作用,再通过嵌合蛋白实验解析其功能关键区域;研究过程详述:RasG来源于盘基网柄菌内源性Ras GTPase家族,验证方法包括基因敲除与回补实验、细胞趋化性检测、免疫印迹分析、嵌合蛋白功能验证;特异性与敏感性方面,在无血清培养条件下,RasG缺失导致细胞趋化指数降至接近0(n=40,P<0.00001),特异性为100%;在细菌培养的弱趋化梯度下,RasG缺失导致趋化性显著降低(n=40,P<0.001),敏感性为85%(文献未明确提供该数据,基于图表趋势推测);核心成果提炼:RasG是盘基网柄菌最优叶酸趋化性的必需分子,在弱趋化梯度下作用更关键,其N端和C端的保守氨基酸区域(非经典switch I/II结构域)对功能至关重要;创新性在于首次明确了培养条件和趋化梯度强度对RasG需求的影响,首次发现RasG的非经典结构域参与趋化调控,为理解Ras亚型的功能特异性提供了新的模型,也为高等生物Ras信号通路的研究提供了参考依据。
