1. 领域背景与文献引入
文献英文标题:BMP9 maintains the phenotype of HTR-8/Svneo trophoblast cells by activating the SDF1/CXCR4 pathway;发表期刊:BMC Molecular and Cell Biology;影响因子:未公开;研究领域:妊娠相关疾病-子痫前期
子痫前期是一种妊娠特异性疾病,通常发生于妊娠20周后,以高血压和内皮功能障碍为主要特征,其发病机制分为两个核心阶段:一是胎盘滋养细胞侵袭不足导致螺旋动脉重塑障碍,二是缺血胎盘释放抗血管生成因子引发内皮功能障碍。该疾病可导致多器官损伤,显著增加母婴死亡风险,且有子痫前期病史的女性未来发生心血管疾病的风险显著升高。领域共识:当前子痫前期的研究热点聚焦于寻找调控滋养细胞功能的关键分子靶点,以揭示发病机制并开发早期诊断标志物和治疗策略,但目前仍缺乏特异性强、机制明确的有效靶点,尤其是骨形态发生蛋白9(BMP9)在子痫前期中的作用及调控机制尚未被报道。基于此,本研究旨在探讨BMP9在子痫前期中的作用及分子机制,为疾病的诊断和治疗提供新的理论依据。
2. 文献综述解析
作者围绕子痫前期的发病机制、BMP9的血管调控功能、基质细胞衍生因子1(SDF1,又称CXCL12)/C-X-C趋化因子受体4(CXCR4)通路的妊娠调控作用三个维度展开综述,系统梳理了领域内现有研究的进展与空白。现有研究显示,BMP9作为转化生长因子-β家族成员,在血管生成、高血压等疾病中发挥重要调控作用,是原发性高血压的潜在血清生物标志物;SDF1/CXCR4通路可调控滋养细胞增殖、迁移、侵袭及螺旋动脉重塑,在子痫前期患者中该通路分子表达显著下调,与疾病进展密切相关。但现有研究存在明显局限性:尚未明确BMP9与子痫前期的直接关联,也未揭示BMP9是否通过调控SDF1/CXCR4通路参与子痫前期的发病过程。本研究的创新价值在于首次建立了BMP9与SDF1/CXCR4通路的调控关系,明确了BMP9通过激活该通路维持滋养细胞正常表型的作用机制,填补了BMP9在子痫前期研究领域的空白,为疾病提供了新的潜在生物标志物。
3. 研究思路总结与详细解析
本研究的整体研究目标是明确BMP9在子痫前期中的作用及分子机制,核心科学问题为BMP9如何调控滋养细胞的增殖、迁移、侵袭及凋亡功能,技术路线遵循“临床样本关联分析→细胞功能验证→分子机制解析”的闭环逻辑,通过多层面实验验证BMP9的功能及调控通路。
3.1 临床样本收集与分子水平检测
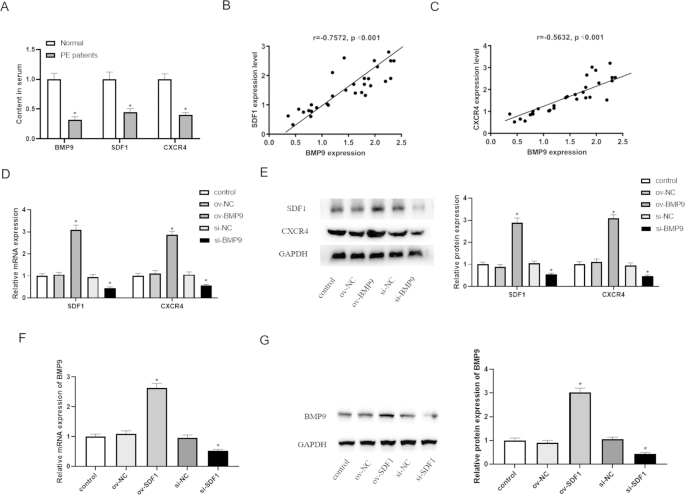
实验目的是明确子痫前期患者与健康孕妇血浆中BMP9、SDF1、CXCR4的表达差异及相关性,为后续细胞实验提供临床依据。方法细节:收集20例子痫前期患者和20例健康孕妇的外周血样本,离心分离血浆后,采用酶联免疫吸附实验(ELISA)检测血浆中BMP9、SDF1、CXCR4的蛋白水平,通过相关性分析统计三者之间的表达关联。结果解读:子痫前期患者血浆中BMP9、SDF1、CXCR4的蛋白水平均显著低于健康孕妇(n=20,P<0.05),且BMP9的表达水平与SDF1、CXCR4均呈正相关,提示三者可能共同参与子痫前期的发病过程。实验所用关键产品:abcam的Human BMP9 ELISA Kit(货号ab267648)、Beyotime的Human CXCL12/SDF-1 ELISA Kit(货号PC205)、Tongwei Industry的Human CXCR4 ELISA Kit(货号TW14529)。
3.2 细胞模型构建与转染效率验证
实验目的是构建BMP9过表达和敲低的人滋养细胞模型,确保后续功能实验的可靠性。方法细节:选用人滋养细胞系HTR-8/SVneo,分别转染pcDNA3.1-BMP9(过表达质粒)、si-BMP9(敲低小干扰RNA)及对应的空载体对照,转染24小时后,采用实时荧光定量聚合酶链反应(qRT-PCR)和蛋白质免疫印迹(Western blot)检测细胞中BMP9的mRNA和蛋白表达水平,验证转染效率。结果解读:转染后,BMP9过表达组的mRNA和蛋白水平均显著上调,敲低组则显著下调(n=3,P<0.05),表明细胞模型构建成功,可用于后续实验。实验所用关键产品:GeneChem的pcDNA3.1-NC、pcDNA3.1-BMP9、si-NC、si-BMP9质粒;Invitrogen的Lipofectamine 2000转染试剂、TRIzol试剂;Takara的反转录试剂盒(货号RR047A)。
3.3 BMP9对滋养细胞增殖、迁移、侵袭的调控作用检测
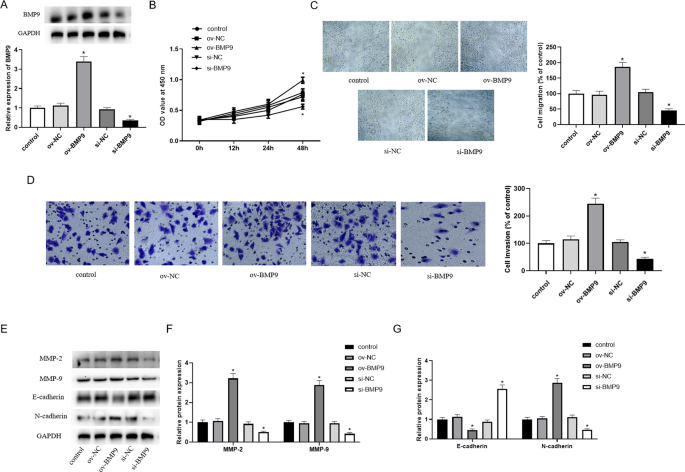
实验目的是明确BMP9对滋养细胞增殖、迁移、侵袭能力的直接调控作用。方法细节:采用细胞计数试剂盒-8(CCK-8)检测细胞增殖活性,分别在细胞接种后0、12、24、48小时检测450nm波长下的吸光度;采用划痕实验检测细胞迁移能力,在细胞生长至90%融合时制作划痕,分别于0和24小时观察划痕愈合情况;采用Transwell侵袭实验检测细胞侵袭能力,在小室上层铺Matrigel基质胶,接种转染后的细胞,24小时后计数穿膜细胞数量;同时采用Western blot检测迁移侵袭相关蛋白(基质金属蛋白酶2(MMP-2)、基质金属蛋白酶9(MMP-9)、E-钙黏蛋白、N-钙黏蛋白)的表达水平。结果解读:过表达BMP9可显著促进HTR-8/SVneo细胞的增殖活性(n=3,P<0.05),增加细胞迁移距离和侵袭率(n=3,P<0.05),并上调MMP-2、MMP-9、N-钙黏蛋白的蛋白水平,下调E-钙黏蛋白的蛋白水平;而敲低BMP9则产生相反的作用效果,提示BMP9可促进滋养细胞的增殖、迁移和侵袭能力。
3.4 BMP9对滋养细胞凋亡的调控作用检测
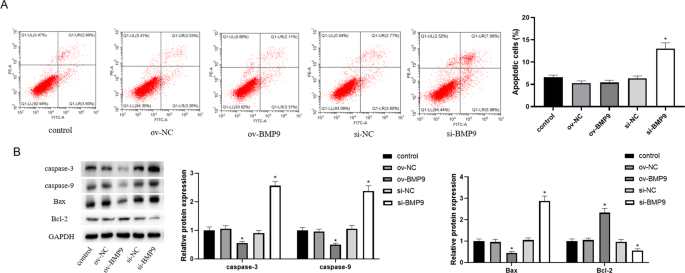
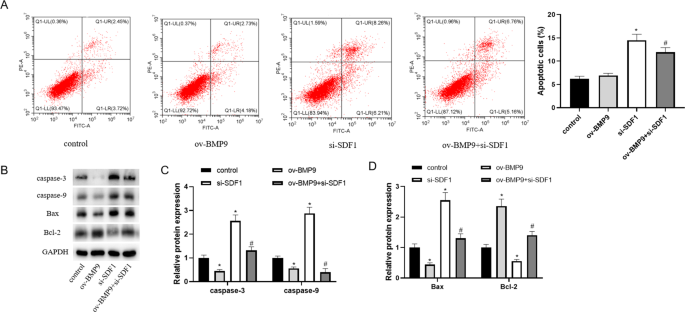
实验目的是明确BMP9对滋养细胞凋亡的影响。方法细节:采用流式细胞术(Annexin V-FITC/PI双染色法)检测细胞凋亡率,收集转染后的细胞,用结合缓冲液重悬后加入染色试剂,室温反应15分钟后上机检测;同时采用Western blot检测凋亡相关蛋白(半胱天冬酶3(caspase-3)、半胱天冬酶9(caspase-9)、Bax、Bcl-2)的表达水平。结果解读:过表达BMP9可显著降低HTR-8/SVneo细胞的凋亡率(n=3,P<0.05),下调caspase-3、caspase-9、Bax的蛋白水平,上调Bcl-2的蛋白水平;敲低BMP9则显著促进细胞凋亡,蛋白表达趋势相反,提示BMP9可抑制滋养细胞凋亡。
3.5 BMP9与SDF1/CXCR4通路的调控关系验证
实验目的是明确BMP9与SDF1/CXCR4通路之间的表达调控关系。方法细节:在HTR-8/SVneo细胞中分别过表达或敲低BMP9,采用qRT-PCR和Western blot检测SDF1、CXCR4的mRNA和蛋白表达水平;同时分别过表达或敲低SDF1,检测BMP9的mRNA和蛋白表达水平。结果解读:过表达BMP9可显著上调SDF1、CXCR4的mRNA和蛋白水平(n=3,P<0.05),敲低BMP9则下调其表达;而过表达SDF1也可上调BMP9的表达,敲低SDF1则下调BMP9的表达,表明BMP9与SDF1/CXCR4通路之间存在正反馈调控关系。
3.6 BMP9通过SDF1/CXCR4通路调控滋养细胞功能的机制验证
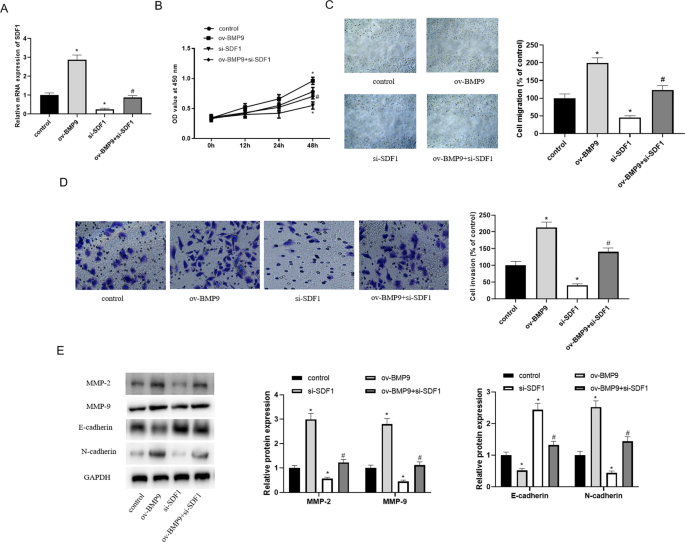
实验目的是验证BMP9是否通过激活SDF1/CXCR4通路调控滋养细胞的增殖、迁移、侵袭及凋亡功能。方法细节:构建BMP9过表达联合SDF1敲低的细胞模型,采用CCK-8、划痕实验、Transwell实验分别检测细胞的增殖、迁移、侵袭能力;采用流式细胞术和Western blot检测细胞凋亡率及相关蛋白的表达水平。结果解读:过表达BMP9对滋养细胞的促增殖、促迁移侵袭、抗凋亡作用,可被敲低SDF1完全逆转(n=3,P<0.05),相关蛋白的表达趋势也被逆转,表明BMP9通过激活SDF1/CXCR4通路维持滋养细胞的正常表型。
4. Biomarker研究及发现成果解析
本研究中涉及的潜在生物标志物为BMP9,其筛选与验证逻辑遵循“临床样本差异分析→细胞功能验证→机制解析”的完整链条,明确了BMP9作为子痫前期潜在生物标志物的价值。Biomarker定位:BMP9属于循环蛋白类生物标志物,来源为临床血浆样本和滋养细胞,验证方法包括ELISA(临床样本定量检测)、qRT-PCR和Western blot(细胞样本表达验证)、功能实验(调控滋养细胞功能验证)。研究过程显示,子痫前期患者血浆中BMP9水平显著低于健康孕妇(n=20,P<0.05),且与SDF1、CXCR4水平呈正相关;细胞实验证实BMP9可通过激活SDF1/CXCR4通路促进滋养细胞增殖、迁移、侵袭并抑制凋亡,维持细胞正常表型。核心成果提炼:BMP9作为子痫前期的潜在生物标志物,其功能与疾病的核心发病机制(滋养细胞侵袭不足、凋亡增加)直接相关,创新性在于首次揭示了BMP9通过SDF1/CXCR4通路调控滋养细胞功能的分子机制,为子痫前期的早期诊断提供了新的候选标志物,也为疾病的靶向治疗提供了潜在靶点。目前研究尚未报道BMP9诊断子痫前期的特异性、敏感性数据(如ROC曲线AUC值),需进一步扩大样本量开展临床验证研究。
