1. 领域背景与文献引入
文献英文标题:Inducible expression of heat shock protein 20 protects airway epithelial cells against oxidative injury involving the Nrf2-NQO-1 pathway;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:呼吸病学-气道上皮细胞氧化损伤与保护机制
氧化应激是慢性炎症性气道疾病(如哮喘、慢性阻塞性肺疾病)发病的核心驱动因素之一,气道上皮细胞作为呼吸道抵御外界刺激的第一道生理屏障,长期暴露于臭氧、过氧化氢等空气源性氧化刺激中,其氧化还原稳态失衡会直接引发上皮损伤、炎症浸润及疾病进展。领域共识:Nrf2-NQO-1通路是细胞内关键的抗氧化防御机制,转录因子Nrf2在氧化应激下入核,调控NQO-1等抗氧化酶的表达,维持细胞氧化还原平衡。小热休克蛋白家族成员在应激条件下可被诱导表达,发挥分子伴侣、抗凋亡及抗氧化等保护作用,但目前针对热休克蛋白20(HSP20)在气道上皮细胞中的表达及功能研究仍处于空白状态,其是否参与气道氧化损伤的调控尚未明确。本研究聚焦这一研究空白,旨在验证氧化应激对气道上皮细胞HSP20的诱导作用,并阐明其通过Nrf2-NQO-1通路发挥保护功能的分子机制,为慢性气道疾病的治疗提供新的潜在靶点。
2. 文献综述解析
本文综述部分以“氧化应激-气道损伤-细胞保护机制”为核心逻辑,从慢性气道疾病的病理基础、细胞内抗氧化通路的作用、小热休克蛋白家族的功能特性三个维度展开,最终聚焦到HSP20在气道领域的研究缺失。
现有研究已证实,氧化应激通过破坏气道上皮屏障完整性、激活炎症信号通路参与慢性气道疾病的发生发展,Nrf2-NQO-1通路作为经典抗氧化通路,其激活可显著减轻氧化损伤,是当前气道疾病研究的热点靶点。小热休克蛋白家族中的HSP27、HSP70等成员已被证实可在气道组织中被诱导表达,发挥抗凋亡、抗氧化作用,但HSP20仅在气道平滑肌中存在组成型表达,其在气道上皮细胞中的表达模式及功能尚未被报道。此外,HSP20在心血管、神经系统中可通过磷酸化修饰发挥抗氧化、抗凋亡保护作用,但其在气道氧化应激中的调控机制完全未知。
本研究的核心创新点在于首次证实氧化应激可特异性诱导气道上皮细胞表达HSP20,且其磷酸化修饰是激活Nrf2-NQO-1通路、发挥氧化损伤保护作用的关键,填补了HSP20在气道上皮细胞功能研究的空白,为慢性气道疾病的靶向治疗提供了新的理论依据。
3. 研究思路总结与详细解析
本研究以“体内模型验证保护作用-体外实验明确分子机制-通路研究阐明调控逻辑”为整体技术路线,核心研究目标是明确HSP20在气道上皮细胞氧化应激中的表达模式及保护功能,解决的核心科学问题是HSP20如何通过调控Nrf2-NQO-1通路实现抗氧化保护作用,通过体内动物实验与体外细胞实验的相互验证,形成完整的研究闭环。
3.1 体内HSP20诱导表达模型构建与验证
本环节核心目标是验证氧化应激可诱导小鼠气道上皮细胞表达HSP20,并构建HSP20稳定高表达的动物模型。实验中首先开展预实验,将6周龄雌性Balb/c小鼠(n=3)分别暴露于过滤空气、0.5ppm及2.0ppm臭氧1小时,24小时后取肺组织行免疫组化(IHC)检测HSP20表达;随后构建预处理模型,将小鼠(n=10)反复暴露于0.5ppm臭氧1小时/次,隔日一次共7天,对照组(n=10)暴露于过滤空气;48小时后,两组各5只小鼠进一步暴露于2.0ppm臭氧3小时,24小时后取肺组织,采用实时荧光定量PCR(RT-qPCR)检测HSP20 mRNA水平,蛋白质免疫印迹(Western blot)检测总HSP20及磷酸化HSP20蛋白表达,IHC检测气道上皮细胞HSP20的定位表达。
结果显示,预实验IHC染色表明臭氧暴露后小鼠气道上皮细胞HSP20表达显著增加(图2a);预处理模型中,RT-qPCR结果显示臭氧预处理组肺组织HSP20 mRNA表达显著高于对照组(n=5,P<0.05);Western blot结果显示预处理组总HSP20及磷酸化HSP20蛋白水平均显著升高(图2c);IHC结果显示预处理组气道上皮细胞HSP20阳性细胞数及占比显著增加(图2d);高浓度臭氧刺激后,对照组HSP20蛋白水平进一步升高,而预处理组无明显变化,表明预处理已成功诱导HSP20稳定高表达。
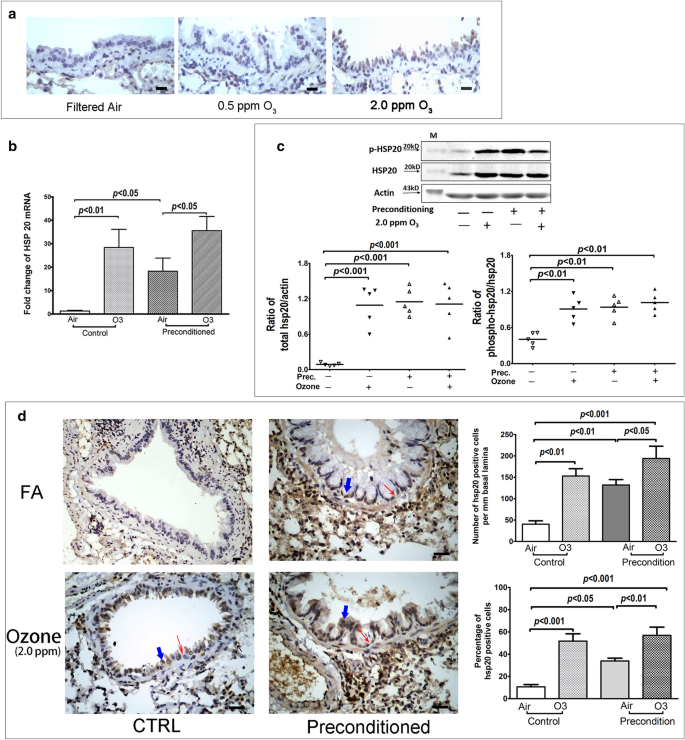
实验所用关键产品:Abcam的抗HSP20抗体(ab184161)、抗磷酸化HSP20抗体(ab58522),CST的抗肌动蛋白抗体(4970)等。
3.2 体内HSP20对气道氧化损伤的保护作用评估
本环节核心目标是验证HSP20高表达对高浓度臭氧诱导的气道上皮损伤的保护作用。实验中对上述预处理模型小鼠,检测体重变化、支气管肺泡灌洗液(BALF)细胞计数、肺组织病理(H&E染色)、气道上皮细胞密度、BALF中白蛋白和E-钙粘蛋白浓度、肺组织丙二醛(MDA)含量和谷胱甘肽过氧化物酶(GSH-Px)活性、NQO-1 mRNA表达水平。
结果显示,高浓度臭氧刺激后,预处理组小鼠体重降低幅度显著小于对照组(图3a);BALF中总白细胞、中性粒细胞增加幅度显著低于对照组,且淋巴细胞未出现显著升高(n=5,P<0.05,图3b);H&E染色显示预处理组气道炎症评分显著低于对照组(图3d);气道上皮细胞密度降低幅度更小(图3e);BALF中白蛋白和E-钙粘蛋白浓度显著低于对照组(n=5,P<0.05,图3f、g);肺组织MDA含量和GSH-Px活性无显著升高,而对照组上述指标显著升高(n=5,P<0.05,图3h、i);预处理组基础状态下NQO-1 mRNA表达显著高于对照组,刺激后两组表达水平相近(图3j)。上述结果表明HSP20高表达可全面减轻氧化应激诱导的气道上皮损伤和炎症反应。
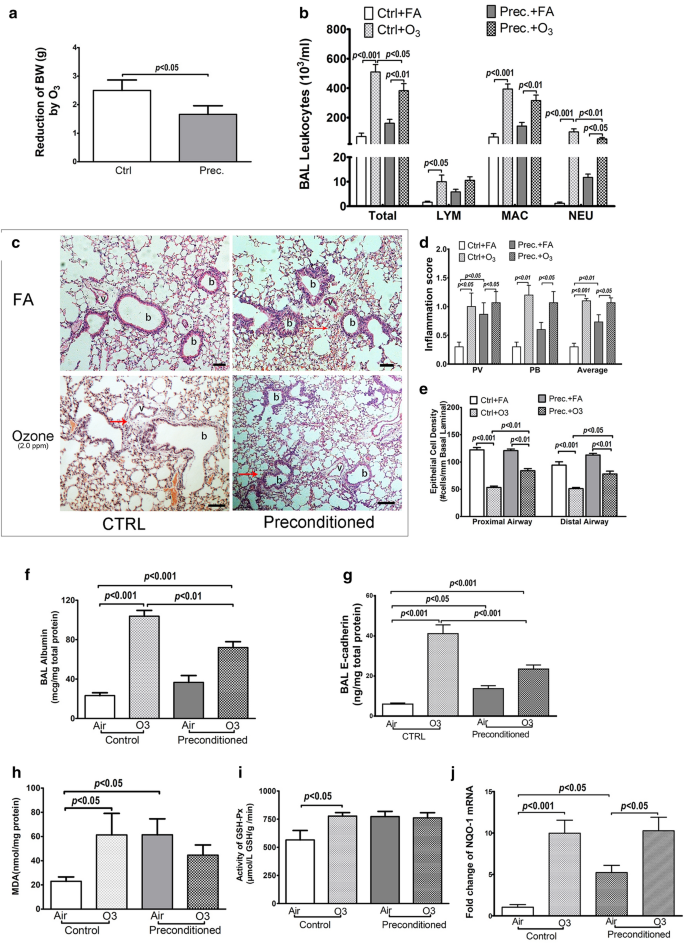
实验所用关键产品:Abcam的白蛋白ELISA试剂盒(ab108792),Thermo Fisher的E-钙粘蛋白ELISA试剂盒(EMCDH1),南京建成生物的MDA和GSH-Px检测试剂盒等。
3.3 体外氧化应激模型验证及HSP20诱导表达检测
本环节核心目标是验证臭氧与H2O2在体外对气道上皮细胞的氧化作用的等效性,并明确H2O2诱导人支气管上皮细胞表达HSP20的最优实验条件。实验中将人支气管上皮细胞16HBE采用气液界面培养,分别暴露于2.0ppm臭氧或不同浓度H2O2(0、25、50、100、200μM)0.5、1、2、4小时,采用MTS法检测细胞活力;检测细胞上清中4-羟基壬烯醛(4-HNE)和细胞DNA中8-羟基脱氧鸟苷(8-OHdG)水平;随后将BEAS-2B细胞采用常规培养,用不同浓度H2O2(0、0.1、1.0、10、100μM)刺激1小时,分别在0、12、24小时后采用MTT法检测细胞活力,Western blot和RT-qPCR检测HSP20表达,免疫细胞化学(ICC)验证HSP20的细胞定位。
结果显示,MTS实验表明2.0ppm臭氧与50-200μM H2O2对细胞活力的影响相当(图4a);4-HNE和8-OHdG检测显示臭氧与H2O2诱导的氧化损伤水平相近(图4b、c);BEAS-2B细胞实验中,10μM H2O2刺激12小时后HSP20蛋白和mRNA表达水平最高(n=3,P<0.05,图4e、f),ICC染色显示HSP20表达显著增加(图4g),最终确定该条件为后续实验的最优参数。
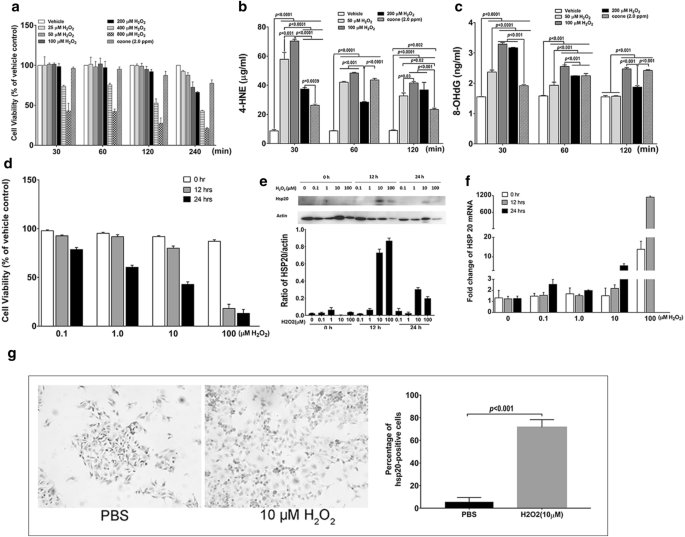
实验所用关键产品:Abcam的4-HNE ELISA试剂盒、8-OHdG ELISA试剂盒,Promega的MTS检测试剂盒,Sigma的MTT试剂盒等。
3.4 体外HSP20过表达对氧化损伤的保护作用验证
本环节核心目标是验证HSP20过表达及其磷酸化修饰对H2O2诱导的BEAS-2B细胞损伤的保护作用。实验中将BEAS-2B细胞分别转染pEX-3-HSP20(野生型)、pEX-3-HSP20(Ala)(非磷酸化突变体)、pEX-3(空载体)质粒,48小时后用10μM H2O2刺激1小时,12小时后检测HSP20 mRNA和蛋白表达、细胞内活性氧(ROS)水平、细胞凋亡情况(Annexin V-FITC/PI染色流式细胞术)。
结果显示,RT-qPCR结果显示转染组HSP20 mRNA表达显著高于空载体组,H2O2刺激后空载体组HSP20 mRNA进一步升高,转染组无明显变化(n=3,P<0.05,图5a);Western blot结果显示转染组总HSP20蛋白水平显著升高,H2O2刺激后野生型转染组磷酸化HSP20比例显著高于突变体组(n=3,P<0.05,图5b);ROS检测显示H2O2刺激后野生型转染组ROS水平无显著升高,而空载体和突变体组ROS水平显著升高(n=3,P<0.05,图5c);凋亡检测显示野生型转染组早期凋亡和坏死(含晚期凋亡)比例显著低于空载体组,突变体组早期凋亡比例显著高于野生型组(n=3,P<0.05,图5d、e、f)。上述结果表明HSP20过表达可抑制氧化诱导的细胞损伤,且磷酸化修饰是其发挥保护作用的关键。
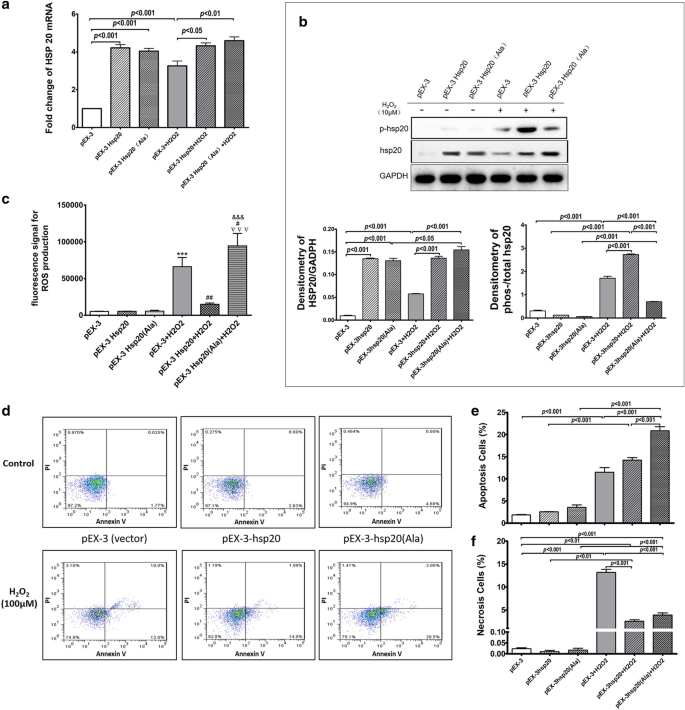
实验所用关键产品:Invitrogen的Lipofectamine 2000转染试剂,BD的Annexin V-FITC凋亡检测试剂盒,Beyotime的ROS检测试剂盒等。
3.5 HSP20对Nrf2-NQO-1通路的调控作用验证
本环节核心目标是明确HSP20通过激活Nrf2-NQO-1通路发挥抗氧化作用的分子机制。实验中对上述转染后的BEAS-2B细胞,H2O2刺激后采用RT-qPCR检测NQO-1 mRNA表达,Western blot检测NQO-1蛋白及核内Nrf2蛋白水平。
结果显示,H2O2刺激后,野生型转染组NQO-1 mRNA表达升高5倍,空载体和突变体组升高3倍(n=3,P<0.05,图6a);Western blot结果显示野生型转染组NQO-1蛋白水平显著高于突变体组(n=3,P<0.05,图6b);核内Nrf2蛋白水平在野生型转染组基础状态下即显著升高,H2O2刺激后升高更显著,而突变体组无明显变化(n=3,P<0.05,图6c)。上述结果表明HSP20磷酸化可促进Nrf2入核,上调NQO-1表达,进而激活细胞内抗氧化通路。
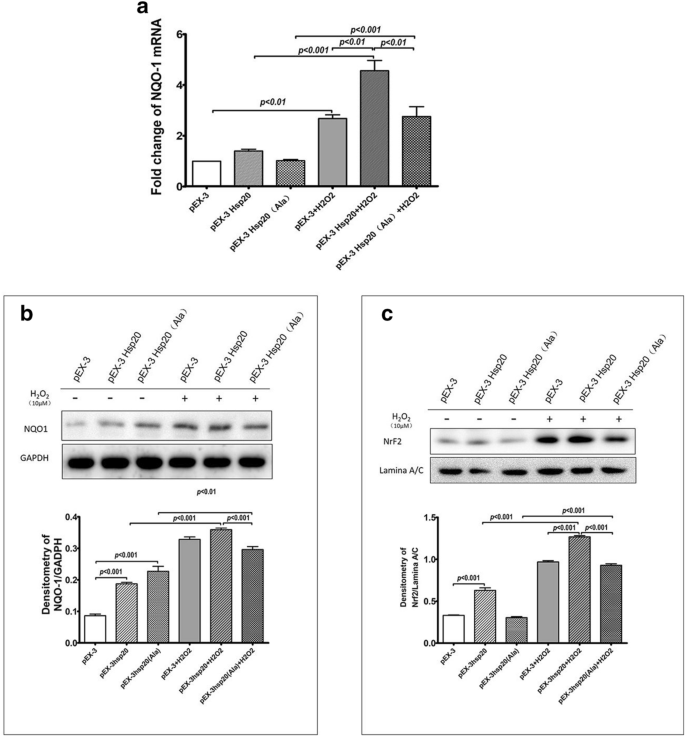
实验所用关键产品:CST的抗NQO-1抗体(62262)、抗Nrf2抗体(12721)、抗Lamina A/C抗体(2032)等。
4. Biomarker研究及发现成果解析
Biomarker定位
本文中HSP20既是气道上皮细胞氧化应激的响应性Biomarker,也是潜在的慢性气道疾病治疗靶点,其筛选验证逻辑为“体内氧化应激模型发现诱导表达→体外细胞实验验证保护作用→分子实验阐明调控通路”,形成了完整的证据链条。
研究过程详述
HSP20来源于气道上皮细胞,在臭氧、H2O2等氧化应激刺激下可被快速诱导表达,其验证方法涵盖体内免疫组化、Western blot、RT-qPCR,体外Western blot、RT-qPCR、ICC等多种技术。特异性方面,HSP20在基础状态下的气道上皮细胞中表达极低,仅在氧化应激刺激后显著升高,具有明确的应激响应特异性;敏感性方面,低至0.5ppm的臭氧暴露即可诱导其表达(图2a),显示出对氧化应激的高敏感性。
核心成果提炼
HSP20作为氧化应激诱导的保护性Biomarker,其磷酸化修饰可通过促进Nrf2入核,激活Nrf2-NQO-1通路,降低细胞内ROS水平,抑制细胞凋亡,从而减轻气道上皮损伤。本研究首次证实了HSP20在气道上皮细胞中的保护作用,为慢性气道疾病的治疗提供了新的潜在靶点。统计学结果显示,体内实验中预处理组与对照组的各项指标差异均具有统计学意义(n=5,P<0.05),体外实验中转染组与空载体组的差异同样显著(n=3,P<0.05),充分验证了研究结论的可靠性。
