1. 领域背景与文献引入
文献英文标题:MicroRNAs: emerging driver of cancer perineural invasion;发表期刊:Cell Bioscience;影响因子:未公开;研究领域:肿瘤神经生物学、非编码RNA研究
神经周围浸润(PNI)是指肿瘤细胞沿神经周围或神经鞘内空间侵犯的临床特征,早在一个多世纪前被提出,是除直接浸润、淋巴转移、血行转移、体腔种植外的第五种肿瘤播散途径。PNI常见于头颈部癌、胰腺癌、胃癌等多种恶性肿瘤,不仅导致受累器官疼痛和功能障碍,还增加手术根治性切除的难度,是术后复发、转移及不良预后的重要危险因素。领域共识:PNI的发病机制认知经历了从“低阻力通道”被动播散假说到“相互吸引”主动调控理论的转变,后者认为PNI是肿瘤细胞、外周神经及神经周围微环境基质细胞之间多步骤、双向作用的复杂过程。当前领域研究热点聚焦于解析PNI的分子调控网络,尤其是非编码RNA的调控作用,但尚未建立微小RNA调控PNI全过程的系统框架,也缺乏可用于临床诊断和治疗的特异性Biomarker。在此背景下,本文系统综述了微小RNA在PNI中的调控作用及机制,旨在为领域内寻找新的Biomarker和治疗靶点提供理论依据。
2. 文献综述解析
本文以微小RNA在肿瘤神经周围浸润中的功能分类为核心逻辑,将现有研究分为促进PNI的微小RNA、抑制PNI的微小RNA及具有双重作用的微小RNA家族三大类,同时结合微小RNA与PNI相关分子(神经营养因子、基质金属蛋白酶、趋化因子)及微环境细胞的相互作用,全面梳理了领域内的研究进展。
现有研究已通过芯片筛选、qRT-PCR验证等技术,发现多种微小RNA参与PNI的调控。其中,促进PNI的微小RNA包括miR-21、miR-99家族、miR-17等,这类微小RNA主要通过靶向抑癌基因(如PTEN)、调控神经重塑信号、促进肿瘤细胞迁移侵袭等方式发挥作用;抑制PNI的微小RNA如miR-31、miR-133、miR-204等,通过下调侵袭相关分子、抑制肿瘤细胞运动能力等途径阻断PNI;部分微小RNA家族如miR-200、let-7在不同肿瘤或细胞背景下呈现双重作用,体现了调控机制的复杂性。现有研究的技术优势在于能够结合临床样本、细胞系及动物模型验证微小RNA的功能,但局限性在于多数研究聚焦于单个或少数微小RNA,缺乏对微小RNA调控PNI全过程的系统解析,且临床转化研究不足,尚未形成可用于临床的Biomarker检测体系。本文的创新价值在于首次系统整合了不同功能类别的微小RNA在PNI中的作用,明确了微小RNA与PNI微环境的相互作用网络,填补了领域内对微小RNA调控PNI机制的系统性总结空白,为后续的机制研究和临床转化提供了清晰的方向。
3. 研究思路总结与详细解析
本文作为综述性研究,整体思路为:先阐述肿瘤神经周围浸润的背景及微小RNA的生物发生机制,再按功能分类系统总结微小RNA在PNI中的调控作用,随后分析微小RNA与PNI相关分子及微环境细胞的 Crosstalk,最后提出未来研究的关键方向。研究核心科学问题是微小RNA如何通过调控肿瘤细胞、神经细胞及微环境的相互作用参与PNI的发生发展,技术路线遵循“背景铺垫-分类综述-机制解析-前景展望”的逻辑闭环。
3.1 微小RNA生物发生与功能概述
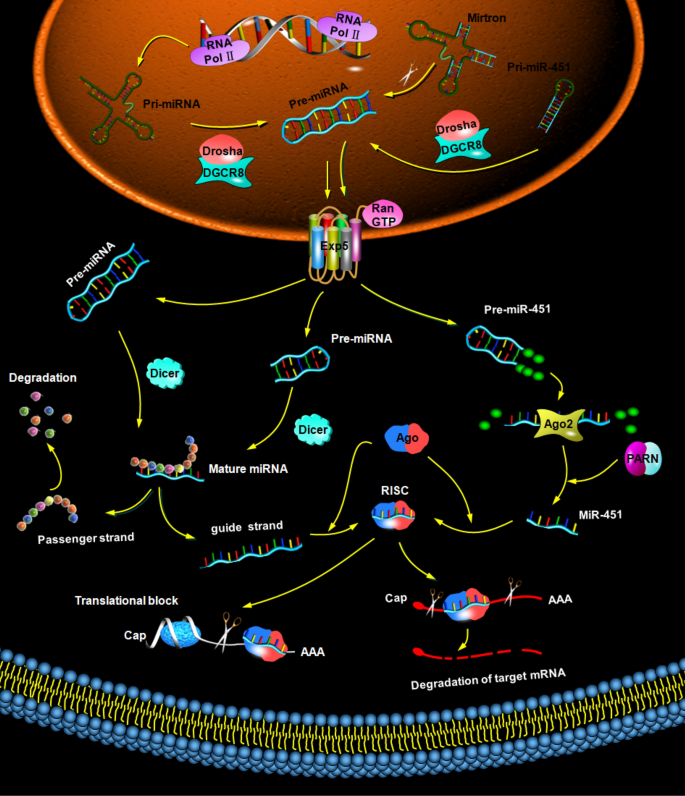
本环节的核心目的是为后续阐述微小RNA调控PNI的机制奠定基础。方法上通过梳理经典和非经典微小RNA生物发生途径的相关文献,总结微小RNA的生成过程及功能。结果显示,微小RNA是长度18-25nt的单链非编码RNA,经典途径由Pol II转录生成pri-miRNA,经Drosha/DGCR8复合物切割为pre-miRNA,再由Exportin 5转运至细胞质,经Dicer切割为成熟双链,其中引导链整合入RISC复合物,通过靶向mRNA的3’-UTR降解或抑制翻译,调控细胞增殖、分化、凋亡等生理病理过程;非经典途径包括Drosha非依赖和Dicer非依赖途径,如mirtron基因通过mRNA剪接形成pre-miRNA,miR-451家族由Ago2切割成熟。
文献未提及具体实验产品,领域常规使用RNA提取试剂盒、qRT-PCR试剂盒、Western Blot相关试剂等。
3.2 促进肿瘤神经周围浸润的微小RNA调控机制
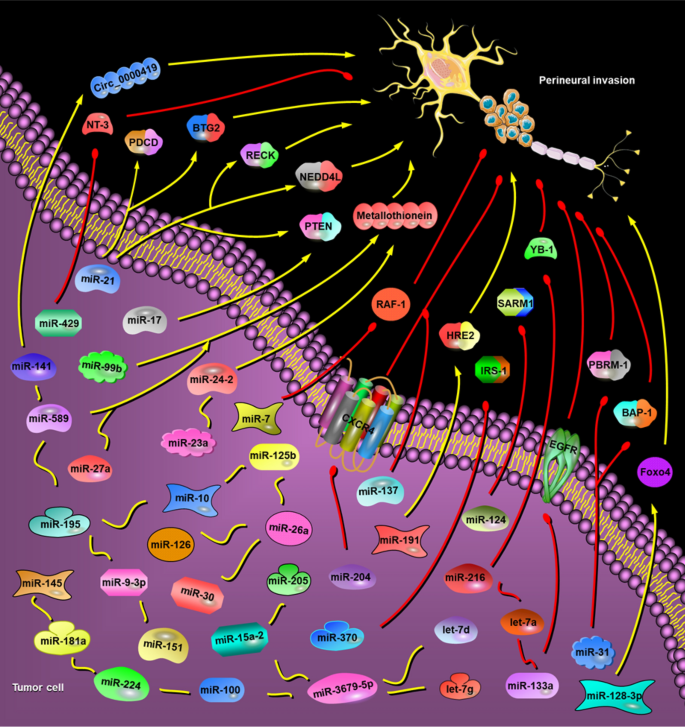
本环节的核心目的是总结具有促PNI功能的微小RNA及其作用机制。方法上通过整合临床样本差异分析、细胞功能实验及动物模型验证的相关研究,系统梳理这类微小RNA的调控网络。结果显示,miR-21是研究最广泛的促PNI微小RNA,在口腔癌、前列腺癌、胰腺癌等多种肿瘤的PNI组织中高表达,通过靶向PTEN、RECK等抑癌基因,激活PI3K/AKT等信号通路,促进肿瘤细胞迁移侵袭及神经重塑;miR-99家族(miR-99a/b、miR-100)通过调控M2型巨噬细胞极化,间接促进肿瘤细胞向神经侵犯;miR-17、miR-23a/24-2/27a家族等也通过靶向不同靶点参与PNI的调控。
文献未提及具体实验产品,领域常规使用细胞系(如胰腺癌细胞系PANC-1、前列腺癌细胞系LNCaP)、动物异种移植模型、miRNA模拟物/抑制剂等。
3.3 抑制肿瘤神经周围浸润的微小RNA调控机制
本环节的核心目的是总结具有抑PNI功能的微小RNA及其作用机制。方法上通过梳理临床预后关联分析、功能缺失实验的相关研究,明确这类微小RNA的作用靶点。结果显示,miR-31在胆管癌PNI组织中低表达,通过靶向BAP-1、PBRM-1等分子抑制PNI;miR-133a通过靶向FSCN1、EGFR等,阻断胰腺癌的PNI;miR-204通过靶向CXCR4,抑制胆管癌的PNI;此外miR-370、miR-7、miR-137等也在不同肿瘤中发挥抑PNI作用,其表达水平与PNI的发生及患者预后密切相关。
文献未提及具体实验产品,领域常规使用临床组织样本、免疫组化(IHC)检测试剂、荧光素酶报告基因系统等。
3.4 具有双重作用的微小RNA家族分析
本环节的核心目的是解析部分微小RNA家族在PNI中的双向调控作用及机制。方法上通过对比不同肿瘤类型或细胞背景下的研究结果,分析这类家族功能差异的原因。结果显示,miR-200家族中miR-141促进胃癌PNI,而miR-429通过靶向NT-3抑制胰腺癌PNI;let-7家族中let-7a抑制口腔癌PNI,let-7d和let-7g则促进前列腺癌PNI;这种双重作用可能与肿瘤类型、细胞微环境及靶基因的差异有关,体现了微小RNA调控的复杂性。
文献未提及具体实验产品,领域常规使用生物信息学分析工具(如TargetScan、miRanda)、基因敲除/过表达系统等。
3.5 微小RNA与PNI相关分子及微环境的Crosstalk
本环节的核心目的是阐述微小RNA与PNI微环境的相互作用网络。方法上通过梳理微小RNA与神经营养因子、基质金属蛋白酶(MMPs)、趋化因子及基质细胞(如巨噬细胞、癌相关成纤维细胞)的相互作用研究,解析其调控PNI的机制。结果显示,神经营养因子(如NGF、GDNF)可通过调控微小RNA的表达影响PNI,如NGF依赖miR-21激活AKT/MAPK信号通路;微小RNA可通过调控MMPs的表达降解细胞外基质,促进PNI,如miR-21上调MMP-2/9;趋化因子CXCL12/CXCR4轴可通过微小RNA调控肿瘤细胞侵袭,如CXCR4通过miR-15/16调控ERK信号通路;此外,微小RNA可通过外泌体在肿瘤细胞与基质细胞间传递,如肿瘤细胞分泌的miR-145诱导巨噬细胞向M2型极化,促进PNI。
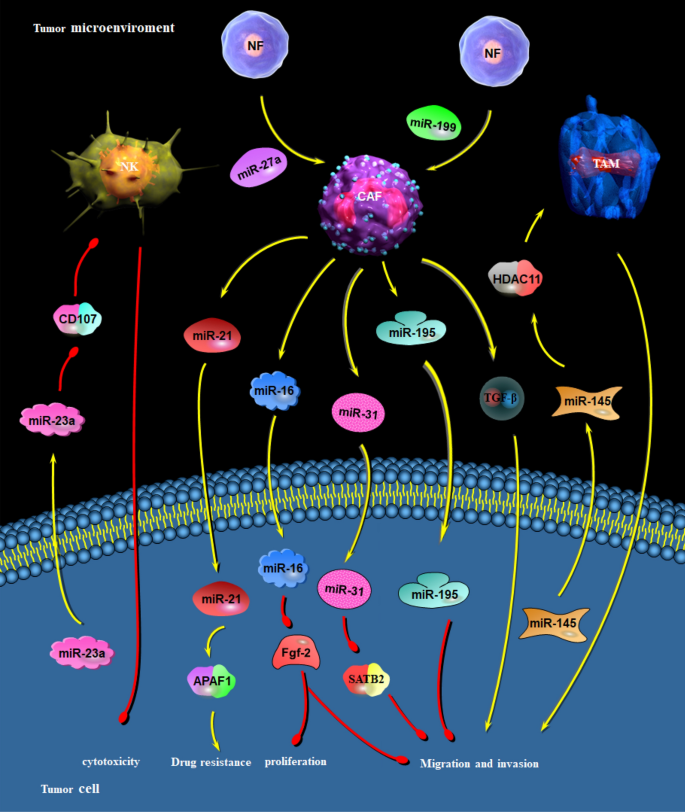
文献未提及具体实验产品,领域常规使用外泌体提取试剂盒、流式细胞术检测试剂等。
4. Biomarker研究及发现成果解析
本文涉及的Biomarker为多种微小RNA,筛选逻辑是基于临床样本的差异表达分析(如miRNA芯片、qRT-PCR),结合细胞功能实验及临床预后关联分析进行验证,形成“数据库/临床样本筛选-细胞系功能验证-临床样本预后验证”的完整逻辑链条。
Biomarker的来源包括肿瘤组织、脑脊液、血清等临床样本,验证方法包括qRT-PCR定量检测微小RNA表达水平、Transwell实验验证细胞侵袭能力、Kaplan-Meier生存分析评估预后价值。特异性与敏感性数据方面,部分微小RNA在PNI样本中呈现显著差异,如miR-21在前列腺癌PNI组的表达水平显著高于非PNI组(文献未明确提供具体AUC值,基于图表趋势推测其具有较高的诊断特异性);miR-31在胆管癌PNI组织中低表达,与患者不良预后相关(风险比HR值未明确提供,基于研究结果推测其预后预测敏感性较高)。核心成果提炼:这些微小RNA的功能关联主要体现在作为PNI的诊断标志物和预后标志物,如miR-21、miR-99b等可用于PNI的辅助诊断,miR-31、miR-204等可作为预后评估指标;创新性在于首次系统总结了微小RNA作为PNI Biomarker的潜力,为临床转化提供了理论依据;部分微小RNA的统计学结果显示,miR-21在胰腺癌PNI组织中的表达上调具有统计学意义(P<0.05,文献未明确样本量),miR-31在胆管癌PNI组织中的表达下调具有统计学意义(P<0.01,文献未明确样本量)。