1. 领域背景与文献
文献英文标题:The role of the striatin family proteins in hippo signaling and cellular regulation;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:细胞信号调控(Hippo通路与支架蛋白功能研究)。
纹蛋白(striatin)家族包含STRN1、SG2NA(STRN3)、zinedin(STRN4)三个成员,属于钙调蛋白结合的WD-40重复蛋白家族,是纹蛋白相互作用磷酸酶与激酶(STRIPAK)复合物的核心支架组分。领域共识:纹蛋白家族最早于2000年被明确为脑特异性表达的信号支架蛋白,后续研究逐步证实其参与细胞黏附、细胞骨架组装、神经发育、肿瘤转移等多个生物学过程,2019年研究首次发现STRIPAK复合物可整合上游信号启动Hippo激酶级联反应,为纹蛋白与Hippo通路的关联提供了初步依据。当前该领域的研究热点包括STRIPAK复合物的动态组装调控、其在肿瘤发生中的促癌机制、以及Hippo通路上游调控的新分子鉴定,尚未解决的核心问题包括纹蛋白家族三个成员的功能特异性与冗余性、其对Hippo通路核心效应分子YAP的调控机制,以及该调控在不同细胞类型中的功能差异。本研究针对上述研究空白,系统分析纹蛋白家族在成纤维细胞和角质形成细胞中的功能,揭示其调控Hippo通路的新机制,可为皮肤稳态维持、肿瘤靶向治疗的相关研究提供新的理论靶点。
2. 文献综述解析
作者对现有研究的评述按研究方向分为三个维度:纹蛋白家族的结构与基本功能、STRIPAK复合物的生物学作用、纹蛋白与相关信号通路的关联。现有研究支持的关键结论包括:纹蛋白家族具有保守的多结构域组成,可通过支架功能招募多种激酶、磷酸酶形成复合物,参与多条信号通路的调控;STRIPAK复合物在进化上高度保守,在真核生物中调控细胞迁移、神经发育、器官发生等多个过程;纹蛋白可与Wnt通路核心组分APC结合,同时STRIPAK复合物可通过去磷酸化MST1/2负调控Hippo通路,促进YAP入核激活下游靶基因。现有研究的技术方法优势在于,通过基因编辑、免疫共沉淀等技术已初步明确纹蛋白的部分互作分子和基本表型,为后续机制研究奠定了基础;局限性在于多数研究聚焦于STRIPAK复合物的整体功能,未区分纹蛋白家族三个成员的特异性作用,且缺乏不同细胞类型中的系统性功能验证,纹蛋白调控Hippo通路的具体分子机制也尚未阐明。
本研究的创新价值体现在三个方面:首次系统比较了纹蛋白家族三个成员在成纤维细胞和角质形成细胞中的功能差异,明确了其功能的细胞特异性与成员特异性;首次揭示纹蛋白家族通过保护磷酸化YAP免受蛋白酶体降解调控Hippo通路的新机制,不同于既往报道的STRIPAK复合物通过调控MST1/2影响Hippo通路的作用模式;证实了纹蛋白调控Hippo通路可影响细胞迁移、增殖等核心生物学功能,为纹蛋白作为疾病治疗靶点提供了实验依据。
3. 研究思路总结与详细解析
本研究的整体目标是明确纹蛋白家族三个成员的共有与特异性功能,揭示其对Hippo信号通路的调控机制及下游生物学效应;核心科学问题为纹蛋白家族如何调控Hippo通路效应分子YAP的稳定性,以及该调控如何影响细胞迁移、增殖等过程;技术路线遵循“细胞模型构建→转录组分析→通路验证→机制解析→功能验证”的闭环逻辑,首先通过shRNA构建纹蛋白家族各成员的稳定敲低细胞模型,随后通过转录组分析明确基因表达变化,进而验证其对Wnt、Hippo通路的调控作用,再通过分子实验解析调控机制,最终验证对细胞功能的影响。
3.1 纹蛋白家族敲低细胞模型构建与验证
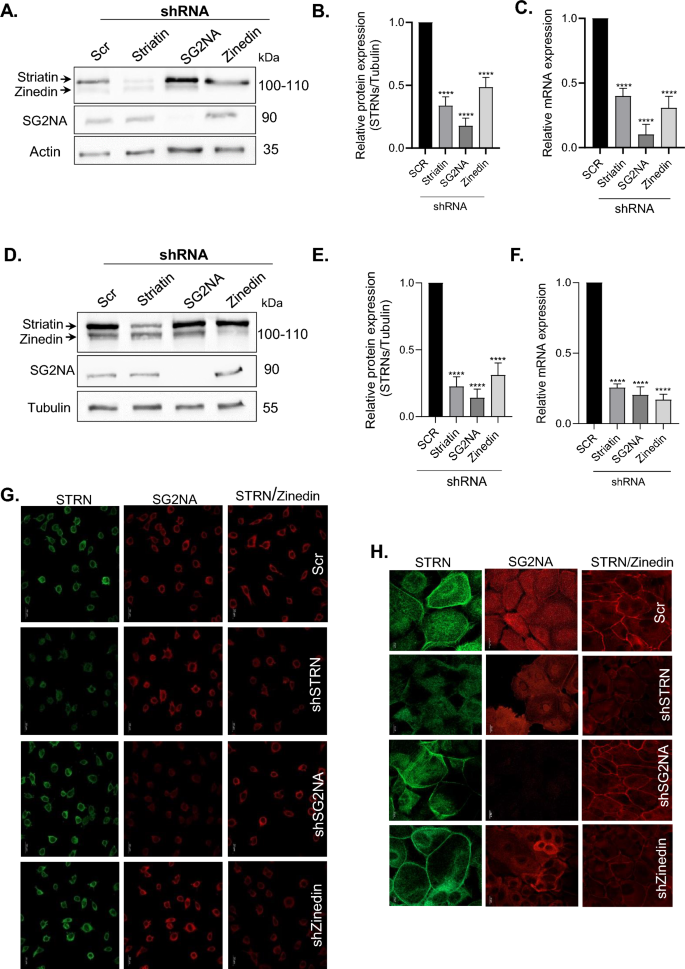
本环节的核心目标是构建纹蛋白家族三个成员稳定敲低的成纤维细胞和角质形成细胞模型,确保后续实验的可靠性。实验采用慢病毒介导的shRNA技术,针对三个纹蛋白家族基因共设计14条shRNA序列,克隆至慢病毒载体后感染细胞,经3μg/ml嘌呤霉素筛选1周获得稳定细胞株,后续通过蛋白质免疫印迹(Western blot)、实时荧光定量PCR(qPCR)、免疫荧光实验验证敲低效率,筛选出敲低效果最显著的shRNA序列(shSTR-79、shSG2NA-17、shZinedin-68)用于后续实验。
实验结果显示,成纤维细胞和角质形成细胞中三个纹蛋白的蛋白水平均显著降低,灰度值统计显示蛋白敲低效率均在70%以上(n=3~4,P<0.0001);实时荧光定量PCR结果显示对应mRNA水平也显著下降(n=3~4,P<0.0001);免疫荧光实验进一步证实细胞中纹蛋白的荧光信号明显降低,表明敲低模型构建成功。
文献未提及具体实验产品,领域常规使用慢病毒包装试剂、嘌呤霉素、抗纹蛋白家族抗体、实时荧光定量PCR试剂盒等试剂。
3.2 纹蛋白家族表达模式与敲低后转录组分析
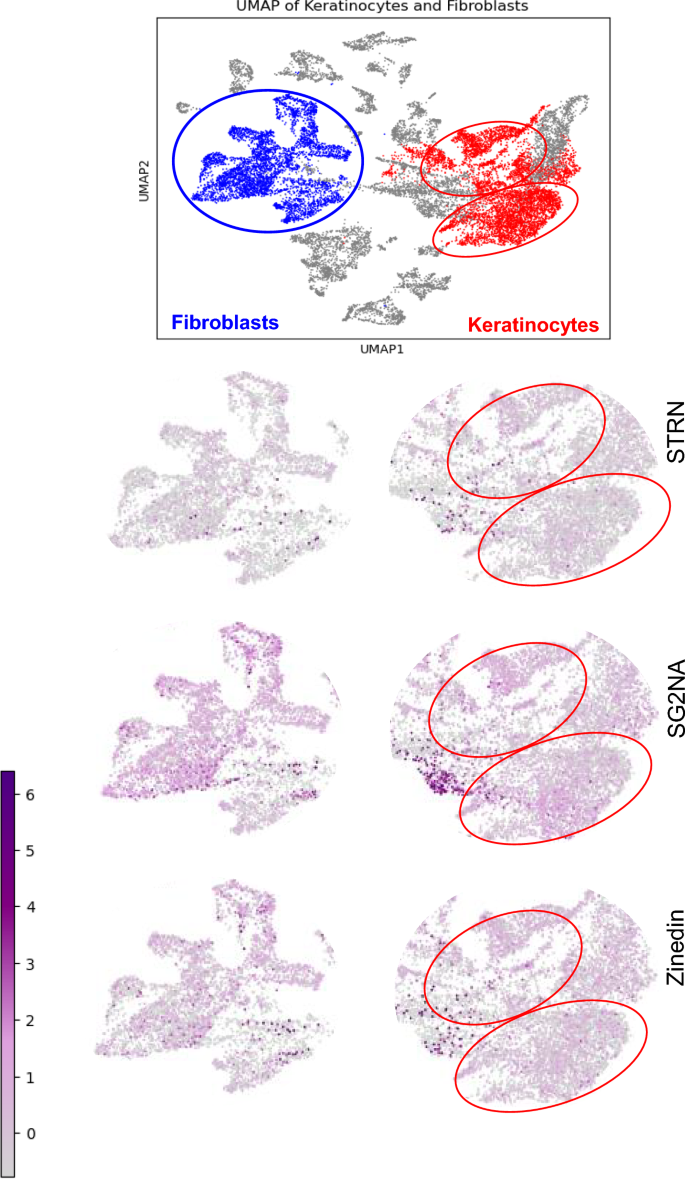
本环节的核心目标是明确纹蛋白家族在不同细胞中的表达特征,以及敲低后基因表达谱的变化,揭示其功能的细胞特异性。实验首先分析GEO数据库中GSE188954的小鼠皮肤单细胞RNA测序数据,通过Scanpy软件进行标准预处理和UMAP聚类,注释成纤维细胞和角质形成细胞簇后分析纹蛋白家族的表达模式;随后对敲低细胞进行RNA测序,采用DAVID、GSEA工具进行差异基因的功能富集分析,通过韦恩图分析差异基因的重叠情况,并用实时荧光定量PCR验证关键差异基因的表达。
实验结果显示,纹蛋白家族三个成员在成纤维细胞和角质形成细胞中具有独特的表达模式,符合其组织表达特异性的既往报道;转录组分析显示,成纤维细胞中SG2NA敲低后特有差异基因占比约50%(159/319),而角质形成细胞中zinedin敲低后特有差异基因最多(224个),两种细胞中STRN1敲低后无共同差异基因,SG2NA和zinedin敲低后仅存在少量共同差异基因,提示纹蛋白家族的功能具有显著的细胞特异性和成员特异性;实时荧光定量PCR验证显示,角质形成细胞中三个纹蛋白敲低后角蛋白16(KRT16)的mRNA表达均显著上调(n=3~4,P<0.05),与RNA测序结果一致。功能富集分析显示,纹蛋白敲低后角质形成细胞中细胞分化相关通路显著上调,而成纤维细胞中细胞定位、迁移相关通路显著上调,符合两种细胞的功能特性差异。
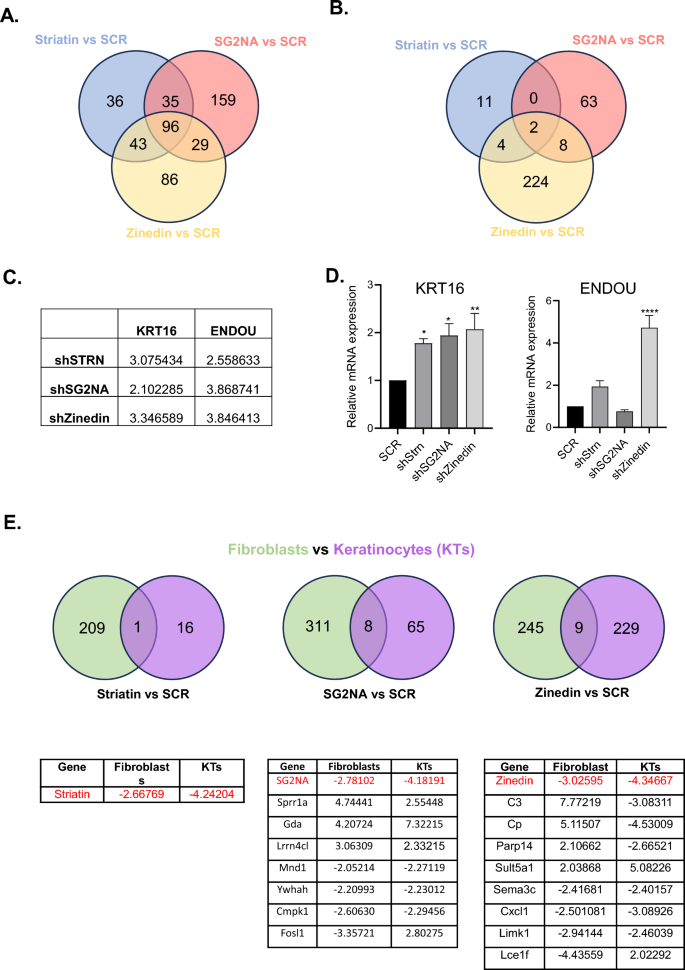
文献未提及具体实验产品,领域常规使用RNA提取试剂、RNA建库试剂盒、高通量测序平台、生物信息学分析软件等。
3.3 纹蛋白对Wnt通路的调控作用验证
本环节的核心目标是验证纹蛋白家族对Wnt信号通路的调控作用,明确其与既往报道的纹蛋白-APC互作的功能关联。实验首先分析RNA测序数据中Wnt通路相关基因的表达变化,通过实时荧光定量PCR和蛋白质免疫印迹检测Wnt通路抑制剂APCDD1和活性β-连环蛋白的表达水平;同时在稳定表达Wnt3A的成纤维细胞中过表达APCDD1,验证其对Wnt通路的抑制作用。
实验结果显示,RNA测序结果显示三个纹蛋白敲低后APCDD1的表达均上调,其中zinedin敲低组上调最为显著(10.12倍);实时荧光定量PCR验证显示APCDD1 mRNA水平上调1.5~2.5倍(n=3,P<0.01),蛋白质免疫印迹结果显示APCDD1蛋白水平小幅但显著升高(n=3,P<0.05),同时活性β-连环蛋白水平仅出现轻微下降,提示纹蛋白敲低对Wnt通路的调控作用较弱,可能存在其他代偿调控机制。在Wnt3A过表达成纤维细胞中的验证实验显示,APCDD1过表达可显著降低活性β-连环蛋白水平,证实了APCDD1的Wnt通路抑制功能。
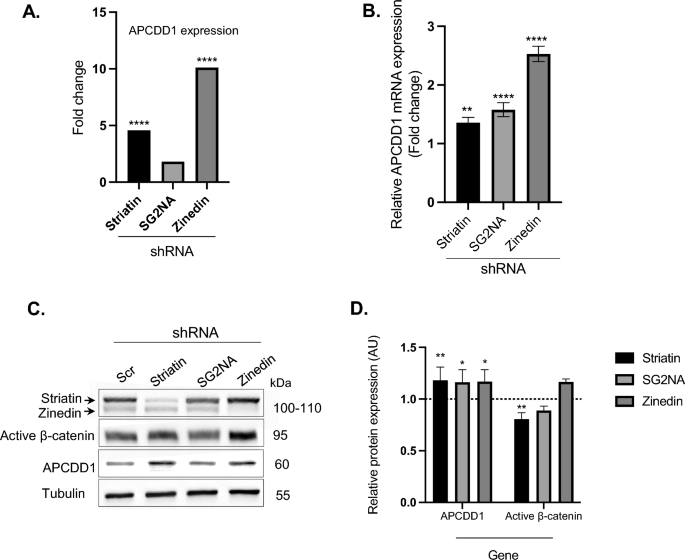
文献未提及具体实验产品,领域常规使用抗APCDD1抗体、抗活性β-连环蛋白抗体、基因过表达载体等试剂。
3.4 纹蛋白对Hippo通路的调控机制研究
本环节的核心目标是明确纹蛋白家族对Hippo信号通路的调控分子机制,揭示其对YAP蛋白的调控模式。实验首先通过RNA测序分析Hippo通路相关基因的表达变化,采用蛋白质免疫印迹检测Hippo通路核心组分YAP、磷酸化YAP(pYAP S127、pYAP S397)的表达水平;随后使用10μM蛋白酶体抑制剂MG132处理细胞4小时,验证pYAP的降解途径;通过质谱分析检测纹蛋白敲低后细胞内蛋白表达的变化,筛选潜在的互作或调控分子。
实验结果显示,纹蛋白敲低后总YAP水平无显著变化,但pYAP S127和pYAP S397的水平均显著下降(n=3,P<0.001),Hippo靶基因Axin2、Slug的mRNA表达也显著下调(n=3,P<0.05),提示纹蛋白调控Hippo通路不影响YAP的总表达,而是影响其磷酸化形式的稳定性;使用MG132抑制蛋白酶体活性后,pYAP的水平显著恢复,提示纹蛋白可保护pYAP免受蛋白酶体降解;质谱分析显示,STRN1或SG2NA敲低后14-3-3蛋白家族的表达下降,该蛋白可结合pYAP S127使其滞留在细胞质中,其表达下降可能促进pYAP的暴露和降解;进一步的泛素化检测实验显示,纹蛋白敲低后YAP的泛素化水平未发生变化,提示pYAP的降解可能通过泛素非依赖的蛋白酶体降解途径介导。
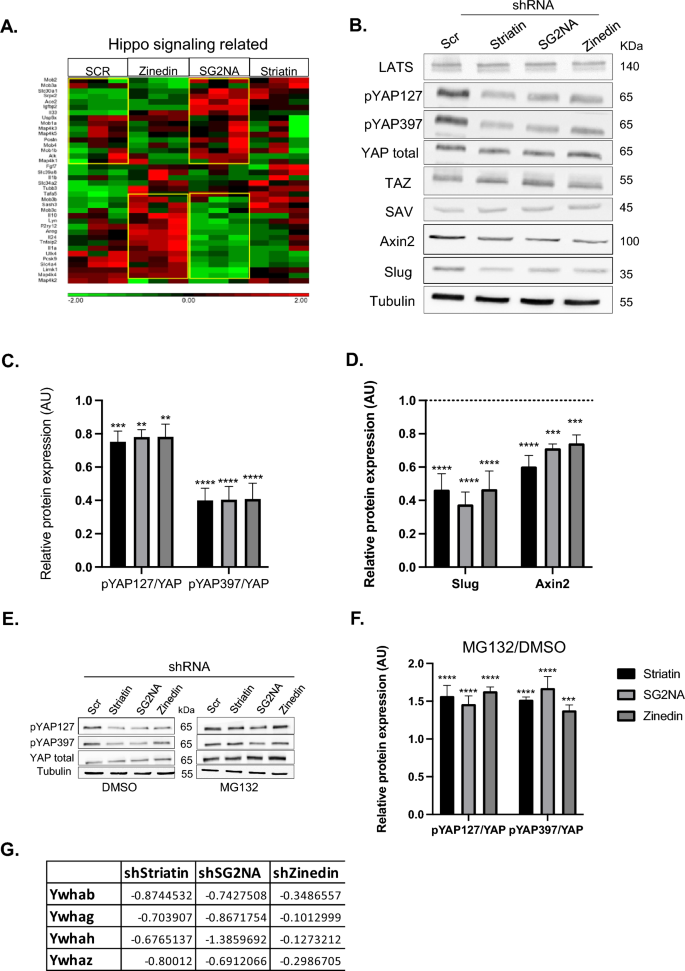
文献未提及具体实验产品,领域常规使用抗YAP抗体、抗磷酸化YAP抗体、蛋白酶体抑制剂MG132、泛素化检测试剂、质谱检测试剂等。
3.5 纹蛋白对细胞迁移和增殖的功能影响验证
本环节的核心目标是验证纹蛋白家族对细胞迁移和增殖的调控作用,明确其生物学功能效应。实验采用自动化伤口愈合实验检测细胞迁移能力,细胞接种至96孔板培养至汇合后,使用伤口制作仪制备划痕,每2小时拍摄图像持续24小时,通过Incucyte软件分析伤口闭合率;采用Ki-67免疫荧光染色检测细胞增殖水平,使用共聚焦显微镜拍摄图像后定量Ki-67阳性细胞比例。
实验结果显示,纹蛋白家族各成员敲低后,细胞在划痕后3~9小时的迁移速率显著降低(n=3);Ki-67染色结果显示,zinedin敲低后细胞增殖水平显著下降(n=3,P=0.0020),其余成员敲低后增殖也出现轻微下降,提示纹蛋白家族可正向调控细胞迁移和增殖,该功能可能通过调控Hippo通路下游靶基因的表达介导。
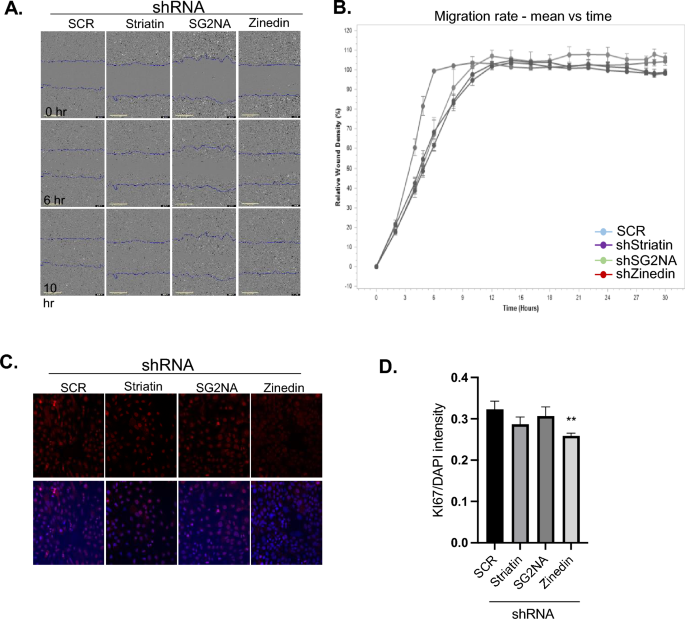
文献未提及具体实验产品,领域常规使用细胞培养耗材、抗Ki-67抗体、活细胞成像系统等。
4. Biomarker研究及发现成果
本研究涉及的功能相关标志物包括磷酸化YAP(pYAP S127、pYAP S397)、角蛋白16(KRT16)、APCDD1,其中pYAP是Hippo通路的核心效应标志物,其筛选验证逻辑为:基于纹蛋白作为STRIPAK核心组分与Hippo通路的关联假设→敲低纹蛋白后检测Hippo通路核心分子的表达变化→通过蛋白酶体抑制实验和互作蛋白分析验证调控机制→明确其与细胞功能的关联。
pYAP的检测样本为小鼠角质形成细胞的总蛋白,验证方法为蛋白质免疫印迹检测,特异性表现为纹蛋白敲低后pYAP水平特异性下降而总YAP水平无变化,使用MG132处理后pYAP水平恢复,统计学显示pYAP S127和pYAP S397的水平下降均具有显著性(n=3,P<0.001);KRT16的检测样本为角质形成细胞的RNA,验证方法为RNA测序和实时荧光定量PCR,结果显示三个纹蛋白敲低后KRT16的mRNA水平均显著上调(n=3~4,P<0.05),既往研究证实KRT16高表达可抑制角质形成细胞迁移,与本研究中纹蛋白敲低后细胞迁移能力下降的表型一致;APCDD1的检测样本同样为角质形成细胞,实时荧光定量PCR显示其mRNA水平上调1.5~2.5倍(n=3,P<0.01),其为已知的Wnt通路抑制剂。
核心成果方面,本研究证实磷酸化YAP的稳定性受纹蛋白家族正向调控,纹蛋白敲低后pYAP发生泛素非依赖的蛋白酶体降解,导致Hippo靶基因(Axin2、Slug)表达下调,进而抑制细胞迁移和增殖,该调控具有细胞特异性,在角质形成细胞中更为显著,该发现首次揭示了纹蛋白调控Hippo通路的新机制;KRT16在三种纹蛋白敲低的角质形成细胞中均上调,可能是纹蛋白调控细胞迁移的下游效应分子,可作为纹蛋白功能异常的潜在标志物;APCDD1在纹蛋白敲低后上调,可轻微抑制Wnt通路活性,但该调控效应较弱。推测:纹蛋白家族的表达水平可作为Hippo通路活性的潜在评估标志物,也有望成为皮肤损伤修复、Hippo通路异常相关肿瘤的治疗靶点。
