1. 领域背景与文献
文献英文标题:Melatonin reduces lung injury in type 1 diabetic mice by the modulation of autophagy;发表期刊:BMC Molecular and Cell Biology;影响因子:未公开;研究领域:糖尿病并发症调控、自噬机制研究、内分泌与呼吸系统交叉研究。
领域共识:1型糖尿病是一类由自身免疫攻击胰岛β细胞导致胰岛素绝对缺乏的慢性代谢疾病,长期高糖状态可诱发多器官慢性并发症,既往研究多聚焦于心脑血管、肾脏、神经等系统损伤,对肺组织损伤的关注相对较少。肺组织富含弹性蛋白、胶原成分及丰富的动脉血管床,在高糖诱导的氧化应激与慢性炎症环境中更易发生结构与功能损伤,但目前糖尿病诱发肺损伤的具体分子机制尚未完全明确。自噬作为细胞维持内环境稳态的关键分解代谢途径,可通过降解受损细胞器与错误折叠蛋白维持细胞功能,领域共识:自噬活性失调与糖尿病、炎症性肺疾病的发生发展密切相关,但自噬在1型糖尿病肺损伤中的具体作用及调控机制仍缺乏充分实验证据。褪黑素是松果体分泌的神经内分泌激素,已被证实具有抗炎、抗氧化、调控自噬的多重生物学效应,但其对1型糖尿病肺损伤的保护作用及相关机制尚未得到验证,本研究针对这一研究空白,通过构建1型糖尿病小鼠模型,探究褪黑素对肺损伤的改善效应及与自噬通路的相关性,为糖尿病肺并发症的干预提供新的实验依据。
2. 文献综述解析
本研究文献综述部分按照“糖尿病并发症特征→自噬的疾病调控作用→褪黑素的治疗潜力”的逻辑展开,对现有研究进行分类梳理。
现有支持性研究结论显示,1型糖尿病状态下的持续高血糖可通过激活氧化应激、促进促炎因子释放,诱导全身多组织器官的病理损伤,临床研究已证实糖尿病患者的肺功能下降风险显著高于健康人群。在技术方法层面,链脲佐菌素诱导的小鼠1型糖尿病模型可稳定模拟临床高血糖病理特征,是目前糖尿病并发症研究的常用体内模型;通过检测Becline-1、LC3、P62三个核心基因的表达,可有效反映细胞自噬流的激活状态,该方法在自噬相关研究中应用广泛。现有研究的局限性主要体现在:多数研究聚焦于自噬在糖尿病心肌病、糖尿病肾病等并发症中的作用,针对肺损伤的自噬调控机制研究较为匮乏;褪黑素对糖尿病多器官损伤的保护效应已得到验证,但尚未有研究明确其对1型糖尿病肺损伤的作用是否与自噬通路调控相关,缺乏对应的体内实验证据支撑。本研究的创新价值在于首次在1型糖尿病小鼠模型中验证了褪黑素对肺组织自噬活性的调控作用,明确了褪黑素减轻肺病理损伤的效应与自噬相关基因、炎症因子表达下调的相关性,填补了该领域的研究空白,为褪黑素在糖尿病肺并发症中的临床应用提供了前期实验基础。
3. 研究思路总结与详细解析
本研究的核心目标是明确褪黑素对1型糖尿病小鼠肺损伤的保护作用,核心科学问题是褪黑素是否通过调控自噬通路减轻糖尿病诱导的肺组织炎症与病理损伤,技术路线遵循“动物模型构建→干预处理→表型验证→分子机制检测”的闭环逻辑,通过设置不同处理组的对照分析,明确褪黑素的干预效应与潜在作用机制。
3.1 动物模型构建与分组干预
实验目的:构建稳定的1型糖尿病小鼠模型,确定褪黑素的干预方案,为后续效应验证提供可靠的动物基础。
方法细节:选用32只初始体重25-30g的小鼠,适应性饲养10天后随机分为4组,每组样本量n=8:对照组仅给予常规饮食与饮水;褪黑素对照组按3mg/kg剂量腹腔注射褪黑素,每周2次,持续4周;糖尿病组小鼠禁食8小时后,单次腹腔注射50mg/kg链脲佐菌素诱导1型糖尿病,注射72小时后尾静脉采集空腹血,采用血糖仪检测血糖,血糖水平≥250mg/dL判定为造模成功;糖尿病+褪黑素组在造模成功2周后,按3mg/kg剂量腹腔注射褪黑素,每周2次,持续4周。末次干预结束48小时后,采用过量麻醉法处死小鼠,分离肺组织,右肺用于组织病理分析,左肺用于基因表达检测。实验所用关键产品:链脲佐菌素、褪黑素均购自Sigma-Aldrich公司,RNA提取试剂盒、cDNA合成试剂盒、SYBR Green荧光定量试剂盒均购自Yekta Tajhiz Azma公司。
结果解读:链脲佐菌素注射后糖尿病组小鼠血糖显著升高,符合1型糖尿病的病理特征,分组方案可有效区分不同处理条件下的小鼠表型,保障后续实验结果的可靠性。
3.2 血糖水平检测与肺组织病理分析
实验目的:验证褪黑素对糖尿病小鼠血糖的调控效应,以及对肺组织病理损伤的改善作用。
方法细节:分别在造模后、干预结束后检测各组小鼠的空腹血糖水平;取右肺组织经10%福尔马林固定后,常规脱水、石蜡包埋,制备5μm厚度的组织切片,采用苏木精-伊红染色,光镜下观察肺组织的病理变化,评估细支气管上皮变性、间质性肺炎、炎症细胞浸润等损伤程度。
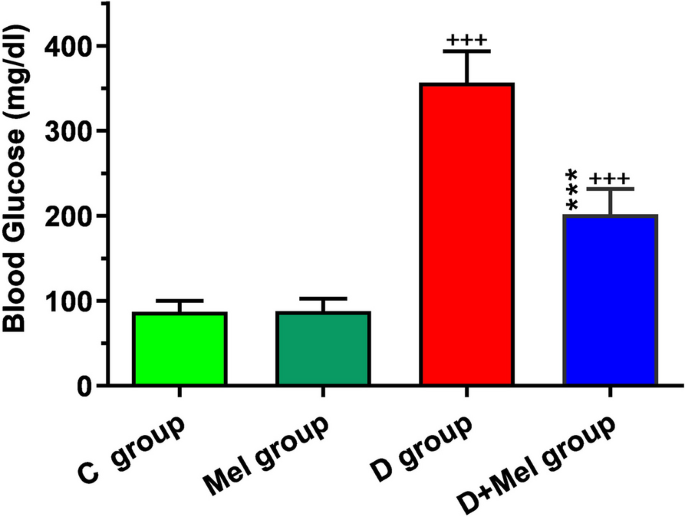
结果解读:干预结束后血糖检测结果显示,与对照组相比,糖尿病组小鼠空腹血糖水平显著升高(n=8,P<0.001);与糖尿病组相比,糖尿病+褪黑素组小鼠血糖水平显著降低(n=8,P<0.001),对应结果如图所示:
肺组织苏木精-伊红染色结果显示,对照组与褪黑素对照组小鼠肺组织结构完整,无明显病理损伤;糖尿病组小鼠肺组织出现明显的间质性肺炎,可见细支气管上皮变性、大量炎症细胞浸润等病理改变;糖尿病+褪黑素组小鼠肺组织的间质性肺炎程度明显减轻,病理损伤得到显著改善,对应染色结果如图所示:
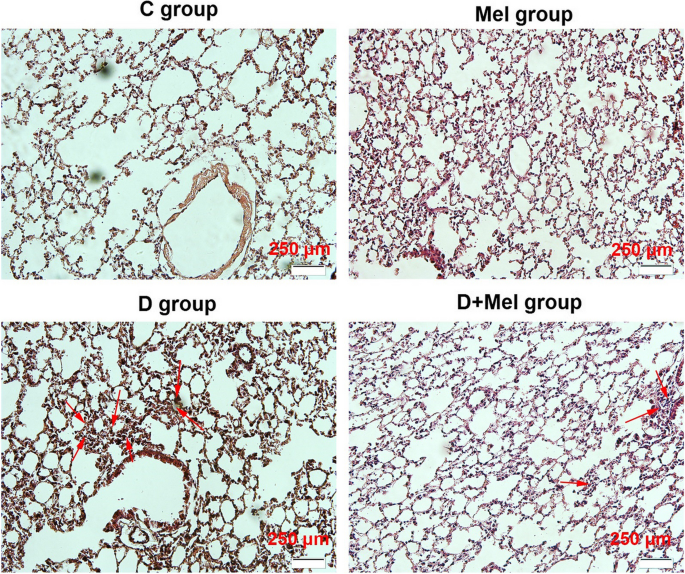
褪黑素对照组与对照组相比,血糖水平及肺组织病理状态均无显著差异(P>0.05),提示单纯褪黑素干预对正常小鼠无明显不良影响。
3.3 肺组织炎症因子与自噬相关基因表达检测
实验目的:探究褪黑素对糖尿病小鼠肺组织炎症反应及自噬活性的调控作用,明确其发挥肺保护作用的分子机制。
方法细节:取左肺组织置于液氮中研磨,按照试剂盒说明书提取总RNA,经Nanodrop分光光度计检测RNA纯度与浓度后,采用反转录试剂盒合成cDNA,通过实时荧光定量PCR检测炎症因子IL-6,以及自噬相关基因Becline-1、LC3、P62的mRNA表达水平,以GAPDH为内参基因,采用2-ΔΔCT法计算各基因的相对表达量。
结果解读:炎症因子IL-6的检测结果显示,与对照组相比,糖尿病组小鼠肺组织IL-6 mRNA表达显著上调(n=8,P<0.001),提示糖尿病状态下肺组织存在明显炎症反应;与糖尿病组相比,糖尿病+褪黑素组IL-6 mRNA表达显著下调(n=8,P<0.05),对应结果如图所示:
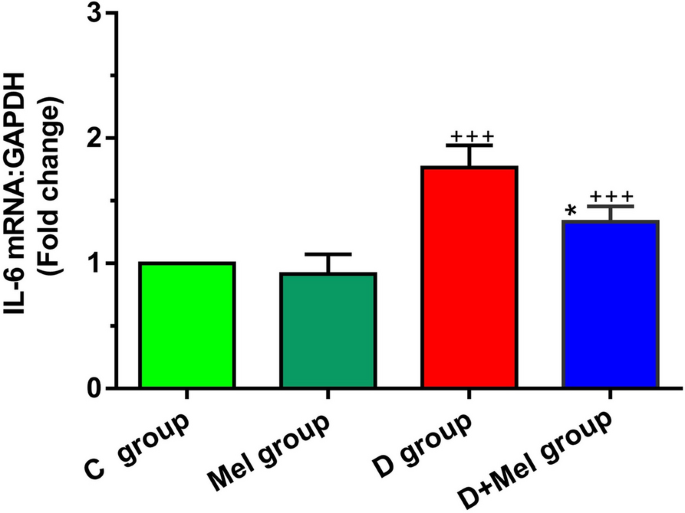
自噬相关基因的检测结果显示,与对照组相比,糖尿病组小鼠肺组织Becline-1、LC3、P62的mRNA表达均显著上调(n=8,P<0.001),提示糖尿病状态下肺组织自噬流过度激活;与糖尿病组相比,糖尿病+褪黑素组上述三个自噬相关基因的表达均显著下调(Becline-1:P<0.01,LC3:P<0.001,P62:P<0.01),且表达水平与对照组无显著差异(P>0.05),对应结果如图所示:
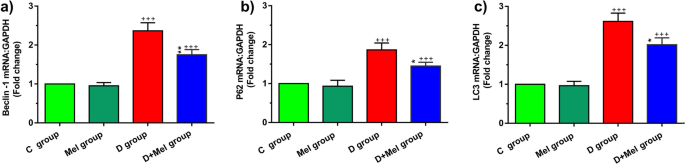
褪黑素对照组与对照组相比,上述基因的表达均无显著差异(P>0.05),进一步验证了单纯褪黑素干预对正常小鼠肺组织的炎症及自噬状态无明显影响。
4. Biomarker 研究及发现成果
本研究涉及的生物标志物包括炎症标志物IL-6,以及自噬活性标志物Becline-1、LC3、P62,筛选验证逻辑为“1型糖尿病模型构建→褪黑素干预→肺组织样本采集→基因表达检测→组间差异关联分析”,明确上述标志物与糖尿病肺损伤及褪黑素干预效应的相关性。
上述生物标志物的检测样本为小鼠肺组织,验证方法为实时荧光定量PCR。其中炎症标志物IL-6在糖尿病组肺组织中的表达较对照组上调超过3倍(n=8,P<0.001),褪黑素干预后较糖尿病组下调约25%(n=8,P<0.05),其表达水平与肺组织炎症损伤程度呈正相关,可有效反映糖尿病诱导的肺组织炎症状态。自噬相关标志物Becline-1、LC3、P62在糖尿病组中的表达较对照组分别上调约2.1倍、2.8倍、2.3倍(n=8,P均<0.001),三个标志物同步升高提示糖尿病状态下肺组织自噬流过度激活;褪黑素干预后三者较糖尿病组分别下调约35%、45%、38%(n=8,P均<0.01),其表达水平与肺组织病理损伤的严重程度呈正相关。
核心成果方面,本研究首次证实1型糖尿病小鼠肺组织中IL-6、Becline-1、LC3、P62的表达同步上调,且褪黑素干预可同时降低上述标志物的表达水平并减轻肺病理损伤,提示上述标志物联合检测可作为1型糖尿病肺损伤的潜在评估指标,同时也可反映褪黑素的干预效果。本研究未检测上述标志物的诊断敏感性与特异性(文献未明确提供该数据,基于图表趋势推测该组合标志物对糖尿病肺损伤的评估具有潜在临床应用价值)。此外,本研究结果提示褪黑素可能通过抑制过度自噬与炎症反应发挥糖尿病肺损伤保护作用,为后续深入研究其调控机制提供了方向。