1. 领域背景与文献
文献英文标题:Optimizing mesenchymal stem cell therapy: from isolation to GMP-compliant expansion for clinical application;发表期刊:BMC Molecular and Cell Biology;影响因子:未公开;研究领域:再生医学·间充质干细胞治疗工艺开发。
领域共识,间充质干细胞(MSC)因具有多向分化潜能、免疫调节功能及低免疫原性,是当前细胞治疗与再生医学领域的核心研究方向。自20世纪60年代首次在骨髓中被发现以来,MSC的基础研究与临床转化经历了多个关键节点:2000年前后MSC的分离培养技术逐步成熟,2010年后大量MSC临床研究启动,2023年美国FDA首次批准MSC产品Ryoncil用于儿童类固醇难治性急性移植物抗宿主病,标志着MSC治疗进入临床应用阶段。当前领域研究热点包括新型MSC来源开发、无血清无动物源培养体系优化、生产工艺的良好生产规范(GMP)标准化三大方向。
现有研究仍存在多个未解决的核心问题:一是传统骨髓来源MSC的提取为有创操作,患者依从性低,且细胞产量与活性存在较高供体异质性;二是多数实验室级MSC培养体系使用胎牛血清等动物源性成分,存在外源性污染风险与批次不一致性,不符合临床用药的申报要求;三是针对新型MSC来源(如脂肪组织来源)的GMP生产工艺研究较少,缺乏完整的全流程验证数据,制约了其临床转化进度。本研究针对上述空白,以髌下脂肪垫来源MSC(FPMSC)为研究对象,旨在开发无动物源、符合GMP规范的分离、扩增、储存全流程工艺,为MSC治疗的临床转化提供标准化的工艺范式。
2. 文献综述解析
作者在综述部分按照“细胞来源→现有培养体系缺陷→GMP转化瓶颈”的逻辑维度梳理现有研究进展,明确本研究的创新定位。
现有研究的核心支持观点包括:骨髓来源MSC是当前临床研究的金标准细胞,已在骨关节炎、组织损伤修复、自身免疫病等多个适应症中显示出治疗潜力;无动物源成分的培养基可有效降低动物源病原体污染风险,减少批次异质性,是MSC培养体系的核心优化方向;GMP级生产工艺的标准化是MSC产品获批上市的核心前提。现有技术的优势体现为:传统含胎牛血清的MSC培养体系技术成熟,可稳定支持细胞增殖,已在大量基础研究中得到应用;部分骨髓来源MSC的GMP生产工艺已初步通过验证,为其他来源MSC的工艺开发提供了参考框架。现有研究的局限性包括:骨髓采集的侵入性限制了其大规模临床应用,且骨髓MSC的增殖能力随供体年龄升高显著下降;含血清培养体系无法满足临床用药的安全性要求,且现有无动物源培养基的性能参差不齐,缺乏针对FPMSC的适配性验证;FPMSC作为手术废弃物来源的新型MSC,现有研究多集中在基础功能层面,缺乏完整的GMP全流程验证数据,无法直接用于临床产品开发。
本研究的创新价值体现在三个层面:一是首次系统对比两种商用无动物源培养基对FPMSC增殖、干性维持的影响,筛选出性能最优的培养基配方;二是首次建立了从FP样本采集、消化、扩增、冻存到质量控制的全流程GMP级FPMSC生产工艺,填补了该领域的工艺空白;三是验证了该工艺的多供体适用性与长期冻存稳定性,为后续FPMSC的临床申报提供了完整的工艺数据支持。
3. 研究思路总结与详细解析
本研究的核心目标是构建可用于临床的GMP级FPMSC生产工艺,核心科学问题为“无动物源培养基是否可在支持FPMSC高效增殖的同时维持其干性特征,以及全流程GMP工艺的可行性与稳定性”,整体技术路线遵循“实验室级培养基筛选→工艺参数优化→GMP级工艺验证→稳定性评估”的闭环逻辑,所有实验数据采用单因素方差分析与Tukey多重比较进行统计学检验。
3.1 无动物源培养基筛选与性能验证
本环节的实验目的是筛选可高效支持FPMSC增殖与干性维持的无动物源培养基,为后续GMP工艺开发奠定基础。方法细节:纳入3例接受前交叉韧带重建手术患者的髌下脂肪垫废弃物样本,分离获得原代FPMSC后,分别在三种培养基中连续传代培养:含10%胎牛血清的标准MSC培养基、MesenCult™-ACF Plus无动物源培养基、MSC-Brew GMP无动物源培养基,分别在第2、3、4代检测细胞倍增时间,通过集落形成单位(CFU)实验评估细胞干性,采用流式细胞术(FCM)检测MSC特征表面标志物(CD45⁻、CD73⁺、CD90⁺、CD105⁺)的阳性比例。
结果解读:倍增时间检测结果显示,MSC-Brew GMP培养基培养的FPMSC在三个代次的倍增时间均显著低于标准培养基组与MesenCult™-ACF Plus组(n=3,P<0.05),提示其增殖效率最高,对应的倍增时间统计结果与细胞形态图见下图:
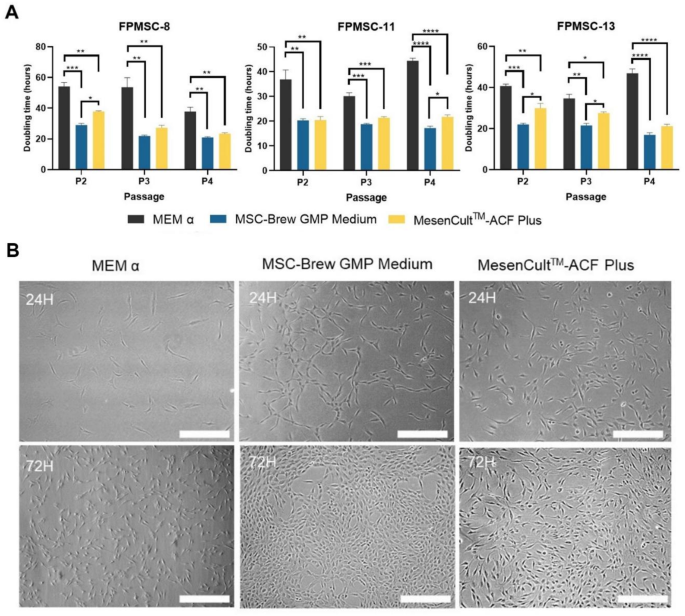
CFU实验结果显示,MSC-Brew GMP组的集落形成数量显著高于另外两组(n=3,P<0.01),且结晶紫染色显示集落细胞密度更高,提示其干性维持能力更优,对应的CFU统计结果与染色图见下图:
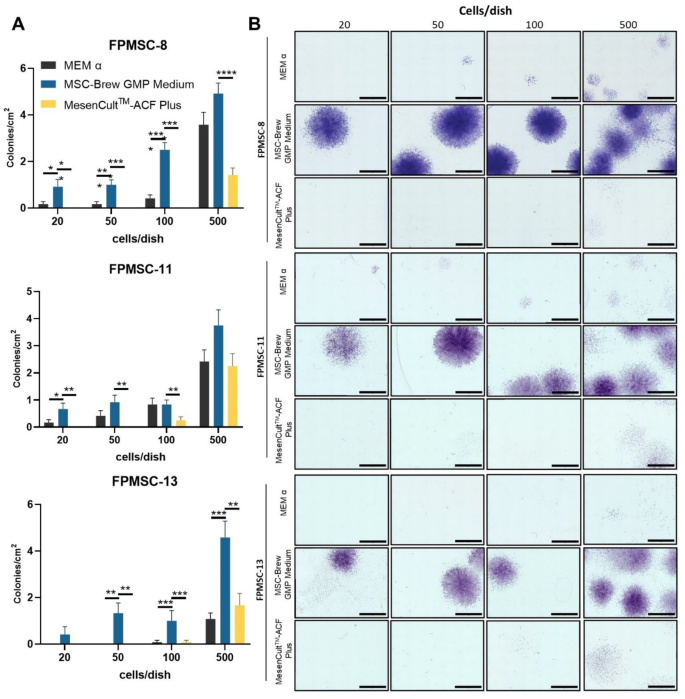
流式细胞术检测结果显示,MSC-Brew GMP组的CD45⁻CD73⁺CD90⁺CD105⁺细胞比例符合国际细胞与基因治疗学会(ISCT)的MSC鉴定标准,且显著高于MesenCult™-ACF Plus组(n=3,P<0.001),对应的流式检测结果与门控策略见下图:
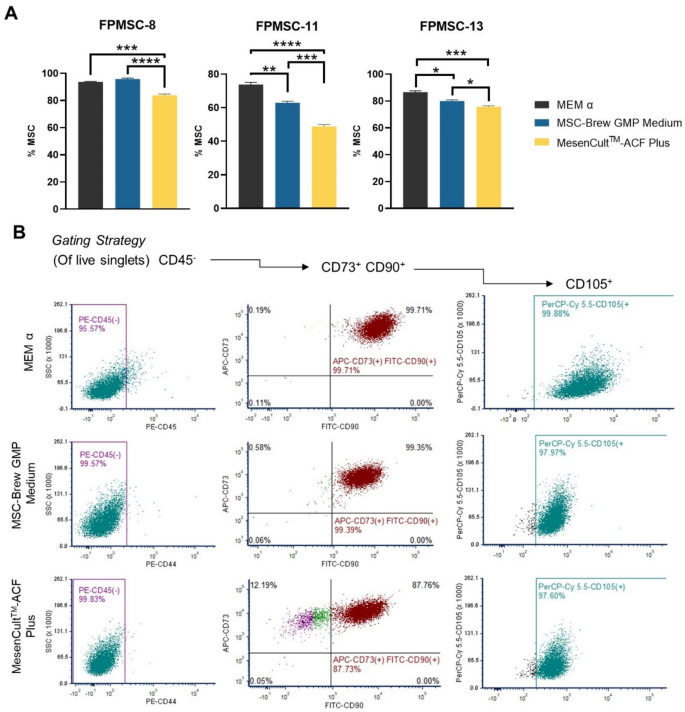
实验所用关键产品:Miltenyi Biotec的MSC-Brew GMP培养基(货号170-076-325)、StemCell Technologies的MesenCult™-ACF Plus培养基(货号05447)、BD的人MSC分析试剂盒(货号562245)、MilliporeSigma的结晶紫染液(货号V5265)。
3.2 GMP级FPMSC生产工艺建立与验证
本环节的实验目的是基于筛选得到的最优培养基,建立符合GMP规范的FPMSC全流程生产工艺,并验证其合规性与可重复性。方法细节:纳入4例额外的供体髌下脂肪垫样本,在经细胞治疗基金会(FACT)认证的细胞治疗中心开展GMP生产,使用GMP级胶原酶NB 6消化脂肪组织,采用MSC-Brew GMP培养基进行扩增,使用无动物源的TrypLE™试剂进行细胞解离,扩增至第1代时转入5层细胞工厂进行规模化培养,达到80%~90%汇合度后收集细胞,采用无血清无蛋白冻存液CS10(含10%二甲基亚砜)以-2℃/min的可控速率降温冻存,全程设置多个质量控制节点,分别检测内毒素水平、无菌性、支原体污染、细胞活率、MSC表面标志物、HLA-DR表达水平,确保符合细胞产品放行标准。
结果解读:本工艺可从18±3.83ml的髌下脂肪垫样本中,在20天内获得1~2×10⁸个FPMSC,细胞活率>95%(n=4);所有4个供体批次的质量检测结果均符合放行标准:内毒素水平≤5EU/kg/hr,无菌检测、支原体检测均为阴性,HLA-DR表达水平<5%,MSC表面标志物阳性率>95%,提示工艺具有良好的可重复性与合规性,对应的GMP生产全流程见下图:
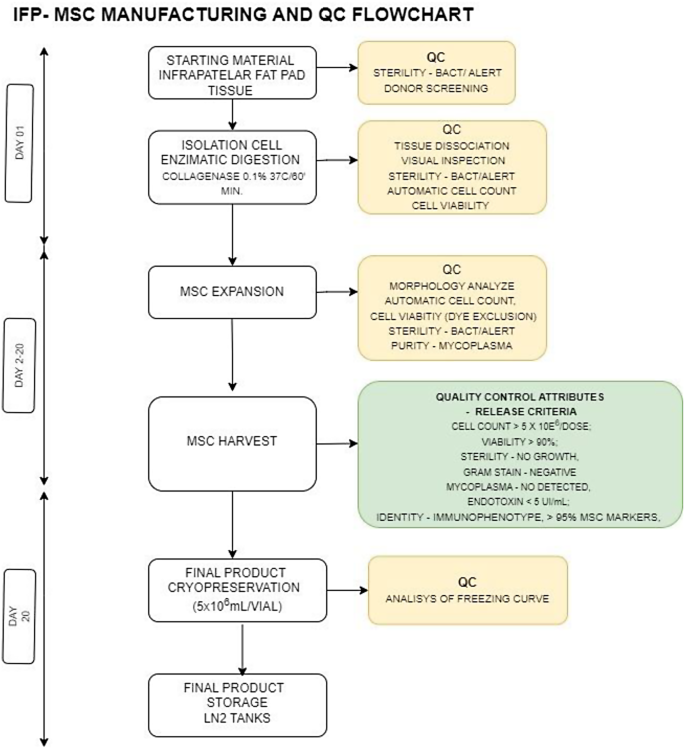
实验所用关键产品:Nordmark的GMP级胶原酶NB 6(货号N0002779)、Gibco的TrypLE™解离液(货号12604013)、康宁的5层细胞工厂(货号3311)、Biolife Solutions的CS10冻存液(货号210202)、Cytiva的程控降温仪(VIA Freeze System)。
3.3 GMP级FPMSC稳定性验证
本环节的实验目的是评估GMP级FPMSC的长期冻存稳定性,以及解冻后的临床使用窗口期,为临床应用提供操作依据。方法细节:将制备得到的GMP级FPMSC置于液氮气相中储存,分别在储存85天、225天后解冻,检测细胞活率与MSC表面标志物表达;另外将解冻后的细胞置于2~8℃条件下储存,每小时检测一次细胞活率,评估其稳定性以确定临床使用窗口期。
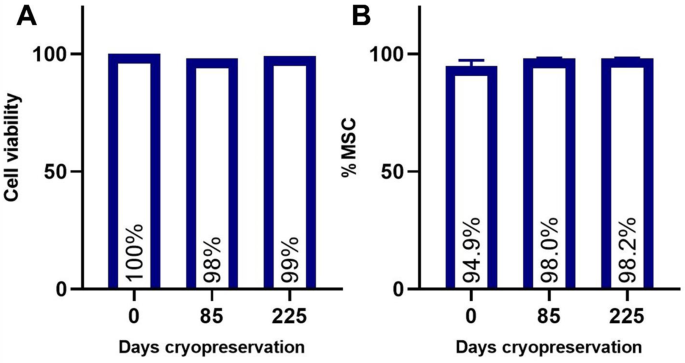
结果解读:冻存85天、225天后的FPMSC活率均维持在95%以上,MSC表面标志物阳性率仍>95%,与冻存前相比无显著统计学差异(n=4,P>0.05),提示长期冻存不会影响细胞的活性与干性特征;解冻后的细胞在2~8℃条件下储存4小时内,活率仍高于70%的最低放行标准,因此确定临床使用窗口期为解冻后4小时内,对应的冻存后细胞活率与标志物检测结果见下图:
文献未提及本环节的额外实验产品,领域常规使用液氮气相存储罐、2~8℃医用冷藏箱开展细胞储存与稳定性测试。
推测:本研究建立的GMP工艺可直接扩展至更大规模的临床级FPMSC生产,后续需开展多中心、大样本量的批次一致性验证,以及MSC多向分化潜能、体内安全性的进一步评估,以满足临床申报的要求。
4. Biomarker研究及发现成果
本研究涉及的Biomarker为FPMSC的质量控制标志物组合,属于细胞表面标志物类,其筛选与验证逻辑遵循“国际标准引入→实验室级验证→GMP生产全流程验证→稳定性验证”的完整链条。
该标志物组合基于ISCT发布的MSC鉴定标准确定,具体包括阳性标志物CD73、CD90、CD105,阴性标志物CD45、HLA-DR。标志物的检测样本覆盖了培养基筛选阶段的细胞、GMP生产各节点的细胞、冻存前后的细胞、解冻后储存不同时间的细胞,检测方法为流式细胞术。特异性数据显示,该标志物组合可有效区分MSC与血液细胞、成纤维细胞等杂细胞,所有GMP生产批次的阳性标志物表达率>95%,阴性标志物CD45表达率<2%,HLA-DR表达率<5%,符合临床细胞产品的质控要求;敏感性数据显示,流式检测的标志物阳性率变异系数<5%,可稳定反映细胞的纯度与干性特征。
核心成果方面,该标志物组合可作为GMP级FPMSC的标准化放行质控指标,所有4个供体批次的检测结果均符合标准,且细胞在冻存225天后仍维持标志物的稳定表达(n=4,P>0.05),提示其可用于全生产流程的质量监控。本研究的创新性在于首次将该标志物组合系统应用于FPMSC的GMP生产全流程质量控制,为后续FPMSC的临床申报提供了统一的质控标准,弥补了现有FPMSC质控体系缺失的空白。