1. 领域背景与文献
文献英文标题:Casein kinase 2 maintains the self-renewal of neural stem cells via prospero phosphorylation in Drosophila;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:发育神经生物学(神经干细胞时序调控方向)。
领域共识:神经干细胞的自我更新与分化时序调控是中枢神经系统正常发育的核心基础,1992年研究者首次证实成体哺乳动物中枢神经系统中存在具有多向分化潜能的神经干细胞,后续研究明确其种群动态具有严格的时间窗口特征:胚胎早期神经干细胞快速扩增,神经发生阶段种群数量维持稳定,随后逐步耗竭,仅在海马、侧脑室下区等特定脑区保留少量成体神经干细胞。该时序调控过程的紊乱会导致神经元数量异常,诱发小头畸形、癫痫等多种神经发育障碍疾病。果蝇的神经干细胞又称成神经细胞,是研究神经干细胞时序调控的经典模式生物,其种群动态与哺乳动物高度保守:约90个成神经细胞从胚胎期维持至幼虫晚期,蛹期启动终末分化并逐步清除,成年果蝇脑中无成神经细胞残留。
现有研究已明确蜕皮激素信号、Hedgehog通路、时序转录因子Castor等上游调控分子参与成神经细胞的终末分化启动,也证实分化促进因子普罗斯佩罗蛋白(Pros)的亚细胞定位是成神经细胞命运决定的核心开关:幼虫期普罗斯佩罗蛋白通过米兰达蛋白锚定在细胞质中,转录活性被抑制;蛹期普罗斯佩罗蛋白进入细胞核,启动分化相关基因表达。但现有研究仍存在两个核心空白:一是普罗斯佩罗蛋白亚细胞定位的翻译后修饰调控机制尚未阐明,二是控制成神经细胞自我维持时间窗口的核心效应分子仍不明确。本研究针对上述空白,聚焦保守丝氨酸/苏氨酸激酶酪蛋白激酶2(CK2)的功能,揭示其通过磷酸化修饰调控普罗斯佩罗蛋白定位的新机制,为神经发育时序调控领域提供了新的分子靶点。
2. 文献综述解析
作者的文献综述按照调控层级分为三个维度展开,系统梳理了现有研究的进展与局限性。
第一类是成神经细胞命运决定的核心调控因子研究,现有研究已明确普罗斯佩罗蛋白是进化保守的同源盒转录因子,作为二元开关调控神经干细胞的自我更新与分化命运,其亚细胞定位直接决定功能活性,这类研究为成神经细胞命运调控提供了核心靶标,但对其定位调控的分子机制,尤其是翻译后修饰的作用认知十分有限。第二类是成神经细胞时序调控的上游信号研究,现有研究发现蜕皮激素通过中介复合物调控能量代谢重编程,使成神经细胞周期停滞并启动分化,还有时序转录因子Castor与Hedgehog信号协同促进普罗斯佩罗蛋白入核,这类研究揭示了上游信号的调控作用,但缺乏直接的下游效应分子机制解析。第三类是酪蛋白激酶2的生理功能研究,酪蛋白激酶2是真核生物中保守的丝氨酸/苏氨酸激酶,在中枢神经系统中广泛表达,参与胚胎脑发育过程,其功能异常与Okur-Chung综合征、癫痫等人类神经发育疾病密切相关,已有研究证实酪蛋白激酶2参与白血病干细胞、间充质干细胞的干性维持,但其在神经干细胞时序调控中的作用尚未被报道。
作者通过对比现有研究的局限性,凸显本研究的创新价值:首次将酪蛋白激酶2与成神经细胞的时序维持关联,明确了普罗斯佩罗蛋白的磷酸化修饰对其亚细胞定位的调控作用,填补了翻译后修饰层面调控成神经细胞自我更新时间窗口的研究空白,同时为酪蛋白激酶相关神经发育疾病的病理机制解析提供了新的理论依据。
3. 研究思路总结与详细解析
本研究的整体框架遵循“表型发现→时间窗口确定→分子机制解析→保守性验证”的闭环逻辑,研究目标是揭示成神经细胞自我更新时间窗口的分子调控机制,核心科学问题是酪蛋白激酶2是否通过翻译后修饰调控普罗斯佩罗蛋白的功能,进而参与成神经细胞的时序维持。研究首先通过基因操作明确酪蛋白激酶2对成神经细胞维持的功能及作用时间窗口,随后通过细胞定位、蛋白互作、点突变实验验证酪蛋白激酶2对普罗斯佩罗蛋白的磷酸化调控作用,最后在人脑类器官模型中验证该调控机制的进化保守性。
3.1 酪蛋白激酶2调控成神经细胞维持的表型鉴定
实验目的:明确酪蛋白激酶2是否参与果蝇成神经细胞的维持过程,并确定其发挥功能的时间窗口。
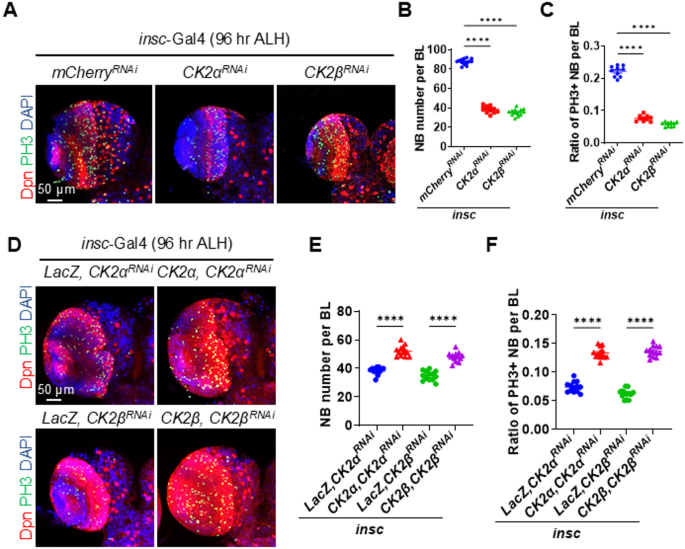
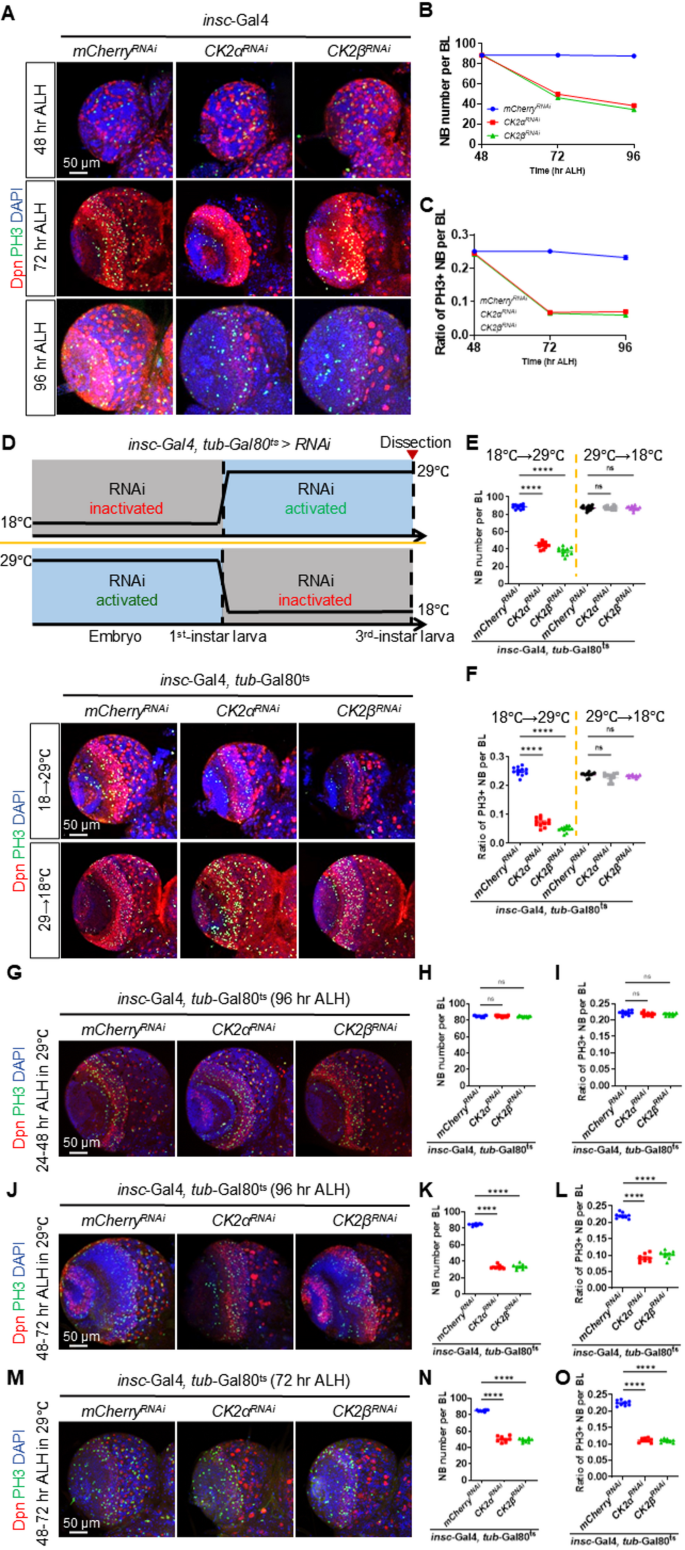
方法细节:采用成神经细胞特异性驱动子insc-GAL4介导的RNA干扰技术,分别敲低酪蛋白激酶2的催化亚基(CK2α)和调节亚基(CK2β),通过免疫组化检测神经干细胞核标志物Deadpan、增殖标志物磷酸化组蛋白H3(PH3)的表达,统计成神经细胞的数量和增殖率;同时采用多株独立RNA干扰株、过表达回复实验验证表型的特异性;利用温度敏感型GAL80系统实现时序特异性基因敲低,精确确定酪蛋白激酶2发挥功能的发育阶段;通过免疫印迹和免疫组化检测酪蛋白激酶2在不同发育阶段的蛋白表达水平。
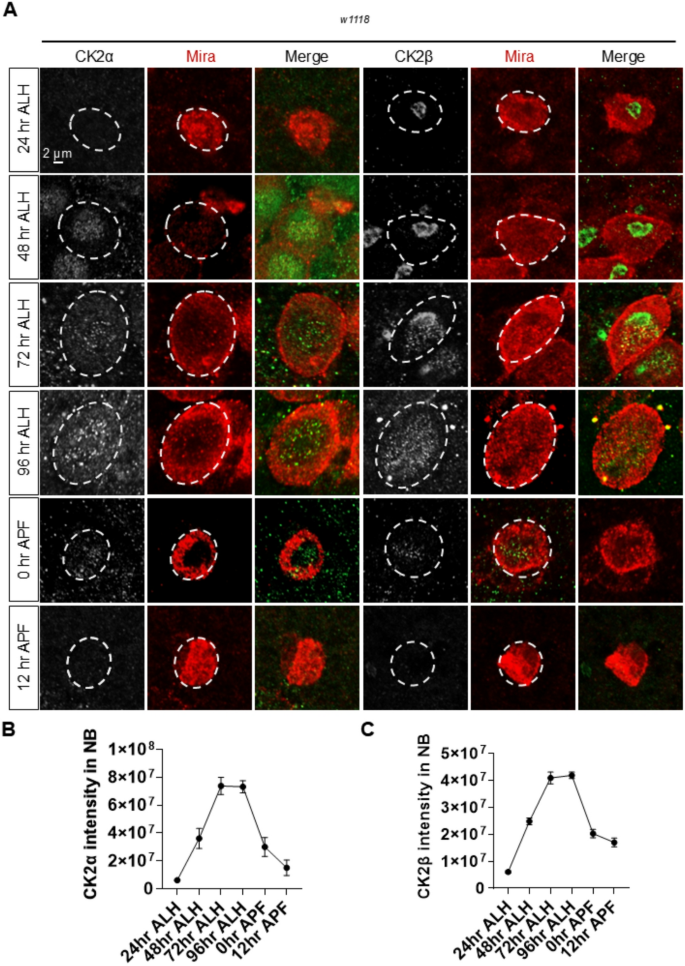
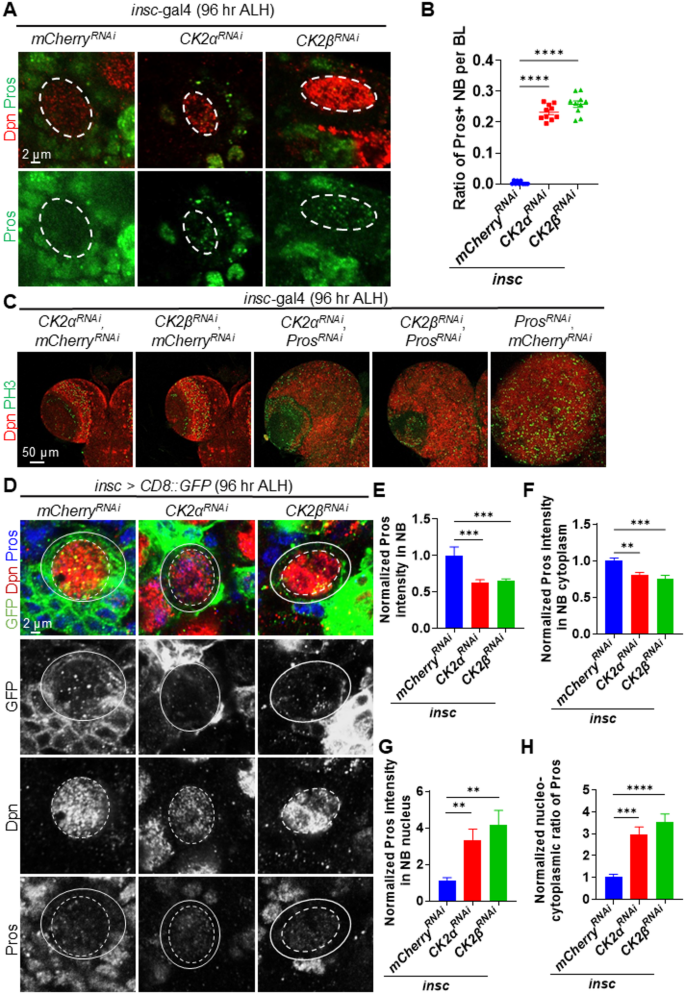
结果解读:免疫荧光结果显示,第三龄幼虫期酪蛋白激酶2敲低组成神经细胞数量较对照组降低约50%(n=13,P<0.0001),增殖率降低约40%(n=10,P<0.0001),该表型可通过过表达对应酪蛋白激酶2亚基完全回复,证实表型特异性。时序敲低实验显示,仅在幼虫孵化后48-72小时敲低酪蛋白激酶2会导致成神经细胞数量减少,早于或晚于该时间窗口均无显著异常,证实酪蛋白激酶2仅在幼虫晚期发挥成神经细胞维持功能。免疫印迹和免疫组化结果显示,酪蛋白激酶2的蛋白表达水平从幼虫早期到晚期逐步升高,在幼虫晚期达到峰值,蛹期显著下降,与其功能窗口完全吻合。
产品关联:实验所用关键产品:Developmental Studies Hybridoma Bank(DSHB)的普罗斯佩罗蛋白抗体(货号MR1A)、Cell Signaling Technology(CST)的磷酸化组蛋白H3抗体(货号9701)、Abcam的米兰达蛋白抗体(货号ab197788);果蝇品系来自布鲁明顿果蝇资源中心、维也纳果蝇资源中心等公共库。
3.2 酪蛋白激酶2敲低导致成神经细胞提前分化的机制验证
实验目的:明确酪蛋白激酶2敲低导致成神经细胞丢失的细胞生物学机制,排除凋亡的作用,验证普罗斯佩罗蛋白为下游效应分子。
方法细节:通过免疫组化检测凋亡标志物半胱天冬酶1(Dcp-1)的表达,同时通过过表达凋亡抑制因子P35或敲低半胱天冬酶1,验证凋亡是否参与表型发生;通过免疫荧光共定位检测普罗斯佩罗蛋白的亚细胞定位,统计其核质分布比例;通过普罗斯佩罗蛋白敲低的回复实验,验证普罗斯佩罗蛋白是否为酪蛋白激酶2的下游效应分子。
结果解读:免疫荧光结果显示,酪蛋白激酶2敲低组的成神经细胞中半胱天冬酶1阳性率与对照组无显著差异(文献未明确提供该数据,基于图表趋势推测无统计学意义),且抑制凋亡无法回复成神经细胞丢失表型,排除凋亡介导的细胞清除作用。普罗斯佩罗蛋白的亚细胞定位分析显示,对照组幼虫晚期成神经细胞中几乎无核定位的普罗斯佩罗蛋白,而酪蛋白激酶2敲低组中核定位普罗斯佩罗蛋白的成神经细胞比例升高至约35%(n=10,P<0.01),胞质普罗斯佩罗蛋白水平降低约40%(n=19,P<0.001),核质比升高约2.1倍(n=17,P<0.0001);同时敲低普罗斯佩罗蛋白可完全回复酪蛋白激酶2敲低导致的成神经细胞丢失表型,证实酪蛋白激酶2通过抑制普罗斯佩罗蛋白入核维持成神经细胞的自我更新能力。
产品关联:实验所用关键产品:CST的半胱天冬酶1抗体(货号9578);其余试剂与3.1一致。
3.3 酪蛋白激酶2磷酸化普罗斯佩罗蛋白调控其定位的分子机制解析
实验目的:明确酪蛋白激酶2是否通过磷酸化修饰调控普罗斯佩罗蛋白的亚细胞定位,确定磷酸化修饰对普罗斯佩罗蛋白功能的影响。
方法细节:通过免疫共沉淀实验检测内源性酪蛋白激酶2与普罗斯佩罗蛋白的相互作用;通过核质分离实验提取成神经细胞的胞质蛋白,采用碱性磷酸酶处理检测普罗斯佩罗蛋白的磷酸化修饰状态;通过NetPhos软件预测普罗斯佩罗蛋白上的酪蛋白激酶2磷酸化位点,共得到17个保守的丝氨酸/苏氨酸候选位点,构建所有位点的非磷酸化突变体(丝氨酸/苏氨酸突变为丙氨酸,记为Pros^A)和模拟磷酸化突变体(突变为天冬氨酸,记为Pros^D),通过时序过表达实验验证磷酸化状态对普罗斯佩罗蛋白定位和功能的影响。
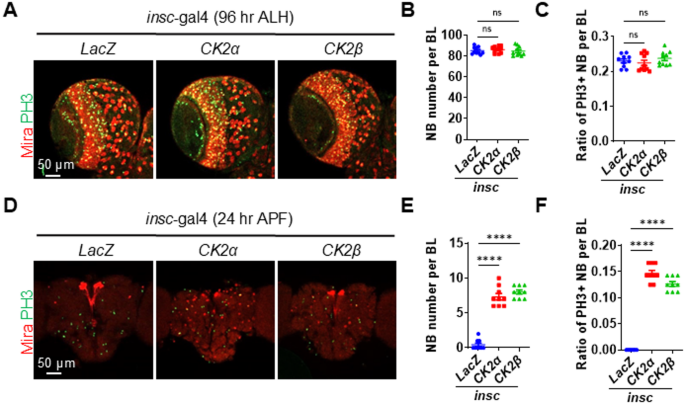
结果解读:免疫共沉淀结果显示,内源性酪蛋白激酶2催化亚基可与普罗斯佩罗蛋白直接结合。核质分离后的免疫印迹结果显示,胞质中的普罗斯佩罗蛋白经碱性磷酸酶处理后分子量显著降低,证实胞质中的普罗斯佩罗蛋白为磷酸化形式。时序过表达实验显示,在幼虫孵化后60-72小时过表达野生型普罗斯佩罗蛋白无明显表型,而过表达非磷酸化突变体Pros^A可导致成神经细胞数量降低约40%(n=10,P<0.0001),核定位普罗斯佩罗蛋白的比例升高约3倍(n=10,P<0.0001);在幼虫孵化后48-72小时过表达野生型普罗斯佩罗蛋白可导致成神经细胞丢失,而过表达模拟磷酸化突变体Pros^D无显著表型,证实酪蛋白激酶2介导的磷酸化修饰可将普罗斯佩罗蛋白滞留在细胞质中,抑制其分化促进活性。
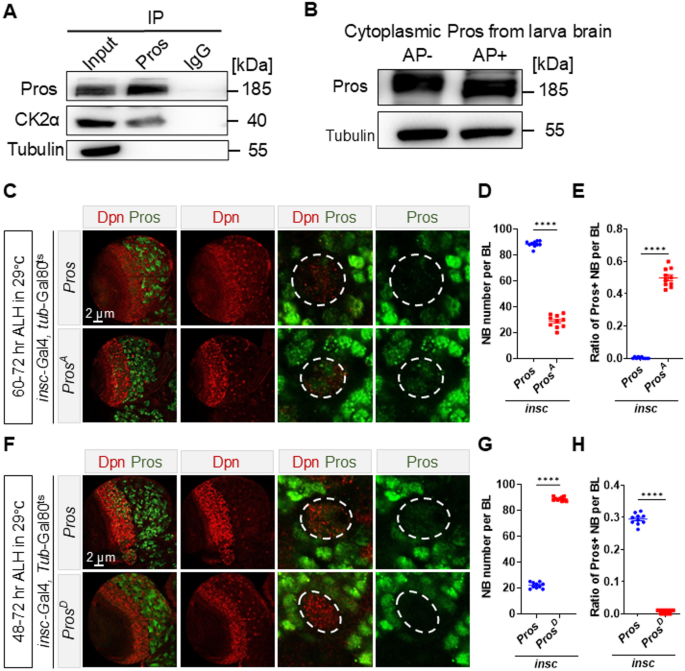
产品关联:实验所用关键产品:赛默飞世尔科技的蛋白A/G磁珠(货号8803)、FastAP热敏碱性磷酸酶(货号EF0651);其余试剂与前序实验一致。
3.4 酪蛋白激酶2调控神经干细胞维持的保守性验证
实验目的:验证酪蛋白激酶2调控神经干细胞自我更新的功能在哺乳动物中的进化保守性。
方法细节:采用H9人胚胎干细胞诱导构建人脑类器官模型,从培养第12天开始用10nM酪蛋白激酶2特异性抑制剂CX-4945处理,第35天收样;通过免疫组化检测人神经干细胞标志物配对盒蛋白6(PAX6)、增殖标志物Ki67的表达,统计配对盒蛋白6阳性细胞的比例和增殖率。
结果解读:免疫荧光结果显示,抑制剂处理组的人脑类器官中神经花环结构紊乱,配对盒蛋白6的荧光强度较对照组降低约45%(n=9,P<0.001),配对盒蛋白6阳性细胞中Ki67共定位的比例降低约35%(n=12,P<0.001),证实抑制酪蛋白激酶2会导致人神经干细胞的自我更新和增殖能力下降,该调控功能在进化上高度保守。
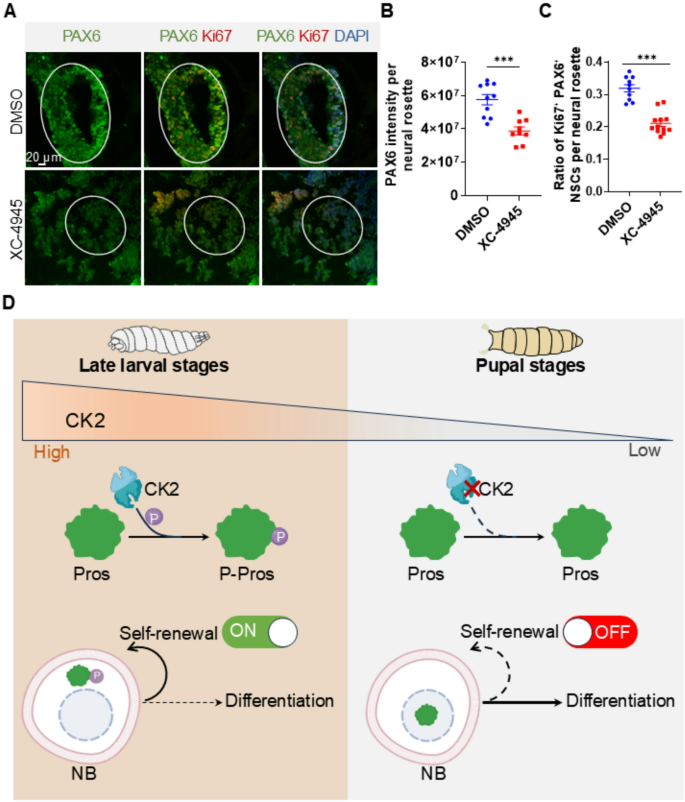
产品关联:实验所用关键产品:Adooq Bioscience的酪蛋白激酶2抑制剂CX-4945(货号A11060)、Proteintech的配对盒蛋白6抗体(货号12323-1-AP)、CST的Ki67抗体(货号9449)。
4. Biomarker研究及发现成果
本研究涉及的生物标志物(Biomarker)分为两类,分别为果蝇成神经细胞的命运标志物和人神经干细胞的功能标志物,可用于指示神经干细胞的自我更新状态和分化阶段。
生物标志物定位:果蝇成神经细胞的核心标志物包括Deadpan蛋白(成神经细胞核标志物)、米兰达蛋白(成神经细胞皮层标志物)、核定位普罗斯佩罗蛋白(成神经细胞分化标志物),筛选逻辑基于领域已验证的经典标志物,通过检测其表达和定位变化反映成神经细胞的命运状态;人神经干细胞的标志物为配对盒蛋白6,用于指示神经干细胞的自我更新能力。
研究过程详述:果蝇标志物的检测采用幼虫脑组织免疫组化,样本为不同发育阶段的果蝇幼虫脑组织,验证方法为荧光共定位分析,核定位普罗斯佩罗蛋白的特异性为:野生型幼虫期成神经细胞中几乎无核定位,蛹期特异性入核,敏感性为100%(所有进入分化程序的成神经细胞均出现核普罗斯佩罗蛋白积累);人配对盒蛋白6的检测采用人脑类器官冰冻切片免疫组化,样本为35天龄的人脑类器官,验证方法为荧光定量分析,其特异性可准确指示神经上皮祖细胞的身份。
核心成果提炼:本研究首次证实核定位普罗斯佩罗蛋白是酪蛋白激酶2功能缺失的特异性效应标志物,酪蛋白激酶2敲低时核普罗斯佩罗蛋白比例升高3倍以上(P<0.01),可作为成神经细胞提前分化的稳定检测指标;同时证实酪蛋白激酶2的表达水平可作为成神经细胞自我维持阶段的时序标志物,其在幼虫晚期高表达,蛹期下降,与成神经细胞的维持窗口完全吻合;在人源系统中,配对盒蛋白6的表达水平可作为酪蛋白激酶2功能的间接标志物,抑制酪蛋白激酶2后配对盒蛋白6水平显著降低(P<0.001),可用于评估人神经干细胞的自我更新状态。
