1. 领域背景与文献
文献英文标题:Cellular prion protein and calcium ions trigger the neurotoxicity of α-synuclein aggregates;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:神经退行性疾病(突触核蛋白病)。
突触核蛋白病是一类以α-突触核蛋白错误折叠、聚集形成神经元内路易小体为核心病理特征的神经退行性疾病,包括帕金森病、路易体痴呆、多系统萎缩等,是全球老龄化进程中发病率持续升高的中枢神经系统疾病类型。领域共识:2010年前后研究逐步明确,α-突触核蛋白的可溶性寡聚体而非成熟纤维是主要神经毒性组分,其与神经元膜的相互作用、钙离子稳态失调是毒性级联反应的起始核心环节;2009年首次报道细胞朊蛋白(PrPC)是β-淀粉样蛋白寡聚体的关键膜受体,后续多项研究提示其可能参与α-突触核蛋白聚集体的识别、内吞与毒性传导,但该结论长期存在争议,不同研究在结合亲和力、毒性贡献度上的结果差异较大。
当前领域未解决的核心问题包括:细胞朊蛋白在α-突触核蛋白聚集体神经毒性中的具体作用阶段(早期膜结合/下游信号传导)尚未明确,是否存在不依赖细胞朊蛋白的独立毒性通路,以及胞外钙离子在α-突触核蛋白-神经元相互作用中的调控机制与功能地位尚未系统解析。本研究针对上述争议问题,采用结构明确的α-突触核蛋白聚集态模型,在多种神经元相关细胞中系统解析细胞朊蛋白与胞外钙离子的差异化作用,为突触核蛋白病的治疗靶点开发提供实验依据。
2. 文献综述解析
作者按照“α-突触核蛋白聚集态的毒性特征→膜受体介导的毒性机制→细胞朊蛋白的争议作用→钙离子的调控效应”的逻辑框架梳理现有研究,对不同方向的结论进行分类整合。
现有研究的关键支持结论包括:B型α-突触核蛋白寡聚体(OB)可通过自身未折叠的N端结构域结合神经元膜,后续将富含β-折叠的核心区域插入脂双层,诱导膜穿孔和钙离子内流;α-突触核蛋白短纤维可作为毒性寡聚体的“储存库”,持续释放具有OB特征的可溶性毒性组分;细胞朊蛋白可作为多种致病淀粉样聚集体(包括β-淀粉样蛋白、tau蛋白、α-突触核蛋白)的膜受体,介导其内吞和下游信号活化,已有研究证实α-突触核蛋白可与细胞朊蛋白的N端95-111位氨基酸结合,诱发钙信号异常与突触功能损伤。现有技术方法的优势包括:当前已建立稳定的α-突触核蛋白不同聚集态(单体、B型寡聚体、短纤维、长纤维)的制备与结构表征体系,可实现毒性组分的精准可控;超分辨受激发射损耗(STED)显微、单分子成像等技术可实现聚集体与膜组分的高分辨定位与动态追踪。现有研究的局限性包括:不同研究采用的α-突触核蛋白聚集体制备方案差异较大,导致细胞朊蛋白结合的结论一致性较差;多数研究未明确区分细胞朊蛋白在毒性早期(膜结合阶段)和晚期(细胞死亡阶段)的差异化作用;尚未系统解析胞外钙离子对α-突触核蛋白-膜相互作用的调控效应,及其与细胞朊蛋白通路的关联性。
本研究的创新价值在于:首次采用结构与毒性均一的B*型寡聚体和短纤维模型,在人神经母细胞瘤细胞、原代大鼠皮层神经元、人诱导多能干细胞(iPSC)衍生多巴胺能神经元三种相关模型中,系统区分细胞朊蛋白介导的早期事件与钙离子主导的晚期毒性,明确了胞外钙离子是α-突触核蛋白持续神经毒性的核心驱动因子,解决了领域内关于细胞朊蛋白作用的长期争议,为突触核蛋白病的干预策略提供了新的理论方向。
3. 研究思路总结与详细解析
本研究的核心目标是明确细胞朊蛋白与胞外钙离子在α-突触核蛋白聚集体神经毒性中的作用机制,核心科学问题是细胞朊蛋白是否为α-突触核蛋白神经毒性的必需介导因子,以及钙离子在该通路中的调控作用,技术路线遵循“聚集体制备与表征→细胞模型构建与验证→膜结合与共定位分析→功能干预(基因沉默/抗体阻断)→毒性指标动态检测→机制分层解析”的闭环逻辑,实验结果可重复性高。
3.1 α-突触核蛋白聚集体制备与细胞模型构建
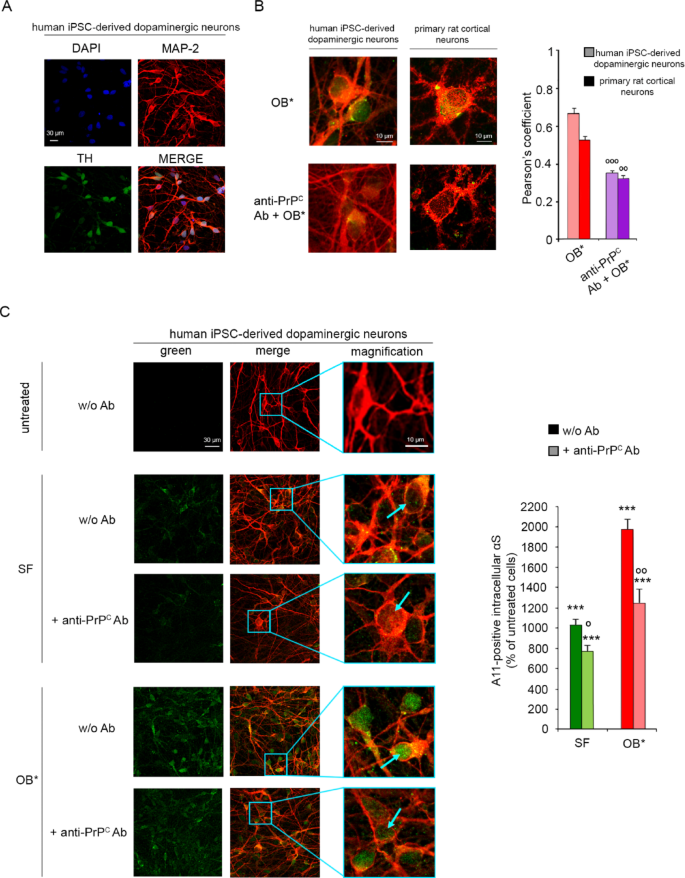
实验目的:获得结构均一、毒性稳定的B型α-突触核蛋白寡聚体与短纤维,并构建三种神经元相关细胞模型用于后续功能实验。方法细节:重组人α-突触核蛋白在大肠杆菌BL21中表达纯化获得单体,B型寡聚体采用已建立的动力学捕获方案制备,短纤维通过单体在37℃、pH7.4磷酸盐缓冲液中振荡孵育4-6天制备,聚集体浓度通过275nm吸光度法定量;细胞模型包括原代大鼠皮层神经元(分离后培养12-16天用于实验)、人SH-SY5Y神经母细胞瘤细胞、人诱导多能干细胞衍生多巴胺能神经元(诱导分化14-18天,经微管相关蛋白2(MAP-2)、酪氨酸羟化酶免疫荧光鉴定为阳性)。结果解读:免疫荧光鉴定结果显示诱导多能干细胞衍生神经元中酪氨酸羟化酶阳性率符合多巴胺能神经元的特征(对应图2A),所有聚集体经结构与毒性表征符合既往报道的标准特征。
产品关联:实验所用关键产品包括安捷伦的大肠杆菌BL21(货号200131)、赛默飞世尔的原代大鼠皮层神经元(货号A1084001)、Gibco的Neurobasal™ Plus培养基(货号A3582901)、Abcam的抗微管相关蛋白2抗体(货号ab32454)、圣克鲁斯的抗酪氨酸羟化酶抗体(货号sc-25269),其余试剂为领域常规蛋白纯化与细胞培养试剂。
3.2 细胞朊蛋白与α-突触核蛋白聚集体的膜共定位及结合验证
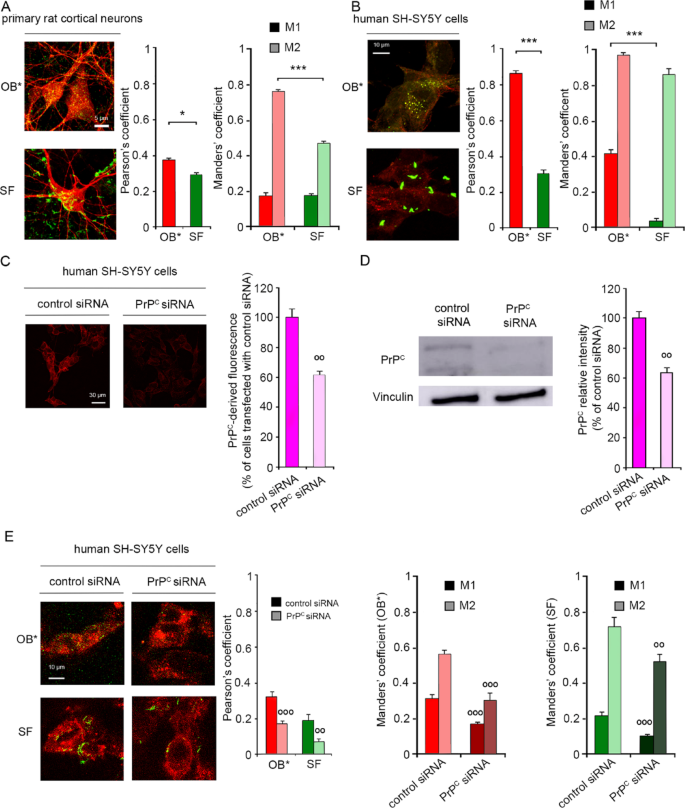
实验目的:验证B型寡聚体和短纤维是否与神经元膜上的细胞朊蛋白共定位,以及细胞朊蛋白是否介导α-突触核蛋白聚集体的膜招募过程。方法细节:采用共聚焦激光扫描显微技术检测荧光标记的α-突触核蛋白聚集体与细胞朊蛋白(抗细胞朊蛋白单克隆抗体标记)的共定位水平;通过小干扰RNA(siRNA)沉默SH-SY5Y细胞的细胞朊蛋白表达(沉默效率约40%,经免疫荧光和免疫印迹(Western blot)验证),或用抗细胞朊蛋白抗体阻断其胞外结构域,细胞经聚集体处理10分钟后,检测α-突触核蛋白聚集体与细胞膜(小麦胚芽凝集素标记)的共定位程度,采用皮尔逊相关系数、曼德斯重叠系数定量共定位水平。结果解读:共定位结果显示,B型寡聚体与细胞朊蛋白的皮尔逊相关系数为0.86±0.01(n=10,P<0.001),短纤维与细胞朊蛋白的皮尔逊相关系数为0.30±0.02(n=6,P<0.01),提示B型寡聚体与细胞朊蛋白的共定位水平更高(对应图1B);细胞朊蛋白沉默后,B型寡聚体与细胞膜的皮尔逊相关系数显著降低(P<0.001),短纤维与细胞膜的共定位也显著下降(对应图1E);抗细胞朊蛋白抗体预处理可使诱导多能干细胞衍生多巴胺能神经元中B*型寡聚体的膜结合水平降低47%,原代皮层神经元中降低39%(n=3,P<0.001)。
产品关联:实验所用关键产品包括圣克鲁斯的抗细胞朊蛋白单克隆抗体(货号sc-47730)、赛默飞世尔的细胞朊蛋白小干扰RNA与Lipofectamine 3000转染试剂(货号L3000008)、Proteintech的多克隆抗细胞朊蛋白抗体(货号12555-1-AP)与抗波形蛋白抗体(货号66305-1-Ig),共定位分析采用ImageJ的JACoP插件。
3.3 细胞朊蛋白对α-突触核蛋白聚集体内化与寡聚体释放的调控作用
实验目的:明确细胞朊蛋白是否调控α-突触核蛋白聚集体的细胞内化,以及短纤维释放毒性寡聚体的过程。方法细节:诱导多能干细胞衍生多巴胺能神经元用B型寡聚体或短纤维处理6小时,采用可特异性识别毒性寡聚体的A11抗体检测细胞内的寡聚体信号,部分细胞预先用抗细胞朊蛋白抗体处理,对比内化水平的差异。结果解读:短纤维处理6小时后细胞内A11阳性信号显著升高,提示短纤维释放的寡聚体被细胞内化;抗细胞朊蛋白抗体预处理可使B型寡聚体的内化水平降低24±11%,短纤维来源寡聚体的内化水平降低37±15%(n=3,P<0.01,对应图2C);细胞朊蛋白沉默后,细胞内A11阳性信号与溶酶体标志物Lamp-1的共定位水平下降,提示细胞朊蛋白参与寡聚体的内吞转运过程;B*型寡聚体和短纤维处理6小时或24小时均未显著改变细胞朊蛋白的表达水平,排除了反馈调控的干扰。
产品关联:实验所用关键产品为赛默飞世尔的A11抗寡聚体抗体(货号AHB0052),其余为领域常规免疫荧光试剂。
3.4 细胞朊蛋白对α-突触核蛋白诱导的钙离子稳态失调与细胞毒性的影响
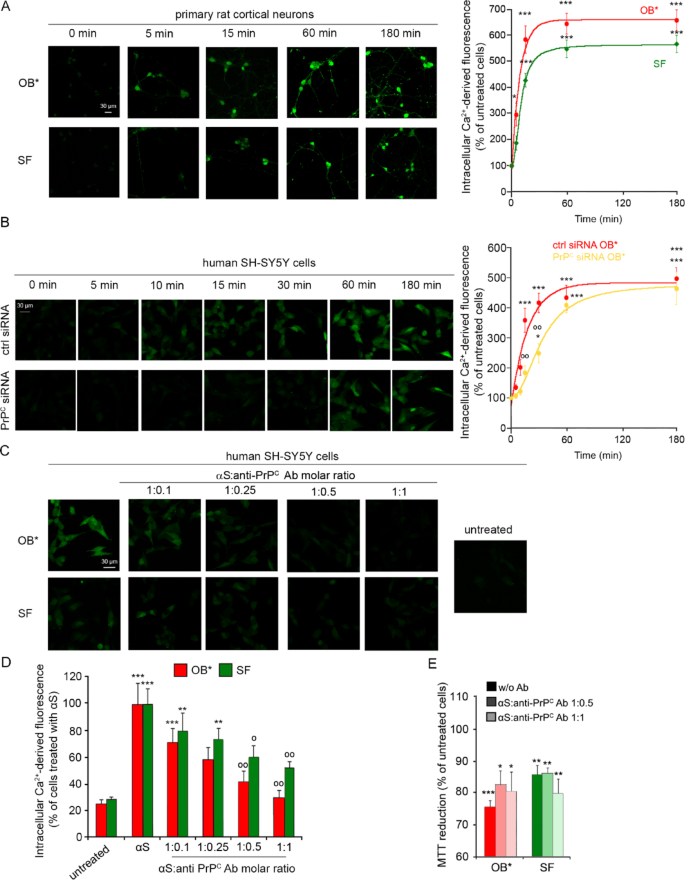
实验目的:解析细胞朊蛋白在α-突触核蛋白诱导的钙离子内流、膜通透性改变及晚期细胞死亡中的作用。方法细节:采用Fluo-4 AM钙离子荧光探针检测细胞内钙离子水平的动态变化,分别在细胞朊蛋白沉默、抗体阻断条件下检测0-180分钟的钙离子浓度变化;采用钙黄绿素泄漏实验检测细胞膜通透性;采用噻唑蓝(MTT)比色法检测24小时的细胞活力。结果解读:B型寡聚体可诱导原代皮层神经元钙离子水平升高约7倍,动力学符合指数增长特征,半峰时间为7.2分钟;短纤维诱导的钙离子升高约5-6倍,符合S型动力学特征,半峰时间为10分钟(对应图3A);细胞朊蛋白沉默可使B型寡聚体诱导的钙离子内流半峰时间从14.5分钟延迟至33.7分钟,但仅抑制早期(<30分钟)的钙离子内流,对60-180分钟的晚期钙离子升高无显著影响(对应图3B);抗细胞朊蛋白抗体在1:1摩尔比下可显著抑制15分钟时的钙离子内流(P<0.001,对应图3C、D);细胞朊蛋白抗体预处理可减少钙黄绿素泄漏,但24小时噻唑蓝比色实验显示其无法显著改善B型寡聚体或短纤维诱导的细胞活力下降(B型寡聚体诱导活力下降25%,短纤维下降14%,抗体处理后无统计学差异,对应图3E)。
产品关联:实验所用关键产品包括赛默飞世尔的Fluo-4 AM探针(货号F14201)、钙黄绿素-AM(货号C3100MP),噻唑蓝比色法试剂文献未提及具体品牌,为领域常规细胞活力检测试剂。
3.5 胞外钙离子对α-突触核蛋白聚集体膜结合与神经毒性的调控作用
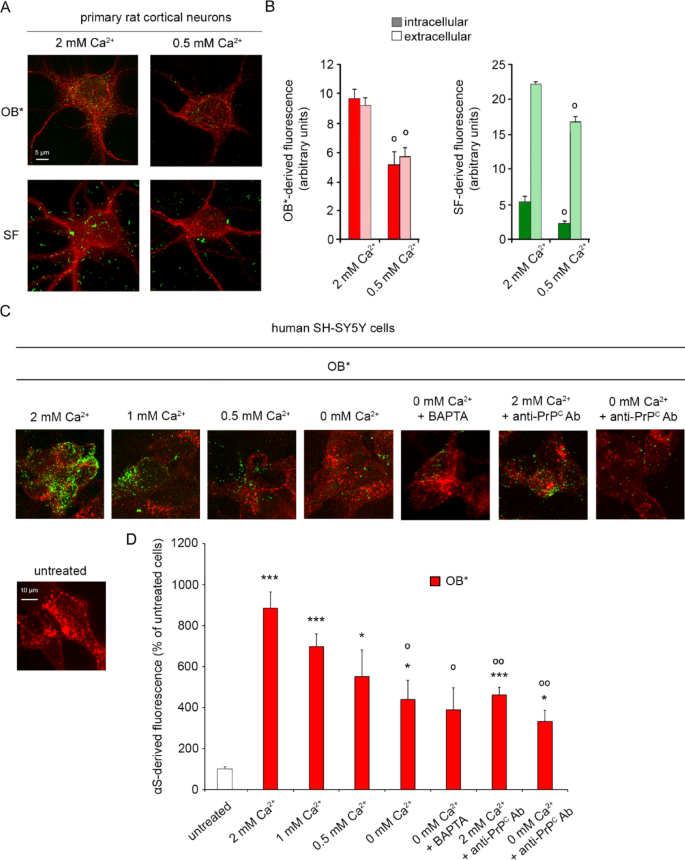
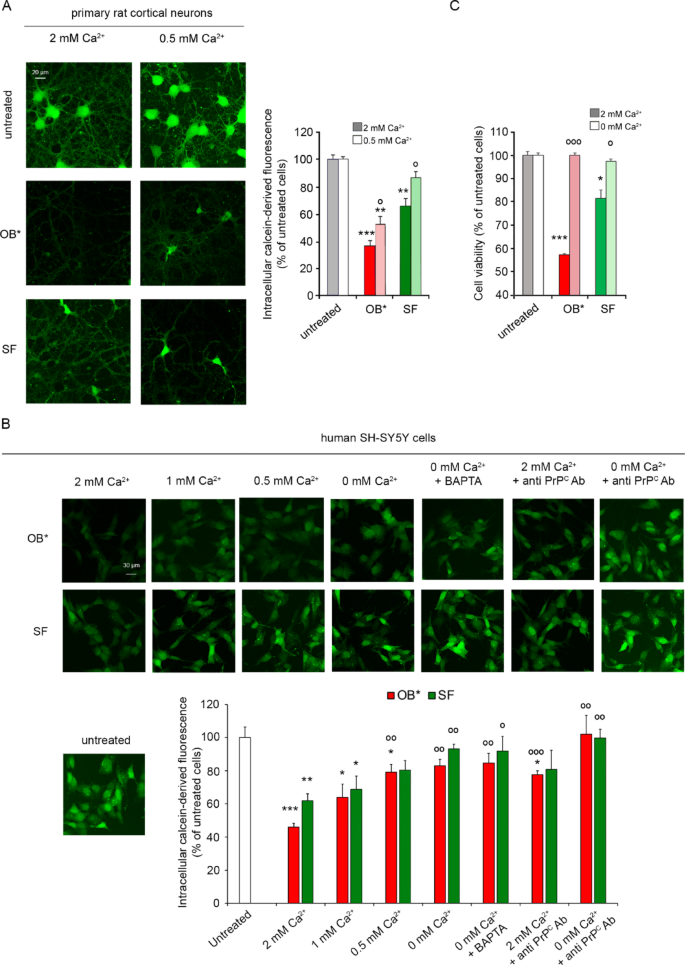
实验目的:明确胞外钙离子在α-突触核蛋白聚集体膜相互作用、内化及毒性中的调控效应,及其与细胞朊蛋白通路的独立性。方法细节:设置不同胞外钙离子浓度梯度(2、1、0.5、0 mM,联合BAPTA钙离子螯合剂),采用受激发射损耗(STED)显微技术检测α-突触核蛋白聚集体的膜结合与内化水平,钙黄绿素泄漏实验检测膜通透性,CellTiter-Glo发光法检测24小时细胞活力。结果解读:胞外钙离子浓度从2 mM降至0.5 mM时,B型寡聚体的膜结合水平降低38±17%,内化水平降低46±24%(n=3,P<0.01,对应图4A、B);短纤维的膜结合水平降低27±10%,内化水平降低56±31%(n=3,P<0.05);0 mM钙联合BAPTA处理可使B型寡聚体的总结合/内化信号降低500±190%(相对于2 mM钙组,n=3,P<0.001,对应图4C、D);钙浓度降低可显著减少钙黄绿素泄漏(P<0.01,对应图5A、B);2 mM钙条件下B*型寡聚体使细胞活力降低43±6%,短纤维降低19±7%,而0 mM钙条件下未观察到显著的活力下降(n=9-18,P<0.001,对应图5C);即使在细胞朊蛋白抗体阻断条件下,降低胞外钙浓度仍可进一步减少α-突触核蛋白的膜结合与毒性,提示钙离子的调控作用独立于细胞朊蛋白通路。
产品关联:实验所用关键产品包括普洛麦格的CellTiter-Glo细胞活力检测试剂盒(货号G7571)、西格玛的BAPTA钙离子螯合剂(货号14510),其余为领域常规试剂。
4. Biomarker研究及发现成果
本研究未涉及临床样本生物标志物的筛选与验证,聚焦于突触核蛋白病的病理机制解析,明确了细胞朊蛋白、胞外钙离子与α-突触核蛋白聚集体的相互作用作为疾病进展关键分子事件的潜在价值。
Biomarker定位:本研究涉及的候选机制类标志物包括神经元膜细胞朊蛋白表达水平、脑脊液/血浆胞外钙离子浓度、α-突触核蛋白寡聚体/短纤维的体液水平,其中α-突触核蛋白寡聚体的筛选验证逻辑遵循“体外结构表征→细胞水平毒性验证→动物水平病理验证→临床样本相关性分析”的标准路径,本研究完成了前两个阶段的验证工作。研究过程详述:本研究未开展临床生物标志物的检测,仅在细胞水平验证了细胞朊蛋白表达降低、胞外钙离子浓度下降可显著抑制α-突触核蛋白聚集体的早期膜结合与晚期毒性,未涉及临床样本的特异性、敏感性及诊断效能评估。
核心成果提炼:本研究首次明确细胞朊蛋白仅介导α-突触核蛋白聚集体的早期膜招募与钙离子内流,不参与晚期神经毒性的调控,而胞外钙离子是α-突触核蛋白聚集体神经毒性的必需调控因子;统计学结果显示,2 mM生理钙条件下B*型寡聚体诱导的细胞活力下降为43±6%(n=9-18,P<0.001),0 mM钙条件下活力下降无统计学意义;抗细胞朊蛋白抗体处理可使早期(15分钟)钙离子内流降低约40%(n=3,P<0.001),但24小时细胞活力无显著改善;上述结果提示,单独靶向细胞朊蛋白的治疗策略无法有效阻断α-突触核蛋白的持续神经毒性,而靶向钙离子通路或联合靶向细胞朊蛋白与钙离子通路可能是更有效的干预策略。推测:后续可在突触核蛋白病动物模型中验证上述结论,进一步评估钙离子通路调节剂的治疗潜力,同时可探索脑脊液中α-突触核蛋白寡聚体与钙离子水平的组合作为疾病进展标志物的可能性。
