1. 领域背景与文献
文献英文标题:Combination of GLP-1 receptor agonist and Akkermansia muciniphila Akk11 reduces adiposity and ameliorates MASLD in T2D mice;发表期刊:Cell & Bioscience;影响因子:7.05(2024年);研究领域:代谢性疾病(2型糖尿病、代谢功能障碍相关脂肪性肝病)的微生物-药物联合治疗。
领域共识:2型糖尿病(T2D)和代谢功能障碍相关脂肪性肝病(MASLD)是全球高发的慢性代谢疾病,2020年国际专家共识正式将非酒精性脂肪性肝病(NAFLD)更名为MASLD,明确其代谢异常的核心病因。当前MASLD全球患病率近1/3,T2D患者的MASLD发病风险较健康人群升高11倍,且两者可相互加重,显著增加心血管并发症及死亡风险,但目前尚无获批的MASLD特效治疗药物,生活方式干预仍是主流管理方案。胰高糖素样肽-1受体激动剂(GLP-1RA)是近年代谢疾病治疗的核心药物,2005年首个GLP-1RA艾塞那肽获批上市,后续司美格鲁肽等药物陆续拓展到肥胖、T2D及并发症治疗领域,但其在严重胰岛素抵抗人群中对MASLD的疗效有限,且长期使用易出现疗效衰减,机制尚未明确。2013年以来,嗜黏蛋白阿克曼菌(Akkermansia muciniphila, AKK)作为下一代益生菌被证实可改善糖脂代谢,但其与GLP-1RA的协同作用及机制尚未被系统探索。
当前领域未解决的核心问题包括:GLP-1RA在晚期胰岛素抵抗人群中MASLD疗效不足的机制不清晰,缺乏可增强其疗效的安全联合治疗策略,肠道微生物与GLP-1RA的互作关系尚未明确。本研究针对这一研究空白,探索GLP-1RA联合灭活AKK菌株Akk11对T2D合并MASLD的治疗效果及调控机制,为代谢疾病的微生物-药物联合治疗提供新的学术依据和实践范式。
2. 文献综述解析
作者对现有研究的评述主要按照“疾病负担-现有治疗局限-肠道微生物调控潜力-AKK协同作用假设”的逻辑维度展开。首先,作者梳理了MASLD的流行病学与临床需求:现有流行病学研究显示MASLD已成为全球最常见的慢性肝病,合并T2D的患者疾病进展更快、预后更差,生活方式干预依从性低,现有药物的肝脏疗效有限,未满足临床需求。其次,作者总结了GLP-1RA的研究进展:现有研究证实GLP-1RA可通过激活GLP-1受体促进葡萄糖依赖性胰岛素分泌、抑制食欲、改善胰岛素敏感性,同时具备心血管、肾脏保护作用,部分基础研究提示其可减轻肝脏脂肪变性,但在严重胰岛素抵抗模型中疗效衰减明显,且领域内对肝细胞是否表达功能性GLP-1受体尚存争议,提示其肝脏作用可能通过肠-肝轴等间接通路介导。第三,作者梳理了肠道微生物与代谢疾病的关联:现有研究证实肠道菌群失调可通过破坏肠屏障、释放代谢毒素加重MASLD,而GLP-1RA可调控肠道菌群组成;AKK的丰度在T2D合并MASLD患者中随疾病进展降低,补充AKK可改善小鼠肥胖、胰岛素抵抗及肝脂肪变性,且AKK可刺激肠道内分泌细胞分泌内源性GLP-1,提示两者可能存在协同作用。
现有研究的优势在于已分别证实GLP-1RA和AKK的代谢调节作用,局限性在于尚无研究探索AKK特定菌株与GLP-1RA联合对T2D合并MASLD的治疗效果,两者的协同作用机制尚未阐明。本研究的创新价值在于首次证实灭活AKK菌株Akk11可显著增强GLP-1RA的抗肥胖及MASLD改善作用,明确了“菌群重塑-肠屏障改善-多器官脂代谢调控-GLP-1信号增强”的正反馈协同机制,填补了GLP-1RA联合益生菌治疗代谢疾病的研究空白,为临床转化提供了新的候选联合方案。
3. 研究思路总结与详细解析
本研究的整体研究目标是明确GLP-1RA联合Akk11对T2D合并MASLD的治疗效果及协同作用机制,核心科学问题为Akk11是否可增强GLP-1RA的代谢疗效,以及两者协同作用的分子及微生物调控机制,技术路线遵循“单药疗效及局限验证→联合治疗效果评估→多组学机制解析→关键通路验证”的闭环逻辑,所有实验均采用随机、盲法设计以减少偏倚。
3.1 GLP-1RA单药治疗的代谢疗效评估
实验目的:明确长期GLP-1RA治疗在T2D合并MASLD模型中的疗效特征及局限性,为联合治疗方案的提出提供依据。
方法细节:采用8周龄雄性C57BL/6J背景的db/db小鼠(T2D合并MASLD经典模型),适应性喂养1周后,随机分为司美格鲁肽治疗组(40μg/kg,每3天皮下注射1次)、生理盐水对照组,同时设置同龄野生型小鼠生理盐水对照组,持续干预14周。干预期间每2周检测体重、摄食量、随机血糖,干预结束后检测空腹血糖,行胰岛素耐量试验(ITT)评估胰岛素敏感性;采用代谢笼检测氧气消耗量、二氧化碳产量、呼吸交换率等能量代谢参数;通过核磁共振分析体成分;采集血清检测肝功能、血脂等生化指标;对肝脏、脂肪、肠道组织行组织学染色、转录组测序及蛋白表达检测;采集粪便行16S rRNA测序分析菌群组成。
结果解读:司美格鲁肽治疗可显著降低db/db小鼠体重(n=9-10,P<0.001),抑制摄食量使其接近野生型小鼠水平;治疗前2周随机血糖显著下降,但12周后回升至未治疗db/db小鼠水平,仅空腹血糖维持较低水平(n=8-10,P<0.01);ITT显示GLP-1RA组胰岛素敏感性轻度改善,光周期呼吸交换率降低(n=3,P<0.05),提示代谢向脂质氧化方向偏移。体成分分析显示GLP-1RA仅显著降低腹股沟白色脂肪重量(n=5,P<0.05),肝脏脂肪变性及脂合成酶ATP-柠檬酸裂解酶(ACLY)、脂肪酸合成酶(FASN)的表达无显著改善,仅肝脏炎症因子一氧化氮合酶2(Nos2)、白细胞介素-6(IL-6)的表达下调(n=3,P<0.05)。肠道转录组显示GLP-1RA可抑制肠道焦亡通路相关基因(Naip、Aim2、Gasdermin D)的表达;粪便16S测序显示GLP-1RA可恢复db/db小鼠的菌群α多样性,升高AKK的相对丰度(n=6,P<0.01)。

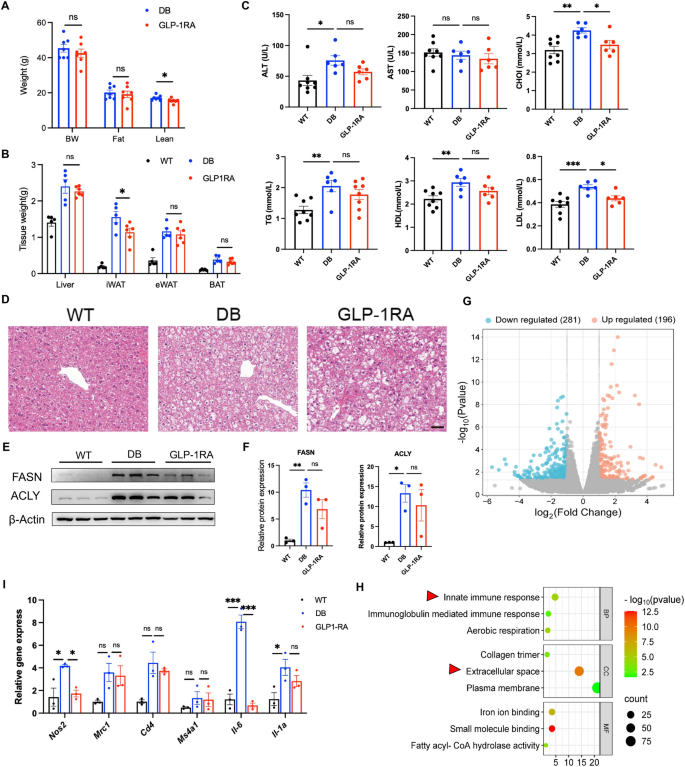
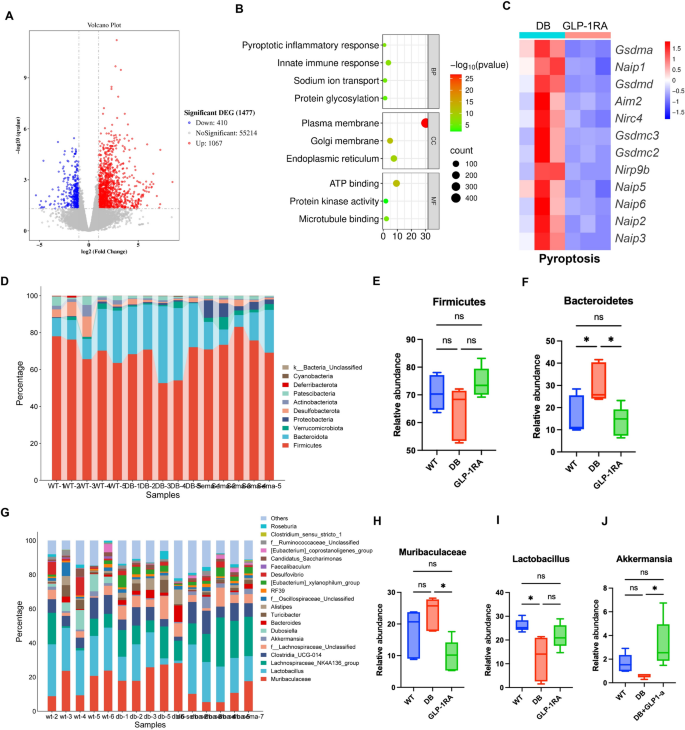
产品关联:实验所用关键产品:诺和诺德的司美格鲁肽,布鲁克的Minispec LF50体成分分析仪,罗氏的Accu-Chek Active血糖仪,Proteintech的HSP90、FASN、线粒体融合蛋白2(MFN2)、过氧化物酶体增殖物激活受体α(PPARα)、ACLY、β-肌动蛋白抗体,Abcam的GLP-1R抗体,Cell Signaling的磷酸化环磷腺苷效应元件结合蛋白(p-CREB)、紧密连接蛋白1(ZO-1)、紧密连接蛋白 Claudin-1抗体,Jackson的辣根过氧化物酶标记二抗;16S rRNA测序及转录组测序为常规科研服务,其余试剂为分子生物学实验常规试剂。
3.2 GLP-1RA联合Akk11的整体代谢疗效验证
实验目的:验证外源性补充灭活Akk11是否可增强GLP-1RA的代谢治疗效果,明确联合治疗的整体获益。
方法细节:db/db小鼠在接受司美格鲁肽(40μg/kg,每3天皮下注射1次)干预的同时,每2天灌胃2×10^8 CFU的灭活Akk11,对照组灌胃等量生理盐水,持续干预后检测体重、血糖、胰岛素敏感性、体成分变化;采集腹股沟白色脂肪、附睾白色脂肪、棕色脂肪进行称重及苏木精-伊红(HE)染色,通过WB检测脂肪组织脂代谢相关蛋白表达;采集血清检测甘油三酯(TG)、脂多糖(LPS)、GLP-1的浓度。
结果解读:联合治疗组小鼠体重较GLP-1RA单药组进一步降低(n=9-10,P<0.01),体成分分析显示脂肪量及瘦量均显著减少(n=7,P<0.05);随机血糖及空腹血糖与单药组无显著差异,但ITT显示联合组胰岛素敏感性进一步改善,注射胰岛素后90min血糖降至最低,120min内血糖下降幅度更大(n=5-10,P<0.05)。联合组的腹股沟白色脂肪、附睾白色脂肪及棕色脂肪重量均较单药组显著降低(n=6,P<0.01),脂肪细胞体积明显更小;腹股沟脂肪中脂解相关蛋白PPARα表达上调,附睾脂肪中脂合成酶FASN表达下调(n=3,P<0.05);血清TG、LPS水平显著降低,内源性GLP-1水平升高(n=3-8,P<0.05),肠道GLP-1R/p-CREB通路激活。
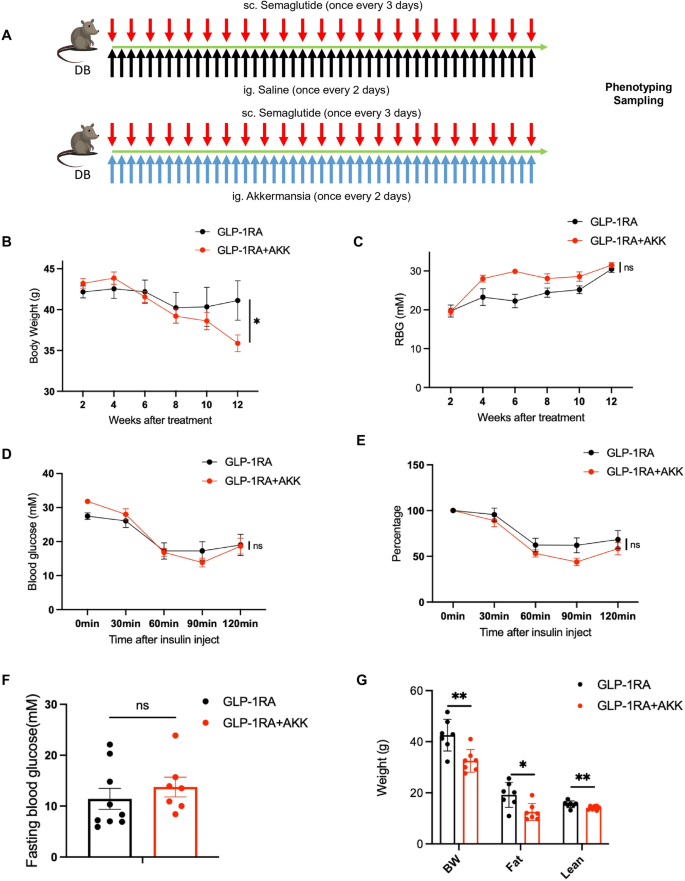
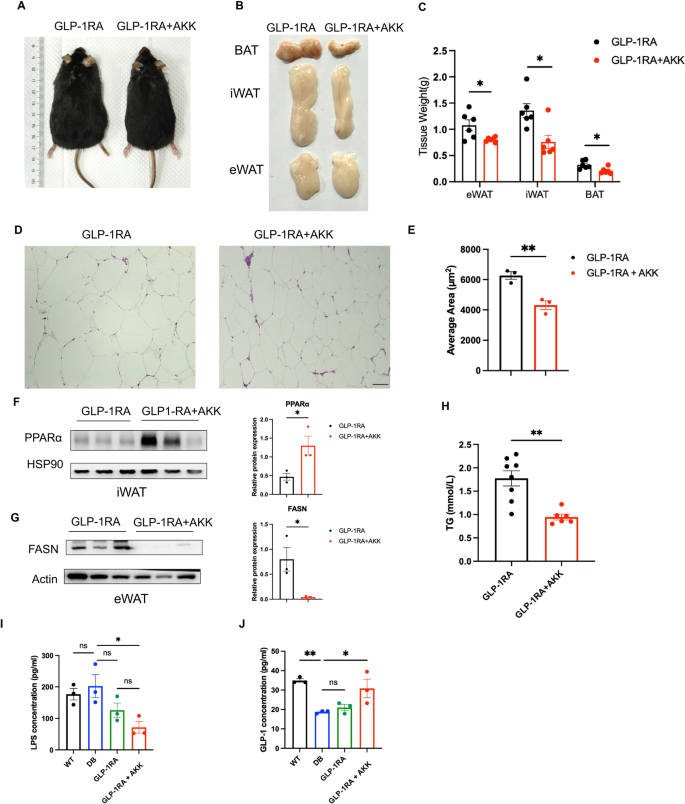
产品关联:实验所用关键产品:微康益生菌的灭活Akk11菌株,依科赛生物的GLP-1 ELISA试剂盒(货号E-EL-M3108)、LPS ELISA试剂盒(货号E-EL-0180),其余试剂同前。
3.3 联合治疗对MASLD的改善效应及分子机制解析
实验目的:明确联合治疗对肝脏病理的改善作用,阐明其调控肝脏脂代谢的分子机制。
方法细节:干预结束后采集小鼠肝脏组织,称重后行HE染色、天狼星红染色、Masson三色染色、油红O染色,分别评估肝脏炎症、纤维化及脂质沉积程度;对肝脏组织进行转录组测序分析差异基因及富集通路;采用WB及实时荧光定量PCR(qRT-PCR)验证脂代谢、线粒体功能及炎症相关分子的表达水平。
结果解读:联合治疗组肝脏重量较单药组显著降低(n=6,P<0.01),外观更接近正常肝脏;组织学染色显示肝脂肪变性、肝细胞气球样变明显减轻,纤维化程度及脂质沉积面积均较单药组显著降低(n=3,P<0.01)。肝脏转录组显示联合治疗组的差异基因富集于线粒体功能、脂肪酸代谢通路,其中脂合成相关基因(Fasn、硬脂酰辅酶A去饱和酶1、乙酰辅酶A羧化酶α)下调,脂肪酸β氧化相关基因(短链酰基辅酶A脱氢酶、烯酰辅酶A水合酶1、乙酰辅酶A酰基转移酶2)上调,胆固醇代谢相关基因(NPC2胆固醇转运蛋白、转位蛋白、电压依赖性阴离子通道3、载脂蛋白A1)上调,炎症因子Il6、趋化因子配体2的表达下调(n=3,P<0.05)。WB结果证实联合组肝脏脂合成酶ACLY、FASN的表达较单药组下调30%以上,线粒体融合蛋白MFN2的表达上调约1.8倍(n=3,P<0.05),提示联合治疗可抑制肝脏脂合成、改善线粒体功能。
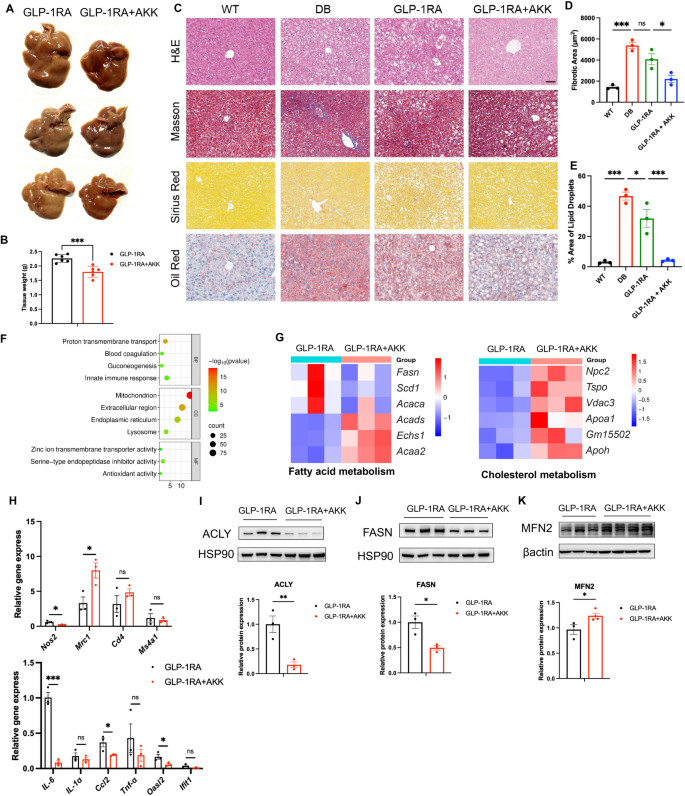
产品关联:实验所用关键产品:赛维尔生物的Masson三色染色试剂盒、天狼星红染色试剂盒、油红O染色试剂盒,其余试剂同前。
3.4 联合治疗对肠道微生态及肠屏障的调控作用
实验目的:阐明联合治疗对肠道菌群、肠屏障功能的调控效应,明确两者协同作用的上游机制。
方法细节:采集小鼠粪便进行16S rRNA测序分析菌群组成变化,采用商业化试剂盒检测粪便游离氨基酸含量;对结肠组织进行转录组测序分析差异通路,采用WB检测肠紧密连接蛋白的表达水平。
结果解读:16S测序显示联合治疗组肠道中拟杆菌门丰度降低、厚壁菌门丰度升高,AKK的相对丰度较单药组进一步显著升高(n=6,P<0.001)。结肠转录组显示差异基因富集于PPAR信号通路、蛋白质消化吸收、胞外基质-受体互作通路:其中PPAR通路中载脂蛋白C3、脂肪酸结合蛋白4下调,提示脂质清除增强;氨基酸转运体基因(溶质载体家族6成员19、溶质载体家族36成员1、溶质载体家族1成员5)上调,粪便游离氨基酸含量降低,提示肠道营养吸收效率提升;胞外基质通路中血小板反应蛋白1、CD44下调,层粘连蛋白α3、Ⅳ型胶原α6等上调,提示胞外基质重塑促进肠屏障修复。WB结果显示联合组肠紧密连接蛋白ZO-1、Claudin-1的表达较单药组显著上调(n=3,P<0.05),证实肠屏障功能改善。

产品关联:实验所用关键产品:南京建成的游离氨基酸含量检测试剂盒(货号2508004002),其余试剂同前。
4. Biomarker 研究及发现成果
本研究涉及的Biomarker可分为三类:肠道微生物标志物嗜黏蛋白阿克曼菌Akk11,循环功能标志物血清GLP-1、LPS、TG,以及组织疗效标志物肝脏ACLY、FASN、MFN2和肠紧密连接蛋白ZO-1、Claudin-1。筛选验证逻辑遵循“单药治疗菌群变化筛选候选菌株→联合干预验证菌株丰度变化→多组织分子标志物验证疗效”的完整链条。
研究过程详述:微生物标志物Akk11为灭活的嗜黏蛋白阿克曼菌菌株,首先通过16S rRNA测序发现GLP-1RA单药治疗可升高db/db小鼠肠道内源性AKK丰度(n=6,P<0.01),外源性补充灭活Akk11后,再次通过16S测序验证其肠道丰度较单药组进一步升高2倍以上(n=6,P<0.001)。循环功能标志物方面,血清GLP-1采用ELISA定量检测,联合治疗组较单药组升高约40%(n=3,P<0.05);血清LPS采用ELISA检测,联合组较单药组降低约32%(n=3,P<0.05);血清TG采用全自动生化分析仪检测,联合组较单药组降低约28%(n=6-8,P<0.05)。组织疗效标志物通过WB及qRT-PCR验证,肝脏ACLY、FASN的表达较单药组下调30%以上(n=3,P<0.05),线粒体融合蛋白MFN2表达上调约1.8倍(n=3,P<0.05);肠道ZO-1表达上调约2.1倍(n=3,P<0.05),上述标志物均具有统计学显著性。
核心成果提炼:Akk11作为新型益生菌类生物标志物,与GLP-1RA联合使用时可发挥显著的协同代谢调节作用:可使T2D小鼠的总体脂肪量降低约25%,肝脏脂质沉积面积减少约40%(n=3,P<0.01),肝脏纤维化面积降低约35%(n=3,P<0.01),血清TG降低约28%(n=6-8,P<0.05)。本研究的创新性在于首次证实灭活AKK菌株可显著增强GLP-1RA的抗肥胖及MASLD疗效,明确了“菌群重塑-肠屏障改善-多器官脂代谢调控-GLP-1信号增强”的正反馈协同机制,所有疗效相关数据均达到P<0.05的统计学显著性水平。推测:肠道AKK丰度可作为GLP-1RA治疗MASLD的疗效预测标志物,血清GLP-1、LPS、TG可作为联合治疗的疗效监测标志物,该结论需后续临床研究进一步验证。