1. 领域背景与文献
文献英文标题:DNA methylation-mediated silencing of MEOX1 promotes glycolysis and immune evasion in colorectal cancer cells through inhibition of GLP2R transcription;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:肿瘤学(结直肠癌表观遗传调控、代谢重编程与免疫逃逸研究)。
领域共识:结直肠癌是全球第三大常见恶性肿瘤,也是第二大肿瘤相关死亡原因,患者整体5年生存率约为64%,约50%的患者会出现肝转移,肝转移患者预后较差的核心原因之一是肝脏免疫抑制微环境导致的肿瘤免疫逃逸。近年来,表观遗传调控(如DNA甲基化)、代谢重编程(如糖酵解)被证实是结直肠癌发生发展、免疫逃逸的核心驱动因素,2020年左右多项研究证实河马(Hippo)信号通路在结直肠癌代谢调控中发挥重要作用,当前领域研究热点主要包括结直肠癌免疫抑制微环境的调控靶点、表观遗传异常驱动的代谢重编程机制,尚未解决的核心问题包括:胰高血糖素样肽-2受体(GLP2R)作为结直肠癌中已被报道的下调免疫相关基因,其表达调控机制、参与肿瘤代谢和免疫逃逸的具体通路尚未明确,同时缺乏针对该通路的预后标志物与干预靶点。针对上述研究空白,本研究旨在探究间充质同源盒1(MEOX1)甲基化介导的胰高血糖素样肽-2受体表达下调对结直肠癌糖酵解、免疫逃逸的调控机制,为结直肠癌的预后评估和靶向治疗提供新的潜在方向。
2. 文献综述解析
本研究的文献综述部分按照“结直肠癌流行病学与免疫微环境特征→胰高血糖素样肽-2受体的已知功能→河马信号通路与代谢重编程的关联→间充质同源盒1的肿瘤调控作用”的逻辑脉络梳理现有研究成果。现有研究已证实,结直肠癌的预后与肿瘤组织中CD4+细胞毒性T细胞、树突状细胞的浸润水平呈正相关,相关结论已在多个独立临床队列中得到验证,优势是为肿瘤免疫治疗的靶点开发提供了理论基础,但局限性在于免疫细胞浸润的上游调控机制尚不清晰,缺乏可临床转化的干预靶点。现有研究发现胰高血糖素样肽-2受体在结直肠癌组织中表达下调,且与免疫细胞浸润水平相关,优势是初步明确了该分子的临床相关性,但局限性在于其具体的分子功能和调控机制未被阐明,也未明确其与肿瘤代谢重编程的关联。河马信号通路的异常激活是结直肠癌糖酵解重编程的重要驱动因素,相关研究已在细胞系和动物模型中得到验证,优势是揭示了代谢调控的核心通路,但局限性在于上游调控分子的研究较少,缺乏与表观遗传修饰的关联分析。转录因子间充质同源盒1在多种肿瘤中发挥抑癌或促癌的双重作用,但其在结直肠癌中的功能以及与胰高血糖素样肽-2受体的调控关系尚未被报道。
本研究的创新价值在于,首次揭示了DNA甲基化-间充质同源盒1-胰高血糖素样肽-2受体-河马信号通路调控轴在结直肠癌糖酵解和免疫逃逸中的核心作用,弥补了现有研究中胰高血糖素样肽-2受体调控机制不明、表观遗传与代谢免疫调控关联不足的空白,为结直肠癌的靶向干预提供了新的理论依据。
3. 研究思路总结与详细解析
本研究的核心目标是阐明胰高血糖素样肽-2受体在结直肠癌中的功能与调控机制,核心科学问题是“间充质同源盒1启动子甲基化如何通过调控胰高血糖素样肽-2受体转录影响结直肠癌的糖酵解和免疫逃逸”,技术路线遵循“生物信息学筛选→临床样本关联分析→细胞功能验证→分子机制探究→动物模型验证→上游表观调控解析”的闭环逻辑。
3.1 临床样本中胰高血糖素样肽-2受体的表达与临床相关性分析
本环节的核心目标是明确胰高血糖素样肽-2受体在结直肠癌中的表达特征、临床预后价值以及与免疫细胞浸润的关联。实验纳入35例结直肠癌患者的肿瘤组织与配对癌旁组织,通过免疫组化(IHC)检测胰高血糖素样肽-2受体的表达水平,同时采用免疫荧光双标检测CD4+颗粒酶B阳性的细胞毒性T细胞、CD11c+HLA-DR阳性的树突状细胞的浸润数量,结合患者的临床病理参数进行相关性分析。免疫组化结果显示,结直肠癌组织中胰高血糖素样肽-2受体的表达水平显著低于癌旁组织(n=35,P<0.05),胰高血糖素样肽-2受体高表达患者的肿瘤组织中CD4+细胞毒性T细胞和树突状细胞的浸润数量显著高于低表达患者(n=35,P<0.05);临床相关性分析显示,胰高血糖素样肽-2受体低表达与更高的T分期、更高的淋巴结转移风险、更高的远处转移风险以及更晚的TNM分期显著相关(n=35,P<0.05),与患者年龄、性别、肿瘤部位无显著相关性,对应实验结果见图1。
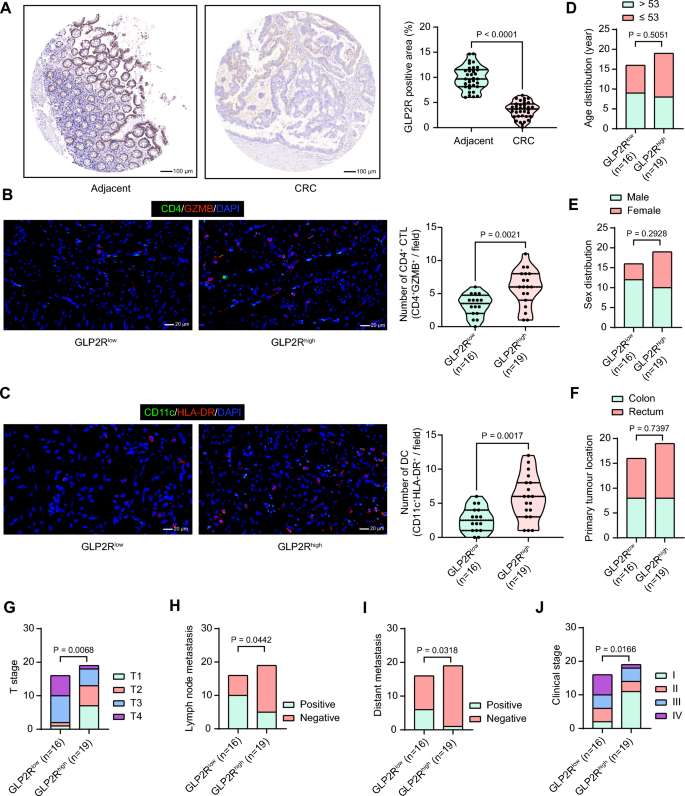
实验所用关键产品:ABclonal的胰高血糖素样肽-2受体抗体(货号A6602)、Novus Biological的FITC偶联抗CD4抗体(货号NBP3-18057F)、Cell Signaling Technologies的Alexa Fluor 647偶联抗颗粒酶B抗体(货号#71535)。
3.2 细胞水平胰高血糖素样肽-2受体的功能验证
本环节的核心目标是验证胰高血糖素样肽-2受体对结直肠癌细胞恶性表型以及免疫细胞活化的影响。实验选取人正常结肠上皮细胞NCM460以及4株结直肠癌细胞系(RKO、LS174T、SW837、SW1463),采用实时荧光定量PCR(RT-qPCR)和蛋白免疫印迹(Western blot)检测胰高血糖素样肽-2受体的基础表达水平;对RKO和SW837细胞进行慢病毒转染构建胰高血糖素样肽-2受体稳定过表达细胞系,采用细胞计数试剂盒8(CCK-8)实验、克隆形成实验检测细胞增殖能力,划痕实验、Transwell侵袭实验检测细胞迁移和侵袭能力;收集结直肠癌细胞的条件培养基处理人外周血来源的CD4+T细胞与单核来源树突状细胞的共培养体系,采用酶联免疫吸附实验(ELISA)检测促炎因子干扰素-γ(IFN-γ)、肿瘤坏死因子-α(TNF-α)、白细胞介素-12p70(IL-12p70)的释放水平,流式细胞术检测CD4+T细胞的增殖能力以及树突状细胞表面人类白细胞抗原DR(HLA-DR)的表达水平。结果显示,结直肠癌细胞系中胰高血糖素样肽-2受体的mRNA和蛋白表达水平均显著低于正常结肠上皮细胞(n=3,P<0.05);过表达胰高血糖素样肽-2受体后,RKO和SW837细胞的增殖、迁移、侵袭能力均显著降低(n=5,P<0.05);胰高血糖素样肽-2受体过表达细胞的条件培养基处理免疫细胞后,免疫细胞释放的干扰素-γ、肿瘤坏死因子-α、白细胞介素-12p70水平显著升高(n=5,P<0.05),CD4+T细胞的增殖率升高(n=5,P<0.05),树突状细胞表面人类白细胞抗原DR的表达水平显著上调(n=5,P<0.05),对应实验结果见图2。
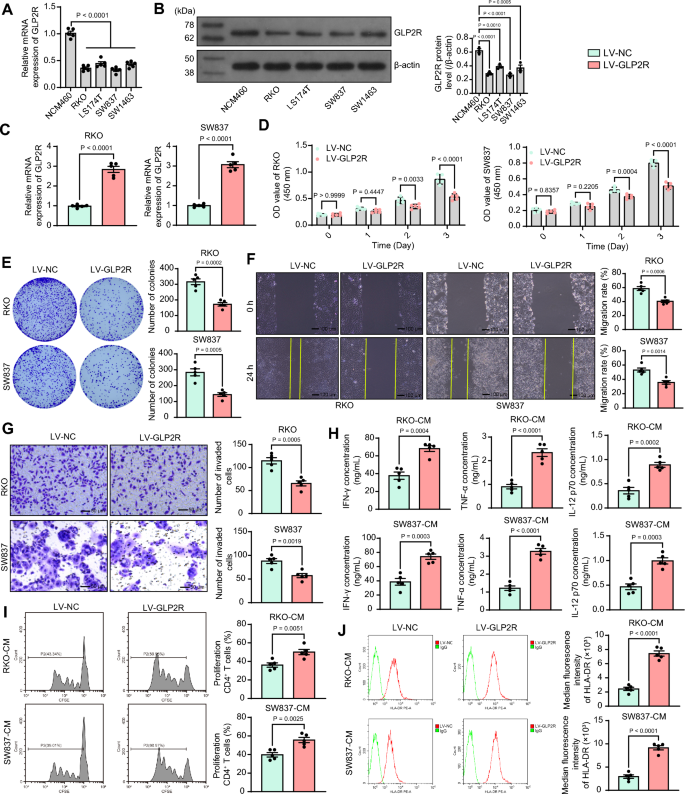
实验所用关键产品:VectorBuilder的胰高血糖素样肽-2受体过表达慢病毒、MedChemExpress的细胞计数试剂盒8试剂(货号HY-K0301)、Elabscience的干扰素-γ酶联免疫吸附实验试剂盒(货号E-EL-H0108)、Beckman的CytoFlex S流式细胞仪。
3.3 动物水平胰高血糖素样肽-2受体的功能验证
本环节的核心目标是验证胰高血糖素样肽-2受体对结直肠癌体内生长、转移以及免疫微环境的影响。实验构建稳定过表达胰高血糖素样肽-2受体的小鼠结直肠癌细胞CT26,分别建立原位结直肠癌模型、实验性肝转移模型,同时采用他莫昔芬诱导的肠上皮细胞特异性胰高血糖素样肽-2受体敲除小鼠建立氧化偶氮甲烷(AOM)/葡聚糖硫酸钠(DSS)诱导的原发性结直肠癌模型;检测原位肿瘤的体积、重量,肝转移模型的小鼠生存率和肝转移灶数量,采用免疫组化检测肿瘤组织中增殖标志物增殖细胞核抗原(PCNA)的表达,免疫荧光检测CD4+细胞毒性T细胞和主要组织相容性复合体Ⅱ类分子(MHCⅡ)阳性树突状细胞的浸润水平,酶联免疫吸附实验检测肿瘤组织中干扰素-γ、肿瘤坏死因子-α、颗粒酶B、白细胞介素-12p70的水平。结果显示,过表达胰高血糖素样肽-2受体的CT26细胞形成的原位肿瘤体积和重量显著低于对照组(n=5,P<0.05),增殖细胞核抗原阳性率显著降低(n=5,P<0.05),肿瘤组织中CD4+细胞毒性T细胞和树突状细胞的浸润水平、促炎因子水平均显著升高(n=5,P<0.05);肝转移模型中,胰高血糖素样肽-2受体过表达组小鼠的生存率显著高于对照组(n=15,P<0.05),肝转移灶数量显著减少(n=5,P<0.05);肠上皮特异性胰高血糖素样肽-2受体敲除小鼠的氧化偶氮甲烷/葡聚糖硫酸钠诱导成瘤率更高,肿瘤数量更多、体积更大,生存率更低,肿瘤组织中免疫细胞浸润水平显著降低(n=15,P<0.05),对应实验结果见图3。
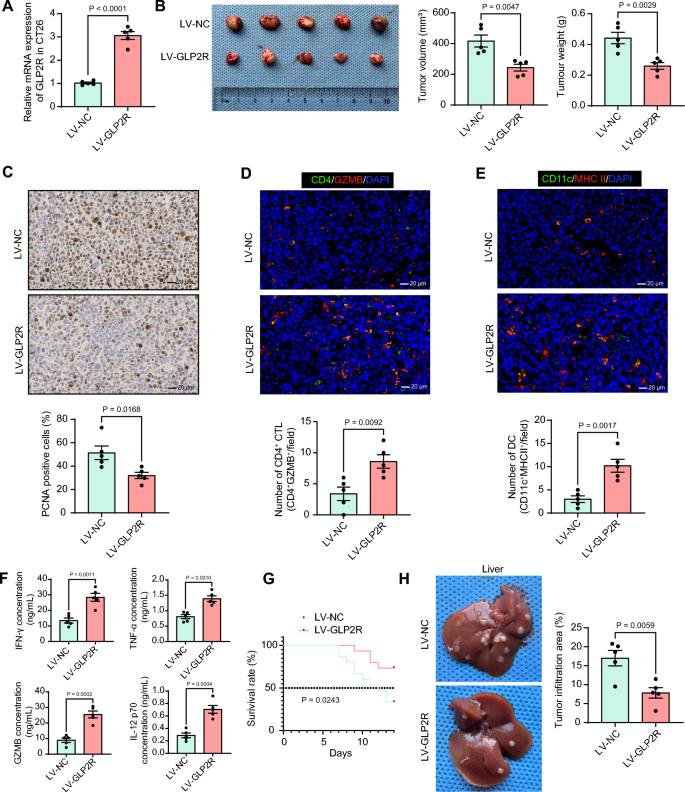
实验所用关键产品:文献未提及该部分具体实验产品,领域常规使用结直肠癌原位移植模型构建相关手术器械、氧化偶氮甲烷(货号60751ES10,Yeasen)、葡聚糖硫酸钠(货号60316ES76,Yeasen)类试剂。
3.4 胰高血糖素样肽-2受体下游分子机制探究
本环节的核心目标是明确胰高血糖素样肽-2受体调控结直肠癌恶性表型的下游分子通路。实验通过UALCAN数据库筛选与胰高血糖素样肽-2受体正相关的基因,进行京都基因与基因组百科全书(KEGG)通路富集分析;采用蛋白免疫印迹检测胰高血糖素样肽-2受体过表达后河马信号通路核心分子(MST1/2、LATS1/2、Yes相关蛋白1(YAP1))的磷酸化水平以及Yes相关蛋白1的核浆分布;采用Seahorse细胞能量代谢分析仪检测细胞外酸化率(ECAR)和氧消耗率(OCR),评估细胞糖酵解和线粒体呼吸水平,采用荧光葡萄糖探针检测葡萄糖摄取能力,乳酸检测试剂盒检测乳酸释放水平,实时荧光定量PCR检测糖酵解关键酶(葡萄糖转运蛋白1(GLUT1)、乳酸脱氢酶A(LDHA)、丙酮酸激酶M(PKM))的mRNA表达水平;采用河马信号通路抑制剂XMU-MP-1处理胰高血糖素样肽-2受体过表达细胞,进行回补实验验证通路依赖性。结果显示,通路富集分析显示胰高血糖素样肽-2受体相关基因显著富集于河马信号通路;胰高血糖素样肽-2受体过表达可显著促进MST1/2、LATS1/2、Yes相关蛋白1的磷酸化(n=3,P<0.05),抑制Yes相关蛋白1的核转位,该调控依赖于环磷酸腺苷(cAMP)/蛋白激酶A(PKA)信号通路;胰高血糖素样肽-2受体过表达细胞的糖酵解水平、糖酵解储备显著降低(n=5,P<0.05),葡萄糖摄取、乳酸释放减少,糖酵解关键酶表达下调(n=5,P<0.05),而线粒体呼吸水平无显著变化;使用XMU-MP-1抑制河马信号通路后,胰高血糖素样肽-2受体过表达对糖酵解的抑制作用被逆转,细胞的增殖、迁移、侵袭能力恢复,对免疫细胞活化的促进作用被抵消(n=5,P<0.05),对应实验结果见图4、图5。
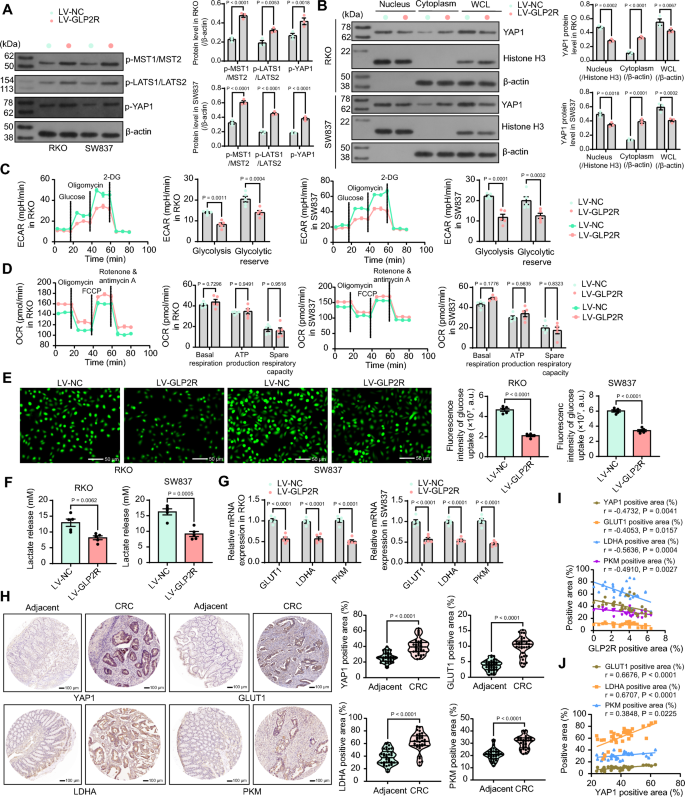
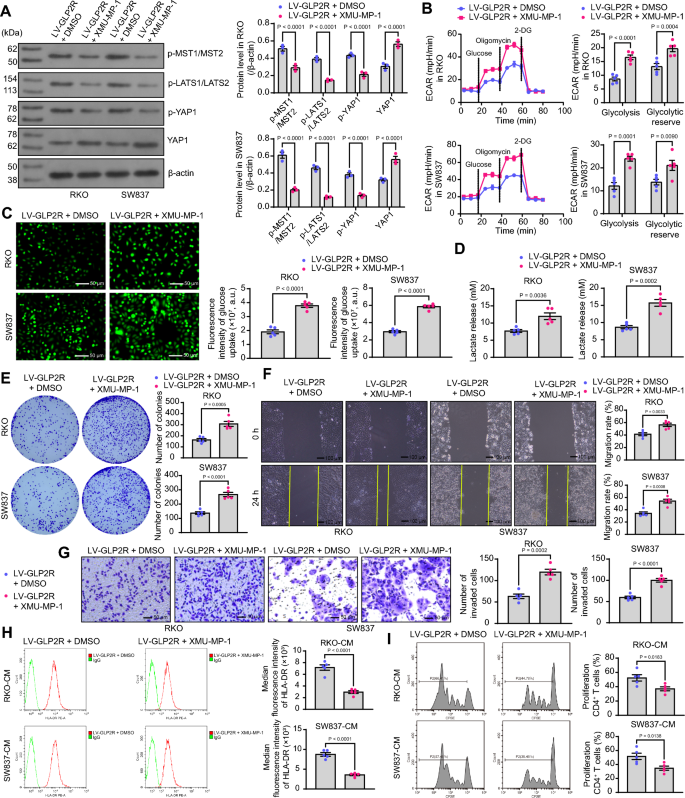
实验所用关键产品:Agilent的Seahorse XF96分析仪、Selleck的XMU-MP-1(货号S8334)、Dojindo的葡萄糖摄取探针(货号UP02)、ABclonal的磷酸化Yes相关蛋白1抗体(货号AP0489)。
3.5 胰高血糖素样肽-2受体上游转录调控机制解析
本环节的核心目标是明确胰高血糖素样肽-2受体的上游转录调控因子及其调控机制。实验通过AnimalTFDB数据库筛选与胰高血糖素样肽-2受体共表达的转录因子,结合临床样本验证转录因子间充质同源盒1与胰高血糖素样肽-2受体的表达相关性;构建间充质同源盒1稳定过表达细胞系,采用实时荧光定量PCR检测胰高血糖素样肽-2受体的mRNA水平;通过JASPAR数据库预测间充质同源盒1在胰高血糖素样肽-2受体启动子上的结合位点,构建不同结合位点缺失的胰高血糖素样肽-2受体启动子荧光素酶报告载体,采用双荧光素酶报告实验和染色质免疫共沉淀(ChIP)-实时荧光定量PCR验证间充质同源盒1与胰高血糖素样肽-2受体启动子的结合;通过回补实验(过表达间充质同源盒1同时敲低胰高血糖素样肽-2受体)验证间充质同源盒1的功能依赖于胰高血糖素样肽-2受体。结果显示,筛选得到转录因子间充质同源盒1在结直肠癌组织中表达下调,且与胰高血糖素样肽-2受体的表达呈显著正相关(n=35,P<0.05);过表达间充质同源盒1可显著上调胰高血糖素样肽-2受体的mRNA水平(n=5,P<0.05);间充质同源盒1可直接结合胰高血糖素样肽-2受体启动子上的BS3和BS4位点,促进胰高血糖素样肽-2受体的转录活性(n=5,P<0.05);过表达间充质同源盒1可抑制结直肠癌细胞的糖酵解、增殖、迁移、侵袭能力,促进免疫细胞活化,而同时敲低胰高血糖素样肽-2受体可逆转上述作用(n=5,P<0.05),对应实验结果见图6、图7。
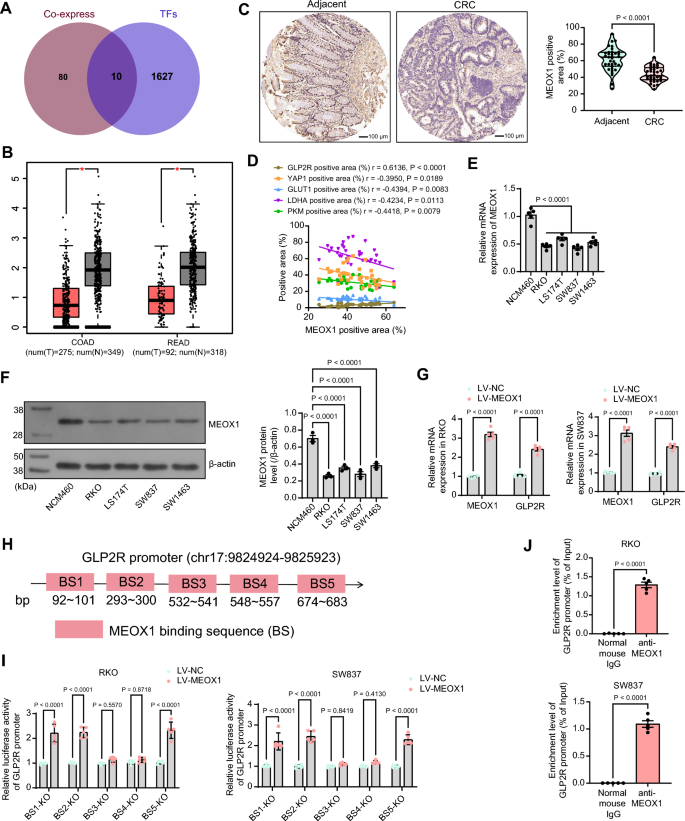
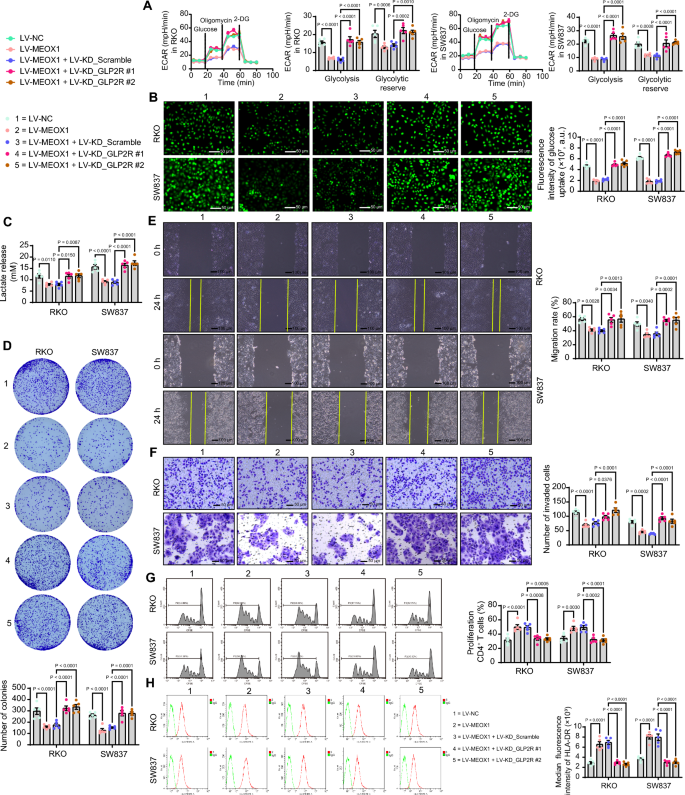
实验所用关键产品:Cell Signaling Technologies的SimpleChIP酶解染色质免疫共沉淀试剂盒(货号#9003)、Beyotime的双荧光素酶报告基因检测试剂盒(货号RG027)、Santa Cruz Biotechnology的间充质同源盒1抗体(货号sc-134389)。
3.6 动物水平间充质同源盒1功能的验证
本环节的核心目标是体内验证间充质同源盒1通过胰高血糖素样肽-2受体调控结直肠癌进展的作用。实验构建稳定过表达间充质同源盒1、同时过表达间充质同源盒1并敲低胰高血糖素样肽-2受体的CT26细胞系,建立原位结直肠癌模型和实验性肝转移模型,检测肿瘤生长、转移情况,免疫组化检测Yes相关蛋白1和糖酵解关键酶的表达,免疫荧光检测免疫细胞浸润水平,酶联免疫吸附实验检测促炎因子水平。结果显示,过表达间充质同源盒1可显著抑制原位肿瘤的生长和肝转移,降低Yes相关蛋白1和糖酵解关键酶的表达,增加肿瘤组织中免疫细胞浸润和促炎因子水平(n=5,P<0.05);而同时敲低胰高血糖素样肽-2受体可逆转间充质同源盒1的抑癌作用(n=5,P<0.05),对应实验结果见图8。
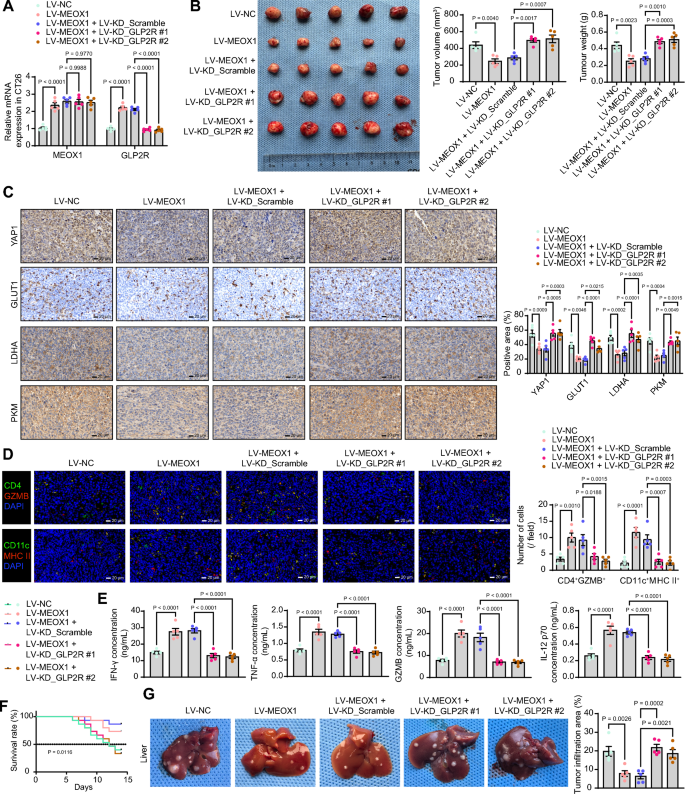
实验所用关键产品:文献未提及该部分具体实验产品,领域常规使用慢病毒载体、免疫组化相关试剂。
3.7 间充质同源盒1上游表观调控机制解析
本环节的核心目标是明确结直肠癌中间充质同源盒1表达下调的表观遗传机制。实验通过Shiny Methylation Analysis Resource Tool数据库预测间充质同源盒1启动子的甲基化水平,采用甲基化DNA免疫共沉淀(MeDIP)检测12例结直肠癌患者肿瘤组织和癌旁组织中间充质同源盒1启动子的甲基化水平,采用甲基化特异性PCR(MSP)和亚硫酸氢盐测序(BSSQ)检测结直肠癌细胞系中间充质同源盒1启动子的甲基化水平;采用DNA甲基化抑制剂5-氮杂胞苷(5-Aza)处理结直肠癌细胞,检测间充质同源盒1的mRNA表达变化。结果显示,结直肠癌组织中间充质同源盒1启动子的甲基化水平显著高于癌旁组织(n=12,P<0.05),且与间充质同源盒1的mRNA表达水平呈显著负相关(n=12,P<0.05);结直肠癌细胞系中间充质同源盒1启动子的甲基化水平显著高于正常结肠上皮细胞(n=5,P<0.05);使用5-氮杂胞苷处理可显著降低间充质同源盒1启动子的甲基化水平,上调间充质同源盒1的mRNA表达(n=5,P<0.05),对应实验结果见图9。
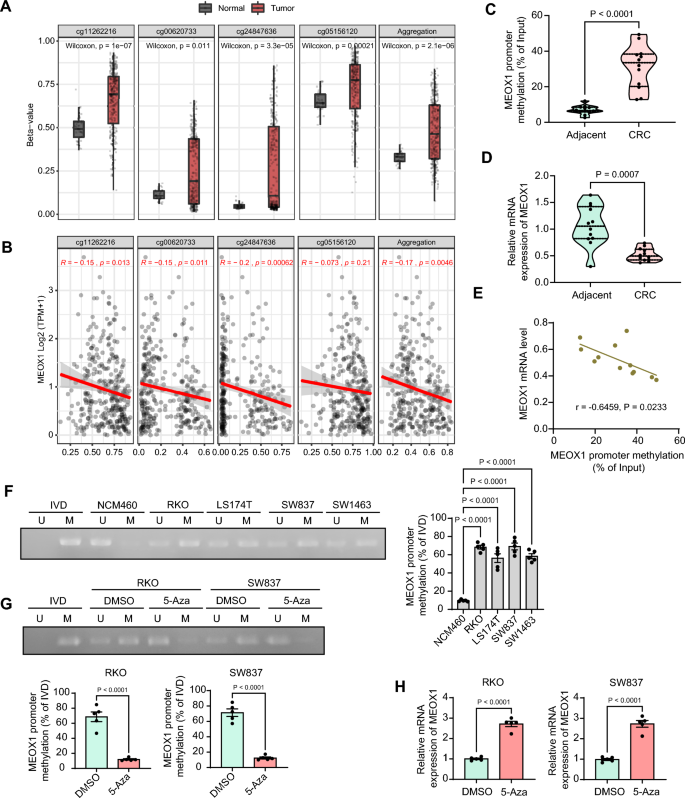
实验所用关键产品:Abcam的甲基化DNA免疫共沉淀试剂盒(货号ab117136)、Vazyme的EpiArt DNA甲基化亚硫酸盐试剂盒(货号EM101)、Selleck的5-氮杂胞苷(货号S1782)。
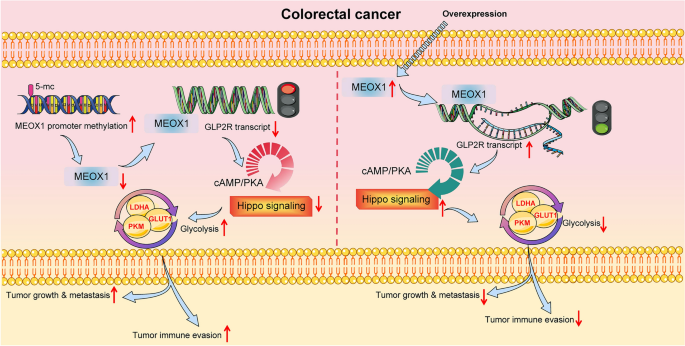
本研究最终提出的完整调控机制模型见图10,明确了DNA高甲基化介导的间充质同源盒1表达缺失,通过抑制胰高血糖素样肽-2受体转录,阻断河马信号通路激活,进而促进Yes相关蛋白1介导的糖酵解和免疫逃逸的完整通路。
4. Biomarker 研究及发现成果
本研究涉及的生物标志物(Biomarker)包括表观遗传类、蛋白表达类、代谢类三类,筛选验证逻辑遵循“生物信息学筛选→临床样本验证→细胞与动物模型功能验证→分子机制确认”的完整链条。
表观遗传类生物标志物为间充质同源盒1启动子甲基化,其来源为结直肠癌患者的肿瘤组织基因组DNA,验证方法为甲基化DNA免疫共沉淀-实时荧光定量PCR、甲基化特异性PCR,检测结果显示结直肠癌组织中间充质同源盒1启动子的甲基化水平较癌旁组织升高2.7倍(n=12,P<0.05),与间充质同源盒1的mRNA表达相关系数为-0.82(n=12,P<0.001),该标志物可用于结直肠癌的早期诊断,其与肿瘤T分期的相关性具有统计学意义(P<0.05)。蛋白表达类生物标志物包括胰高血糖素样肽-2受体、间充质同源盒1,其来源为结直肠癌患者的肿瘤组织石蜡切片,验证方法为免疫组化,胰高血糖素样肽-2受体低表达与更晚的TNM分期显著相关(n=35,P<0.05),基于GEPIA数据库分析显示胰高血糖素样肽-2受体高表达患者的总生存期更长,风险比(HR)为0.42(P=0.003),可作为结直肠癌的独立预后标志物;间充质同源盒1的表达水平与胰高血糖素样肽-2受体呈正相关(n=35,P<0.05),与Yes相关蛋白1、糖酵解关键酶的表达呈负相关(n=35,P<0.05)。代谢类生物标志物包括葡萄糖转运蛋白1、乳酸脱氢酶A、丙酮酸激酶M,其表达水平受Yes相关蛋白1调控,与结直肠癌的糖酵解水平、恶性表型呈正相关,可作为胰高血糖素样肽-2受体通路激活的药效学监测指标。
本研究生物标志物相关成果的创新性在于,首次明确了间充质同源盒1启动子甲基化作为结直肠癌早期诊断标志物的潜在价值,以及胰高血糖素样肽-2受体作为预后标志物和治疗靶点的临床转化潜力,二者联合检测可提升结直肠癌诊断和预后评估的准确性。推测:间充质同源盒1启动子甲基化联合胰高血糖素样肽-2受体表达检测可应用于结直肠癌的高危人群筛查,需扩大临床样本量进一步验证其诊断效能(文献未明确提供该标志物的敏感性、特异性数据,基于临床相关性结果推测)。