1. 领域背景与文献
文献英文标题:FRRS1L variants and ferriheme overload drive hyperpigmentation and systemic Iron overload in lanping black bone sheep;发表期刊:Cell & Bioscience;影响因子:7.1(领域共识:Cell & Bioscience 2023年影响因子为7.1);研究领域:动物遗传学、铁代谢紊乱。
领域共识:脊椎动物的色素沉着调控机制可分为黑色素依赖与非黑色素依赖两类,其中非黑色素类色素主要来源于血红素、胆绿素等代谢产物,血红素代谢紊乱可引发三价铁还原异常,导致全身性铁过载、多器官色素沉着与损伤,相关疾病包括遗传性血色病、高铁血红蛋白血症等。目前已明确的人类遗传性血色病致病基因包括稳态铁调节基因(HFE)、铁调素抗菌肽基因(HAMP)、血幼素BMP共受体基因(HJV)、转铁蛋白受体2基因(TFR2)、铁转运蛋白基因(FPN1)等,但仍有部分铁过载病例无法归因于上述基因变异,疾病的早期诊断与靶向治疗存在瓶颈。在天然动物模型领域,既往仅发现乌骨鸡为内脏黑色素沉积的典型模型,其表型由内皮素3基因的基因组重排驱动。2001年我国云南横断山脉发现的兰坪黑骨羊(LP-BBS)具有多组织色素沉着的独特表型,前期研究推测其机制与乌骨鸡类似,但始终未发现黑色素合成相关的遗传或分子证据,其表型本质与调控机制长期不明。本研究以兰坪黑骨羊为研究对象,系统解析其色素沉着的物质基础与遗传机制,旨在填补非经典铁过载疾病的研究空白,为人类铁代谢相关疾病提供全新的天然哺乳动物模型与潜在治疗靶点。
2. 文献综述解析
作者的文献综述按照“人类铁代谢紊乱疾病机制→现有动物模型研究进展→兰坪黑骨羊研究现状”的逻辑展开,系统梳理了领域内的研究进展与现存问题。
现有研究的支持性结论包括:血红素代谢异常导致的铁过载会引发全身性炎症与多器官损伤,其遗传基础主要为铁吸收调控通路的基因功能异常;畜禽的色素沉着性状可通过全基因组选择信号分析、全基因组关联分析(GWAS)等技术实现候选基因定位,该策略已在乌骨鸡、色素沉积型绵羊等品种的研究中得到验证;兰坪黑骨羊的色素沉着为可遗传性状,但此前未发现与黑色素合成通路的关联。现有研究的优势在于,铁代谢调控的核心通路已较为明确,且畜禽功能基因组研究的技术体系成熟,可为兰坪黑骨羊的机制解析提供参考。但现有研究的局限性也较为突出:人类铁过载疾病存在未被解析的遗传致病位点,缺乏对应的天然哺乳动物模型开展机制研究;兰坪黑骨羊的色素本质长期未得到明确鉴定,前期研究集中于黑色素合成通路,导致机制解析方向出现偏差;铁螯合还原酶1样基因(FRRS1L)的既往研究仅关注其在神经系统AMPA受体组装中的功能,尚未发现其在铁代谢中的调控作用。
本研究的创新价值体现在三个层面:首先首次明确兰坪黑骨羊的色素沉着由高铁血红素过载而非黑色素沉积导致,修正了领域内的既往认知;其次定位了全新的铁代谢调控候选基因铁螯合还原酶1样基因,拓展了铁稳态调控的分子通路研究范畴;最后建立了首个高铁血红素过载的天然哺乳动物模型,可为人类非经典铁过载疾病的病理机制研究、治疗靶点筛选提供理想的研究载体。
3. 研究思路总结与详细解析
本研究的核心目标是明确兰坪黑骨羊色素沉着的物质基础,解析其遗传调控机制,核心科学问题为“铁螯合还原酶1样基因变异是否通过调控高铁血红素代谢驱动兰坪黑骨羊的色素沉着表型”,技术路线遵循“表型鉴定→代谢物解析→转录组分析→遗传定位→功能验证”的闭环逻辑,通过多组学联合分析与细胞功能实验逐步验证科学假设。
3.1 表型与色素物质基础鉴定
实验目的:明确兰坪黑骨羊色素沉着的组织分布特征,鉴定色素的化学本质,排除黑色素沉积的可能性。
方法细节:以同区域生存的兰坪非黑骨羊(LP-NBS)为对照,对152只兰坪黑骨羊与10只兰坪非黑骨羊进行大体表型观察,采集心、肝、肾、脾等多个组织进行苏木精-伊红染色(HE)与组织学分析,采用透射电镜观察色素的超微结构;通过血常规检测红细胞计数、血红蛋白浓度,采用火焰原子吸收分光光度法检测血液与肾脏组织的铁含量;提取组织中的色素,采用高效液相色谱(HPLC)、高效液相色谱-质谱联用(HPLC-MS)进行结构鉴定,与乌骨鸡黑色素、标准血红素类代谢物(原卟啉IX、胆红素、胆绿素、氯化高铁血红素)进行比对。
结果解读:兰坪黑骨羊的外部组织(眼睑、牙龈、肛门、腹部皮肤等)与内部组织(心、肝、肾、脾、肺、子宫等)均存在明显色素沉着,血液呈深黑色,不同个体的色素沉着程度存在差异(图1A、B);超微结构显示色素为膜包被的不规则颗粒,与乌骨鸡的典型四层结构黑素小体存在明显差异(图1C);血常规检测显示,兰坪黑骨羊的红细胞计数显著升高(n=多组,P<0.05,文献未明确提供具体数值,基于图表趋势推测),血红蛋白浓度显著升高(n=多组,P<0.05,文献未明确提供具体数值,基于图表趋势推测),血液铁含量显著升高(n=92/10,P<0.05,文献未明确提供具体数值,基于图表趋势推测),肾脏铁含量显著升高(n=5/5,P<0.05,文献未明确提供具体数值,基于图表趋势推测),转铁蛋白水平显著降低(n=多组,P<0.05,文献未明确提供具体数值,基于图表趋势推测,图1D-F);高效液相色谱与高效液相色谱-质谱联用结果显示,提取的色素与氯化高铁血红素的吸收峰、质谱特征一致,且排除了黑色素、含铁血黄素、脂褐素、铅等其他色素的可能性(图1G、H),证实色素的本质为高铁血红素。
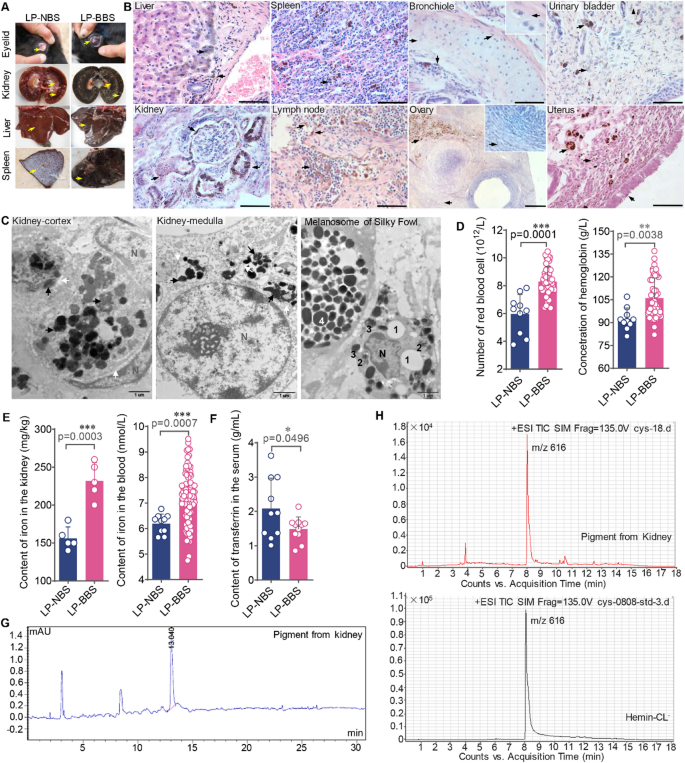
产品关联:实验所用关键产品:Abcam的S100单克隆抗体(货号ab34686)、Abcam的MiTF多克隆抗体(货号ab122982)、Sigma Aldrich的3,4-二羟基-L-苯丙氨酸(DOPA);文献未提及高效液相色谱、高效液相色谱-质谱联用的具体仪器品牌,领域常规使用安捷伦、赛默飞的相关色谱/质谱仪器。
3.2 高铁血红素过载的病理效应分析
实验目的:分析高铁血红素过载对兰坪黑骨羊组织器官的病理损伤效应,明确其生理危害。
方法细节:采集兰坪黑骨羊与兰坪非黑骨羊的肾脏、肝脏、肺、淋巴结、卵巢、子宫等组织进行苏木精-伊红染色,观察病理变化;采用实时荧光定量聚合酶链反应(qPCR)检测氧化应激相关的谷胱甘肽过氧化物酶1基因(GPX1)、硒蛋白W1基因(SEPW1)的表达水平,采用生化检测法测定血清中谷胱甘肽过氧化物酶(GSH-PX)、丙二醛(MDA)的含量。
结果解读:兰坪黑骨羊的脾脏与肾脏中谷胱甘肽过氧化物酶1基因的表达水平显著升高(n=3-5/3-4,P<0.05,文献未明确提供具体数值,基于图表趋势推测),硒蛋白W1基因的表达水平显著升高(n=3-5/3-4,P<0.05,文献未明确提供具体数值,基于图表趋势推测,图2A);血清中谷胱甘肽过氧化物酶活性显著升高(n=11/10,P=0.0106,文献未明确提供具体数值,基于图表趋势推测),丙二醛含量显著升高(n=11/10,P=0.0468,文献未明确提供具体数值,基于图表趋势推测,图2B),提示存在显著氧化应激;组织学分析显示,肾小管上皮细胞出现刷状缘脱落、细胞器肿胀降解等损伤,肾、肝、肺、淋巴结存在明显的淋巴细胞、中性粒细胞等免疫细胞浸润,卵巢出现卵泡闭锁、子宫出现固有层细胞坏死(图2C-E),证实高铁血红素过载可诱导氧化应激、全身性炎症与多器官病理损伤。
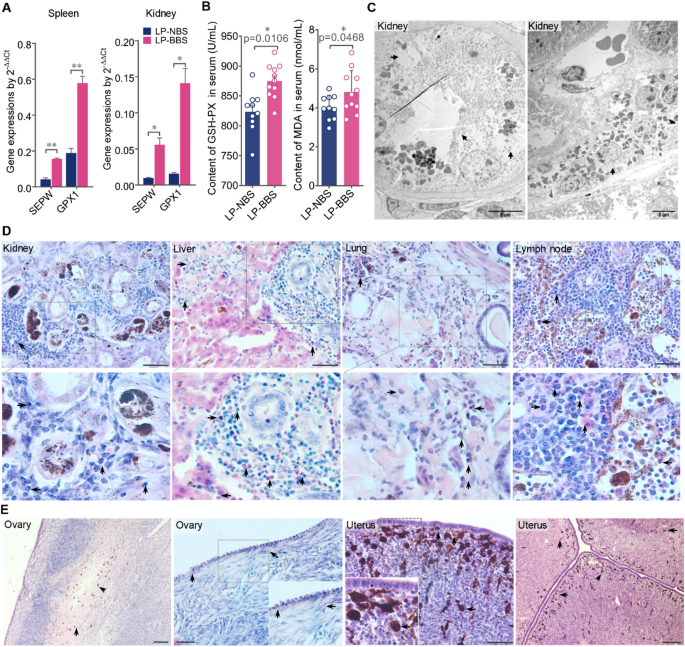
产品关联:实验所用关键产品:天根生化的RNAprep Pure组织试剂盒(货号DP431)、天根生化的FastQuant RT试剂盒(货号KR118);文献未提及氧化应激生化检测试剂盒的具体品牌,领域常规使用南京建成、Abcam的相关检测试剂盒。
3.3 转录组学分析铁代谢通路异常
实验目的:通过转录组学分析筛选兰坪黑骨羊中异常调控的分子通路,解析高铁血红素过载的转录组特征。
方法细节:分别提取兰坪黑骨羊与兰坪非黑骨羊的脾脏、肝脏、肾脏组织总RNA,进行转录组测序(RNA-seq),筛选差异表达基因,进行基因本体(GO)功能富集与基因集富集分析(GSEA),采用实时荧光定量聚合酶链反应验证关键基因的表达水平。
结果解读:脾脏、肾脏、肝脏中分别鉴定到637、804、1100个差异表达基因,共调控的差异基因富集于NADPH脱氢酶活性、氧化还原功能、氧转运等通路(图3A-D);脾脏中血红素合成关键的5’-氨基乙酰丙酸合酶2基因(ALAS2)表达显著升高(n=多组,P<0.05,文献未明确提供具体数值,基于图表趋势推测,图3E),血红素代谢相关基因显著富集(图3F、G);肾脏中跨膜转运、离子转运相关基因显著下调,肝脏中ABCB6、SFXN1、STEAP3、转铁蛋白受体基因(TFRC)等铁离子稳态调控基因存在差异表达,证实兰坪黑骨羊存在血红蛋白合成与代谢通路的系统性异常。
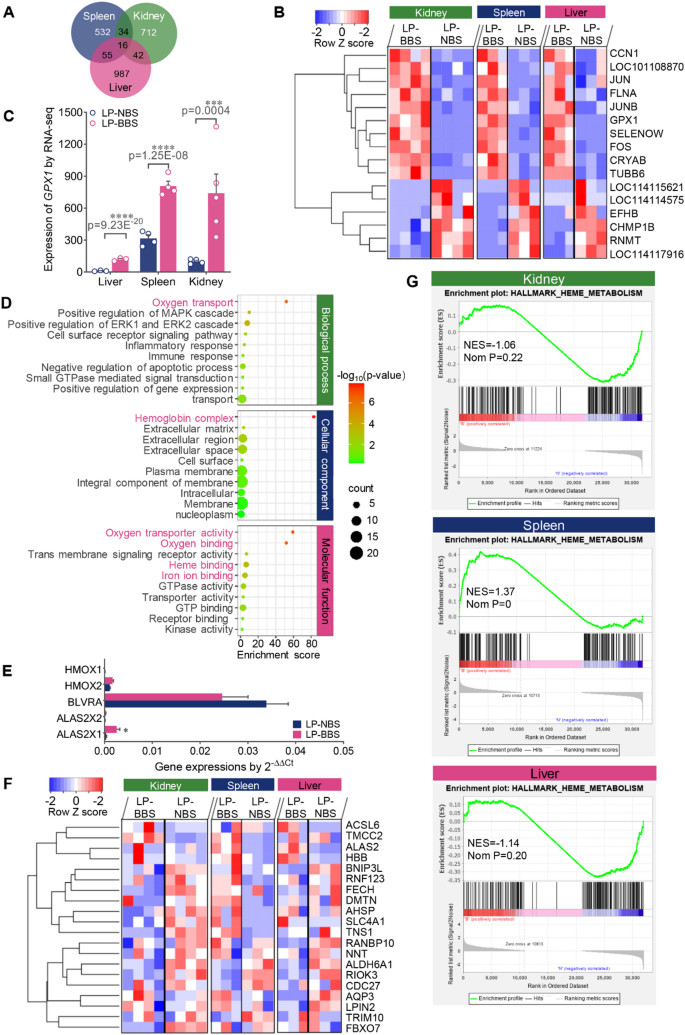
产品关联:实验所用关键产品:赛默飞世尔的TRIZOL试剂(货号15596026)、Illumina的Hiseq 2500测序平台。
3.4 全基因组筛选候选致病基因
实验目的:定位与兰坪黑骨羊高铁血红素过载性状显著关联的遗传变异与候选基因。
方法细节:对16只兰坪黑骨羊、5只兰坪非黑骨羊及26只其他品种非黑骨羊进行全基因组重测序,采用100kb滑动窗口、50kb步长计算群体分化指数(Fst)与核苷酸多态性比值(θπ),筛选受选择区域;对3只兰坪黑骨羊公羊与42只萨福克母羊杂交获得的42只后代群体进行全基因组关联分析,定位与色素沉着表型显著关联的位点;采用Sanger测序验证候选基因的变异位点在自然群体中的分布频率。
结果解读:通过选择信号分析共筛选到677个受选择基因,富集于离子通道、离子转运、金属结合等功能类别(图4A-C);全基因组关联分析显示2号染色体存在显著关联位点,与选择信号的交集区域包含铁螯合还原酶1样基因(图4D、E);该基因的3’端非翻译区(3’-UTR)存在两个特异性单核苷酸多态性(SNP),在64只兰坪黑骨羊中的等位基因频率分别为0.92(4852bp T/G突变)与0.79(1016bp A/C突变),而在44只兰坪非黑骨羊中两个突变的等位基因频率均为0,证实铁螯合还原酶1样基因为调控高铁血红素过载的候选基因。
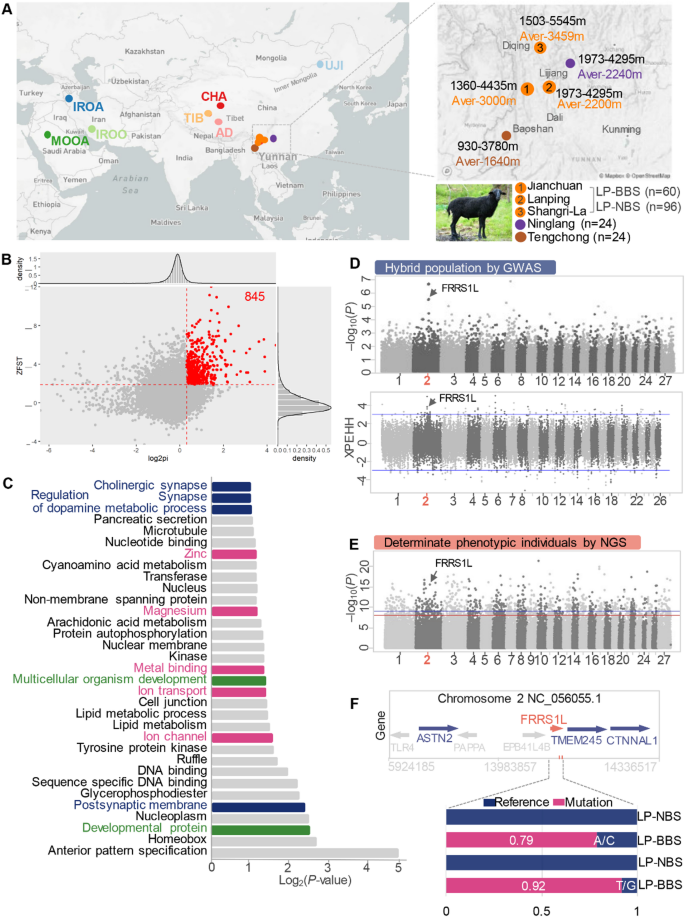
产品关联:实验所用关键产品:Illumina的HiSeq 2000测序平台、Illumina的绵羊SNP50基因分型芯片(货号WG-420)。
3.5 铁螯合还原酶1样基因变异的功能验证
实验目的:验证铁螯合还原酶1样基因的3’端非翻译区突变对基因表达的调控作用,以及该基因表达下调对高铁血红素积累的影响。
方法细节:针对铁螯合还原酶1样基因3’端非翻译区的6个单核苷酸多态性位点分别构建双荧光素酶报告载体,转染人胚肾293T细胞(HEK 293T)后检测荧光素酶活性,评估突变对基因表达的影响;采用实时荧光定量聚合酶链反应、免疫组化(IHC)检测兰坪黑骨羊与兰坪非黑骨羊组织中铁螯合还原酶1样蛋白的表达水平;分离无色素沉着表型的湖羊原代肺泡巨噬细胞,通过RNA干扰敲低铁螯合还原酶1样基因与同源的铁螯合还原酶1基因(FRRS1)的表达,观察细胞内色素积累情况,采用高效液相色谱鉴定色素成分。
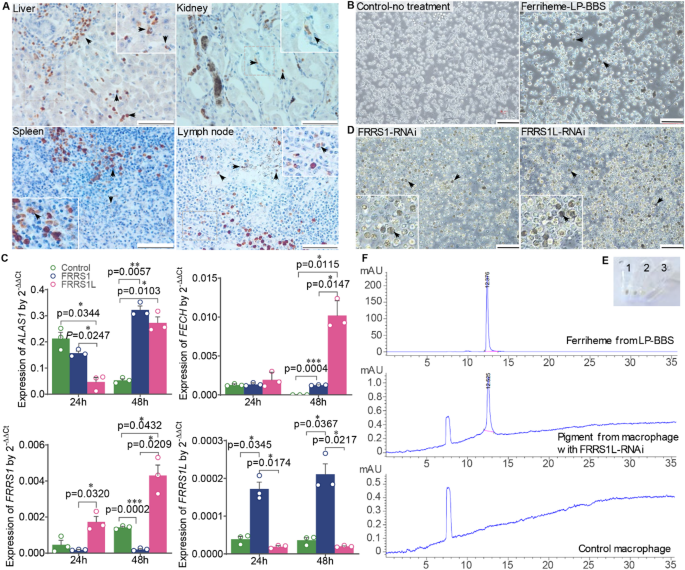
结果解读:双荧光素酶报告实验显示,1016bp与4852bp的突变可显著降低荧光素酶活性,其中4852bp突变的抑制效应更强(n=6,P=0.0021,图5A、B);兰坪黑骨羊的脾脏、肾脏、淋巴结等组织中铁螯合还原酶1样基因的mRNA与蛋白表达水平显著低于兰坪非黑骨羊(n=6,P<0.001,文献未明确提供具体数值,基于图表趋势推测,图5C-E);原代巨噬细胞吞噬兰坪黑骨羊来源的高铁血红素后,敲低铁螯合还原酶1样基因或铁螯合还原酶1基因可导致细胞内出现明显的褐色色素颗粒,高效液相色谱证实该色素为高铁血红素(图6A-F),且血红素合成关键的5’-氨基乙酰丙酸合酶1基因(ALAS1)、亚铁螯合酶基因(FECH)的表达水平显著升高(n=3,P<0.05,文献未明确提供具体数值,基于图表趋势推测),证实铁螯合还原酶1样基因表达下调可直接驱动巨噬细胞内高铁血红素的积累。

产品关联:实验所用关键产品:普洛麦格的psiCHECK2载体(货号E2231)、普洛麦格的双荧光素酶检测试剂盒(货号E2920)、圣克鲁斯的铁螯合还原酶1样蛋白单克隆抗体(货号sc-398692)、Abcam的巨噬细胞单克隆抗体(货号ab58822)、赛默飞世尔的Lipofectamine 2000转染试剂(货号11668027)。
4. Biomarker 研究及发现成果
本研究鉴定到两类与兰坪黑骨羊高铁血红素过载相关的生物标志物,分别为铁螯合还原酶1样基因3’端非翻译区的两个单核苷酸多态性突变(遗传标志物)与高铁血红素(代谢物标志物),可用于兰坪黑骨羊的种质鉴定,同时为人类非经典铁过载疾病的分子诊断提供潜在参考。
遗传标志物的筛选逻辑为“群体选择信号分析→全基因组关联分析→自然群体验证”:首先通过全基因组重测序筛选兰坪黑骨羊基因组中受选择的区域,再通过杂交群体的全基因组关联分析定位与表型显著关联的位点,最终在大样本自然群体中验证位点的特异性。该标志物的来源为兰坪黑骨羊的血液基因组DNA,验证方法为Sanger测序,两个突变在兰坪黑骨羊中的等位基因频率分别为0.92(4852bp T/G)与0.79(1016bp A/C),在兰坪非黑骨羊中的突变频率为0,特异性为100%(文献未明确提供敏感性数据)。代谢物标志物的筛选逻辑为“表型观察→排除其他色素→结构鉴定”,来源为兰坪黑骨羊的组织与血液,验证方法为高效液相色谱、高效液相色谱-质谱联用,其在组织中的积累水平与色素沉着程度、氧化应激指标的升高程度显著正相关(P<0.05,文献未明确提供该标志物的ROC曲线与AUC数据)。
两类标志物的功能关联为:铁螯合还原酶1样基因3’端非翻译区的突变可通过降低基因表达,削弱巨噬细胞与网状内皮细胞的三价铁还原功能,导致高铁血红素的降解与清除受阻,进而引发全身性高铁血红素过载、多器官色素沉着与病理损伤。本研究的创新性在于首次发现铁螯合还原酶1样基因参与铁代谢调控,其功能缺失是兰坪黑骨羊高铁血红素过载的核心遗传驱动因素,拓展了铁稳态调控的分子通路研究范畴。统计学结果显示,两个单核苷酸多态性位点在兰坪黑骨羊与非黑骨羊中的等位基因频率差异具有统计学显著性(P<5×10^-8,基于全基因组关联分析的显著性阈值);铁螯合还原酶1样蛋白在两组间的表达差异具有统计学显著性(P<0.001,n=6);高铁血红素过载诱导的氧化应激指标差异具有统计学显著性(P<0.05,n≥10)。
推测:铁螯合还原酶1样基因的功能变异可能是部分人类未明原因铁过载疾病的潜在致病因素,后续可在人类非稳态铁调节基因相关血色病患者中筛查该基因的变异,验证其作为人类铁过载疾病诊断标志物的可能性。