1. 领域背景与文献
文献英文标题:TonEBP/NFAT5 expression is associated with cisplatin resistance and migration in macrophage-induced A549 cells;发表期刊:BMC Molecular and Cell Biology;影响因子:未公开;研究领域:肿瘤学(非小细胞肺癌肿瘤微环境与耐药机制)。
领域共识显示,肺癌是全球范围内癌症相关死亡的首要原因,其中非小细胞肺癌占比约85%,转移复发和化疗耐药是导致患者预后不佳的核心因素。顺铂作为非小细胞肺癌一线化疗的铂类药物,其疗效受肿瘤细胞耐药性限制,高剂量使用又会引发肾毒性、神经毒性等严重不良反应,临床亟需明确顺铂耐药的调控机制以优化治疗方案。肿瘤微环境中的肿瘤相关巨噬细胞是间质细胞的重要组成部分,既往研究已证实其可通过分泌细胞因子、趋化因子等旁分泌因子,促进多种癌症的血管生成、转移及化疗耐药,巨噬细胞浸润水平与肺癌、乳腺癌等多种癌症的不良预后呈正相关。张力反应增强子结合蛋白/活化T细胞核因子5(TonEBP/NFAT5)是经典的渗透压调控转录因子,近年研究发现其还参与炎症反应、细胞分化调控,在肾癌、结肠癌细胞中可通过上调S100A4表达促进转移,且其高表达与肺癌患者术后生存率降低显著相关,但肿瘤微环境中的巨噬细胞是否通过调控该分子介导肺癌细胞的顺铂耐药及迁移,此前尚未明确。本研究针对这一研究空白开展机制解析,可为非小细胞肺癌的耐药干预和转移阻断提供新的潜在靶点。
2. 文献综述解析
作者的文献综述按照“临床困境→微环境调控→分子靶点研究”的逻辑展开,系统梳理了非小细胞肺癌耐药与转移的研究现状、巨噬细胞的促癌功能及张力反应增强子结合蛋白/活化T细胞核因子5的相关研究进展。
现有研究的核心结论可分为三个层面,一是临床层面,非小细胞肺癌的转移和化疗耐药是患者死亡的主要原因,肿瘤微环境对化疗应答的调控作用已成为领域研究热点;二是微环境层面,肿瘤相关巨噬细胞可分泌CC类趋化因子配体18、粒细胞-巨噬细胞集落刺激因子等多种因子,促进乳腺癌转移、胰腺癌吉西他滨耐药、肺癌依托泊苷耐药等表型,M2型巨噬细胞与多种癌症的不良预后密切相关;三是分子层面,张力反应增强子结合蛋白/活化T细胞核因子5除调控渗透压稳态外,还参与肿瘤恶性表型调控,其在肾癌、结肠癌中发挥促转移作用,且与肺癌患者预后负相关。现有研究的方法优势在于,体外间接共培养、条件培养基处理等模型可较好模拟肿瘤微环境中的旁分泌调控作用,RNA干扰技术可实现目标基因的精准敲低以验证功能。但现有研究存在明显局限性,即大多单独关注巨噬细胞的促癌作用或张力反应增强子结合蛋白/活化T细胞核因子5的肿瘤相关功能,尚未明确两者在肺癌顺铂耐药和迁移调控中的上下游关系,也缺乏对具体介导信号通路的解析。本研究的创新价值在于,首次揭示巨噬细胞通过旁分泌作用上调肺腺癌细胞中张力反应增强子结合蛋白/活化T细胞核因子5的表达,进而介导顺铂耐药和迁移侵袭表型,明确了胞外调节蛋白激酶(ERK)、核因子κB(NF-κB)等通路在该过程中的差异化调控作用,填补了两者调控关系的研究空白,为肺癌耐药干预提供了新的潜在靶点。
3. 研究思路总结与详细解析
本研究的核心目标是明确巨噬细胞对肺腺癌A549细胞顺铂耐药和迁移的调控作用及分子机制,核心科学问题为“巨噬细胞是否通过调控张力反应增强子结合蛋白/活化T细胞核因子5表达介导肺癌细胞的恶性表型,具体涉及哪些信号通路”,技术路线遵循“表型验证→通路解析→分子靶点验证”的闭环逻辑:首先通过共培养和条件培养基处理验证巨噬细胞对A549细胞顺铂耐药、迁移的诱导作用,其次检测相关信号通路的激活情况并通过抑制剂验证通路功能,最后检测张力反应增强子结合蛋白/活化T细胞核因子5的表达变化并通过RNA干扰敲低验证其功能。
3.1 巨噬细胞对A549细胞顺铂耐药及迁移的表型诱导验证
实验目的:明确巨噬细胞是否能诱导A549细胞产生顺铂耐药和迁移能力增强的表型。
方法细节:采用Transwell小室将A549细胞与THP-1诱导的巨噬细胞进行间接共培养,或收集巨噬细胞培养上清制备条件培养基处理A549细胞;设置0~400μM的顺铂浓度梯度处理细胞24h后,采用噻唑蓝(MTT)法检测细胞活力;通过伤口愈合实验、Transwell迁移实验检测细胞迁移能力;采用膜联蛋白V-异硫氰酸荧光素/碘化丙啶染色、4",6-二脒基-2-苯基吲哚(DAPI)染色、免疫印迹实验检测凋亡相关蛋白(聚腺苷二磷酸核糖聚合酶PARP、半胱天冬酶-3 caspase-3的剪切体)水平,验证耐药效应是否与凋亡抑制相关。同时在Calu-3、H460、H1299等多株非小细胞肺癌细胞系中验证表型的普遍性。
结果解读:噻唑蓝检测结果显示,单独培养的A549细胞在200μM顺铂处理后细胞活力不足20%,而与巨噬细胞共培养24h的A549细胞在相同顺铂浓度下活力仍达80.2%(n≥6,P<0.001),耐药诱导效应在共培养8h时即可显现(活力65.7%,n≥6,P<0.01);巨噬细胞条件培养基处理可完全重现该耐药效应,而单核细胞条件培养基无此作用。凋亡检测结果显示,顺铂处理后对照组早期凋亡率为41.5%,巨噬细胞条件培养基处理组仅为11.7%(n≥3,P<0.01),且细胞核DNA碎片化水平降低,剪切型聚腺苷二磷酸核糖聚合酶、半胱天冬酶-3的蛋白水平显著下降,证实耐药效应与凋亡抑制相关。迁移实验结果显示,巨噬细胞条件培养基处理后A549细胞的Transwell迁移率提升至对照组的423.2%(n≥5,P<0.001),伤口愈合速率也显著加快。多细胞系验证显示,巨噬细胞条件培养基可在Calu-3、H460细胞中诱导顺铂耐药,在Calu-3、H1299细胞中诱导迁移增强,提示该效应具有细胞系特异性,与不同细胞的表面受体表达及信号通路本底差异相关。
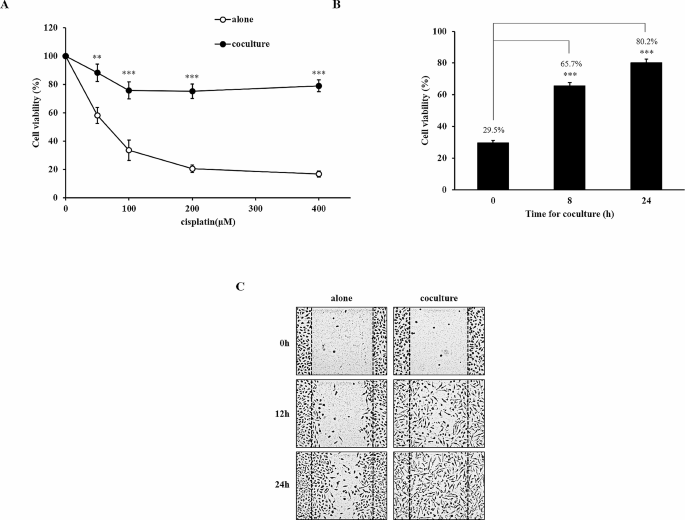
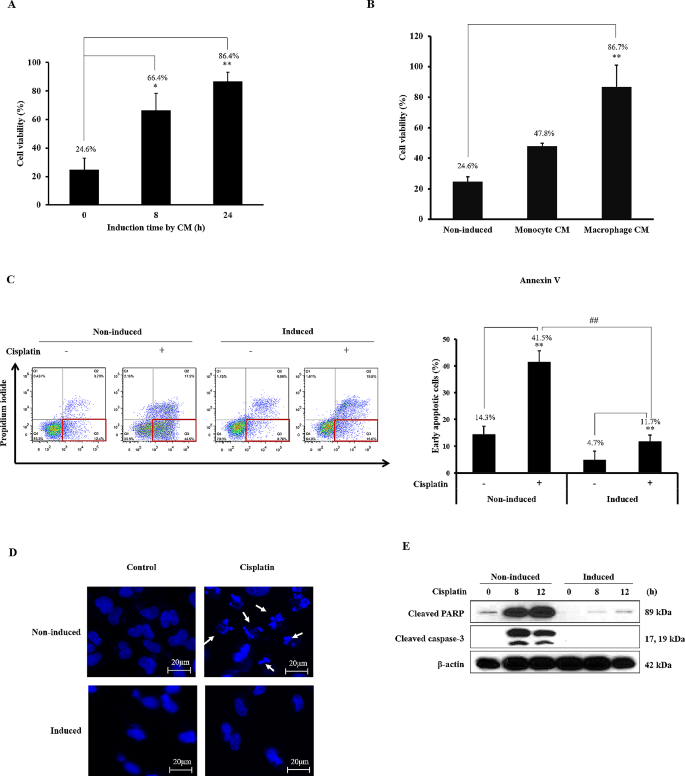
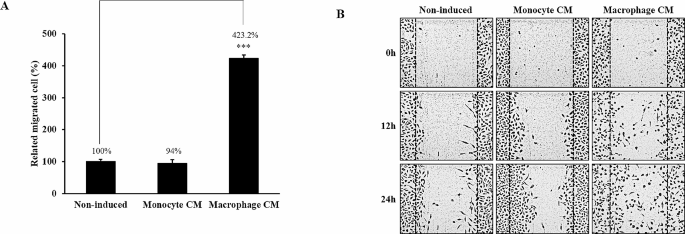

产品关联:文献提及的实验关键产品包括Sigma-Aldrich的佛波酯(PMA)、BD Biosciences的Annexin V-FITC凋亡检测试剂盒、Corning的Transwell小室;未明确提及的试剂领域常规使用RPMI 1640培养基、胎牛血清、噻唑蓝试剂等开展相关实验。
3.2 巨噬细胞诱导表型的相关信号通路解析
实验目的:明确巨噬细胞诱导A549细胞顺铂耐药和迁移所依赖的下游信号通路。
方法细节:采用免疫印迹实验检测巨噬细胞条件培养基处理不同时间(0~120min)后,A549细胞中胞外调节蛋白激酶(ERK)、p38丝裂原活化蛋白激酶(p38)、c-Jun氨基末端激酶(JNK)的磷酸化水平,以及核因子κB抑制蛋白α(IκBα)的降解水平;通过核因子κB荧光素酶报告基因实验检测核因子κB的转录活性;分别使用胞外调节蛋白激酶抑制剂PD98059、p38丝裂原活化蛋白激酶抑制剂SB203580、c-Jun氨基末端激酶抑制剂SP600125、IKK2抑制剂IV预处理细胞,验证各通路对顺铂耐药和迁移的调控作用。
结果解读:免疫印迹结果显示,巨噬细胞条件培养基处理15~30min即可显著诱导胞外调节蛋白激酶、p38丝裂原活化蛋白激酶、c-Jun氨基末端激酶的磷酸化及核因子κB抑制蛋白α的降解,其中胞外调节蛋白激酶的磷酸化可维持2h,其余通路的激活在1h后逐渐消退;核因子κB报告基因活性在处理8h后提升至对照组的234%(n≥3,P<0.01),单核细胞条件培养基无该激活效应。抑制剂实验结果显示,抑制胞外调节蛋白激酶或核因子κB活性可分别使顺铂处理后的细胞活力降至33%、47.2%(n≥3,P<0.01),显著逆转巨噬细胞诱导的耐药效应,而p38丝裂原活化蛋白激酶、c-Jun氨基末端激酶抑制剂对耐药无显著影响;凋亡检测显示,胞外调节蛋白激酶抑制剂处理可恢复顺铂诱导的半胱天冬酶-3和聚腺苷二磷酸核糖聚合酶剪切,核因子κB抑制剂则无该效应。迁移实验结果显示,抑制胞外调节蛋白激酶、c-Jun氨基末端激酶或核因子κB活性均可显著降低巨噬条件培养基诱导的迁移能力提升,p38丝裂原活化蛋白激酶抑制剂无显著作用。上述结果提示,巨噬细胞诱导的顺铂耐药主要依赖胞外调节蛋白激酶通路,而迁移表型则受胞外调节蛋白激酶、c-Jun氨基末端激酶、核因子κB通路的共同调控。
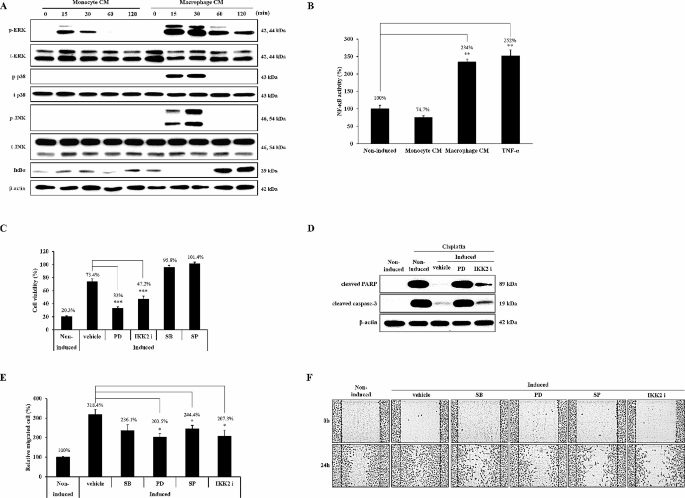
产品关联:文献未提及具体抑制剂的品牌,领域常规使用MCE或Selleck的相关通路特异性抑制剂开展实验,荧光素酶报告基因检测常规使用Promega的双荧光素酶检测试剂盒。
3.3 张力反应增强子结合蛋白/活化T细胞核因子5的功能验证
实验目的:明确张力反应增强子结合蛋白/活化T细胞核因子5在巨噬细胞诱导的顺铂耐药、迁移及侵袭中的调控作用。
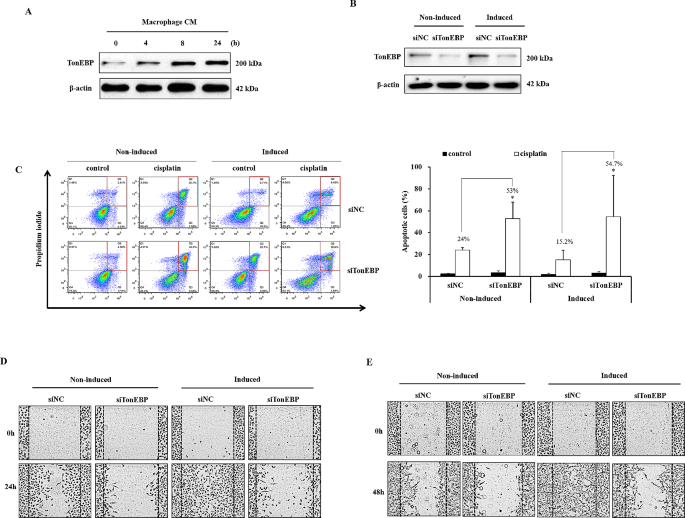
方法细节:采用免疫印迹实验检测巨噬细胞条件培养基处理不同时间(0~24h)后A549细胞中张力反应增强子结合蛋白/活化T细胞核因子5的表达水平;使用小干扰RNA转染敲低A549细胞中该分子的表达,通过膜联蛋白V染色检测顺铂诱导的凋亡率变化,通过伤口愈合实验和基质胶包被的Transwell实验分别检测细胞迁移和侵袭能力的变化。
结果解读:免疫印迹结果显示,巨噬细胞条件培养基处理4h后张力反应增强子结合蛋白/活化T细胞核因子5的表达开始升高,24h达到峰值。小干扰RNA敲低该分子后,非诱导组顺铂处理的凋亡率从24.0%升至53.0%(n≥3,P<0.05);巨噬条件培养基处理组的顺铂凋亡率从15.2%升至54.7%(n≥3,P<0.05),耐药表型被完全逆转。功能实验显示,敲低该分子可完全抑制巨噬条件培养基诱导的细胞迁移和侵袭能力提升。上述结果证实张力反应增强子结合蛋白/活化T细胞核因子5是巨噬细胞介导A549细胞顺铂耐药、迁移及侵袭的关键下游调控分子。
产品关联:实验所用关键产品包括Integrated DNA Technologies的张力反应增强子结合蛋白/活化T细胞核因子5小干扰RNA、Invitrogen的Lipofectamine™ 2000转染试剂,其余试剂与前述实验一致。
4. Biomarker研究及发现成果
本研究涉及的核心生物标志物为张力反应增强子结合蛋白/活化T细胞核因子5,属于转录因子类生物标志物,其筛选及验证逻辑为“基于前期临床相关性研究(该分子高表达与肺癌患者不良预后相关)提出功能假设→体外细胞模型中验证巨噬细胞对其表达的上调作用→基因敲低验证其对顺铂耐药、迁移侵袭表型的调控功能”,逻辑链条完整。
该生物标志物的检测样本为A549细胞的全蛋白裂解液,表达水平验证方法为免疫印迹实验,功能验证采用小干扰RNA敲低技术,结合凋亡检测、迁移侵袭实验开展。统计结果显示,敲低该分子后,巨噬条件培养基处理组的顺铂凋亡率提升39.5%(n≥3,P<0.05),迁移和侵袭能力的提升被完全抑制,本研究未开展临床样本的敏感性、特异性检测。
核心成果方面,该生物标志物是巨噬细胞介导肺腺癌细胞顺铂耐药、迁移及侵袭的关键调控分子,其表达上调是肺癌细胞恶性表型的重要驱动因素;创新性在于首次明确了肿瘤微环境中巨噬细胞与肺癌细胞张力反应增强子结合蛋白/活化T细胞核因子5表达的调控关系,为肺癌顺铂耐药和转移的干预提供了新的潜在靶点;所有功能实验的组间差异均具有统计学意义(P<0.05),未涉及临床样本的预后风险比、受试者工作特征曲线等临床相关性数据。
推测:张力反应增强子结合蛋白/活化T细胞核因子5可能通过调控下游耐药相关的ATP结合盒转运体、DNA修复基因,或迁移相关的基质金属蛋白酶、尿激酶型纤溶酶原激活物发挥功能,后续需通过转录组测序、染色质免疫共沉淀等实验明确其直接靶基因,验证其在临床肺癌样本中的预后价值。